修回日期: 2024-08-21
接受日期: 2024-09-03
在线出版日期: 2024-09-28
我国幽门螺杆菌(Helicobacter pylori, H. pylori)感染率居高不下, 而高剂量二联疗法(high-dose dual therapy, HDDT)已被逐步应用于临床, 并取得较为满意的治疗效果, 这与高强度抑酸及抗生素充分发挥作用有关, 但基于国产集采药物的相关研究较少.
探讨基于国产集采药物的高剂量二联疗法根除H. pylori感染的疗效及安全性.
连续性纳入316例H. pylori感染的初治患者, 随机分为2组: HDDT组(艾司奥美拉唑肠溶胶囊20 mg qid, 阿莫西林750 mg qid, 共14 d)和含铋剂常规四联疗法(Bismuth-containing quadruple therapy, BQT)组(艾司奥美拉唑肠溶胶囊20 mg bid, 枸橼酸铋钾胶囊220 mg bid, 阿莫西林1000 mg bid, 呋喃唑酮片100 mg bid, 共14 d), 主要观察指标为H. pylori根除率, 次要观察指标为两组方案的安全性及患者依从性.
意向性治疗分析显示HDDT组与BQT组H. pylori根除率分别为88.0%和87.3%, 改良意向性治疗分析两组H. pylori根除率分别为91.4%和92.0%, 符合方案(PP)分析两组H. pylori根除率分别为93.3%和93.9%, 组间比较均无统计学差异. HDDT组总体不良事件发生率显著低于BQT组(P = 0.001). 两组患者的依从性无统计学差异.
基于国产集采药物的HDDT的H. pylori根除率与BQT相似, 不良事件发生率更低, 是临床值得选择的治疗方案.
核心提要: 幽门螺杆菌(Helicobacter pylori, H. pylori)感染在我国仍高达42.3%, 而基于国产集采药物的高剂量二联疗法根除H. pylori感染的疗效及安全性未能明确, 推断其安全性高, 且疗效不劣于含铋剂常规四联疗法.
引文著录: 叶长根, 朱晓佳, 胡娜, 吴白慧, 方军, 杨力. 高剂量二联疗法根除幽门螺杆菌的疗效及安全性分析. 世界华人消化杂志 2024; 32(9): 665-670
Revised: August 21, 2024
Accepted: September 3, 2024
Published online: September 28, 2024
The infection rate of Helicobacter pylori (H. pylori) in China remains high, and high-dose dual therapy (HDDT) has been progressively applied in clinical practice and has achieved satisfactory treatment outcomes. This is related to the strong acid inhibition and the full effectiveness of antibiotics. However, there is limited research available on domestically procured drugs.
To evaluate the efficacy and safety of high-dose dual therapy based on domestically procured drugs for eradicating H. pylori.
A total of 316 patients with newly diagnosed H. pylori infection were consecutively enrolled and randomly divided into two groups: HDDT group (esomeprazole enteric-coated capsules 20 mg qid and amoxicillin 750 mg qid for a total of 14 d) and bismuth-containing quadruple therapy (BQT) (esomeprazole enteric-coated capsules 20 mg bid, potassium citrate bismuth capsules 220 mg bid, amoxicillin 1000 mg bid, and furazolidone 100 mg bid for a total of 14 d). The primary observation index was the H. pylori eradication rate, and the secondary observation indexes were the safety of and patient compliance to the two treatment regimens.
Intention-to-treat (ITT) analysis showed that the H. pylori eradication rates in the HDDT and BQT groups were 88.0% and 87.3%, respectively. Modified ITT (MITT) analysis showed H. pylori eradication rates of 91.4% and 92.0% in the two groups, and per-protocol (PP) analysis showed H. pylori eradication rates of 93.3% and 93.9% in the two groups, with no significant difference between the groups (P > 0.05). The incidence of adverse events in the HDDT group was significantly lower than that of the BQT group (P = 0.001). There was no significant difference in treatment compliance between the two groups (P > 0.05).
HDDT based on domestically procured drugs has a similar eradication rate of H. pylori to BQT, but with a lower incidence of adverse events, making it a good treatment option worth considering in clinical practice.
- Citation: Ye CG, Zhu XJ, Hu N, Wu BH, Fang J, Yang L. Efficacy and safety of high-dose dual therapy in eradicating Helicobacter pylori. Shijie Huaren Xiaohua Zazhi 2024; 32(9): 665-670
- URL: https://www.wjgnet.com/1009-3079/full/v32/i9/665.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v32.i9.665
幽门螺杆菌(Helicobacter pylori, H. pylori)感染已成为全球性公共卫生问题, 尽管在过去的30年当中, 全球成人H. pylori感染的下降幅度已有15.9%, 但我国成人H. pylori感染率仍高达42.3%[1]. 含铋剂常规四联疗法(bismuth-containing quadruple therapy, BQT)是目前最为常用的治疗方案, 然而, 随着H. pylori对克拉霉素、左氧氟沙星、甲硝唑等抗生素的耐药性增加, 其根除率亦明显受到影响[2,3]. 质子泵抑制剂联合阿莫西林的高剂量二联疗法(high-dose dual therapy, HDDT)已被逐步应用于临床, 并取得较为满意的治疗效果[4-7]. 然而, 目前研究采用的药物多为合资或进口的非集采药物, 随着国家集采药物的推广普及, 众多基层医院甚至部分三级医院并不具备此类药物. 为明确国产集采药物在根除H. pylori治疗中的价值, 我们实施了一项前瞻性随机对照试验, 以探讨基于国产集采药物的高剂量二联疗法根除H. pylori感染的疗效及安全性.
本研究为前瞻性、单中心、随机对照临床试验, 于2022-03/2023-08在景德镇市第三人民医院消化内科实施. 研究方案获得医院伦理委员会批准(批准号: 202202). 所有研究入组者均签署了书面知情同意书. 本试验已在中国临床试验注册中心(http://www.chictr.org.cn)注册, 注册号为ChiCTR2200056895.
至我院消化内科门诊/住院的H. pylori阳性初治患者, 纳入标准: (1)年龄18-70岁; (2)13C-尿素呼气试验(UBT)/14C-尿素呼气试验明确H. pylori感染. 排除标准: (1)既往曾行H. pylori根除治疗; (2)近4 wk内曾使用质子泵抑制剂、抗生素、H2受体拮抗剂、胃黏膜保护剂、益生菌、非甾体类抗炎药、抗凝剂或激素等药物; (3)怀孕或哺乳期的女性或计划妊娠; (4)既往有相关药物过敏史; (5)曾行胃肠道相关手术; (6)其它疾病如严重肝病、心脏病、肾脏病、恶性肿瘤、精神疾病等; (7)活动性出血或缺铁性贫血; (8)诊断为黏膜相关淋巴组织淋巴瘤; (9)拒绝签署知情同意书. 研究终止标准: 患者在用药过程中出现与药物相关的严重不良事件, 无法按照既定方案治疗, 则终止试验.
收集患者的基线资料和临床特征, 按照1:1随机分为高剂量二联治疗组(HDDT组)和含铋剂常规四联治疗组(BQT组). 随机序列号由计算机生成, 并放入按顺序编号的密封不透明信封中, 在入组时信封被打开. HDDT组方案为艾司奥美拉唑镁肠溶胶囊(正大天晴, 中国)20 mg qid, 阿莫西林胶囊(华北制药, 中国)750 mg qid, 疗程14 d; 按照《第五次全国幽门螺杆菌感染处理共识报告》[8]建议方案, BQT组方案为艾司奥美拉唑镁肠溶胶囊(正大天睛, 中国)20 mg bid, 枸橼酸铋钾胶囊(苏州东瑞制药, 中国)220 mg bid, 阿莫西林胶囊(华北制药, 中国)1000 mg bid和呋喃唑酮(河北天成药业, 中国)100 mg bid, 疗程14 d. 治疗后第7天、14天以及治疗结束复查H. pylori时, 由专人通过微信或电话与患者保持沟通, 收集治疗相关信息. 治疗结束后4 wk-8 wk复查13C-尿素呼气试验(UBT).
主要观察指标为H. pylori根除率. 次要观察指标为患者的不良事件(adverse events, AE)以及治疗的依从性. AE是指患者用药过程中出现与药物相关的不良反应包括腹胀、大便干结、过敏、恶心、呕吐、腹痛及其它事件[4,9]. 依从性则是通过服用药物数量来监测, 按照既定方案服用药物数量超过80%的患者认为依从性良好, 反之认为依从性差[4].
样本量针对以下参数进行估算: 既往研究显示BQT组的H. pylori根除率为88%[10]. 假设HDDT组根除率不劣于BQT组, 据此假定HDDT组根除率至少达到87%, 界值为-10%, α值为0.025, 功效为80%. 由PASS 15软件计算所需样本量为284例(按1:1分组, 每组142例)纳入试验, 考虑到可能存在10%左右的样本量丢失, 预计每组需要158例患者入组.
统计学处理 所有数据使用SPSS 25.0进行统计分析. 分类数据以患者数量和百分比表示, 而连续数据以mean±SD表示. 使用χ2和配对检验, P<0.05有统计学意义. 所有入组受试者采用意向治疗(intension to treat, ITT)分析进行根除率分析, 服用药物后完成/未完成13C-UBT或14C-UBT复查的患者, 使用改良ITT(modified ITT, MITT)分析进行根除率分析; 服用药物后完成13C-UBT或14C-UBT复查的患者, 采用符合方案(per-protocol, PP)分析进行根除率分析.
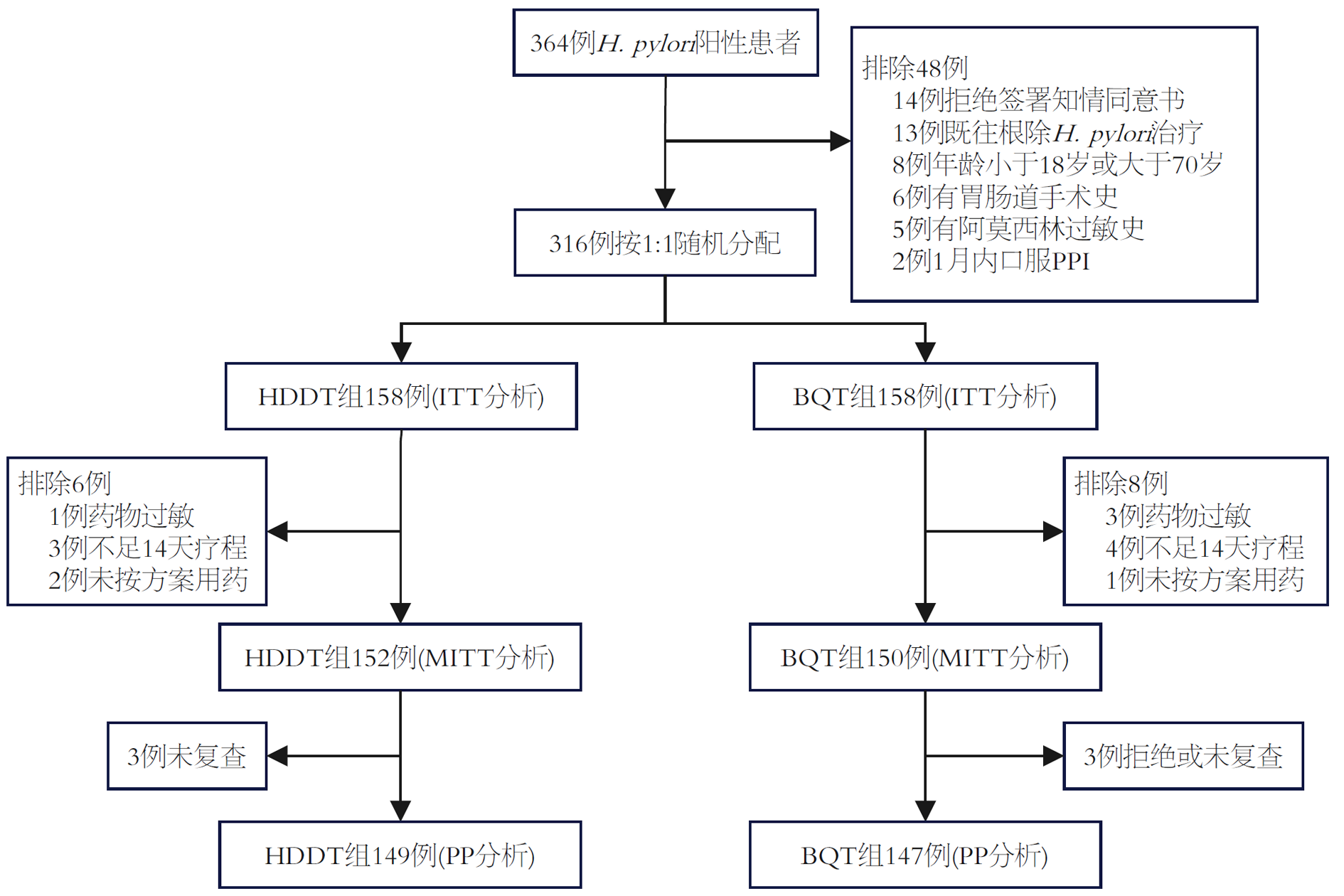
2022-03/2023-08期间共收集364例H. pylori阳性初治患者, 其中48例被排除, 最终316例患者纳入ITT分析(见图1). 两组患者基线资料见表1, 患者年龄、性别等组间比较未见统计学差异.
| HDDT组(n = 158) | BQT组(n = 158) | P值 | |
| 年龄(岁) | 47.4±12.3 | 47.3±16.4 | 0.99 |
| 性别(男) | 90 | 86 | 0.65 |
| 身高(cm) | 164.22±7.5 | 164.81±7.3 | 0.47 |
| 体重(kg) | 63.1±12.3 | 63.3±10.6 | 0.69 |
如表2所示, ITT分析显示HDDT组与BQT组H. pylori根除率分别为88.0%和87.3%, MITT分析显示两组H. pylori根除率分别为91.4%和92.0%, PP分析显示两组H. pylori根除率分别为93.3%和93.9%, 组间比较均无统计学差异.
| HDDT组 | BQT组 | P值 | |
| ITT分析 | 139/158(88.0%) | 138/158(87.3%) | 0.864 |
| 95%CI | 82.8-93.1 | 82.1-92.6 | |
| MITT分析 | 139/152(91.4%) | 138/150(92.0%) | 0.862 |
| 95%CI | 87.0-95.9 | 87.6-96.4 | |
| PP分析 | 139/149(93.3%) | 138/147(93.9%) | 0.836 |
| 95%CI | 89.2-97.4 | 90.0-97.8 |
两组患者在根除H. pylori过程中出现的腹胀、大便干结、过敏、恶心、呕吐、腹痛及其它不良事件见表3, 均为轻症, 治疗结束后可自行缓解, 未见严重的不良事件. HDDT组总体不良事件发生率明显低于BQT组(17.1% vs 32.9%, P = 0.001). 其中, HDDT组恶心、呕吐发生率明显低于BQT组(4.4% vs 10.1%, P = 0.047), 而其它不良事件发生率两组间并无统计学差异.
依从性分析显示, HDDT组有6例退出(药物过敏1例、疗程未满14 d 3例、未按照规定方案用药2例), 而BQT组有8例退出(过敏3例、疗程未满14 d 4例、未按照规定方案用药1例), 两组间患者依从性比较无统计学差异(96.2% vs 94.9%, χ2 = 0.299).
在这项单中心前瞻性研究中, 我们比较了14 d HDDT与标准14 d BQT作为一线幽门螺杆菌治疗的有效性和安全性. PP分析显示HDDT疗法的根除率达到93.3%, 与文献报道的合资或进口药物疗效(90.8%-94.5%)相似[11,12], 在ITT、mITT和PP分析中, 其H. pylori根除率与BQT疗法亦无统计学差异. 此外, 两组不良事件发生率比较, HDDT组明显低于BQT组(17.1% vs 32.9%, P = 0.001), 尤其是在恶心、呕吐方面(4.4% vs 10.1%, P = 0.047). 两种方案均具有良好的依从性 (96.2% vs 94.9%).
与BQT相比, HDDT具有一定的优势. 首先, H. pylori治疗方案的成本效益是患者考虑的关键因素, 本研究两组均使用国家集采药物, 然而HDDT方案所需药物种类少, 医疗费用亦低, HDDT方案的平均费用为198.1元/例, 而BQT方案为306.3元/例, 每例费用减少了35.3%. 较文献报道的基于非集采药物的HDDT方案费用明显降低(348.6元/例)[11,13]. 其次, 阿莫西林具有众所周知的优点, 如高适用性、耐药性低, 同时对肠道菌群的影响较小[14]. 在高耐药地区, 阿莫西林750 mg qid呈现出更好的疗效及安全性[14,15]. 另外, 高剂量PPI存在更强、更持久的酸抑制作用, 通过降低最小抑菌浓度、增加化学稳定性和提高胃液中抗生素的浓度, 增强了抗生素的作用[16,17].
目前BQT治疗疗程指南大多推荐14 d[18,19]. 对于HDDT, Zullo等[20]证实埃索美拉唑+阿莫西林的10 d治疗组可以达到较高的H. pylori根除率(接近90%), 但作者仍建议14 d疗程可能更为有效, 尤其是在耐药性高的个体中. Zhang等[7]一项前瞻性随机对照研究比较10 d和14 d疗程的H. pylori根除率, 显示两组间根除率无显著差异, 但10 d治疗组的根除率略低于14 d治疗组(79.8% vs 83.5%). 近期一项倾向评分匹配分析进一步显示HDDT 14 d疗程组的H. pylori根除率高于10 d组(92.9% vs 80.0%)[21]. 因此, 我们选择了14 d疗程的治疗方案, 本研究ITT分析结果亦显示基于国家集采药物的14 d HDDT具有良好的H. pylori根除疗效(88.0%).
本项研究也存在一些不足之处: (1)本试验为单中心研究, 需要扩大样本量及研究单位, 进一步明确该方案的适用性; (2)本研究没有检测CYP2C19基因多态性、H. pylori抗生素敏感性测试以及胃内pH值在根除治疗期间的变化, 未来还需要评估进一步其在根除治疗中的影响; (3)由于本研究主要观察H. pylori根除率, 并未分析H. pylori根除前后症状改善情况.
总之, 本研究表明基于国家集采药物的高剂量二联疗法与含铋剂四联疗法根除H. pylori均可获得满意的疗效, 其中, 高剂量二联疗法的不良事件发生率更低, 是临床值得选择的治疗方案.
随着幽门螺杆菌(Helicobacter pylori, H. pylori)对克拉霉素、甲硝唑及左氧氟沙星等抗生素的耐药性增加, 含铋剂四联疗法(Bismuth-containing quadruple therapy, BQT)的H. pylori根除率下降, 而高剂量二联疗法(high-dose dual therapy, HDDT)可达到满意效果, 但大多为合资或进口药物, 基于国产集采药物的相关研究较少.
本研究旨在探讨基于国产集采药物高剂量二联疗法的疗效及安全性, 并初步明确其在根除H. pylori中的价值, 为H. pylori感染患者提供高效、价㾾的治疗方案.
本研究主要观察目标是国产集采药物HDDT根除H. pylori的疗效, 次要观察目标是其安全性及依从性, 可以发现国产集采药物HDDT的H. pylori根除率比较理想, 未发现严重不良反应, 且患者依从性良好.
本研究为前瞻性、随机对照临床实验, 将HDDT和BQT进行对比, 分别观察其H. pylori根除率、安全性及依从性, 分别采用意向治疗(intension to treat, ITT)分析、改良ITT(modified ITT, MITT)分析、符合方案(per-protocol, PP)分析进行H. pylori根除率分析, 并采用χ2检验分析对比两者的疗效、安全性及依从性.
HDDT的H. pylori根除率不劣于BQT, 其ITT、MITT、PP分析的H. pylori根除率分别达88.0%、91.4%、93.3%, 且不良反应低、依从性好.
HDDT的H. pylori根除率不低于BQT的H. pylori根除率, 且其不良事件发生率更低, 是临床值得选择的治疗方案.
本研究为单中心临床试验, 其样本存在区域性限制, 同时样本量相对偏少, 需进一步扩大样本量,并进行多中心研究, 进一步证实其疗效.
学科分类: 胃肠病学和肝病学
手稿来源地: 江西省
同行评议报告学术质量分类
A级 (优秀): A
B级 (非常好): 0
C级 (良好): C
D级 (一般): D
E级 (差): 0
科学编辑: 张砚梁 制作编辑:张砚梁
| 1. | Chen YC, Malfertheiner P, Yu HT, Kuo CL, Chang YY, Meng FT, Wu YX, Hsiao JL, Chen MJ, Lin KP, Wu CY, Lin JT, O'Morain C, Megraud F, Lee WC, El-Omar EM, Wu MS, Liou JM. Global Prevalence of Helicobacter pylori Infection and Incidence of Gastric Cancer Between 1980 and 2022. Gastroenterology. 2024;166:605-619. [PubMed] [DOI] |
| 2. | Liu WZ, Xie Y, Lu H, Cheng H, Zeng ZR, Zhou LY, Chen Y, Wang JB, Du YQ, Lu NH; Chinese Society of Gastroenterology, Chinese Study Group on Helicobacter pylori and Peptic Ulcer. Fifth Chinese National Consensus Report on the management of Helicobacter pylori infection. Helicobacter. 2018;23:e12475. [PubMed] [DOI] |
| 3. | Wang B, Lv ZF, Wang YH, Wang H, Liu XQ, Xie Y, Zhou XJ. Standard triple therapy for Helicobacter pylori infection in China: a meta-analysis. World J Gastroenterol. 2014;20:14973-14985. [PubMed] [DOI] |
| 4. | Bi H, Chen X, Chen Y, Zhao X, Wang S, Wang J, Lyu T, Han S, Lin T, Li M, Yuan D, Liu J, Shi Y. Efficacy and safety of high-dose esomeprazole-amoxicillin dual therapy for Helicobacter pylori rescue treatment: a multicenter, prospective, randomized, controlled trial. Chin Med J (Engl). 2022;135:1707-1715. [PubMed] [DOI] |
| 5. | Cao Y, Zhang J, Liu Y, Zhang L, Wang L, Wang J, Qi Y, Lv H, Liu J, Huo L, Wei X, Shi Y. The efficacy and safety of different bismuth agents in Helicobacter pylori first-line eradication: A multicenter, randomized, controlled clinical trial. Medicine (Baltimore). 2021;100:e27923. [PubMed] [DOI] |
| 6. | Zhu YJ, Zhang Y, Wang TY, Zhao JT, Zhao Z, Zhu JR, Lan CH. High dose PPI-amoxicillin dual therapy for the treatment of Helicobacter pylori infection: a systematic review with meta-analysis. Therap Adv Gastroenterol. 2020;13:1756284820937115. [PubMed] [DOI] |
| 7. | Zhang Y, Zhu YJ, Zhao Z, Zhao JT, Wang TY, Yang J, Chen DF, Lan CH. Efficacy of modified esomeprazole-amoxicillin dual therapies for Helicobacter pylori infection: an open-label, randomized trial. Eur J Gastroenterol Hepatol. 2020;32:563-568. [PubMed] [DOI] |
| 9. | Yu L, Luo L, Long X, Liang X, Ji Y, Graham DY, Lu H. High-dose PPI-amoxicillin dual therapy with or without bismuth for first-line Helicobacter pylori therapy: A randomized trial. Helicobacter. 2019;24:e12596. [PubMed] [DOI] |
| 10. | Song Z, Zhou L, Xue Y, Suo B, Tian X, Niu Z. A comparative study of 14-day dual therapy (esomeprazole and amoxicillin four times daily) and triple plus bismuth therapy for first-line Helicobacter pylori infection eradication: A randomized trial. Helicobacter. 2020;25:e12762. [PubMed] [DOI] |
| 11. | Peng X, Yao JY, Ma YQ, Li GH, Chen HW, Wan Y, Liang DS, Zhang M, Zhi M. Efficacy and Safety of Vonoprazan-Amoxicillin Dual Regimen With Varying Dose and Duration for Helicobacter pylori Eradication: A Multicenter, Prospective, Randomized Study. Clin Gastroenterol Hepatol. 2024;22:1210-1216. [PubMed] [DOI] |
| 12. | Yan TL, Wang JH, He XJ, Zhu YB, Lu LJ, Wang YJ, Wang ZW, Gao JG, Xu CF, Ma H, Luan SM, Li L, Chen Y. Ten-Day Vonoprazan-Amoxicillin Dual Therapy vs Standard 14-Day Bismuth-Based Quadruple Therapy for First-Line Helicobacter pylori Eradication: A Multicenter Randomized Clinical Trial. Am J Gastroenterol. 2024;119:655-661. [PubMed] [DOI] |
| 13. | Liu Z, Chen X, Sun DJ, Zhao WW, Kou L, Zheng WW, Hao JR, Gao FY. Comparison of vonoprazan-based dual therapy with vonoprazan-based bismuth quadruple therapy for treatment-naive patients with Helicobacter pylori infection: A propensity score matching analysis. Medicine (Baltimore). 2024;103:e37476. [PubMed] [DOI] |
| 14. | Hu Y, Xu X, Ouyang YB, He C, Li NS, Xie C, Peng C, Zhu ZH, Shu X, Xie Y, Lu NH, Zhu Y. Altered Gut Microbiota and Short-Chain Fatty Acids After Vonoprazan-Amoxicillin Dual Therapy for Helicobacter pylori Eradication. Front Cell Infect Microbiol. 2022;12:881968. [PubMed] [DOI] |
| 15. | Yeh JA, Huang HK, Chou AL, Lin HJ, Feng CL, Kuo CJ, Lai CH. Helicobacter pylori eradication with high-dose proton pump inhibitor-amoxicillin dual therapy: A systematic review and meta-analysis. Int J Antimicrob Agents. 2024;63:107159. [PubMed] [DOI] |
| 16. | Scarpignato C, Howden CW, Leifke E, Mulford DJ, Lahu G, Facius A, Hunt R. A translational pharmacokinetic/pharmacodynamic approach supports optimal vonoprazan dosing for erosive oesophagitis and Helicobacter pylori infection. Aliment Pharmacol Ther. 2023;58:16-25. [PubMed] [DOI] |
| 17. | Kiyotoki S, Nishikawa J, Sakaida I. Efficacy of Vonoprazan for Helicobacter pylori Eradication. Intern Med. 2020;59:153-161. [PubMed] [DOI] |
| 19. | Malfertheiner P, Megraud F, O'Morain CA, Gisbert JP, Kuipers EJ, Axon AT, Bazzoli F, Gasbarrini A, Atherton J, Graham DY, Hunt R, Moayyedi P, Rokkas T, Rugge M, Selgrad M, Suerbaum S, Sugano K, El-Omar EM; European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017;66:6-30. [PubMed] [DOI] |
| 20. | Zullo A, Ridola L, Francesco VD, Gatta L, Hassan C, Alvaro D, Bellesia A, de Nucci G, Manes G. High-dose esomeprazole and amoxicillin dual therapy for first-line Helicobacter pylori eradication: a proof of concept study. Ann Gastroenterol. 2015;28:448-451. [PubMed] |
| 21. | Zou PY, Hu J, Zhao JT, Zhao Z, Mei H, Yang J, Zhu YJ, Zhang Y, Lan CH. 10-Day and 14-day high-dose dual therapy for the treatment of Helicobacter pylori: A propensity score matching analysis. Helicobacter. 2021;26:e12833. [PubMed] [DOI] |