修回日期: 2021-10-22
接受日期: 2021-12-20
在线出版日期: 2022-01-08
自身免疫性肝炎(autoimmune hepatitis, AIH)和原发性胆汁性胆管炎(primary biliary cholangitis, PBC)的AIH-PBC重叠综合征在肝病中并非少见, 同时合并进行性家族性肝内胆汁淤积症则较为罕见, 通常容易造成漏诊.
本例患者因为肝功能异常伴黄疸11年均未能明确诊断. 在本院住院期间, AIH-PBC重叠综合征获得确诊. 在接受正规治疗后, 效果欠佳. 给与遗传性肝病基因检测, 发现ABCB4基因突变, 提示患者同时合并进行性家族性肝内胆汁淤积症3型(progressive familial intrahepatic cholestasis type 3, PFIC3). 2020年和2021年, 患者先后因为"上消化道出血"又2次入住我院, 病情呈现不断加重的趋势.
对于1例久未获得确诊的肝病患者, 通过生化学、血清学、影像学、组织学等检查, 明确了AIH-PBC重叠综合征的诊断. 但本病例由于脾脏明显肿大, 似不能完全以AIH-PBC重叠综合征加以解释, 因此对患者进行了遗传性肝病相关的基因检测, 发现了ABCB4基因突变, 避免了PFIC3的漏诊.
核心提要: 对于肝细胞酶和胆系酶反复升高的患者, 在排除其他肝胆疾病以外, 诊断要考虑自身免疫性肝炎(autoimmune hepatitis, AIH)和原发性胆汁性胆管炎(primary biliary cholangitis, PBC)的AIH-PBC重叠综合征. 但对于免疫抑制剂联合熊去氧胆酸治疗效果不佳, 黄疸不退, 脾脏肿大明显的患者, 要考虑合并遗传性肝内胆汁淤积性肝病.
引文著录: 王月, 王银玲, 朱月萍, 许炜璐, 黄金龙, 柴晓哲, 李明, 钱峰, 朱传武. 进行性家族性肝内胆汁淤积症3型合并AIH-PBC重叠综合征1例. 世界华人消化杂志 2022; 30(1): 56-60
Revised: October 22, 2021
Accepted: December 20, 2021
Published online: January 8, 2022
Autoimmune hepatitis-primary biliary cholangitis (AIH-PBC) overlap syndrome is not uncommon in autoimmune liver disease, but autoimmune liver disease combined with progressive familial intrahepatic cholestasis is relatively rare, which usually makes the diagnosis more complicated and difficult, and thus easily leads to a missed diagnosis and misdiagnosis.
A 32-year-old woman complained of "abnormal liver function and jaundice for 11 years", and was first admitted to our hospital in 2019. She visited different hospitals previously and could not achieve a clear diagnosis. During her first hospitalization in our hospital, a diagnosis of AIH-PBC overlap syndrome was made by the indicators of liver function enzymology, levels of IgG and IgM, autoantibodies related to liver disease, and the pathology of liver biopsy. The patient received the treatment of ursodeoxycholic acid plus glucocorticoid, and her liver function improved but the overall effects were suboptimal. Due to the patient's significantly enlarged spleen unexplained by AIH-PBC overlap syndrome, she was advised to undergo gene sequencing for the detection of potential genetic liver diseases. The findings showed heterozygous deletion mutations in the ABCB4 gene, suggesting that the patient had type 3 progressive familial intrahepatic cholestasis (PFIC3). In 2020 and 2021, the patient was twice admitted to our hospital because of upper gastrointestinal bleeding.
A clear diagnosis of AIH-PBC overlap syndrome was first made for the patient whose liver disease could not be clearly diagnosed for a long time. Due to the apparent splenomegaly not explained satisfactorily by AIH-PBC overlap syndrome, gene sequencing was permormed, which revealed the presence of ABCB4 gene mutations, resulting in a final diagnosis of PFIC3.
- Citation: Wang Y, Wang YL, Zhu YP, Xu WL, Huang JL, Chai XZ, Li M, Qian F, Zhu CW. Type 3 progressive familial intrahepatic cholestasis combined with autoimmune hepatitis-primary biliary cirrhosis overlap syndrome: A case report. Shijie Huaren Xiaohua Zazhi 2022; 30(1): 56-60
- URL: https://www.wjgnet.com/1009-3079/full/v30/i1/56.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v30.i1.56
自身免疫性肝病包括自身免疫性肝炎(autoimmune hepatitis, AIH)、原发性胆汁性胆管炎(primary biliary cholangitis, PBC)、原发性硬化性胆管炎(primary sclerosing cholangitis, PSC)等. 如兼有AIH、PBC或PSC特征者称为重叠综合征, 其中以AIH-PBC重叠综合征最为多见. 自身免疫性肝病起病隐匿, 就诊时往往进展至肝硬化, 治疗不及时可短时间内进展至肝功能衰竭[1,2]. 进行性家族性肝内胆汁淤积症3型(progressive familial intrahepatic cholestasis type 3, PFIC3)是由于基因突变所致的一种遗传性肝病, 可引起严重的肝内胆汁淤积, 临床预后不良. 现将我院收治的1例PFIC3合并AIH-PBC重叠综合征患者的资料报道如下.
患者, 女, 32岁. 2年前因"肝功能异常伴黄疸11年, 加重1月"于2019-07-15首次收住我院感染病科. 患者于2008年体检发现肝功能异常, 当地医院给与"护肝、降酶"等药物治疗, 肝功能异常有所改善. 期间2次怀孕, 均伴有肝功能异常, 当地医院诊断为"妊娠期肝内胆汁淤积症(intrahepatic cholestasis of pregnancy, ICP)", 予对症治疗, 分娩后肝功能未恢复正常. 2014-03-26复查肝功能: 总胆红素(total bilirubin, Tbil) 26 μmol/L、直接胆红素(direct bilirubin, Dbil) 15.8 μmol/L、谷丙转氨酶(alanine aminotransferase, ALT) 255 U/L、谷草转氨酶(aspartate aminotransferase, AST) 212 U/L、碱性磷酸酶(alkaline phosphatase, ALP) 896 U/L、谷氨酰转肽酶(glutamyl transpeptidase, GGT) 605 U/L; B超示肝内钙化灶, 脾脏172 mm × 40 mm, 间断口服保肝药物治疗.
入院前于2019-06-28在门诊检查肝功能: Tbil 190.4 μmol/L、Dbil 101.1 μmol/L、ALT 118 U/L、AST 114 U/L、ALP 382 U/L、GGT 626 U/L、白蛋白43.0 g/L、球蛋白35.9 g/L; 免疫球蛋白G(immunoglobulin G, IgG) 17.4 g/L、免疫球蛋白M(immunoglobulin M, IgM) 3.12 g/L; 甲乙丙丁戊型病毒性肝炎血清学标志物均阴性; 自身免疫性肝病抗体: 抗核抗体(antinuclear antibody, ANA)阳性、抗线粒体抗体(anti-mitochondrial antibody, AMA)等其他自身抗体均为阴性. 入院查体: 神志清, 精神疲软, 面色晦暗, 肝掌阳性, 未见蜘蛛痣, 皮肤巩膜中度黄染. 腹平软, 未见腹壁静脉显露, 肝肋下未及, 剑突下5 cm, 质地中等, 无触痛. 脾脏肿大, 下缘平脐, 右侧超过腹中线, 质地中等, 无触痛. Murphy's征阴性, 全腹无压痛及反跳痛, 移动性浊音阴性, 无肝区叩击痛, 双下肢无凹陷性水肿.否认慢性病史及传染病史, 无吸烟及饮酒史. 已婚, 育有2子, 子女及父母体健.
入院后化验及检查: 肝功能: Tbil 139 μmol/L、Dbil 74.8 μmol/L、ALT 123 U/L、AST 127 U/L、ALP 291 U/L 、GGT 512 U/L、白蛋白37.9 g/L、球蛋白32.9 g/L; 血常规: 白细胞3.0×109/L、红细胞3.23×1012/L、血红蛋白103 g/L、血小板85×109/L; IgG 13.4 g/L、IgM 2.65 g/L; EB病毒、巨细胞病毒抗体、弓形虫抗体、HIV抗体、梅毒抗体均阴性; 凝血功能、甲状腺功能、肿瘤指标均未见异常; α1-酸性糖蛋白、铜蓝蛋白均正常; 自身免疫性肝病抗体: ANA阳性、抗核点型抗体阴性、抗核糖核蛋白抗体阴性、AMA-M2阴性、抗SP-100抗体和抗GP210抗体均阴性, IgG4阴性; 无创肝纤维化检测: LSM 12.6 kPa, CAP 198 db/mL. 腹部B超: 肝损害声像图, 肝内增强回声(结石?钙化灶?), 门静脉内径10 mm, 脾静脉内径8 mm; 胆囊轻中度炎性改变; 脾肿大.
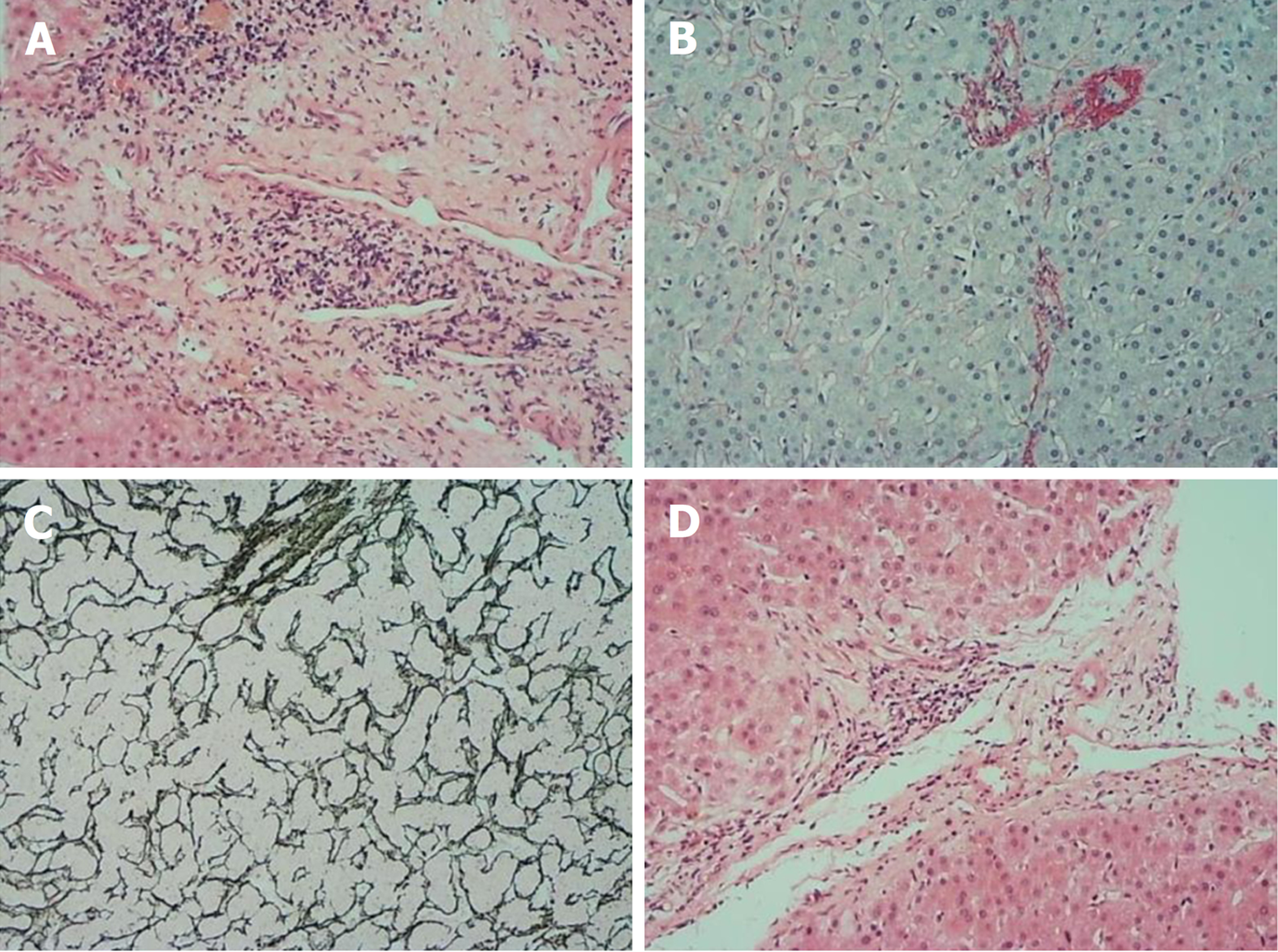
入院后初步诊断考虑为AIH-PBC重叠综合征可能, 给予熊去氧胆酸、甘草酸制剂等药物治疗, 同时进一步给予检查. 2019-07-22肝穿刺活检, 病理结果提示: 轻中度界面炎, 汇管区局部桥接坏死, 汇管区及纤维隔内有较多淋巴细胞、少量浆细胞浸润, 可见小胆管损伤, 部分汇管区与小动脉伴行的小胆管减少或消失; 肝细胞轻度水肿, 少许气球样变及脂肪变性, 可见点状坏死, 玫瑰花结样肝细胞, 汇管区周围肝细胞内见淤胆性色素颗粒. 结论: 符合原发性胆汁性胆管炎叠加自身免疫性肝炎(PBC+AIH), 改良Scheuer评分: G3S3(见图1).
2019-07-28腹部磁共振成像(magnetic resonance imaging, MRI)和磁共振胰胆管造影(magnetic resonance cholangiopancreatography, MRCP)提示: (1)脾脏肿大; (2)肝脏形态异常, 考虑肝硬化可能;(3)右肝管及部分分支显影不清, 肝左叶远端部分肝内胆管略显扩张; (4)肝脏多发小囊肿; (5)胆汁粘稠.
综合病史及入院后检查以及肝穿刺病理结果, AIH综合诊断积分系统评分为19分, 简化诊断标准评分为7分, AIH可以确诊; ALP和GGT显著增高, IgM水平增高, 肝组织学显示小胆管损伤、部分汇管区小胆管减少或消失, PBC诊断明确. 因此, 患者诊断为AIH-PBC重叠综合征. 遂予"泼尼松20 mg qd, 熊去氧胆酸(ursodeoxycholic acid, UDCA)250 mg tid"联合治疗. 治疗期间复查血生化指标, ALT、AST、ALP及GGT等有所下降, 但均未恢复正常; Tbil无明显下降, 维持在(100-160) μmol/L之间; IgG恢复正常, IgM 2.65 g/L, 仍高于正常值上限.
由于患者脾脏肿大明显, 显著异于常见的AIH-PBC重叠综合征患者, 且患者也无疟疾、伤寒、血液系统疾病及心血管疾病史, 因此, 于2019-08-05建议患者做黄疸相关的基因检测. 基因测序高通量检测结果提示: ABCB4基因存在大片段杂合缺失突变, 见图2.
患者给予"甲泼尼龙片联合UDCA"治疗, 于2019-08-10带药出院. 结合患者病史、临床症状和体征、相关实验室及影像学检查、黄疸相关基因测序结果及诊疗经过, 出院诊断为: (1)PFIC3合并AIH-PBC重叠综合征; (2)肝硬化(代偿期). 出院时肝脏Child-Pugh评分6分, 对疾病发展的不良预后也对患者和家属做了交代. 考虑此疾病为常染色体隐性遗传性疾病, 建议其直系亲属完善相关基因检测, 同时建议患者早做肝移植准备, 患者因经济原因暂缓.
2020-04-21患者因"上消化道出血"第二次收住我院肝病科. 呕血2次, 鲜红色, 量约300 mL. 期间检查肝功能: Tbil 63 μmol/L、Dbil 53.9 μmol/L、ALT 36 U/L、AST 79 U/L、ALP 267 U/L 、GGT 446 U/L、白蛋白30.0 g/L、球蛋白34.8 g/L; 凝血功能: 凝血酶原时间(prothrombin time, PT)14.8秒, 凝血酶原活动度(prothrombin activity, PTA) 64.8%; 血常规: 白细胞6.83×109/L、红细胞2.18×1012/L、血红蛋白51 g/L、血小板117×109/L; IgG 15.6 g/L、IgM 2.08 g/L; 甲胎蛋白(alpha-fetoprotein, AFP)正常; 自身免疫性肝病抗体: ANA阳性、AMA-M2阳性、抗SP-100抗体和抗GP210抗体均阴性. 经过止血、输血、抑酸护胃、补充白蛋白等治疗, 出血控制, 病情好转. 因处于新冠肺炎疫情期间, 胃镜检查未开放, 故未行胃镜检查, 于2020-05-01带药出院, 嘱咐定期随访. 出院诊断为: (1)PFIC3合并AIH-PBC重叠综合征; (2)肝硬化(失代偿期); (3)上消化道出血.
2021-06-04患者因再次呕血第三次住院, 消化科给与内镜下精细精准食管胃底静脉曲张断流术(endoscopic selective variceal devascularization, ESVD)止血治疗, 镜下见食管静脉重度曲张并破裂出血. 入院后检查肝功能: Tbil 218.0 μmol/L、Dbil 176.8 μmol/L、ALT 29 U/L、AST 58 U/L、ALP 121 U/L 、GGT 70 U/L、白蛋白26.3 g/L、球蛋白31.8 g/L; 凝血功能: 凝血酶原时间19.1秒, 凝血酶原活动度 42.9%; 血常规: 白细胞6.91×109/L、红细胞2.93×1012/L、血红蛋白94 g/L、血小板136×109/L; IgG 18.7 g/L、IgM 2.88 g/L; 血氨38 μmol/L; AFP正常, CA125 232.2 U/mL; 腹水常规提示为漏出液, 培养无细菌生长. 腹部B超示肝硬化、脾肿大、门静脉内径10 mm, 脾静脉内径9 mm, 腹腔积液. 经止血、补充白蛋白、利尿等治疗, 出血停止、腹水消退, 于2021-07-09出院. 2021-08-11随访, 肝功能: Tbil 487.4 μmol/L、Dbil 367.9 μmol/L、ALT 131 U/L、AST 171 U/L、ALP 97 U/L 、GGT 63 U/L、白蛋白31.8 g/L、球蛋白33.6 g/L; 凝血功能: 凝血酶原时间 15.3秒, 凝血酶原活动度60.1%; 血常规: 白细胞11.82×109/L、红细胞3.38×1012/L、血红蛋白113 g/L、血小板73×109/L. 患者病情的逐步进展也使其认识到肝移植为最终治疗方案, 目前在当地医院住院, 等待行肝移植治疗.
AIH表现为血清IgG水平升高, ANA或抗平滑肌抗体(anti-smooth muscle antibody, ASMA)高滴度阳性, 组织学特征为肝实质细胞炎症, 胆管损害较轻[3,4]. PBC是一种自身免疫介导的、针对胆管上皮细胞的自身免疫性肝病, 其病理损害特征是小叶间胆管非化脓性破坏性胆管炎, 亚临床期可长达10-15年, 但在出现临床症状后可迅速进展至胆汁淤积、肝硬化和肝功能衰竭[5]. AIH-PBC重叠综合征占所有PBC患者的5%-15%, 兼有AIH和PBC的血清生化学特征, 主要包括血清ALT、AST、ALP、GGT升高, 同时伴有IgG、IgM水平不同程度的升高; 自身抗体中多出现ANA、ASMA、AMA或抗SP-100、抗GP210抗体阳性.
本例患者有反复肝功能异常史10余年, 曾在多家医院就诊, 筛查临床常见的病毒性肝炎血清学指标、自身免疫性肝病相关抗体等, 均未见明显异常, 故一直未能明确诊断. 在本院首次住院期间, 检查肝功能酶学指标、IgG和IgM水平、肝病相关自身抗体, 并结合肝穿刺病理学检查, 患者的诊断符合AIH-PBC重叠综合征的诊断标准. 关于AMA-M2, 患者首次住院前和住院期间检查均为阴性, 但在第二次住院期间复查AMA-M2为阳性, 说明在高度怀疑自身免疫性肝病时, 相关自身抗体的检测需要多次复查, 有时最好应用不同的检测试剂复查.在确诊后, 给与患者糖皮质激素联合熊去氧胆酸治疗, 肝功能指标有所改善, 但总体效果欠佳. 特别是患者脾脏显著肿大, 显著异于常见的AIH-PBC重叠综合征患者. 因此, 为了解是否存在其他黄疸相关的肝病, 进一步完善了血清IgG4检测以及遗传代谢性肝病的基因测序. 结果发现ABCB4基因存在大片段杂合缺失突变, 提示患者同时合并遗传性胆汁淤积性肝病.
PFIC是一组常染色体隐性遗传性疾病, 其特征是由于胆汁合成和运输障碍引起的肝内胆汁淤积[6,7], 多发生在婴幼儿时期, 少部分类型可于成年后出现肝硬化.根据已知的致病基因, PFIC分为3型. PFIC3的特征是ABCB4基因发生突变, 导致其编码的多药耐药蛋白3(multidrug resistance protein 3, MDR3)缺失, 使胆汁磷脂酰胆碱分泌所需要的脂肪酶缺乏或功能异常[8,9]. MDR3蛋白是肝细胞毛细胆管面上的磷脂转运酶, 负责将磷脂从肝细胞内转运至毛细胆管面, 在胆管中与胆盐混合形成微粒排泌至胆汁中. ABCB4基因突变导致MDR3蛋白表达下降或缺失, 引起胆汁中磷脂比例降低或缺乏, 不能形成磷脂与胆盐的混合微粒, 造成胆盐游离, 对胆管细胞和肝细胞发生毒性去垢作用.持续的细胞损伤及炎症因子浸润最终导致胆汁淤积、小胆管增生、广泛门管区纤维化和肝硬化, 最后发展为终末期肝病[10]. PFIC1型和2型分别由ATP8B1和ABCB11基因突变引起, PFIC3型由ABCB4基因突变引起. PFIC3型区别于1型和2型的临床特征是血清GGT水平升高, 本病例符合PFIC3型的诊断标准, 但是因为合并有AIH-PBC重叠综合征, 使得病情更为复杂, 也更为少见.
本病例是由于血清胆红素、ALT、AST、ALP和GGT水平长期异常, 影像学显示肝内外胆管通畅, 经过自身免疫性肝病相关抗体检测, 以及肝组织活检病理学检查, 首先确诊了AIH-PBC重叠综合征.但是在糖皮质激素联合UDCA治疗下, 肝功能指标改善并不显著, 并且患者的脾脏显著肿大也不能完全以AIH-PBC重叠综合征的诊断得到合理解释, 因此, 考虑是否合并有引起肝内胆汁淤积的其他肝病存在, 比如PFIC或者良性复发性肝内胆汁淤积症(benign recurrent intrahepatic cholestasis, BRIC)等. 通过基因测序检查, 确认患者同时合并PFIC3. 目前报道的ABCB4基因突变有很多种, 包括错义、无义及缺失突变等, 基因突变的类型与病情严重程度有关, 严重者在儿童早期即可发展为肝功能衰竭. 另外, ABCB4基因突变也可引起诸如ICP、胆石症、PBC、药物性肝内胆汁淤积症等疾病. 本例患者在首次入院的诊治过程中, 各项检查支持AIH、PBC和PFIC3各自的诊断标准, 因此, PFIC3合并AIH-PBC重叠综合征是明确的. 从随后的病情演变看, 肝病进展较快, 肝移植治疗是最后的治疗手段.
目前, 综合利用生化学、血清学、影像学、组织学、基因学等方法, 能够让绝大多数病因不明的肝病患者获得确诊. 但是, 类似于本例因为肝功能反复异常, 辗转就医, 且疗效不佳, 病情进展而久未获得确诊的疑难复杂性肝病在临床上也并不鲜见. AIH-PBC重叠综合征诊断相对容易, 糖皮质激素等免疫抑制剂联合UDCA治疗对大多数患者是有效的, 但对于少数治疗效果不佳的成人胆汁淤积性肝病, 要考虑到合并PFIC3等遗传性胆汁淤积性肝病的可能. 如果不仔细分析病情, 很容易导致漏诊. 本病例在明确AIH-PBC重叠综合征的诊断后, 再确诊了PFIC3, 虽不能为患者提供有效的治疗方案, 但有助于了解疾病发展的不良预后, 减少患者因为诊断不明而反复就医的成本, 同时也为临床医生诊治疑难性肝病提供了参考.
学科分类: 胃肠病学和肝病学
手稿来源地: 江苏省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C
D级 (一般): D
E级 (差): E
科学编辑: 张砚梁 制作编辑:张砚梁
| 2. | Aguilar-Nájera O, Velasco-Zamora JA, Torre A. Overlap syndromes of autoimmune hepatitis: diagnosis and treatment. Rev Gastroenterol Mex. 2015;80:150-159. [PubMed] [DOI] |
| 3. | Chinese Society of Hepatology, Chinese Society of Gastroenterology & Chinese Society of Infectious Diseases. Chinese consensus on the diagnosis and management of autoimmune hepatitis (2015). J Dig Dis. 2017;18:247-264. [PubMed] [DOI] |
| 4. | Wang Q, Yang F, Miao Q, Krawitt EL, Gershwin ME, Ma X. The clinical phenotypes of autoimmune hepatitis: A comprehensive review. J Autoimmun. 2016;66:98-107. [PubMed] [DOI] |
| 5. | Boberg KM, Chapman RW, Hirschfield GM, Lohse AW, Manns MP, Schrumpf E; International Autoimmune Hepatitis Group. Overlap syndromes: the International Autoimmune Hepatitis Group (IAIHG) position statement on a controversial issue. J Hepatol. 2011;54:374-385. [PubMed] [DOI] |
| 6. | Morotti RA, Suchy FJ, Magid MS. Progressive familial intrahepatic cholestasis (PFIC) type 1, 2, and 3: a review of the liver pathology findings. Semin Liver Dis. 2011;31:3-10. [PubMed] [DOI] |
| 7. | Bull LN, Thompson RJ. Progressive Familial Intrahepatic Cholestasis. Clin Liver Dis. 2018;22:657-669. [PubMed] [DOI] |
| 8. | Reichert MC, Lammert F. ABCB4 Gene Aberrations in Human Liver Disease: An Evolving Spectrum. Semin Liver Dis. 2018;38:299-307. [PubMed] [DOI] |
| 9. | van der Woerd WL, Houwen RH, van de Graaf SF. Current and future therapies for inherited cholestatic liver diseases. World J Gastroenterol. 2017;23:763-775. [PubMed] [DOI] |
| 10. | Degiorgio D, Crosignani A, Colombo C, Bordo D, Zuin M, Vassallo E, Syrén ML, Coviello DA, Battezzati PM. ABCB4 mutations in adult patients with cholestatic liver disease: impact and phenotypic expression. J Gastroenterol. 2016;51:271-280. [PubMed] [DOI] |