修回日期: 2021-04-11
接受日期: 2021-06-02
在线出版日期: 2021-07-28
幽门螺杆菌(Helicobacter pylori, H. pylori)是公认的胃癌致病因子, 慢性萎缩性胃炎(chronic atrophic gastritis, CAG)并H. pylori感染的诊治一直是临床研究重点.
探讨CAG并H. pylori, 感染患者吹气定量检测值(delta over baseline, DOB)与白介素-32(interleukin-32, IL-32)、胃泌素-17(gastrin 17, G-17)、可溶性白细胞介素-2受体(soluble interleukin 2 receptor, sIL-2R)水平及胃镜下病理变化的关系.
选取2017-01/2019-12体检中心224例CAG患者作为研究对象, 其中合并H. pylori感染患者124例作为观察组, 未合并H. pylori感染患者100例作为对照组. 观察对比两组临床资料、DOB与G-17、IL-32、sIL-2R水平, 以Logistic回归分析CAG并H. pylori感染影响因素, 并分析DOB与G-17、IL-32、sIL-2R相关性, 对比不同胃镜下病理变化患者DOB与G-17、IL-32、sIL-2R水平, 绘制ROC曲线, 评价DOB、G-17、IL-32、sIL-2R对CAG并H. pylori感染的评估价值.
两组病程、胃镜下病理变化(慢性炎症、萎缩、肠上皮化生、上皮内瘤变)相比, 差异有统计学意义(P<0.05); 观察组DOB、IL-32、sIL-2R水平高于对照组, G-17水平低于对照组, 差异有统计学意义(P<0.05); Logistic回归分析可知, 病程、慢性炎症、萎缩、肠上皮化生、上皮内瘤变、DOB、G-17、IL-32、sIL-2R水平均为CAG并H. pylori感染影响因素(P<0.05); Pearson相关性分析可知, CAG并H. pylori感染患者DOB与G-17呈负相关关系, 与IL-32、sIL-2R呈正相关关系(P<0.05); Spearman相关性分析可知, CAG并H. pylori感染患者DOB、G-17、IL-32、sIL-2R水平与慢性炎症、萎缩、肠上皮化生、上皮内瘤变有关(P<0.05); ROC曲线显示, DOB、G-17、IL-32、sIL-2R联合评估AUC最大, 为0.975>0.9, 具有较高评估价值, 最佳敏感度、特异度分别为85.48%、98.00%.
CAG并H. pylori感染患者G-17、IL-32、sIL-2R水平与DOB相关, H. pylori感染可能通过影响G-17、IL-32、sIL-2R表达, 参与CAG患者胃黏膜病理改变发生和进展, 各指标联合检测可有效预测H. pylori感染, 对临床诊治有重要意义.
核心提要: 慢性萎缩性胃炎并幽门螺杆菌(Helicobacter pylori, H. pylori)感染患者吹气定量测定值、胃泌素-17、白介素-32、可溶性白细胞介素-2受体水平与胃黏膜病理改变相关, 并可有效预测H. pylori感染.
引文著录: 倪冰颖, 鲍洛文, 黄秋菊, 吴蓓蕾, 李伟. 慢性萎缩性胃炎并幽门螺杆菌感染患者吹气定量测定值与G-17、IL-32、sIL-2R水平及胃镜下病理变化的关系. 世界华人消化杂志 2021; 29(14): 816-824
Revised: April 11, 2021
Accepted: June 2, 2021
Published online: July 28, 2021
Helicobacter pylori (H. pylori) is a recognized causative factor of gastric cancer. The diagnosis and treatment of chronic atrophic gastritis (CAG) and H. pylori infection have always been the focus of clinical research.
To investigate the relationship of the delta over baseline (DOB) and serum gastrin 17 (G-17), interleukin-32 (IL-32), soluble interleukin 2 receptor (sIL-2R) levels and gastroscopic pathological changes in patients with CAG and H. pylori infection.
A total of 224 CAG patients at the Physical Examination Center of Wenzhou Central Hospital from January 2017 to December 2019 were selected as the research subjects, including 124 patients with H. pylori infection as an observation group, and 100 patients without H. pylori infection as a control group. The clinical data, DOB, and serum levels of G-17, IL-32, and sIL-2R in the two groups were compared. Logistic regression analysis was used to identify the influencing factors of CAG and H. pylori infection, and the correlation of DOB with serum G-17, IL-32, and sIL-2R was analyzed. The levels of DOB and serum G-17, IL-32, and sIL-2R in patients with different gastroscopic pathological changes were compared, and ROC curves were drawn to evaluate the value of DOB, G-17, IL-32, and sIL-2R in assessing CAG and H. pylori infection.
There were statistically significant differences in the course of disease and gastroscopic pathological changes (chronic inflammation, atrophy, intestinal metaplasia, and intraepithelial neoplasia) between the two groups (P < 0.05). The DOB and serum levels of IL-32 and sIL-2R were significantly higher and serum G-17 level was significantly lower in the observation group than in the control group (P < 0.05). Logistic regression analysis showed that the course of disease, chronic inflammation, atrophy, intestinal metaplasia, intraepithelial neoplasia, DOB, and serum G-17, IL-32, and sIL-2R levels were all influencing factors of CAG and H. pylori infection (P < 0.05). Pearson correlation analysis showed that the DOB of patients with CAG and H. pylori infection was negatively correlated with G-17, and positively correlated with IL-32 and sIL-2R (P < 0.05). Spearman correlation analysis showed that the DOB and serum levels of G-17, IL-32, and sIL-2R in patients with CAG and H. pylori infection were significantly related to chronic inflammation, atrophy, intestinal metaplasia, and intraepithelial neoplasia (P < 0.05). ROC curve analysis showed that the area under the curve of combined DOB, G-17, IL-32, and sIL-2R was the largest (0.975), and the best sensitivity and specificity were 85.48% and 98.00%, respectively.
Serum levels of G-17, IL-32, and sIL-2R in patients with CAG and H. pylori infection are related to DOB. H. pylori infection may be involved in the occurrence and progression of gastric mucosal pathological changes in CAG patients by affecting the expression of G-17, IL-32, and sIL-2R. Combined detection of all the above indicators can effectively predict H. pylori infection, which is of great significance for clinical diagnosis and treatment.
- Citation: Ni BY, Bao LW, Huang QJ, Wu BL, Li W. Relationship of delta over baseline with serum levels of gastrin 17, interleukin-32, and soluble interleukin 2 receptor and gastroscopic pathological changes in patients with chronic atrophic gastritis and Helicobacter pylori infection. Shijie Huaren Xiaohua Zazhi 2021; 29(14): 816-824
- URL: https://www.wjgnet.com/1009-3079/full/v29/i14/816.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v29.i14.816
慢性萎缩性胃炎(chronic atrophic gastritis, CAG)是消化科常见疾病, 据统计, 我国CAG发病率约为10%-30%[1,2]. 幽门螺杆菌(Helicobacter pylori, H. pylori)感染与CAG发病相关, 研究报道, 60%-90% CAG患者胃黏膜中可培养出H. pylori, 且H. pylori是公认的胃癌致病因子[3]. 因此, 临床需对CAG并H. pylori感染患者的诊治给予充分重视. 吹气定量检测值(delta over baseline, DOB)是衡量H. pylori感染情况的常用定量指标[4]. CAG黏膜层内的慢性炎性细胞浸润为主要表现, 促炎因子白介素-32(interleukin-32, IL-32)参与胃黏膜炎症反应[5]. 胃泌素-17(gastrin 17, G-17)是评估胃功能的常用生化指标, 且可用于胃癌前病变和胃癌诊断[6]. 另研究证实, CAG发生、发展与机体免疫功能, 尤其可溶性白细胞介素-2受体(soluble interleukin 2 receptor, sIL-2R)密切相关[7]. 本研究首次分析CAG并H. pylori感染患者DOB与G-17、IL-32、sIL-2R水平及胃镜下病理变化的关系, 以指导临床治疗. 报道如下.
选取2017-01/2019-12体检中心224例CAG患者作为研究对象, 其中合并H. pylori感染患者124例作为观察组, 未合并H. pylori感染患者100例作为对照组. 纳入标准: 均符合《消化内科学高级教程》[8]中CAG诊断标准; 合并H. pylori感染患者均经13C尿素酶呼吸试验证实; 1 mo内未接受抗H. pylori治疗; 患者及家属知情同意. 排除标准: 1 mo内服用抗生素、非甾体消炎药等相关药物; 合并消化系统其他严重疾病; 心、脑等其他严重原发性疾病; 精神病史; 妊娠及哺乳期妇女. 本研究符合医学伦理学标准, 经医院伦理委员会批准.
DOB检测: 入组24 h内进行测定, 采用北京勃然制药有限公司尿素[13C]呼气试验试剂, 服药前吹一袋气, 记为0 min气体, 服药后静坐0.5 h再次吹一袋气, 吹气过程中平缓, 禁止倒吸气、憋气, 利用十通道设备对定量测定DOB. 入组24 h内采集外周静脉血5 mL, 离心(半径8 cm, 3500 r/min, 9 min), 取血清, 采用酶联免疫吸附法测定G-17、IL-32、sIL-2R, 均采用深圳晶美生物工程有限公司试剂盒.
(1)两组临床资料; (2)两组DOB、G-17、IL-32、sIL-2R水平; (3)慢性萎缩性胃炎并H. pylori感染影响因素; (4)DOB与G-17、IL-32、sIL-2R相关性; (5)不同胃镜下病理变化患者DOB、G-17、IL-32、sIL-2R水平; (6)DOB、G-17、IL-32、sIL-2R对慢性萎缩性胃炎并H. pylori感染的评估价值.
统计学处理 采用统计学软件SPSS 22.0处理数据, 计数资料以例数描述, 计量资料采取Bartlett方差齐性检验与Kolmogorov-Smirnov正态性检验, 均确认具备方差齐性且近似服从正态布, 以(mean±SD)描述; 影响因素采用Logistic回归分析; 采用Pearson、Spearman分析相关性; 评估价值采用受试者工作特征(receiver operating characteristic curve, ROC)曲线, 获取曲线下面积(area under the cure, AUC)、置信区间、敏感度、特异度及cut-off值, 联合预测实施Logistic二元回归拟合, 返回预测概率logit(p), 将其作为独立检验变量. 均采用双侧检验, α = 0.05.
两组病程、胃镜下病理变化(慢性炎症、萎缩、肠上皮化生、上皮内瘤变)相比, 差异有统计学意义(P<0.05). 见表1.
| 临床资料 | 观察组(n = 124) | 对照组(n = 100) | u/χ2 | P值 |
| 性别 | ||||
| 男 | 69(55.65) | 56(56.00) | 0.003 | 0.958 |
| 女 | 55(44.35) | 44(44.00) | ||
| 年龄 | ||||
| ≤45岁 | 65(52.42) | 52(52.00) | 0.004 | 0.950 |
| >45岁 | 59(47.58) | 48(48.00) | ||
| 病程 | ||||
| ≤5年 | 48(38.71) | 54(54.00) | 5.219 | 0.022 |
| >5年 | 76(61.29) | 46(46.00) | ||
| 体质量指数(kg/m2) | ||||
| ≤23 kg/m2 | 64(51.61) | 49(49.00) | 0.151 | 0.697 |
| >23 kg/m2 | 60(48.39) | 51(51.00) | ||
| 胃镜下病理变化 | ||||
| 慢性炎症 | ||||
| 轻度 | 15(12.10) | 47(47.00) | 5.630 | <0.001 |
| 中度 | 72(58.06) | 45(45.00) | ||
| 重度 | 37(29.84) | 8(8.00) | ||
| 萎缩 | ||||
| 轻度 | 53(42.74) | 68(68.00) | 3.164 | 0.002 |
| 中度 | 56(45.16) | 24(24.00) | ||
| 重度 | 15(12.10) | 8(8.00) | ||
| 肠上皮化生 | ||||
| 阴性 | 31(25.00) | 45(45.00) | 3.556 | <0.001 |
| 轻度 | 36(29.03) | 32(32.00) | ||
| 中度 | 42(33.87) | 16(16.00) | ||
| 重度 | 15(12.10) | 7(7.00) | ||
| 上皮内瘤变 | ||||
| 阴性 | 54(43.55) | 61(61.00) | 6.749 | 0.009 |
| 阳性 | 70(56.45) | 39(39.00) |
观察组DOB、IL-32、sIL-2R水平高于对照组, G-17水平低于对照组, 差异有统计学意义(P<0.05). 见表2.
| 组别 | 例数 | DOB | G-17(pmol/L) | IL-32(pg/mL) | sIL-2R(ng/mL) |
| 观察组 | 124 | 7.64±1.13 | 5.10±1.24 | 76.28±9.29 | 456.78±35.69 |
| 对照组 | 100 | 2.27±0.38 | 8.02±1.45 | 57.82±6.38 | 378.25±30.12 |
| t | 45.477 | 16.241 | 16.910 | 17.535 | |
| P | <0.001 | <0.001 | <0.001 | <0.001 |
以CAG并H. pylori感染为因变量(因变量赋值: 否 = 0, 是 = 1), 将表1、2中差异有统计学意义指标纳入Logistic回归分析可知, 病程、慢性炎症、萎缩、肠上皮化生、上皮内瘤变、DOB、G-17、IL-32、sIL-2R水平均为CAG并H. pylori感染影响因素(P<0.05). 见表3.
| 因素 | β | S.E. | Waldχ2 | P | OR | 95%CI |
| 病程 | 1.538 | 0.325 | 22.408 | <0.05 | 4.657 | 3.125-6.941 |
| 胃镜下病理变化 | ||||||
| 慢性炎症 | 1.094 | 0.301 | 13.220 | <0.05 | 2.987 | 2.096-4.258 |
| 萎缩 | 1.529 | 0.347 | 19.428 | <0.05 | 4.616 | 3.529-6.037 |
| 肠上皮化生 | 1.565 | 0.302 | 26.869 | <0.05 | 4.785 | 3.987-5.742 |
| 上皮内瘤变 | 1.611 | 0.341 | 22.316 | <0.05 | 5.007 | 4.125-6.078 |
| DOB | 1.875 | 0.369 | 25.817 | <0.05 | 6.520 | 5.124-8.297 |
| G-17 | -0.838 | 0.226 | 13.737 | <0.05 | 0.433 | 0.319-0.587 |
| IL-32 | 1.431 | 0.392 | 13.329 | <0.05 | 4.184 | 3.026-5.784 |
| sIL-2R | 1.464 | 0.319 | 21.069 | <0.05 | 4.324 | 2.745-6.812 |
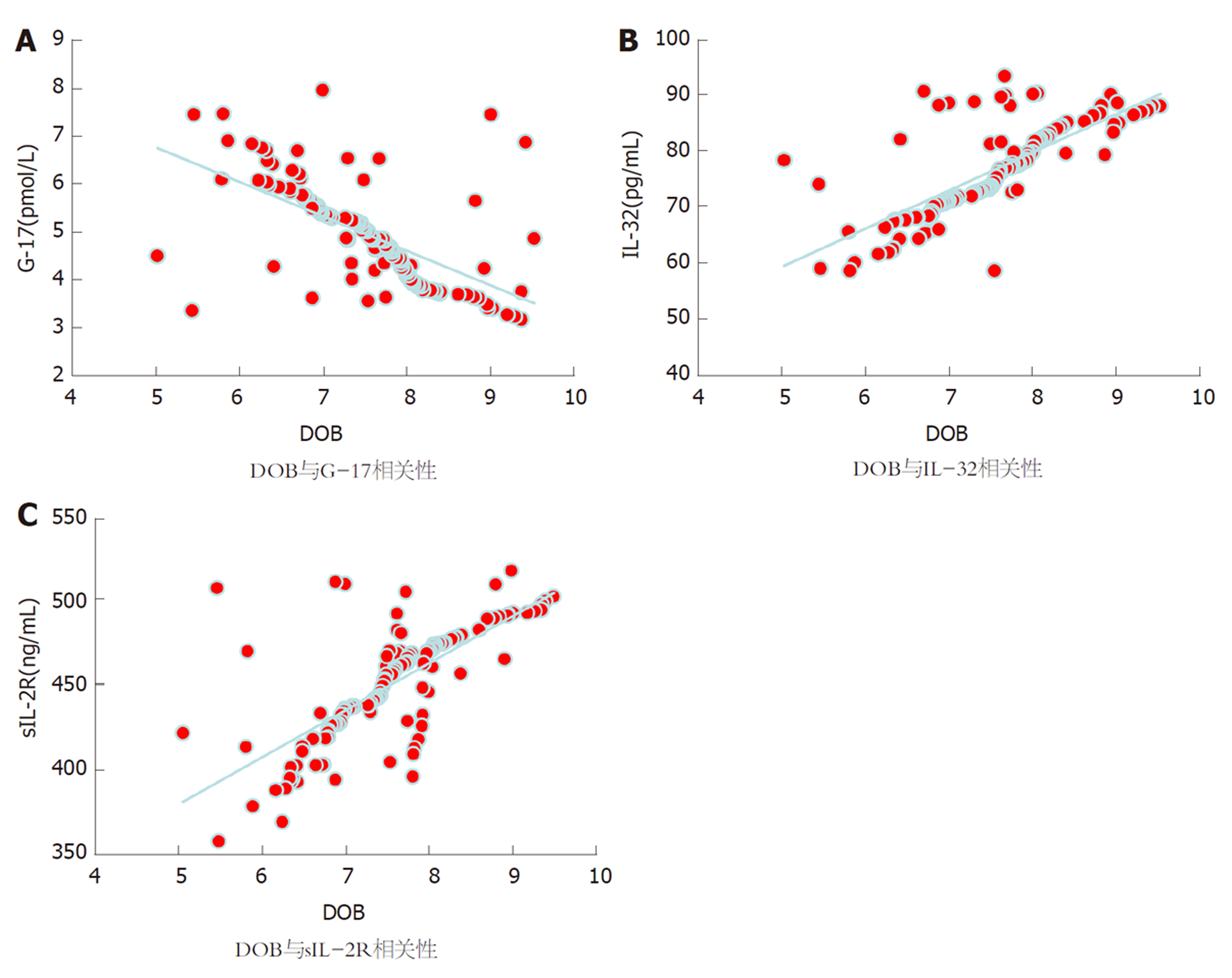
Pearson相关性分析可知, CAG并H. pylori感染患者DOB与G-17呈负相关关系, 与IL-32、sIL-2R呈正相关关系(r = -0.612, 0.740, 0.719, P<0.05). 见图1.
CAG并H. pylori感染不同胃镜下病理变化患者DOB、G-17、IL-32、sIL-2R水平相比, 差异有统计学意义(P<0.05), 进一步采用Spearman相关性分析可知, CAG并H. pylori感染患者DOB、G-17、IL-32、sIL-2R水平与慢性炎症、萎缩、肠上皮化生、上皮内瘤变有关(P<0.05). 见表4, 表5.
| 胃镜下病理变化 | 例数 | DOB | G-17(pmol/L) | IL-32(pg/mL) | sIL-2R(ng/mL) |
| 慢性炎症 | |||||
| 轻度 | 15 | 5.15±0.98 | 6.78±1.31 | 60.12±7.39 | 382.41±30.12 |
| 中度 | 72 | 7.49±1.25 | 5.21±1.12 | 75.36±8.31 | 449.37±36.74 |
| 重度 | 37 | 8.94±1.69 | 4.20±0.78 | 84.62±10.23 | 501.35±40.15 |
| F | 41.847 | 32.797 | 42.011 | 58.265 | |
| P | <0.001 | <0.001 | <0.001 | <0.001 | |
| 萎缩 | |||||
| 轻度 | 53 | 5.94±1.07 | 6.08±1.16 | 65.87±8.25 | 421.39±32.87 |
| 中度 | 56 | 8.12±1.31 | 4.72±0.98 | 80.12±9.80 | 467.94±40.69 |
| 重度 | 15 | 11.85±1.56 | 3.06±0.74 | 98.73±12.83 | 540.16±48.25 |
| F | 139.007 | 56.304 | 76.831 | 59.760 | |
| P | <0.001 | <0.001 | <0.001 | <0.001 | |
| 肠上皮化生 | |||||
| 阴性 | 31 | 5.58±0.67 | 6.49±1.06 | 63.74±5.39 | 385.63±30.26 |
| 轻度 | 36 | 6.87±1.05 | 5.43±0.92 | 72.87±7.92 | 439.54±38.41 |
| 中度 | 42 | 8.29±1.32 | 4.52±0.87 | 81.39±8.83 | 486.31±42.37 |
| 重度 | 15 | 11.93±1.58 | 3.06±0.64 | 96.07±10.26 | 561.80±45.63 |
| F | 112.773 | 56.092 | 63.405 | 81.314 | |
| P | <0.001 | <0.001 | <0.001 | <0.001 | |
| 上皮内瘤变 | |||||
| 阴性 | 54 | 5.98±1.16 | 5.84±1.25 | 65.27±10.31 | 398.32±35.26 |
| 阳性 | 70 | 8.92±1.47 | 4.53±1.12 | 84.77±14.28 | 501.88±40.13 |
| t | 12.076 | 6.139 | 8.472 | 15.011 | |
| P | <0.001 | <0.001 | <0.001 | <0.001 |
| 组别 | DOB(r/P) | G-17(r/P) | IL-32(r/P) | sIL-2R(r/P) |
| 慢性炎症 | 0.527/<0.001 | -0.549/<0.001 | 0.541/<0.001 | 0.528/<0.001 |
| 萎缩 | 0.631/<0.001 | -0.614/<0.001 | 0.579/<0.001 | 0.541/<0.001 |
| 肠上皮化生 | 0.569/<0.001 | -0.637/<0.001 | 0.562/<0.001 | 0.599/<0.001 |
| 上皮内瘤变 | 0.602/<0.001 | -0.528/<0.001 | 0.594/<0.001 | 0.621/<0.001 |
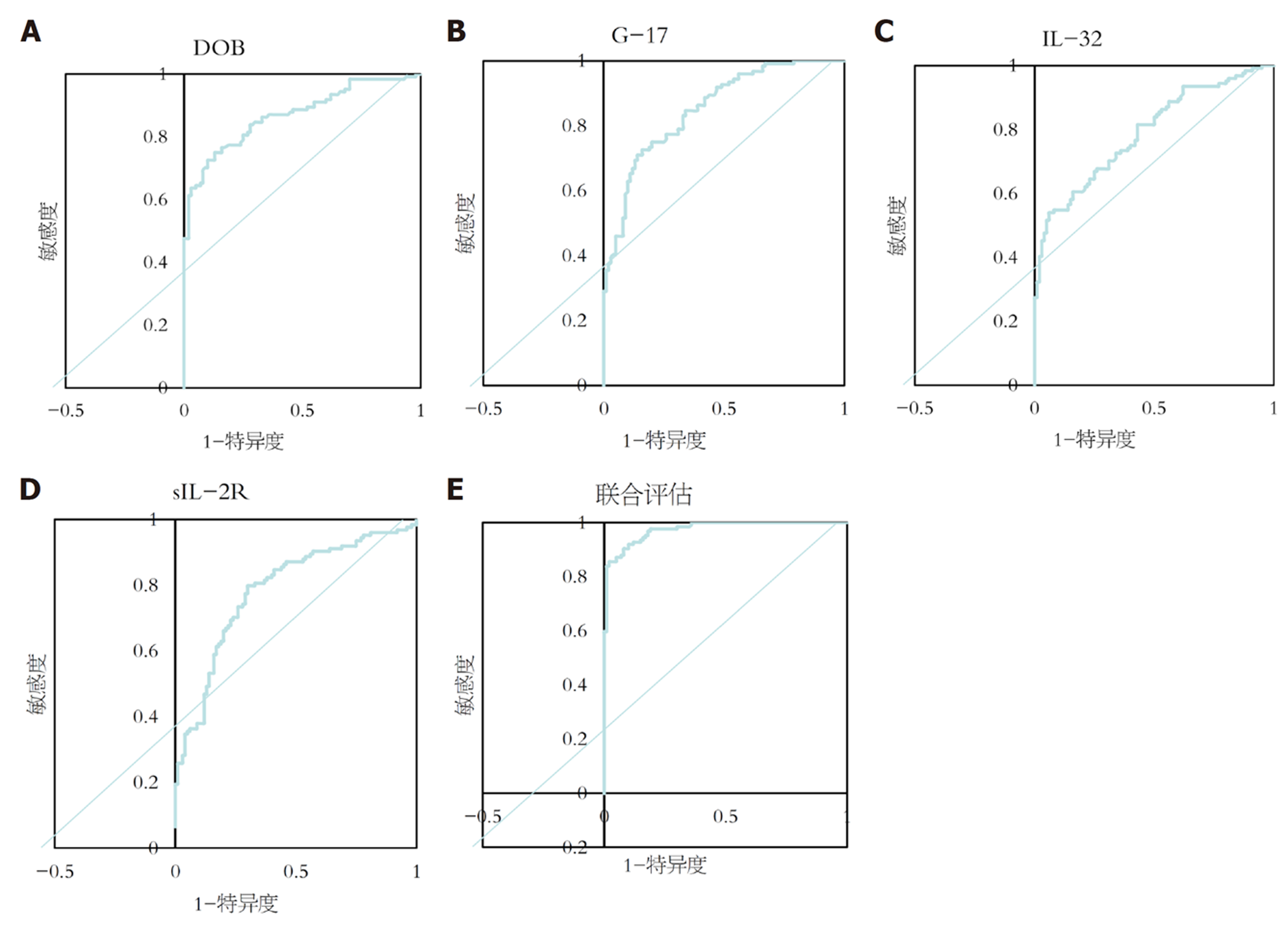
绘制ROC曲线, 评价DOB、G-17、IL-32、sIL-2R单一及联合对CAG并H. pylori感染的评估价值, 结果显示DOB、G-17、IL-32、sIL-2R联合评估AUC最大, 为0.975>0.9, 具有较高评估价值, 最佳敏感度、特异度分别为85.48%、98.00%. 见表6, 图2.
| 指标 | AUC | 95%CI | Z统计 | P | 截断值 | 敏感度 | 特异度 |
| DOB | 0.871 | 0.819-0.912 | 15.867 | <0.001 | >5.17 | 72.58% | 90.00% |
| G-17 | 0.853 | 0.799-0.896 | 14.372 | <0.001 | ≤5.97 pmol/L | 70.97% | 86.00% |
| IL-32 | 0.790 | 0.731-0.842 | 9.878 | <0.001 | >70.13 pg/mL | 54.03% | 94.00% |
| sIL-2R | 0.787 | 0.728-0.839 | 9.382 | <0.001 | >400.31 ng/mL | 79.84% | 70.00% |
| 联合评估 | 0.975 | 0.945-0.991 | 59.270 | <0.001 | 85.48% | 98.00% |
CAG是公认的胃癌前病变, H. pylori感染是其最主要致病因素[9,10]. H. pylori感染可通过参与血清炎症反应、同型半胱氨酸代谢等途径参与CAG形成与发展[11]. H. pylori高毒力菌株存在细胞毒素相关基因A(Cytotoxin-associated gene A, CagA), 是H. pylori产生致病作用的原始动力, 并增加胃癌发病风险[12]. 本研究, 相较于CAG未合并H. pylori感染患者, CAG并H. pylori感染者胃镜下病理变化(慢性炎症、萎缩、肠上皮化生、上皮内瘤变)更为严重, 提示H. pylori感染是CAG病情加重乃至恶化的主要因素之一, 与既往研究[13,14]一致.
G-17是消化道G细胞分泌的胃肠激素, 可调节消化道功能, CAG早期, G细胞分泌胃酸的功能受抑制, 胃酸抑制作用导致胃窦部G细胞显著降低, 进而使G-17水平下降; 随CAG病情进展, 胃窦腺体丧失, 胃窦G细胞大量减少, 血清G-17水平下降[15,16]. IL-32参与CAG患者胃黏膜炎症反应, 损及胃黏膜表层, 诱导腺体分泌功能衰退, 而H. pylori感染可促使中性粒细胞、淋巴细胞等炎症细胞在胃黏膜的浸润, 促进IL-32、肿瘤坏死因子等炎症因子释放, 引起炎症反应损伤[17]. 研究证实, CAG发生、发展与细胞免疫功能密切相关[18]. sIL-2R是活化淋巴、单核细胞产生的多肽, 通过竞争性结合IL-2抑制T细胞增殖, 进而影响机体免疫功能, CAG患者血清sIL-2R显著高表达[19]. 本研究数据显示, CAG并H. pylori感染者IL-32、sIL-2R水平高于未合并H. pylori感染者, G-17水平低于未合并H. pylori感染者, 且G-17、IL-32、sIL-2R水平均为CAG并H. pylori感染影响因素. 分析原因在于, (1)CAG并H. pylori感染者胃窦G细胞减少更多, G-17分泌量更少, 同时, H. pylori感染可增加胃酸分泌, 影响胃酸对胃泌素的反馈调节作用, 进而影响G-17合成和释放; (2)CagA所表达的CagA蛋白可促使炎症细胞(淋巴细胞、中性粒细胞等)在胃黏膜浸润, 促进IL-32、肿瘤坏死因子等炎症因子释放, 促进炎症反应损伤; (3)H. pylori感染后, 机体免疫系统被激活, 细胞因子及受体表达增加, 可溶性受体大量产生, 抑制IL-2与其膜受体结合, 进而抑制机体免疫反应[20,21].
DOB是H. pylori感染严重程度的定量评估指标, 且可预测病情发展趋势和预后成效, 指导临床治疗方案的制定[22]. 本研究创新性探讨发现, CAG并H. pylori感染患者DOB与G-17呈负相关关系, 与IL-32、sIL-2R呈正相关关系, 推测DOB、G-17、IL-32、sIL-2R可能协同用于CAG并H. pylori感染的临床诊断及病情评估. 进一步研究发现, CAG并H. pylori感染患者DOB、G-17、IL-32、sIL-2R水平与慢性炎症、萎缩、肠上皮化生、上皮内瘤变有关, 提示G-17、IL-32、sIL-2R在胃黏膜炎症及CAG向肠上皮化生、异型增生至胃癌进展中可能发挥重要作用. 因此, 临床医生应当针对CAG并H. pylori感染患者积极实施抗H. pylori感染、保护胃黏膜、抑制胃酸分泌、改善G-17、IL-32、sIL-2R表达等措施, 以控制病情, 增强疗效. 此外, 本研究首次采用DOB、G-17、IL-32、sIL-2R联合评估CAG并H. pylori感染, ROC曲线显示, DOB>5.17、G-17≤5.97 pmol/L、IL-32>70.13 pg/mL、sIL-2R>400.31 ng/mL时, 均高度怀疑合并H. pylori感染, 联合评估AUC最高, 达0.975. 临床可同时检测DOB、G-17、IL-32、sIL-2R, 为评估CAG并H. pylori感染提供更全面、可靠的参考信息.
综上可知, CAG并H. pylori感染患者G-17、IL-32、sIL-2R水平与DOB相关, H. pylori感染可能通过影响G-17、IL-32、sIL-2R表达, 参与CAG患者胃黏膜病理改变发生和进展, 各指标联合检测可有效预测H. pylori感染, 对临床诊治有重要意义. 针对CAG并H. pylori感染患者, 临床医生应积极抗H. pylori治疗, 调节G-17、IL-32、sIL-2R水平, 以期达到理想疗效.
幽门螺杆菌(Helicobacter pylori, H. pylori)是公认的胃癌致病因子, 慢性萎缩性胃炎(chronic atrophic gastritis, CAG)并H. pylori感染的诊治一直是临床研究重点.
白介素-32(interleukin-32, IL-32)、胃泌素-17(gastrin 17, G-17)、可溶性白细胞介素-2受体(soluble interleukin 2 receptor, sIL-2R)均与CAG发生、发展有关. 探讨IL-32、G-17、sIL-2R与吹气定量检测值(delta over baseline, DOB)的关系, 及各指标预测CAG并H. pylori感染的价值, 有望为H. pylori感染临床诊治提供新手段. CAG并H. pylori感染的关系, 旨在为H. pylori感染临床诊治提供参考.
探讨IL-32、G-17、sIL-2R与CAG并H. pylori感染的关系, 旨在为H. pylori感染临床诊治提供参考.
Logistic回归分析CAG并H. pylori感染影响因素; Pearson分析DOB与G-17、IL-32、sIL-2R相关性; Spearman分析DOB、G-17、IL-32、sIL-2R水平与胃镜下病理变化相关性; ROC曲线分析DOB、G-17、IL-32、sIL-2R对CAG并H. pylori感染的评估价值.
DOB、G-17、IL-32、sIL-2R水平均为CAG并H. pylori感染影响因素; CAG并H. pylori感染患者DOB与G-17、IL-32、sIL-2R相关, DOB、G-17、IL-32、sIL-2R水平与胃镜下病理变化相关; DOB、G-17、IL-32、sIL-2R均可有效评估评估CAG并H. pylori感染, 各指标联合评估价值最高.
CAG并H. pylori感染患者G-17、IL-32、sIL-2R水平与DOB相关, H. pylori感染可能通过影响G-17、IL-32、sIL-2R表达, 参与CAG患者胃黏膜病理改变发生和进展, 各指标联合检测可有效评估H. pylori感染.
本研究明确了G-17、IL-32、sIL-2R对H. pylori感染的评估价值, 但尚未明确G-17、IL-32、sIL-2R与H. pylori感染通过哪种通路形成反馈调节关系, 后续研究可对此展开探讨.
学科分类: 胃肠病学和肝病学
手稿来源地: 浙江省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C
D级 (一般): D
E级 (差): E
科学编辑: 张砚梁 制作编辑:张砚梁
| 1. | Tong Y, Wu Y, Song Z, Yu Y, Yu X. The potential value of serum pepsinogen for the diagnosis of atrophic gastritis among the health check-up populations in China: a diagnostic clinical research. BMC Gastroenterol. 2017;17:88. [PubMed] [DOI] |
| 4. | 李 超, 汪 志兵, 张 振玉. 13C-尿素呼气试验DOB值与幽门螺杆菌根除率关系的研究. 胃肠病学和肝病学杂志. 2017;26:670-672. [DOI] |
| 6. | Zahedi L, Jafari E, Torabi Parizi M, Shafieipour S, Hayat Bakhsh Abbasi M, Darvish Moghadam S, Zahedi MJ. The Association between Oral Hygiene and Gastric Pathology in Patients with Dyspepsia: a Cross-Sectional Study in Southeast Iran. Middle East J Dig Dis. 2017;9:33-38. [PubMed] [DOI] |
| 7. | 陈 朝聪, 蔡 水苗, 刘 海珊. 质子泵抑制剂联合抗生素治疗对HP阳性慢性萎缩性胃炎患者血清胃泌素SIL-2R CRP水平及免疫功能的影响. 河北医学. 2020;26:429-432. [DOI] |
| 9. | Hwang YJ, Kim N, Lee HS, Lee JB, Choi YJ, Yoon H, Shin CM, Park YS, Lee DH. Reversibility of atrophic gastritis and intestinal metaplasia after Helicobacter pylori eradication - a prospective study for up to 10 years. Aliment Pharmacol Ther. 2018;47:380-390. [PubMed] [DOI] |
| 10. | Moon HW, Lee SY, Hur M, Yun YM. Characteristics of Helicobacter pylori-seropositive subjects according to the stool antigen test findings: a prospective study. Korean J Intern Med. 2018;33:893-901. [PubMed] [DOI] |
| 12. | 杨 静, 冯 庆涛, 杨 铸锋, 龙 润, 杨 金国, 郭 虹忆. 慢性萎缩性胃炎大鼠胃黏膜中HP阳性对表皮生长因子表达的影响. 东南大学学报(医学版). 2018;37:1041-1044. [DOI] |
| 13. | 黄 懋敏, 董 丹丹, 亓 丹丹, 凌 晨, 张 丁丁. 慢性萎缩性胃炎患者HP感染与TGF-性胃Ⅱ、IL-6和TNF-性的表达研究. 中国免疫学杂志. 2018;34:751-756. [DOI] |
| 14. | 李 莉, 朱 蕾蕾, 孙 祝美, 王 慧雯, 从 军, 陈 昶州, 顾 志坚, 李 娜. 慢性萎缩性胃炎中医证型分布及幽门螺杆菌感染、胃黏膜病理变化情况分析. 上海中医药杂志. 2019;52:20-23. [DOI] |
| 15. | 李 晓琴, 单 文杰, 董 文福, 王 桦, 陈 利, 王 海英, 段 秀芳, 韩 学军. 胃蛋白酶原和胃泌素对萎缩性胃炎、胃癌的筛查价值及与幽门螺旋杆菌感染的关系. 宁夏医科大学学报. 2017;39:1062-1065. [DOI] |
| 16. | Kotachi T, Ito M, Yoshihara M, Boda T, Kiso M, Masuda K, Matsuo T, Tanaka S, Chayama K. Serological Evaluation of Gastric Cancer Risk Based on Pepsinogen and Helicobacter pylori Antibody: Relationship to Endoscopic Findings. Digestion. 2017;95:314-318. [PubMed] [DOI] |
| 17. | 杜 三军, 张 娅娟, 孙 晓冉, 高 会斌, 于 永强. 幽门螺旋杆菌感染与胃癌患者血清IL-32、IL-12、TNF-2的关系研究. 现代生物医学进展. 2019;19:4740-4743. [DOI] |
| 19. | 乔 会侠, 王 玥, 陈 晓岩, 黄 雅慧. 自拟萎平舒胶囊联合西药对慢性萎缩性胃炎患者血清MTL、sIL-2R及T淋巴细胞亚群的影响. 中国中西医结合消化杂志. 2020;28:433-436, 443. [DOI] |
| 20. | Anjiki H, Mukaisho KI, Kadomoto Y, Doi H, Yoshikawa K, Nakayama T, Vo DT, Hattori T, Sugihara H. Adenocarcinoma arising in multiple hyperplastic polyps in a patient with Helicobacter pylori infection and hypergastrinemia during long-term proton pump inhibitor therapy. Clin J Gastroenterol. 2017;10:128-136. [PubMed] [DOI] |
| 21. | 袁 林, 丁 松泽, 张 延瑞, 祁 亚宾, 周 颖蕾, 李 点点, 赵 俊波. 不同类型幽门螺杆菌在慢性胃病中感染情况及对胃泌素-17和胃蛋白酶原的影响. 中华实用诊断与治疗杂志. 2020;34:382-385. [DOI] |