修回日期: 2016-01-11
接受日期: 2016-01-19
在线出版日期: 2016-02-28
目的: 研究叶黄素对于核因子相关因子2(nuclear factor erythroid-2 related factor 2, Nrf-2)和血红素加氧酶-1(heme oxygenase-1, HO-1)表达的影响, 从而研究叶黄素对人结肠癌HT29细胞增殖的抑制作用及其可能的机制.
方法: 用不同浓度的叶黄素(20、40、80、120、160 mg/L)和空白对照组(0 mg/L)处理HT29细胞24、48、72 h, 用CCK8法检测叶黄素对该细胞增殖的抑制作用. 流式细胞仪检测细胞周期. RT-PCR检测Nrf-2和HO-1 RNA表达水平的变化. Western blot检测Nrf-2和HO-1的蛋白表达水平的变化.
结果: 叶黄素能够抑制人结肠癌HT29细胞的增殖, 160 mg/L叶黄素作用72 h后, 抑制率可高达78.09%, 且具有剂量依赖性和时间依赖性. 流式细胞仪检测细胞周期结果显示: 叶黄素作用于HT29细胞48 h后, G0/G1期细胞显著增加. 表明叶黄素可阻滞HT29细胞生长于G0/G1期. RT-PCR检测和Western blot检测的结果共同显示, 经过不同浓度的叶黄素处理后, Nrf-2和HO-1 RNA的表达水平以及蛋白的表达水平与未经叶黄素处理的对照组相比明显上调, 且具有剂量依赖性(P<0.01).
结论: 叶黄素可显著抑制HT29细胞的增殖, 使其细胞周期阻滞在G0/G1期. 同时诱导Nrf-2和HO-1 RNA和蛋白的表达, 这可能是其抑制HT29细胞增殖、发挥保护作用的重要机制.
核心提示: 本文探讨人结肠癌细胞(HT29)中叶黄素对Nrf-2/ARE通路的影响. 发现其可以显著抑制HT29细胞的增殖, 使细胞周期阻滞在G0/G1期. 采用RT-PCR和Western blot技术检测Nrf-2和HO-1的表达情况. 结果显示在HT29中叶黄素可诱导Nrf-2和HO-1的表达, 这可能是其抑制细胞增殖的重要机制.
引文著录: 刘志方, 吴凤秀, 王丽平, 王明臣, 付蕾. 叶黄素介导Nrf-2/ARE信号途径抑制人结肠癌HT29细胞增殖的作用机制. 世界华人消化杂志 2016; 24(6): 858-865
Revised: January 11, 2016
Accepted: January 19, 2016
Published online: February 28, 2016
AIM: To observe the anti-proliferative effect of lutein on human colon cancer HT29 cells and to explore the possible mechanisms involved by detecting the expression of nuclear factor erythroid-2 related factor 2 and heme oxygenase-1.
METHODS: HT29 cells were treated with different concentrations of lutein (20, 40, 80, and 160 mg/L) for 24, 48 or 72 h. After treatment, CCK8 method was used to detect cell proliferation. Cell cycle progression was analyzed by flow cytometry. The levels of Nrf-2 and HO-1 mRNAs were determined by RT-PCR. The levels of Nrf-2 and HO-1 proteins were determined by Western blot.
RESULTS: Lutein inhibited the proliferation of HT29 cells in a dose- and time-dependent manner. Treatment with 160 mg/L lutein for 72 h resulted in an inhibition rate of 78.09%. After treatment with lutein for 48 h, it was found by flow cytometry that lutein arrested HT29 cell growth at G0/G1 phase. Compared with the blank control group, lutein upregulated the mRNA and protein expression levels of Nrf-2 and HO-1 in a dose-dependent manner (P < 0.01).
CONCLUSION: Lutein can significantly inhibit the proliferation of HT29 cells, arrest cells in G0/G1 phase, and induce the mRNA and protein expression of Nrf-2 and HO-1. The inhibitory effect of lutein on cell proliferation may involve the Nrf-2/ARE signal transduction pathway.
- Citation: Liu ZF, Wu FX, Wang LP, Wang MC, Fu L. Lutein suppresses cell proliferation in human colon cancer cell line HT29 via Nrf-2/ARE signal transduction pathway. Shijie Huaren Xiaohua Zazhi 2016; 24(6): 858-865
- URL: https://www.wjgnet.com/1009-3079/full/v24/i6/858.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v24.i6.858
结肠癌是一种常见的消化系恶性肿瘤, 在欧美等发达国家有较高的发病率. 近年来, 随着人们生活水平和饮食结构的不断改变, 结肠癌在我国的发病率和死亡率也呈逐年升高的趋势[1]. 目前关于结肠癌的治疗手段非常单一, 化疗常常使用5-氟尿嘧啶(5-fluorouracil, 5-Fu)、丝裂霉素和甲环亚硝脲, 但是临床效果尚不理想[2]. 故进一步寻求有效的干预阻断结肠癌发生发展的线索和物质具有重要的理论及实用意义[3]. 叶黄素系广泛存在于瓜果蔬菜中的含氧类胡萝卜素, 是一种天然的抗氧化的植物化学物[4]. 在防治视网膜病变和色素变性、延缓动脉硬化及预防肿瘤等方面有重要作用. 已有研究[5]表明, 叶黄素对结肠癌细胞有一定的增殖抑制作用.
核因子相关因子2(nuclear factor erythroid 2-related factor 2, Nrf-2)属于碱性亮氨酸拉链蛋白家族(basic leucine-zipper, bZIP)的成员, 在各种组织细胞中都能广泛的表达, 是细胞调节抗氧化应激反应的重要转录因子[6]. Nrf-2主要通过与抗氧化顺势作用元件(anti-inflammatory response element, ARE)结合, 从而调控ARE所控制的基因的表达. ARE控制基因包括抗氧化酶基因、Ⅱ相解毒酶基因、应激基因等[7]. 在通常情况下, Nrf-2与Kelch样环氧氯丙烷相关蛋白-1(Kelch-like ECH-associated protein-1, Keap-1)结合在细胞质中[8]. Keap-1是一种富含巯基的蛋白, 在氧化应激等情况下, 细胞接受到胞外信号后, Keap-1的巯基发生交联反应, 使Nrf-2脱落进入细胞核内, 然后Nrf-2与ARE相结合, 参与影响ARE调控的下游第Ⅱ相解毒酶及抗氧化酶基因的表达, 从而增强细胞对氧化应激和亲核化合物的抗性[9]. HO属微粒体酶系, 是血红素分解代谢的限速酶. HO有3种同工酶, 分别是HO-1、HO-2和HO-3. 其中HO-1为氧化应激诱导型酶, 参与血红素的代谢, 是Nrf-2/ARE信号通路下游Ⅱ相代谢酶中的一种[10]. 本文旨在研究基于Nrf-2/ARE信号通路的叶黄素在抗结肠癌HT29细胞增殖效应中的分子机制.
人结肠癌HT29细胞株由河南省医药科学研究院馈赠. 叶黄素(Food Research Program, Agriculture and Agri-Food Canada提供). CCK-8试剂盒购自碧云天生物技术公司; Western blot试剂盒购自美国SAB公司; Nrf-2(兔抗人)抗体购自Cell Signaling Technology公司; HO-1(兔抗人)抗体购自北京博奥森生物公司.
1.2.1 细胞培养: 将人结肠癌HT29细胞株常规接种于培养瓶当中, 培养于含10%胎牛血清的RPMI 1640完全培养基中, 在50 mL/L CO2和饱和湿度的培养箱中, 37 ℃恒温培养.
1.2.2 药品配制: 叶黄素用DMSO溶解, 配制成浓度为8×104 mg/L的储备液, 使用0.22 μm的微孔滤膜过滤除菌, 4 ℃避光保存. 在实验使用时, 用不含青霉素、链霉素的RPMI 1640培养基将其稀释成终浓度分别为20、40、80、120、160 mg/L. 同时0 mg/L浓度组用等体积的DMSO作为对照组.
1.2.3 CCK8法检测叶黄素对HT29细胞增殖的抑制作用: 将生长于对数期的HT29细胞接种在96孔细胞培养板中, 细胞计数, 调整细胞的接种浓度为每孔1×104个/mL, 每孔200 μL. 在细胞培养24 h后, 每孔分别加入终浓度为20、40、80、120、160 mg/L的叶黄素溶液, 同时用等体积的DMSO作为对照组, 每组设6个复孔, 重复3次. 在用叶黄素分别处理细胞24、48、72 h后, 用CCK8染色. 全波长酶标仪515 nm波长下检测各孔OD值. 按抑制率(%) = (1-实验组OD值/对照组OD值)×100%公式计算抑制率.
1.2.4 流式细胞仪检测叶黄素对HT29细胞的细胞周期影响: 选取生长于对数期的HT29细胞, 以1×106个/孔的浓度接种于6孔细胞培养板中. 待细胞培养24 h后, 分别加入浓度为80、160 mg/L的叶黄素溶液, 同时用DMSO设空白溶剂对照组. 作用48 h后, 收集细胞, 先PBS洗涤, 用1 mL 700 mL/L乙醇将细胞重悬, 置于4 ℃中固定24 h. 然后12000 r/min离心5 min, 弃去上清液, PBS再洗涤. 加入0.5 mL PBS, 加入RNase A和PI至终浓度为50 μg/mL, 室温避光标记30 min, 流式细胞仪上机检测.
1.2.5 RT-PCR检测Nrf-2和HO-1 RNA表达水平的变化: 选取生长于对数期的HT29细胞, 以5×105个/mL细胞每瓶分装到细胞培养瓶中. 待细胞培养24 h后, 分别加入浓度为40、80、120、160 mg/L的叶黄素溶液, 同时用DMSO设空白溶剂对照组. 作用48 h后, 收集细胞, 提取总RNA. 用GenBank检索设计引物序列: Nrf-2引物大小为291 bp, 上游序列: 5'-TCTCCATATCCCATTCCC-3'; 下游序列: 5'-AAGGTGCTGAGTTGTTTT-3'. HO-1的引物大小为324 bp, 上游序列: 5'-GCACCGGCCGGATGGAGCGTCC-3'; 下游序列为: 5'-CGTCTCGGGTCACCTGGCCCTTCT-3'. β-actin的引物大小为536 bp, 上游序列: 5'-CTTCCAGCCTTCCTTCCTGG-3'; 下游序列: 5'-TTCTGCATCCTGTGGCAAT-3'. 按照PCR扩增试剂盒说明书将所需试剂加入200 μL的离心管中, 放入PCR扩增仪内进行扩增, 反应条件为: 94 ℃预变性2 min, 1个循环, 94 ℃变性30 s, 55 ℃退火30 s, 72 ℃延伸2 min, 共35个循环, 76 ℃总延伸6 min. 将PCR产物进行1.5%琼脂糖凝胶电泳, 在紫外透射分析仪下观察电泳条带并拍照, 用D-140图像记录系统记录, Quantity One软件分析电泳条带. 目的基因表达量 = 目的基因DNA条带灰度值/β-actin DNA条带灰度值.
1.2.6 Western blot检测Nrf-2和HO-1蛋白表达水平的变化: 选取生长于对数期的HT29细胞, 以5×105个/mL细胞每瓶分装到细胞培养皿中. 待细胞培养24 h后, 分别加入浓度为40、80、120、160 mg/L的叶黄素溶液, 同时用DMSO设空白溶剂对照组. 作用48 h后, 消化离心收集细胞, 预冷的冰PBS洗涤, 加入细胞裂解液, 冰上裂解20 min. 然后用冷冻高速离心机于4 ℃, 12000 r/min离心15 min, 取含有蛋白的上清液. 用BCA蛋白试剂盒测量总蛋白的浓度, 并计算20 μg蛋白的上样体积. 总蛋白与5×SDS-PAGE蛋白上样缓冲液以4:1混合, 煮沸5 min. 在制备好的SDS-PAGE凝胶中上样处理好的蛋白样品, 用120 V恒压进行电泳2 h, 用300 mA恒流进行转膜2 h. 孵育一抗(1:1000), 4 ℃过夜. TBST洗膜3次, 每次10 min, 室温孵育二抗(1:10000)2 h. 暗室中用ECL发光液(A液:B液 = 1:1)曝光显影定影. 用Image-Pro Plus 6.0软件比较条带的积分光密度.
统计学处理 实验数据用mean±SD表示, 采用SPSS20.0统计软件进行分析. 采用单因素方差分析(ANVOA)和LSD组间多重比较检验. P<0.05认为差异有统计学意义.
不同浓度的叶黄素(0、20、40、80、120、160 mg/L)作用于HT29细胞后, 可明显抑制HT29细胞的增殖, 并呈时间依赖性和剂量依赖性(P<0.01, 表1).
| 叶黄素(μg/mL) | 24 h | 48 h | 72 h | |||
| OD值 | IR(%) | OD值 | IR(%) | OD值 | IR(%) | |
| 对照组 | 0.317±0.0731 | 0.470±0.1141 | 0.639±0.0808 | |||
| 20 | 0.289±0.0652 | 8.83 | 0.393±0.0143 | 16.30 | 0.497±0.0259 | 22.22 |
| 40 | 0.256±0.1525 | 19.24 | 0.302±0.0583a | 35.74 | 0.373±0.0536b | 41.63 |
| 80 | 0.238±0.0975b | 24.92 | 0.258±0.0378b | 45.11 | 0.296±0.0078b | 53.68 |
| 120 | 0.221±0.0904b | 30.28 | 0.222±0.0191b | 52.77 | 0.205±0.0532b | 67.92 |
| 160 | 0.219±0.0812b | 30.91 | 0.195±0.0748b | 58.51 | 0.140±0.0606b | 78.09 |
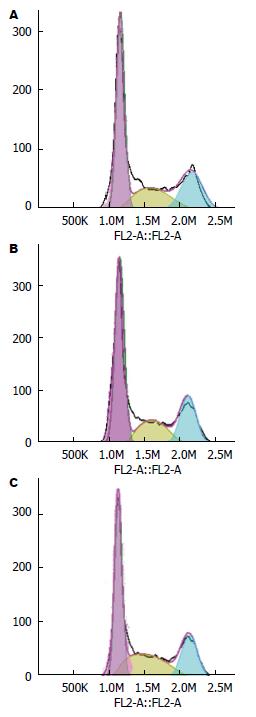
不同浓度的叶黄素(80、160 mg/L)作用于HT29细胞48 h后, G0/G1期细胞由53.74%增加至69.73%, 表现为显著的G1期阻滞(P<0.01), 且随叶黄素浓度的增加, S期细胞显著减少, G2/M期细胞则变化不明显. 结果显示, 叶黄素可将HT29细胞阻滞于G0/G1期, 并呈剂量依赖性(P<0.01, 表2, 图1).
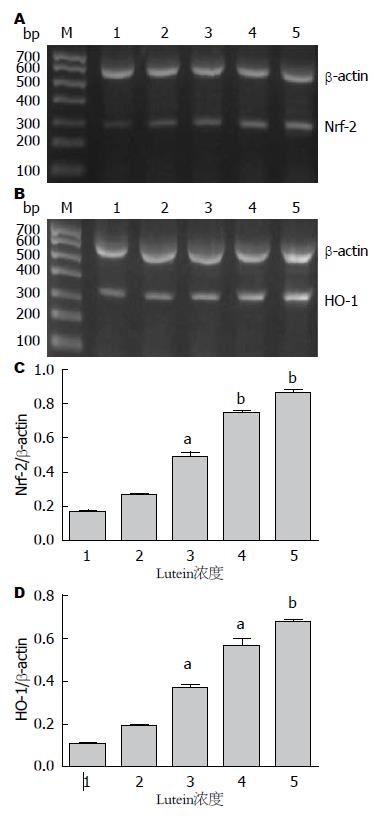
浓度为40、80、120、160 mg/L的叶黄素溶液作用于HT29细胞48 h后, 与空白对照组相比, β-actin的表达水平不受叶黄素的影响, 而Nrf-2和HO-1的RNA表达水平呈显著升高的状态(P<0.01), 且随着叶黄素浓度的增加, Nrf-2和HO-1的RNA表达均呈上升趋势, 呈剂量依赖性(图2).
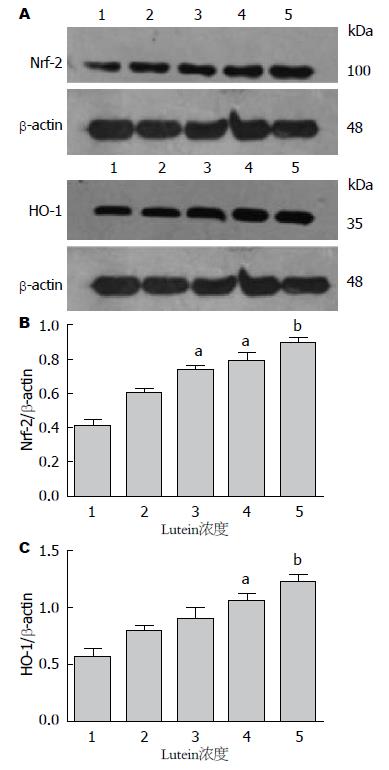
与空白对照组相比, 浓度为40、80、120、160 mg/L的叶黄素溶液作用于HT29细胞48 h后, β-actin的表达水平不受叶黄素的影响, 而Nrf-2和HO-1的蛋白表达水平均呈显著升高的状态(P<0.01), 且随着叶黄素浓度的增加, Nrf-2和HO-1的蛋白表达也呈上升趋势, 呈剂量依赖性(图3).
叶黄素是含氧胡萝卜素类中的一种天然抗氧化剂, 又名植物黄体素, 广泛存在于玉米、蔬菜、水果、花卉等植物中, 是其植物色素的主要组分. 近年来, 越来越多的流行病学证据表明, 叶黄素对多种癌症如结肠癌、直肠癌、乳腺癌、前列腺癌、皮肤癌等具有抑制作用[11]. Kwon等[12]研究表明, 癌症的发生和血清中叶黄素的低含量密切相关, 增加饮食中叶黄素的摄入能降低多种肿瘤的发生几率. 本研究结果明确显示, 叶黄素对人结肠癌HT29细胞的增殖有显著的抑制作用, 且存在剂量和时间依赖性. 我们用不同浓度(0、20、40、80、120、160 mg/L)的叶黄素作用于HT29细胞相同时间后, 其抑制率呈逐步上升趋势, 说明了叶黄素抑制肿瘤细胞的增殖具有剂量依赖性. 其中用160 mg/L浓度的叶黄素作用于HT29细胞24、48、72 h后, 其抑制率分别为30.91%、58.51%和78.09%, 证明了叶黄素抑制肿瘤细胞的增殖具有时间依赖性. Sowmya等[13]的研究结果显示, 在致癌因素的作用下, 细胞周期容易发生失控, 导致异常细胞无限增殖, 进而形成肿瘤. 在细胞周期的3个阶段中, 存在影响细胞周期的调控位点, 药物通过作用于这些位点来影响细胞周期, 进而影响细胞的分裂增殖[14]. 本实验分别用80、160 mg/L浓度的叶黄素分别作用于HT29细胞48 h后, 进行细胞周期检测, 结果显示, G0/G1期细胞由53.74%增加至69.73%, 表现为显著的G1期阻滞, S期细胞显著减少, G2/M期细胞变化不明显. 研究结果表明叶黄素可阻滞HT29细胞于G0/G1期, 且呈剂量依赖性. 叶黄素诱导Nrf-2/ARE通路表达上调, 可能是其阻滞细胞周期、抑制HT29细胞增殖的机制之一.
Nrf-2/ARE通路广泛存在于细胞中, 具有细胞保护的作用, 并能通过产生HO-1发挥抗炎抗肿瘤的作用[15-17]. 近年来研究[18,19]表明, 在许多肿瘤如结肠癌、食管癌、喉癌、乳腺癌等的发生发展均与Nrf-2/ARE通路有密切关联. 其中Nrf-2是内源性抗氧化应激的重要调控因子[20,21]. Frohlich等[18]的研究表明, 在致癌剂的作用下, 由于Nrf-2基因敲除小鼠体内Nrf-2的缺失, 由其启动的抗氧化蛋白酶谷胱甘肽S-转移酶(glutathione S-transferase, GST)的表达也相应减少, 而活性氧ROS的水平增高, 导致DNA损伤引起肿瘤的发生[22]. Nrf-2信号通路在肿瘤的化学预防中至关重要, 通路中Nrf-2的激活具有一定的防止细胞癌变的作用, Nrf-2基因的缺失或低表达使机体患癌的风险增高[23]. 本实验用浓度呈梯度递增的叶黄素作用于HT29细胞48 h后, 通过RT-PCR技术和Western blot检测HT29细胞中Nrf-2的含量, 结果显示叶黄素作用于HT29细胞后, HT29细胞中Nrf-2的RNA和蛋白的表达含量都呈递增的状态, 说明叶黄素可以诱导Nrf-2/ARE通路的表达, 上调Nrf-2的含量, 且呈剂量依赖性.
Nrf-2/ARE通路调控的下游抗氧化蛋白有HO-1、GST、谷胱甘肽等[24,25], 这些酶和蛋白形成一个复杂的网络, 相互作用, 保持细胞的氧化平衡状态, 能够保护机体免受活性氧(reactive oxygenspecies, ROS)的侵害[26,27]. HO-1就是其Ⅱ相代谢酶中的一种. HO-1作为一种高度保守的应激蛋白, 可以保护器官、组织和细胞抵御各种刺激因素和病理过程的伤害[28,29]. 本研究采用梯度递增的不同浓度的叶黄素处理HT29细胞48 h, 然后通过RT-PCR技术和Western blot检测HT29细胞中HO-1的表达情况. 实验结果显示随着叶黄素浓度的上升, HT29细胞中HO-1的RNA和蛋白的表达含量都呈递增的状态, 且呈剂量依赖性. 本研究结果说明叶黄素可以激活HT29细胞中的Nrf-2/ARE通路, 明显的上调Nrf-2和HO-1的RNA的表达水平, 从而诱导Nrf-2和HO-1的蛋白的含量增加, 且存在剂量依赖性.
综合研究结果表明, 叶黄素能够显著抑制HT29细胞的增殖, 并阻滞细胞周期于G0/G1期, 其机制可能是通过介导Nrf-2/ARE通路, 上调Nrf-2和HO-1的表达而实现的. 但是近年来有相关研究[30]表明, Nrf-2和HO-1的过度表达与肿瘤的发生发展和耐药性有密切关联, 故平衡Nrf-2和HO-1的双刃剑作用尚需深入研究. 并且与细胞增殖抑制相关的信号通路存在复杂的交叉对话, Nrf-2/ARE通路与其他信号通路的相互联系及影响作用尚需深入研究.
结肠癌是一种常见的消化系恶性肿瘤, 近年来, 随着人们生活水平和饮食结构的不断改变, 结肠癌在我国的发病率和死亡率呈逐年升高的趋势. 结肠癌的治疗手段非常单一, 化疗常常使用5-Fu、丝裂霉素和甲环亚硝脲, 但是临床效果尚不理想. 故进一步寻求有效的干预阻断结肠癌发生发展的线索和有效的天然植物药物具有重要的理论及实用意义.
齐晓薇, 副主任医师, 江南大学附属医院(无锡市第四人民医院)病理科; 姜洪伟, 主任医师, 内蒙古自治区人民医院胃肠外科
叶黄素作为一种含氧胡萝卜素类中的天然抗氧化剂, 在抗氧化、预防白内障、延缓动脉硬化以及抗癌等方面有重要作用. Nrf-2/ARE通路是介导抗氧化应激反应的重要通路, 广泛存在于细胞中, 他可以帮助细胞抵抗外界不利因子的刺激, 起到保护细胞的作用. 亟待研究的问题是Nrf-2/ARE通路对肿瘤耐药性的影响.
Kwon等研究表明, 癌症的发生和血清中叶黄素的低含量密切相关, 增加饮食中叶黄素的摄入能降低多种肿瘤的发生几率. Frohlich等发现Nrf-2基因敲除小鼠的肿瘤的发生率升高, Nrf-2/ARE信号通路在肿瘤的化学预防中至关重要.
本文观察了Nrf-2/ARE信号通路对人结肠癌HT29细胞中Nrf-2和HO-1表达含量的影响. 探讨了叶黄素通过介导Nrf-2/ARE信号通路抑制人结肠癌HT29细胞增殖的相关分子机制. 为叶黄素预防结肠瘤的发生发展提供了实验依据.
本研究发现叶黄素可以通过介导Nrf-2/ARE信号通路上调Nrf-2和HO-1的表达含量, 从而达到抑制人结肠癌HT29细胞增殖的目的. 本研究为利用天然植物药物预防结肠癌的发生发展提供了新的依据和思路.
核因子相关因子: 属于碱性亮氨酸拉链蛋白家族的成员, 在各种组织细胞中都能广泛的表达, 是细胞调节抗氧化应激反应的重要转录因子;
血红素氧合酶: 三种亚型中一种, 属微粒体酶系, 是血红素分解代谢的限速酶, 参与血红素的代谢, 是细胞对抗应激反应和抗氧化损伤的重要组成部分.
本文通过采用RT-PCR和Western blot技术检测Nrf-2和HO-1的表达情况, 初步解释了叶黄素介导Nrf-2/ARE信号通路抑制人结肠癌HT29细胞增殖的分子机制. 该文章思路清晰, 研究内容新颖合理, 文章具有一定创新性, 有一定的科学意义.
编辑: 于明茜 电编:闫晋利
| 1. | 张 剑, 吴 敏, 张 自森, 王 利娟, 张 红巧, 师 广勇, 巴 楠, 闫 琳, 郑 晓珂, 邢 鑫. 结肠癌组织中SLP-2蛋白的表达及SLP-2基因对HCT-116细胞侵袭、迁移力的影响. 郑州大学学报(医学版). 2014;49:513-516. |
| 4. | Safafar H, van Wagenen J, Møller P, Jacobsen C. Carotenoids, Phenolic Compounds and Tocopherols Contribute to the Antioxidative Properties of Some Microalgae Species Grown on Industrial Wastewater. Mar Drugs. 2015;13:7339-7356. [PubMed] [DOI] |
| 5. | 付 蕾, 陈 晓哲, 张 慧娟, 张 源渊, 王 凌飞, 徐 少博, 张 玉杰, 王 明臣. 叶黄素对人结肠癌HT29细胞增殖的抑制及其机制. 世界华人消化杂志. 2013;21:1239-1244. [DOI] |
| 6. | Park SY, Kim YH, Park G. Cucurbitacins attenuate microglial activation and protect from neuroinflammatory injury through Nrf2/ARE activation and STAT/NF-κB inhibition. Neurosci Lett. 2015;609:129-136. [PubMed] [DOI] |
| 7. | Lau A, Whitman SA, Jaramillo MC, Zhang DD. Arsenic-mediated activation of the Nrf2-Keap1 antioxidant pathway. J Biochem Mol Toxicol. 2013;27:99-105. [PubMed] [DOI] |
| 8. | Suzuki T, Yamamoto M. Molecular basis of the Keap1-Nrf2 system. Free Radic Biol Med. 2015;88:93-100. [PubMed] [DOI] |
| 9. | Shan JL, He HT, Li MX, Zhu JW, Cheng Y, Hu N, Wang G, Wang D, Yang XQ, He Y. APE1 promotes antioxidant capacity by regulating Nrf-2 function through a redox-dependent mechanism. Free Radic Biol Med. 2015;78:11-22. [PubMed] [DOI] |
| 10. | Kim CS, Kwon Y, Choe SY, Hong SM, Yoo H, Goto T, Kawada T, Choi HS, Joe Y, Chung HT. Quercetin reduces obesity-induced hepatosteatosis by enhancing mitochondrial oxidative metabolism via heme oxygenase-1. Nutr Metab (Lond). 2015;12:33. [PubMed] [DOI] |
| 11. | Leenders M, Leufkens AM, Siersema PD, van Duijnhoven FJ, Vrieling A, Hulshof PJ, van Gils CH, Overvad K, Roswall N, Kyrø C. Plasma and dietary carotenoids and vitamins A, C and E and risk of colon and rectal cancer in the European Prospective Investigation into Cancer and Nutrition. Int J Cancer. 2014;135:2930-2939. [PubMed] [DOI] |
| 12. | Kwon SH, Ma SX, Hwang JY, Lee SY, Jang CG. Involvement of the Nrf2/HO-1 signaling pathway in sulfuretin-induced protection against amyloid beta25-35 neurotoxicity. Neuroscience. 2015;304:14-28. [PubMed] [DOI] |
| 13. | Sowmya PR, Arathi BP, Vijay K, Baskaran V, Lakshminarayana R. Role of different vehicles in carotenoids delivery and their influence on cell viability, cell cycle progression, and induction of apoptosis in HeLa cells. Mol Cell Biochem. 2015;406:245-253. [PubMed] [DOI] |
| 14. | Noori S, Hassan ZM. Tehranolide inhibits proliferation of MCF-7 human breast cancer cells by inducing G0/G1 arrest and apoptosis. Free Radic Biol Med. 2012;52:1987-1999. [PubMed] [DOI] |
| 15. | Hashem RM, Rashd LA, Hashem KS, Soliman HM. Cerium oxide nanoparticles alleviate oxidative stress and decreases Nrf-2/HO-1 in D-GALN/LPS induced hepatotoxicity. Biomed Pharmacother. 2015;73:80-86. [PubMed] [DOI] |
| 16. | Lv H, Yu Z, Zheng Y, Wang L, Qin X, Cheng G, Ci X. Isovitexin Exerts Anti-Inflammatory and Anti-Oxidant Activities on Lipopolysaccharide-Induced Acute Lung Injury by Inhibiting MAPK and NF-κB and Activating HO-1/Nrf2 Pathways. Int J Biol Sci. 2016;12:72-86. [PubMed] [DOI] |
| 17. | Lu SH, Hsu WL, Chen TH, Chou TC. Activation of Nrf2/HO-1signaling pathway involves the anti-inflammatory activity of magnolol in Porphyromonas gingivalis lipopolysaccharide-stimulated mouse RAW 264.7 macrophages. Int Immunopharmacol. 2015;29:770-778. [PubMed] [DOI] |
| 18. | Frohlich DA, McCabe MT, Arnold RS, Day ML. The role of Nrf2 in increased reactive oxygen species and DNA damage in prostate tumorigenesis. Oncogene. 2008;27:4353-4362. [PubMed] [DOI] |
| 19. | Das S, Pandey K, Rabidas VN, Mandal A, Das P. Effectiveness of miltefosine treatment in targeting anti-leishmanial HO-1/Nrf-2-mediated oxidative responses in visceral leishmaniasis patients. J Antimicrob Chemother. 2013;68:2059-2065. [PubMed] [DOI] |
| 20. | Sahin K, Tuzcu M, Gencoglu H, Dogukan A, Timurkan M, Sahin N, Aslan A, Kucuk O. Epigallocatechin-3-gallate activates Nrf2/HO-1 signaling pathway in cisplatin-induced nephrotoxicity in rats. Life Sci. 2010;87:240-245. [PubMed] [DOI] |
| 21. | Slattery ML, Pellatt DF, Mullany LE, Wolff RK. Differential gene expression in colon tissue associated with diet, lifestyle, and related oxidative stress. PLoS One. 2015;10:e0134406. [PubMed] [DOI] |
| 22. | Barone E, Cenini G, Sultana R, Di Domenico F, Fiorini A, Perluigi M, Noel T, Wang C, Mancuso C, St Clair DK. Lack of p53 decreases basal oxidative stress levels in the brain through upregulation of thioredoxin-1, biliverdin reductase-A, manganese superoxide dismutase, and nuclear factor kappa-B. Antioxid Redox Signal. 2012;16:1407-1420. [PubMed] [DOI] |
| 23. | Sahoo S, Singh P, Kalha B, Singh O, Pal R. Gonadotropin-mediated chemoresistance: Delineation of molecular pathways and targets. BMC Cancer. 2015;15:931. [PubMed] [DOI] |
| 24. | Zhang S, Li D, Yang JY, Yan TB. Plumbagin protects against glucocorticoid-induced osteoporosis through Nrf-2 pathway. Cell Stress Chaperones. 2015;20:621-629. [PubMed] [DOI] |
| 25. | Chang YJ, Chen WY, Huang CY, Liu HH, Wei PL. Glucose-regulated protein 78 (GRP78) regulates colon cancer metastasis through EMT biomarkers and the NRF-2/HO-1 pathway. Tumour Biol. 2015;36:1859-1869. [PubMed] [DOI] |
| 26. | Sahin K, Tuzcu M, Sahin N, Ali S, Kucuk O. Nrf2/HO-1 signaling pathway may be the prime target for chemoprevention of cisplatin-induced nephrotoxicity by lycopene. Food Chem Toxicol. 2010;48:2670-2674. [PubMed] [DOI] |
| 27. | Seo SH, Jeong GS. Fisetin inhibits TNF-α-induced inflammatory action and hydrogen peroxide-induced oxidative damage in human keratinocyte HaCaT cells through PI3K/AKT/Nrf-2-mediated heme oxygenase-1 expression. Int Immunopharmacol. 2015;29:246-253. [PubMed] [DOI] |
| 28. | Weis S, Bielow T, Sommerer I, Iovanna J, Malicet C, Mössner J, Hoffmeister A. P8 deficiency increases cellular ROS and induces HO-1. Arch Biochem Biophys. 2015;565:89-94. [PubMed] [DOI] |
| 29. | Lee DS, Jeong GS, Li B, Park H, Kim YC. Anti-inflammatory effects of sulfuretin from Rhus verniciflua Stokes via the induction of heme oxygenase-1 expression in murine macrophages. Int Immunopharmacol. 2010;10:850-858. [PubMed] [DOI] |
| 30. | Huang Y, Li W, Su ZY, Kong AN. The complexity of the Nrf2 pathway: beyond the antioxidant response. J Nutr Biochem. 2015;26:1401-1413. [PubMed] [DOI] |