修回日期: 2015-12-21
接受日期: 2016-01-06
在线出版日期: 2016-02-18
随着技术的进步, 胰十二指肠切除术已逐渐在基层医院开展, 该术式是治疗壶腹周围肿瘤及胰头癌的首选术式. 壶腹周围及胰腺肿瘤极易累及周围的重要血管, 意外损伤后如果处理不当可造成严重后果. 因此, 该术式是考验并且反映手术者对上腹部器官解剖、手术技巧以及处理术中突发事件的应变能力. 因此, 在胰十二指肠切除术发生重要血管意外损伤时, 术者应当正确判断并掌握正确的紧急应对措施, 尽量避免意外损伤造成术中死亡及术后并发症的发生.
核心提示: 胰十二指肠切除术由于壶腹周围肿瘤及胰头肿瘤的发病率增高而在二级以上医院广泛应用. 术中发生重要血管意外损伤, 导致患者术中或术后72 h以内死亡以及术后并发症并非罕见. 在术中发生重要血管意外损伤时, 及时、正确、准确的应对策略, 修复、重建损伤的血管, 是避免发生患者死亡和术后并发症发生的重要措施.
引文著录: 管小青, 郑向欣, 吴骥, 顾书成, 吴际生. 胰十二指肠切除术中血管损伤的原因及防治措施. 世界华人消化杂志 2016; 24(5): 657-663
Revised: December 21, 2015
Accepted: January 6, 2016
Published online: February 18, 2016
Pancreaticoduodenectomy is the first choice for the treatment of periampullary tumors, bile duct cancer and pancreatic cancer. The consequence of improper handling during the operation for ampullary carcinoma, pancreatic tumors, and bile duct tumors involving major vessels is serious. Surgeons should master the anatomy of abdominal organs, surgical technique and the ability of handling emergent events. In case of vascular damage in pancreaticoduodenectomy, correct judgment and emergency response measures are important for avoiding intraoperative death and postoperative complications.
- Citation: Guan XQ, Zheng XX, Wu J, Gu SC, Wu JS. Reasons and preventive measures for vascular damage in pancreaticoduodenectomy. Shijie Huaren Xiaohua Zazhi 2016; 24(5): 657-663
- URL: https://www.wjgnet.com/1009-3079/full/v24/i5/657.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v24.i5.657
胰头癌及壶腹周围癌(vater ampulla carcinoma, VPC)常常需要施行胰十二指肠切除术(pancreaticoduodenectomy, PD). PD是消化道外科的经典术式, 其具有一定的风险性和复杂性. 同时PD具有一定的挑战性, 说他具有挑战性是基于PD所涉及的手术创面巨大, 与邻近血管关系复杂, 操作难度大, 手术过程中避免医源性血管损伤, 尤其肠系膜上动脉(superior mesenteric artery, SMA)损伤是每个腹部外科医生所关心的问题. PD术中医源性血管损伤具有突发性和隐匿性等特点, 往往是在术前没有判断出血管的变异或血管受到肿瘤的侵犯, 极易发生损伤, 尤其是重要动脉的损伤可直接威胁患者生命, 并给手术者带来巨大压力, 如果处理不当可导致灾难性的后果, 应引起高度重视.
在应用腔镜施行PD成为热点的今天[1-3], 常规的PD仍然有许多并发症发生, 其发生率在20%-40%之间[4,5]. 这些并发症包括术后出血、胰瘘、感染和胃排空障碍等, 经过近年来手术技术的改进, 这些并发症已经明显下降. 随着PD范围的扩大和手术例数的增多, 术中血管损伤应予重视也值得探讨. 而术中血管损伤是PD最为凶险的情况, 也会使手术者处于最为尴尬的境地.
PD由于手术方式复杂, 切除范围较大, 术中发生重要血管意外损伤的比例相对较多, 这些血管的损伤, 无疑都是医源性损伤(iatrogenic vascular injury, IVI)[6,7], 多数是肠系膜上静脉(superior mesenteric vein, SMV)、门静脉(portal vein, PV)系统, 苏州大学附属第三医院张彤等[8]于2004年报道该院施行64例PD, 在PD术中意外损伤SMV/PV 5例, 占同期PD的7.1%, 5例中死于术中大出血3例. 云南省临沧市人民医院肝胆外科李留峥等[9]于2014年报道该院于2006-01/2014-04在施行PD中共发生SMV/PV 8例, 其中也有2例因术中大出血死亡.
上海第二医科大学附属瑞金医院的上海消化外科研究所彭承宏等[10]于2005年报道该研究所施行207例PD, 术中发生医源性重要动脉损伤5例, 占同期PD的2.4%.
PD术中发生意外损伤的重要血管, 分为动脉损伤和静脉损伤[11]. 这里不包括因为肿瘤浸润而主动行血管切除、修补或者重建等情况.
标准的PD术中需要处理的主要动脉有以下动脉, 包括胃网膜右动脉(right gastroepiploic artery)、胃右动脉(right gastric artery, RGA)、胃十二指肠动脉(gastroduodenal artery)、胰十二指肠上前动脉(ASPDA)、上后动脉(PSPDA)、胰十二指肠下前动脉(AIPDA)、下后动脉(PIPDA)、空肠起始部的系膜内动脉等. 在处理这些动脉时或者在PD术中行淋巴结廓清对肝固有动脉(proper hepatic artery, PHA)、肝动脉(hepatic artery, HA)、SMA骨骼化时, 特别容易损伤这些重要动脉. 按照发生率的排序动脉损伤包括肝右动脉、肝左动脉、肝总动脉、肠系膜上动脉等[5,9,12].
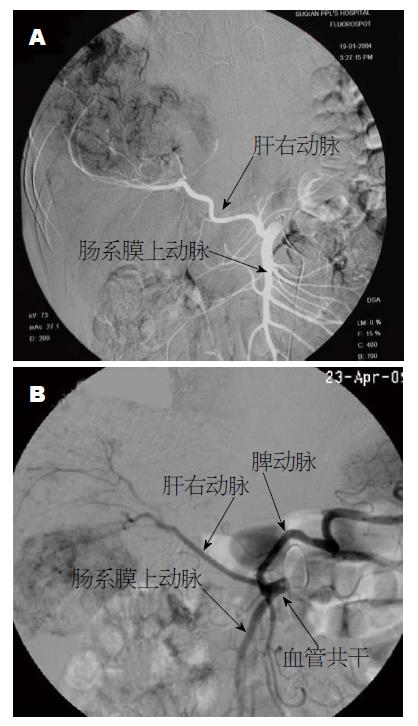
3.1.1 肝动脉损伤: 由于肿瘤巨大局部侵及HA, 切除肿瘤时致使HA血管侧壁的损伤是肝动脉损伤的主要原因. 另外, HA变异也是PD术中发生动脉损伤的重要原因之一, 据报道55%-79%的患者存在HA变异, 其中异位肝右动脉者占11.0%-21.0%, 多起源于SMA(图1A); 异位肝左动脉者占3.8%-10.0%, 多起源于胃左动脉; 异位肝总动脉者占0.4%-4.5%, 也多发源于SMA[13,14]; 变异的HA有时起源于腹腔干, 与胃十二指肠动脉关系易造成混淆, 术中可能在错误的位置离断胃十二指肠动脉同时导致变异肝动脉损伤[15,16]. 术中损伤异位肝右动脉或异位肝总动脉, 可能导致相应肝段、胆管缺血致吻合口漏、胆汁瘤形成, 甚至肝脓肿、肝功能衰竭.
3.1.2 肠系膜上动脉损伤: SMA受到肿瘤侵犯时, 离断胰腺钩突时因牵拉过度, 将SMA拉至SMV右侧缘, 进行胰腺沟突的切除极易造成损伤, 甚至被结扎、切断; 术中在处理小分支出血时操作不当也易于引起SMA主干的撕裂. 虽然, 临床上报道[9]认为SMA很少发生变异, 但是我们在从事PD手术时, 曾发现1例SMA位于SMV的右侧, 术中被误切、并结扎, 所幸发现及时、应对得当, 未发生术后并发症. 此外, 我们还在术前进行DSA造影检查时发现1例SMA与肝右动脉、脾动脉共干的特殊类型血管变异, 这是术前进行DSA造影检查时发现的重要血管的变异(图1B).
3.2.1 肠系膜上静脉损伤: (1)壶腹部肿瘤、胰腺肿瘤和/或胰腺慢性的炎症对SMV的影响不容忽视, 由于胰腺癌的早期侵袭性生长以及胰腺与SMV的紧邻解剖关系, 特别是当部分胰腺癌患者合并有慢性胰腺炎时, 术中极易在分离过程中发生血管的撕裂伤. 目前随着辅助检查的完善, 螺旋计算机断层扫描(computed tomography, CT)的双期扫描、磁共振扫描能够较为准确的显示出肿瘤对血管壁的包绕及肿瘤或炎症对血管的侵犯、黏连情况, 但是, 如何避免术中重要血管的损伤仍取决于手术者的精细操作; (2)过度的牵拉造成血管的损伤, 从解剖学上看, 胰腺段的门脉系统主要有SV在胰体背侧的中下水平汇入到SMV共同形成PV主干. 在胰腺颈部的下缘右侧有胃结肠静脉的共干即Henle's干汇入SMV. 在胰腺段的SMV的右侧与胰头和钩突之间有2-4支小静脉. 在离断胰颈的同时, 过度的牵拉胰头侧可能会造成这些小静脉在汇入SMV主干部位的撕裂, 发生汹涌的出血. 当过度的牵拉胰体侧也可能会造成SV与SMV交汇处的撕裂. 当过度的牵拉胰腺钩突, 特别是在处理钩突部肿瘤时, 极易造成SMV后壁的撕裂; (3)解剖结构辨认不清的时候, 在游离暴露胰腺头、钩突部及其与肠系膜血管间的关系, 特别是肿瘤发生在胰腺钩突时, 由于解剖结构的辨认不清或经验不足, 可能会在未游离胰腺颈部与血管之间的间隙之前就将SMV甚至连同SMA一并损伤或离断; (4)在分离、断扎分支血管的时候处理不当, 表现在离断胰腺颈部进一步处理血管的下后侧的胰腺钩突时, 由于过度牵拉或分离不当, 可能会造成该部位的分支血管的离断或撕裂. 此时由于出血凶猛、术者惊慌或经验不足, 盲目的钳夹、缝扎会造成更大的损伤, 甚至将SMV完全缝闭. SMV的缝扎表现为小肠颜色变暗、淤血、水肿.
3.2.2 门静脉损伤: (1) 胰腺癌的早期诊断较为困难, 往往就诊时多属中晚期, 病变多已浸润周围组织或已经发生转移, 且胰腺癌、壶腹周围癌多伴有胆道梗阻、胰管阻塞, 导致不同程度的胰腺炎而产生增生、黏连或纤维化, 尤其在合并有慢性胰腺炎的同时而与PV致密黏连, 导致正常解剖间隙不清, 盲目横断胰腺, 分离PV和胰腺之间的间隙时, 易导致PV损伤; (2)PV是由SMV、SV在胰后汇合而成. 胰头、胰颈处有数支小静脉经PV、SMV的侧壁或后壁汇入, 而PV与胰腺的间隙很小, 在分离此间隙及切除钩突时极易撕裂损伤小分支.
3.2.3 脾静脉损伤: (1) 肿瘤累及胰腺体部, 在处理SV向胰腺发出的分支时撕扯造成SV损伤; (2)PD术中SV损伤绝大部分发生在胰腺颈体交界部后方, SV与SMV汇合部附近, 也是在处理分支血管的时候处理不当, 表现在离断胰腺颈部进一步处理血管的下后侧的胰腺钩突时, 由于过度牵拉或分离不当, 可能会造成该部位的分支血管的离断或撕裂到SV.
PD术中发生重要血管意外损伤, 不同于扩大PD术[17-19]. 扩大PD术的定义按照国际胰腺手术研究组(Intenational Study Group for Pancreatic Surgery, ISGPG)规定是指在原有的PD手术基础上, 再切除主要包括邻近侵犯的血管、器官切除及重要血管的重建, 而扩大淋巴结清扫术目前不被纳入其范畴[20,21]. 之所以不同于扩大PD术, 是因为PD术中发生重要血管意外损伤, 是在没有预兆、无心理准备的情况下发生的, 手术者对可能发生的危险没有充分的认知和警觉. 此时, 手术者往往因为术中出血凶猛、助手配合不佳、与术前判断不符等不利因素的情况下, 情绪急躁, 视野不佳时又盲目钳夹止血, 结果适得其反, 造成更大的损伤和出血, 甚至是出现患者死于手术中或手术后72 h以内的尴尬局面[22-24].
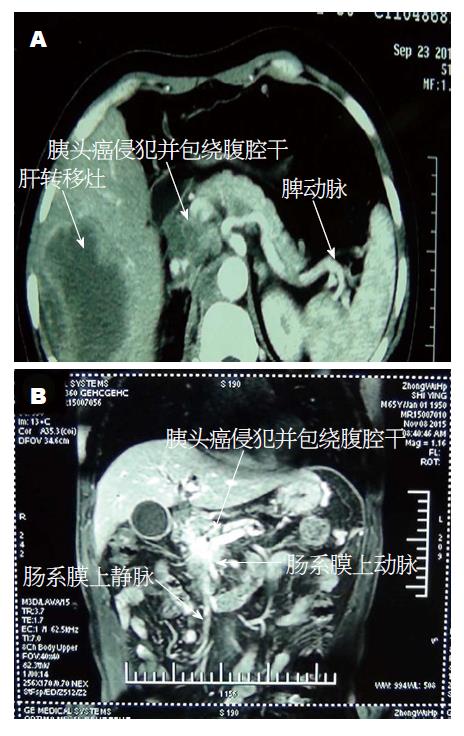
PD术中发生重要血管损伤的预防, 除了在术前认真进行中对胰腺癌的可切除性进行评估时, 对病程、临床表现、肿瘤分期和术前影像学检查是否有血管浸润和远处转移等指标进行评估, 术前认真阅读CT或磁共振成像(magnetic resonance imaging, MRI), 对于胰腺肿瘤巨大累及SMV/PV系统不是手术禁忌, 但是同时累及SMA等重要血管时, 就要做姑息性减黄手术, 或者放弃手术治疗, 进行化学治疗[25,26](图2).
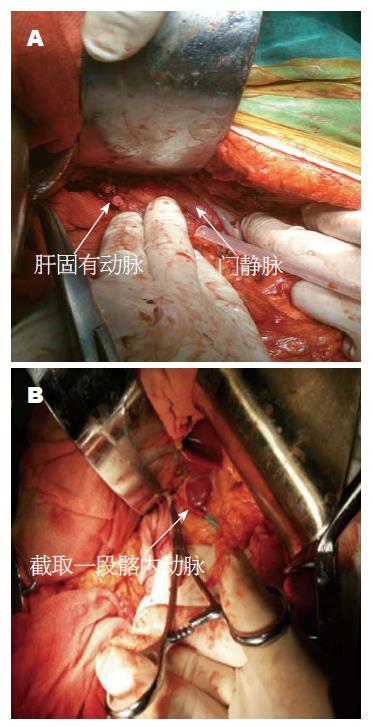
由于重要动脉损伤后, 动脉的压力高, 以至于在瞬间发生大量出血, 而且此时动脉周围尚未充分得到分离和显露, 情急之下术者有时会用血管钳或组织钳钳夹破口, 然后行局部修补. 但是, 破口处的钳夹, 往往越夹破口就越大, 其原因主要是动脉内膜脆弱、易断; 加之此类患者多数年龄较大, 多有动脉硬化, 钳夹损伤的动脉时导致血管内膜局部脱落, 造成血管腔部分阻塞或形成血栓从而影响血流. 此时, 手术者应当以左手拇指、食指和中指, 捏压出血处的血管, 迅速吸出积血, 充分显露出血处的术野, 根据损伤的血管进行不同方式的应急处理. 如果确定损伤的是一可结扎的小动脉断端, 离主干有2 mm以上, 可直接用血管钳夹并结扎; 如在1 mm以下则需用5-0、6-0的Prolene线缝扎; 若是一可结扎小动脉的侧壁, 应缝扎出血点的两端予以止血. 如果是重要动脉侧壁的出血, 手术者在边压边吸边退缩压迫, 以显露出一小部分出血的动脉侧壁, 在直视下用Prolene线迅速逐针缝合修补, 也可用无损伤血管夹或Satinsky钳夹住后修补. 对于损伤的动脉壁大于管壁的1/4以上, 修补后可能会导致的动脉狭窄、影响血供时, 应当进一步对损伤动脉充分游离, 用动脉哈巴狗钳夹住两端, 果断行节段切除, 修剪断端内膜面用5-0、6-0的Prolene线外翻端端吻合, 进行动脉重建(图3A). 我们有1例, 为SMA位于SMV右侧, 被误切长度>4 cm以上, 无法进行端端吻合, 而裁剪PHA后, 利用PHA近端与SMA远端进行端端吻合重建SMA, 再应用胃左动脉与PHA远端进行端端吻合, 重建PHA并获得成功(图1). 对于HA和/或PHA损伤, 是否需要进行重建, 有两种不同的观点: 一种观点是正常HA或PHA仅提供肝脏25%血供和30%-50%的氧, 而SMV或PV为肝脏提供了至少75%血供和50%-70%氧; 此外, HA或PHA血流阻断后, 45%病例96 h内就有侧支循环来自膈、肋间血管、镰状韧带以及邻近的肝叶[36-38]. 因此, 不必为损伤、切断HA或PHA而担忧肝脏的血供和氧供[39,40]. 另一种观点是HA或PHA损伤后不进行重建修复, 会增加肝功能衰竭、肝脓肿、胆瘘等并发症的发生率, 原因是虽然肝实质由动脉和门静脉双重供血, 但是胆管及其上皮组织仅依赖于动脉供血, 其血液来源于肝动脉大部分终末分支所形成的肝门部胆管周围血管丛(peribiliary blood plexus, PBP), 因此直接结扎损伤的HA、PHA会造成患者肝组织缺血性损害, 如肝坏死、肝脓肿、胆肠吻合口漏等并发症发生率会明显增高[41-44]. 我们比较倾向于后一观点, 在不增加手术难度的前提下, 尽可能的应用自体血管修复、重建损伤的HA、PHA. 修复、重建损伤的HA、PHA的方法: 损伤<4 cm长度的肝动脉和/或肝固有动脉, 直接行HA和/或、PHA端端吻合; HA和/或PHA损伤长度>4 cm行胃左动脉-肝固有动脉端端吻合; 或切取一段髂内动脉或大隐静脉行HA和/或PHA吻合重建, 可修复损伤HA和PHA长度达到8 cm(图3B).
PD是壶腹周围肿瘤及胰头癌的主要术式. 该术式的实施需要术者术前对患者的病情充分评估, 包括一般情况, 影像学检查等, 同时对术中可能出现的突发事件能有及时有效的应对措施, 应用动静脉优先显露方法进行解剖、分离, 避免或减少术后并发症的发生. 我们结合自己在PD中所遇到的实际问题, 总结了术中血管损伤的原因、预防及应对措施, 希望能对临床医生的工作有所帮助.
胰十二指肠切除术手术创面大, 操作难度大, 术中医源性血管损伤具有突发性和隐匿性等特点, 特别是肠系膜血管损伤可直接威胁患者生命, 并给手术者带来巨大压力, 如果处理不当可导致灾难性的后果.
翟博, 副主任医师, 哈尔滨医科大学附属第四医院普通外科; 李哲夫, 主任医师, 青岛市中心医院肝胆外科
对于胰十二指肠切除术血管损伤的处理, 有两种不同的观点, 即肝动脉(hepatic artery, HA)或肝固有动脉(proper hepatic artery, PHA)损伤后是否予以重建修复, 目前大多数学者的观点是在不增加手术难度的前提下, 尽可能的应用自体血管修复、重建损伤的HA或PHA.
彭承宏等于2005年报道该研究所施行207例胰十二指肠切除术, 术中发生医源性重要动脉损伤5例, 占同期胰十二指肠切除术的2.4%.
在实施胰十二指肠切除术中, 术中若出现血管损伤时, 研究者给出了积极的处理措施, 特别是对于肠系膜上、动静脉等重要血管损伤的处理, 给出了具体的处理措施, 如吻合方式及选用的材料等.
结合我们在临床上的经验和教训, 总结胰十二指肠切除术中血管损伤的原因、预防及处理措施, 避免或减少术后并发症的发生.
动、静脉优先处理: 是指在胰十二指肠切除术中优先全程游离门静脉和/或肠系膜上静脉、肠系膜上动脉, 使之与胰头、胰腺钩突完全分离, 避免术中发生重要血管意外损伤.
本文对胰十二指肠切除术中血管损伤的原因及防治措施进行全面论述, 具有一定的临床参考价值.
编辑: 郭鹏 电编:都珍珍
| 1. | Mollberg N, Rahbari NN, Koch M, Hartwig W, Hoeger Y, Büchler MW, Weitz J. Arterial resection during pancreatectomy for pancreatic cancer: a systematic review and meta-analysis. Ann Surg. 2011;254:882-893. [PubMed] [DOI] |
| 6. | Mandolfino T, Canciglia A, Taranto F, D'Alfonso M, Tonante A, Mamo M, Sturniolo G. Outcome of iatrogenic injuries to the abdominal and pelvic veins. Surg Today. 2008;38:1009-1012. [PubMed] |
| 7. | Rudström H, Bergqvist D, Björck M. Iatrogenic vascular injuries with lethal outcome. World J Surg. 2013;37:1981-1987. [PubMed] |
| 10. | 彭 承宏, 程 东峰, 沈 柏用, 杨 卫平, 陶 宗元, 丁 家增, 李 宏为. 胰十二指肠切除术中医源性动脉损伤的处理和预防(附5例报告). 中国实用外科杂志. 2005;25:540-542. |
| 11. | Chiang KH, Chang PY, Lee SK, Yen PS, Ling CM, Lee WH, Lee CC, Chou ASB. Angiographic evaluation of hepaticartery variations in 405 cases. Chin J Radial. 2005;30:75-81. |
| 13. | Shukla PJ, Barreto SG, Kulkarni A, Nagarajan G, Fingerhut A. Vascular anomalies encountered during pancreatoduodenectomy: do they influence outcomes? Ann Surg Oncol. 2010;17:186-193. [PubMed] |
| 17. | 管 小青, 陈 焰, 顾 书成, 吴 骥, 吴 建强, 吴 际生, 惠 本军, 张 亚锦, 陈 冬民, 凌 冰. 扩大胰十二指肠切除术中联合肝动脉、肝固有动脉与髂内静脉切除重建应用的可行性研究. 中国普外基础与临床杂. 2012;19:181-187. |
| 19. | 管 小青, 顾 书成, 吴 骥, 郑 向欣, 张 旭旭, 袁 牧, 吴 建强, 陈 焰, 吴 际生. 联合肝叶及入肝血管切除和重建治疗肝门部胆管癌的临床研究. 中国普外基础与临床杂志. 2015;22:64-69. |
| 20. | Hartwig W, Vollmer CM, Fingerhut A, Yeo CJ, Neoptolemos JP, Adham M, Andrén-Sandberg A, Asbun HJ, Bassi C, Bockhorn M. Extended pancreatectomy in pancreatic ductal adenocarcinoma: definition and consensus of the International Study Group for Pancreatic Surgery (ISGPS). Surgery. 2014;156:1-14. [PubMed] |
| 21. | Worni M, Castleberry AW, Clary BM, Gloor B, Carvalho E, Jacobs DO, Pietrobon R, Scarborough JE, White RR. Concomitant vascular reconstruction during pancreatectomy for malignant disease: a propensity score-adjusted, population-based trend analysis involving 10,206 patients. JAMA Surg. 2013;148:331-338. [PubMed] [DOI] |
| 22. | 李 留峥, 俸 家伟, 彭 联芳, 向 春明, 徐 雷升, 王 志萍, 张 洪波, 于 杰. 肠系膜上静脉损伤8例教训分析. 中国普外基础与临床杂志. 2015;22:95. |
| 25. | 杨 尹默, 高 红桥, 庄 岩, 田 孝东. 胰十二指肠切除术若干技术问题的探讨. 中华普外科手术学杂志(电子版). 2015;9:235-239. |
| 27. | Perwaiz A, Singh A, Singh T, Chaudhary A. Incidence and management of arterial anomalies in patients undergoing pancreaticoduodenectomy. JOP. 2010;11:25-30. [PubMed] |
| 33. | 彭 淑牗, 李 江涛, 秦 仁义, 刘 颖斌, 洪 德飞, 王 建伟, 王 敏, 吴 文广, 黄 从云. 腹膜后淋巴脂肪板层根治性切除术-胰头癌根治术的新策略. 中华肝胆外科杂志. 2015;21:437-441. |
| 34. | 王 敏, 朱 峰, 田 锐, 石 程剑, 彭 丰, 徐 盟, 秦 仁义. 全动脉优先离断法在Ⅱ型胰头癌根治性切除中的应用价值. 中华肝脏外科手术学电子杂志. 2014;3:341-344. |
| 37. | 洛 树东, 高 振平. 医用局部解剖学(第7版). 北京: 人民卫生出版社 2008; 193. |
| 38. | 黄 洁夫, 陈 孝平, 董 家鸿. 肝胆胰外科学(第4版). 北京: 人民卫生出版社 2010; 37. |
| 42. | 李 文岗, 李 滨, 黄 志强, 万 涛, 许 东辉, 薛 斌党, 姜 志国. 失去肝动脉血液供应后大鼠肝门部胆管周围血管丛变化的三维构像研究. 中华器官移植杂志. 2006;27:149-151. |
| 46. | Christians K, Evans DB. Pancreaticoduodenectomy and vascular resection: persistent controversy and current recommendations. Ann Surg Oncol. 2009;16:789-791. [PubMed] [DOI] |
| 49. | Zhou Y, Zhang Z, Liu Y, Li B, Xu D. Pancreatectomy combined with superior mesenteric vein-portal vein resection for pancreatic cancer: a meta-analysis. World J Surg. 2012;36:884-891. [PubMed] [DOI] |
| 50. | Ouaissi M, Hubert C, Verhelst R, Astarci P, Sempoux C, Jouret-Mourin A, Loundou A, Gigot JF. Vascular reconstruction during pancreatoduodenectomy for ductal adenocarcinoma of the pancreas improves resectability but does not achieve cure. World J Surg. 2010;34:2648-2661. [PubMed] [DOI] |
| 51. | Chu CK, Farnell MB, Nguyen JH, Stauffer JA, Kooby DA, Sclabas GM, Sarmiento JM. Prosthetic graft reconstruction after portal vein resection in pancreaticoduodenectomy: a multicenter analysis. J Am Coll Surg. 2010;211:316-324. [PubMed] [DOI] |
| 52. | 李 星, 王 孟皓, 张 艳, 龚 建平. 手术治疗乏特壶腹区恶性肿瘤的疗效评估. 中国现代普通外科进展. 2015;18:196-201. |