修回日期: 2014-11-03
接受日期: 2014-11-12
在线出版日期: 2015-01-08
目的: 评价利那洛肽与安慰剂对比在便秘型肠易激综合征(irritable bowel syndrome with constipation, IBS-C)患者中的疗效及安全性.
方法: 中国期刊全文数据库(China National Knowledge Internet, CNKI)、中国生物医学文献数据库(China Biology Medicine, CBM)、中国万方数据库、中国维普数据库、PubMed、Embase、Web of science、Cochrane library和clinical trials.gov等数据库中关于利那洛肽应用于成人IBS-C的与安慰剂对照的随机对照试验. 结果用RevMan v5.2版本统计了相对危险因素(relative risk, RR)和95%可信区间(confidence intervals, CI)等二分类资料.
结果: 检索出符合要求的关于利那洛肽用于IBS-C的3个随机对照试验的4篇公开发表的文章. 主要观察指标为: 腹痛的效果(RR = 1.58, 95%CI: 1.02-2.46); 对完全性自发排便(complete spontaneous bowel movements, CSBMs)的改善(RR = 3.19, 95%CI: 2.40-4.25); 患者生活质量的改善(RR = 1.38, 95%CI: 1.09-1.74). 利那洛肽还在改善大便性状、减少腹痛、腹胀和所有严重症状方面发挥作用. 与安慰剂相比, 腹泻是利那洛肽最常发生的不良反应.
结论: 通过本研究比较得知, 利那洛肽与安慰剂相比, 能改善肠道功能, 减轻腹痛症状和改善IBS-C患者的生活质量.
核心提示: 利那洛肽在能改善便秘型肠易激综合征(irritable bowel syndrome with constipation, IBS-C)患者的肠道功能, 腹痛和IBS-C患者的生活质量. 合并效应的估计利那洛肽比安慰剂治疗IBS-C的患者大. 这种效果大小的估计, 再加上良好的安全性和耐受性, 表明利那洛肽在IBS-C的治疗效果显著.
引文著录: 黄显斌, 郭天康, 杨屹立, 王辉. 利那洛肽对便秘型肠易激综合征有效并改善患者生活质量的Meta分析. 世界华人消化杂志 2015; 23(1): 156-162
Revised: November 3, 2014
Accepted: November 12, 2014
Published online: January 8, 2015
AIM: To perform a meta-analysis to determine the efficacy and the safety of linaclotide, compared with placebo, for patients with irritable bowel syndrome with constipation (IBS-C).
METHODS: CNKI, CBM, Wanfang, VIP, PubMed, EMBASE, clinical trials.gov and the Cochrane library were searched for randomized, placebo controlled trials examining the effect of linaclotide in adults with IBS-C. Dichotomous results were pooled by using the RevMan v.5.2 software to yield relative risks (RRs) and 95% confidence intervals (CIs).
RESULTS: The search identified three randomized controlled trials of linaclotide in patients with IBS-C published in four papers. Meta-analysis suggested that linaclotide significantly improved abdominal pain (RR = 1.58, 95%CI: 1.02-2.46), complete spontaneous bowel movements (CSBMs) (RR = 3.19, 95%CI: 2.40-4.25) and quality of life (RR = 1.38, 95%CI: 1.09-1.74). Linaclotide also improved stool form and reduced the severity of abdominal pain, bloating and overall symptoms in patients with IBS-C. Diarrhoea was the most frequent adverse event (AE) in the group of linaclotide.
CONCLUSION: Our study suggests that linaclotide significantly improves bowel function, reduces abdominal pain and improves quality of life in patients with IBS-C.
- Citation: Huang XB, Guo TK, Yang YL, Wang H. Linaclotide improves quality of life in patients with irritable bowel syndrome with constipation: A Meta-analysis. Shijie Huaren Xiaohua Zazhi 2015; 23(1): 156-162
- URL: https://www.wjgnet.com/1009-3079/full/v23/i1/156.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i1.156
肠易激综合征(irritable bowel syndrome, IBS)是一种病因不明确的以结肠慢性和复发性症状为特点的一种疾病. 这种特征为慢性或复发性的腹痛、腹胀、黏液便和排便的不规律[1]. 全世界大约有10%-20%的成年人和青少年受IBS的影响[1-3]. 但是不同的国家发病率有所差别, 据报道北美的发病率为10%-15%, 平均为11.8%; 欧洲的发病率为6.2%-12%, 平均为11.5%; 我国统计的肠易激综合征的发病率为5%-6%[2-7]. IBS的症状不仅对患者的健康相关的生活质量产生不利影响[8], 而且还会增加社会的财政负担, 因为减少工作效率和对疾病治疗、研究相关的投入的增高[9,10]. 肠易激综合征包括便秘型、腹泻型、混合型和不能定型四个亚型[11]. 便秘型肠易激综合征(irritable bowel syndrome with constipation, IBS-C)大约占IBS的1/3[8], 女性发病率高于男性[12], 并经常包括诸如腹胀、大便干燥、排便费力及里急后重等症状[1,6]. 目前IBS-C的治疗主要是针对患者的腹部疼痛不适症状的, 应用最多抗抑郁药物减轻患者腹痛等症状, 但是抗抑郁药有加重患者便秘的可能性, 因此, 需要寻找新的药物来治疗IBS-C. 利那洛肽, 一种新研制的用于治疗IBS-C的药物. 一种含14个氨基酸残基的鸟苷酸环化-C(GC-C)激动剂. 在动物身上, 利那洛肽减少内脏疼痛的机制被认为是由增加的细胞外cGMP降低疼痛感觉神经的活性所介导[13-16]. 在临床试验中, 利那洛肽在改善IBS-C患者的肠道和腹部症状方面显示出有效而被美国食品和药品监督管理局(Food and Drug Administration, FDA)批准用于成人IBS-C的治疗[17]. 本研究主要是对利那洛肽与安慰剂对照治疗IBS-C的随机对照试验进行系统评价, 应用Meta分析方法对利那洛肽改善IBS-C患者症状及生活质量做一评价.
该Meta分析在整个过程中始终遵循PRISMA原则, 结果也按此呈现[18]. 本研究检索了中国期刊全文数据库(China National Knowledge Internet, CNKI)、中国生物医学文献数据库(China Biology Medicine, CBM)、中国万方数据库、中国维普数据库、PubMed、Embase、Web of science、Cochrane library和clinical trials.gov等数据库. 检索的主题词包括: 利那洛肽, 肠易激综合征, Linaclotide, M-100, Irritable Bowel Syndrome, IBS, Bowel dysfunction, Intestinal disorders, Intestinal dysfunction. 本检索条件无时间限制, 其中评估利那洛肽应用于成人IBS的有效性, 与安慰剂随机对照试验符合纳入标准. IBS的诊断可基于罗马Ⅱ或Ⅲ标准.
1.2.1 文献的筛选: 两个人研究者独立的对符合标准的文献进行系统的筛选. 那些具有前瞻性的公开发表的关于口服利那洛肽和安慰剂治疗IBS-C的有效性, 并报道了纳入病例数的最终的药物有效的病例数的原始资料的随机对照试验(randomized clinical trial, RCT)属于最终符合纳入标准. 文章与两个独立的研究者根据预先制定的纳入和排除标准进行筛选评估. 两个研究者对某些文献有分歧时通过讨论解决. 所要求的研究必须具有一个主要的观察指标, 无论是二分类的计数资料或者是肠道症状或腹痛从基线水平改变, 或者他们的任意组合.
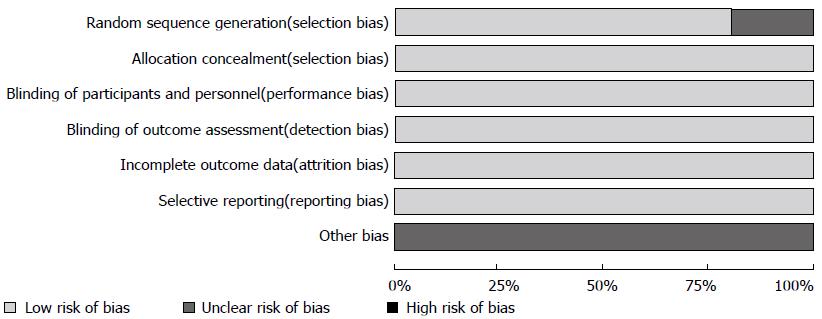
1.2.2 数据提取和偏倚风险评估: 两个研究者对数据进行提取, 除了实验纳入的病例数, 对利那洛肽治疗的结果的观察指标外, 还提取了各实验的病例的年龄, 性别, 诊断标准和治疗周期等一般资料. 偏倚的风险是根据Cochrane小组的建议进行评估. 在6个领域评估偏倚, 分别是: 随机序列生成(选择偏倚)、分配和隐藏(选择偏倚)、参与者和工作人员双盲(实施偏倚)、不完整的数据结果(数据丢失偏倚)、选择性报告(报告偏倚)以及其他偏倚(如利益冲突). 用来评估一个研究偏倚风险高低的标准在Cochrane手册第8章中进行了描述. 在评估偏倚风险的6个方面, 只要有一个属于高风险, 则该研究的偏倚风险为高风险, 所有6个方面都是低风险, 则该研究属于低偏倚风险, 而偏倚风险不明确是指在6个方面不清楚属于高风险还是低风险[19,20].
为了防止重复的数据导致最后疗效被高估, 对检索的研究分别通过作者单位、姓名和研究发表时间进行审查和评估. 这在Cochrane手册上关于干预性系统评价有说明[19]. 由于试验数偏少, 将通过主要结果来评估发表偏倚.
1.2.3 结果评价: 主要的结果评价为利那洛肽与安慰剂对比治疗IBS-C的有效性. 主要的评价结果为消化系症状从基线水平的改善程度, 如每周CSBMs的次数; 或者腹部症状, 比如腹痛、腹胀; 12 wk腹部疼痛/不适的缓解率; 患者生活质量的改善. 这些观察指标是作者所选定的, 我们所研究的二分类结果是基于肠道功能、腹部症状或者他们的结合的有意义的变化所占的比例. 这是在与FDA建议或欧洲药品管理局(European Medicines Agency, EMA)的建议一致的.
统计学处理 所有的统计学分析都是由RevMan v.5.2软件[21]实现的. 首先, 每个研究中利那洛肽与安慰剂的有效性的相对危险因素(relative risk, RR)和95%可信区间(confidence intervals, CI)是基于意向性治疗(intention-to-treat, ITT)人群来计算的, 治疗的不良反应的比值比(odds ratio, OR)和95%CI也是基于ITT人群计算的. 而不同研究之间的异质性通过I2统计量来检验[22](I2<50%说明同质性好, 各研究之间的异质性小). 用事先设定好的随机效应模型来评估效果的大小[23]. 95%CI通过危险差的倒数来计算. 因为随机对照试验中采取了多个剂量组[24], 我们从中选取290 µg剂量组来进行比较, 而这也是通过FDA批准的安全剂量.
总共检索出符合要求的4篇文献[24-27], 涉及3个RCT, 其中1篇文献报道了符合EMA标准的两个实验(实验31和实验302)[26]. 各文献特征如表1. 各文献的偏倚风险如图1.
| 纳入的文献 | 研究方法 | 患者总数 | 利那洛肽用量 | 治疗时间 | IBS-C患者诊断标准 | 观察结果 |
| Johnston等[24], 2010 | RCT、分配隐藏、双盲 | 419 | 75 μg; 150 μg; 300 μg; 600 μg口服, 1次/d | 12 wk治疗期 | 罗马Ⅱ | CSBMs |
| Chey等[25], 2012 | RCT、分配隐藏、双盲 | 804 | 290 μg口服, 1次/d | 26 wk治疗期 | 罗马Ⅱ | 腹痛, CSBMs |
| Quigley等[26], 2013 | ||||||
| 实验31 | RCT、分配隐藏、双盲 | 800 | 同Rao等[27], 2012 | 生活质量 | ||
| 实验302 | RCT、分配隐藏、双盲 | 804 | 同Chey等[25], 2012 | 生活质量 | ||
| Rao等[27], 2012 | RCT、分配隐藏、双盲 | 800 | 290 μg口服, 1次/wk | 12 wk治疗, 停药4 wk | 罗马Ⅱ | 腹痛, CSBMs |
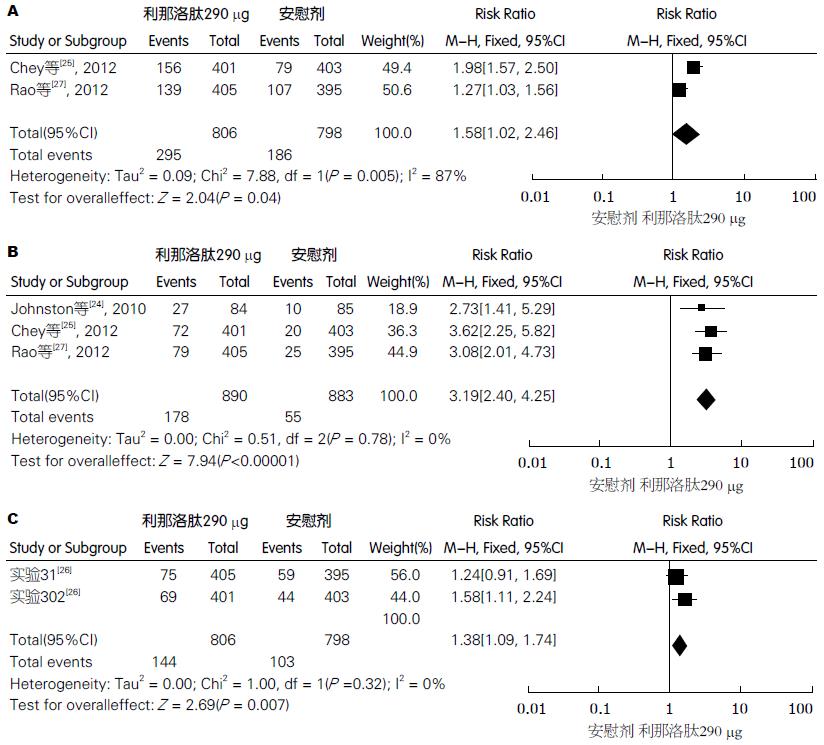
纳入的2个RCT实验[25,27]报道了腹痛的有效性(12个治疗周中有9个治疗周中每周从基线中有≥30%的缓解)的RR = 1.58, 95%CI: 1.02-2.46, 各研究资料之间存在较大的异质性(I2 = 87%; P = 0.005)(图2A).
纳入的3个RCT实验[24,25,27]报道了对CSBMs的作用(12个治疗周中有9个治疗周中每周≥3次或者每周从基线中增加≥1次)RR = 3.19, 95%CI: 2.40-4.25, 各研究之间没有显著的异质性(I2 = 0%, P = 0.78)(图2B)
纳入的2个RCT实验[26]报道了患者生活质量的变化(包括焦虑、对活动的干扰、身体形象、对健康的忧虑、对食物的禁忌、社交、性生活、人际关系)的RR = 1.38和95%CI: 1.09-1.74, 各研究之间没有显著的异质性(I2 = 0%, P = 0.32)(图2C).
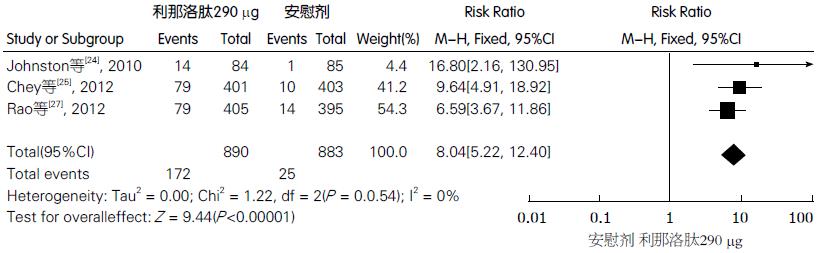
利那洛肽组和安慰剂组分别有525和463例患者在治疗期间至少出现1次治疗相关不良反应(P<0.05), 合并OR = 1.31, 95%CI: 1.08-1.58. 在接受利那洛肽治疗组中有3.8%的患者出现严重不良反应, 而在安慰剂组这一比例为2.3%. 最常见的治疗后出现的不良事件(treatment-emergent adverse events, TEAE)是腹泻, 他在利那洛肽组中更加频繁地发生(图3). 通过所有的研究比较, 利那洛肽组与安慰剂组发生腹泻的OR = 8.04, 95%CI: 5.22-12.40. 其他不良反应有: 腹痛、胀气、头痛、腹胀、上呼吸道感染等在利那洛肽组和安慰剂组之间差异无统计学意义.
该系统评价和Meta分析表明, 利那洛肽治疗比安慰剂治疗IBS-C更有效. 利那洛肽治疗组的所有观察结果: 主要结果腹痛, 排便频率都有所改善, 利那洛肽还能改善患者的生活质量.
利那洛肽被证实是安全的, 耐受性好; 所有不良反应为中度和轻度, 利那洛肽组和安慰剂组之间没有显著差异, 除了腹泻, 与安慰剂相比, 这更频繁的发生在利那洛肽组患者中. 但腹泻并没有减少IBS-C患者的治疗满意度[28,29].
此系统评价和Meta分析的优势包含严格的方法学. 对检索策略, 纳入资格标准和数据的提取过程进行了详细的描述. 另外文献检索, 纳入资格评估, 并提取数据分别由两个人进行了评论, 有任何差异, 通过协商解决. 采用ITT分析方法, 所有失访的人群认为治疗失败, 并应用随机效应模型汇总数据, 以减少利那洛肽疗法对IBS-C的任何有益的影响被高估的可能性.
本研究的限制, 与任何系统评价和Meta分析一样, 源于实验研究的质量和报告的真实性. 本Meta分析存在一下不足: (1)利那洛肽在IBS-C的随机对照试验的绝对数量很少. 在循证医学的时代, 随机对照试验被广泛接受为不同的治疗方法进行比较的黄金标准工具. 虽然各个试验由大量的受试者参加对此进行了补偿, 在未来的临床试验利那洛肽的效应是否将保持不变仍有待证实; (2)IBS-C的患者的入选和排除标准是基于广泛接受罗马标准, 目前还不清楚时, 如果IBS-C的临床定义发生变化的话, 在未来的试验中应用利那洛肽的作用大小是否会保持不变; (3)这个Meta分析的观察结果是基于FDA和EMA建议, 可能无法反映真实情况, 利那洛肽的效果评价标准在不同的国家是不同的, 此两项建议(FDA和EMA建议)在实际上对IBS-C患者我们应该使用哪一个[30]. 然而, 利那洛肽与安慰剂比较改善个人的症状和最终结果所带来的好处得到实际研究的支持; (4)有两个试验[25,27]没有利那洛肽剂量范围的研究, 也没有和别的药物的对比研究, 人们可以假设更低剂量的利那洛肽可耐受性更好而完全没有失去效力. 包括在研究中的另一个固有的限制可能是因为对大便习惯和症状的判定而自发揭盲. 当测量结果是通过对患者主观报告来评价时这揭盲则具有更大的相关性, 因为如果患者知道他或她正在接受哪种治疗方案时, 两种治疗方案的治疗效果和不良事件信息可能会受到影响[31].
在腹痛效果研究之间的异质性显著, 然而, 这两个试验[25,27]的一致性是很好. 应当强调的是, 虽然这些治疗在短期内是安全的, 但是他们的长期安全性仍然是未知的. 更多利那洛肽的随机对照试验正在进行中, 让我们期待这些研究的结果吧. 对于治疗IBS-C, 这也似乎是有效的新药物, 对正在开发中的新药物, IBS-C患者和医生有理由保持谨慎乐观.
总之, 在大型, 高品质, 和同质试验中, 利那洛肽在能改善IBS-C患者的肠道功能, 腹痛和IBS-C患者的生活质量. 合并效应的估计利那洛肽比安慰剂治疗IBS-C的患者大. 这种效果大小的估计, 再加上良好的安全性和耐受性, 表明利那洛肽在IBS-C的治疗效果显著. 在更广泛的人群中药物的有效性, 与更多症状的严重程度不同的患者中的有效性值得进一步研究.
肠易激综合征(irritable bowel syndrome, IBS)是一种病因不明确的以结肠慢性和复发性症状为特点的一种疾病. 全世界大约有10%-20%的成年人和青少年受IBS的影响. IBS对患者的健康和生活质量产生不利影响, 目前无特效治疗药物, 近来有研究表明利那洛肽可缓解便秘型肠易激综合征(irritable bowel syndrome with constipation, IBS-C)的症状并改善患者生活质量. 本课题从循证医学的角度做进一步研究.
白爱平, 副教授, 江西省南昌大学第一附属医院消化病研究所
本课题纳入目前为止关于利那洛肽治疗IBS-C的研究, 利那洛肽治疗IBS-C并改善患者生活质量. 纳入的研究都是国外的研究, 国内缺乏这方面的研究.
本课题研究了利那洛肽治疗IBS-C的主要症状方面的效果及安全性, 并研究了利那洛肽在改善IBS-C患者生活质量方面的疗效.
本课题结果提示利那洛肽治疗IBS-C有效并安全, 能成为IBS-C治疗的一种新的方法.
意向性治疗(intention-to-treat, ITT): 临床情况错综复杂, 在任何一项临床试验中, 患者对治疗的实施率不可能达到100%, 在试验和进一步观测过程中, 会出现出组情况. 这种出组在临床试验的特定情况, 常常各组之间例数是不平衡的, 这种差别影响到他们之间作比较的合理性. 在具体处理时有一个非常简单而重要的原则, 就是不按患者在研究过程中实际所接受的治疗分组, 而仍按患者入组时的组别分析, 也即按治疗意向ITT分析, 否则就会引入偏差.
本文作者荟萃分析了那洛肽与安慰剂对比在IBS-C患者中的疗效及安全性, 选题准确.
编辑: 郭鹏 电编:都珍珍
| 1. | Rhee PL. [Definition and epidemiology of irritable bowel syndrome]. Korean J Gastroenterol. 2006;47:94-100. [PubMed] |
| 2. | Saito YA, Schoenfeld P, Locke GR. The epidemiology of irritable bowel syndrome in North America: a systematic review. Am J Gastroenterol. 2002;97:1910-1915. [PubMed] [DOI] |
| 3. | Lovell RM, Ford AC. Global prevalence of and risk factors for irritable bowel syndrome: a meta-analysis. Clin Gastroenterol Hepatol. 2012;10:712-721.e4. [PubMed] [DOI] |
| 4. | Quigley EM, Abdel-Hamid H, Barbara G, Bhatia SJ, Boeckxstaens G, De Giorgio R, Delvaux M, Drossman DA, Foxx-Orenstein AE, Guarner F. A global perspective on irritable bowel syndrome: a consensus statement of the World Gastroenterology Organisation Summit Task Force on irritable bowel syndrome. J Clin Gastroenterol. 2012;46:356-366. [PubMed] [DOI] |
| 5. | Liu J, Hou X. A review of the irritable bowel syndrome investigation on epidemiology, pathogenesis and pathophysiology in China. J Gastroenterol Hepatol. 2011;26 Suppl 3:88-93. [PubMed] [DOI] |
| 6. | Hungin AP, Whorwell PJ, Tack J, Mearin F. The prevalence, patterns and impact of irritable bowel syndrome: an international survey of 40,000 subjects. Aliment Pharmacol Ther. 2003;17:643-650. [PubMed] [DOI] |
| 8. | Drossman DA, Camilleri M, Mayer EA, Whitehead WE. AGA technical review on irritable bowel syndrome. Gastroenterology. 2002;123:2108-2131. [PubMed] [DOI] |
| 9. | Paré P, Gray J, Lam S, Balshaw R, Khorasheh S, Barbeau M, Kelly S, McBurney CR. Health-related quality of life, work productivity, and health care resource utilization of subjects with irritable bowel syndrome: baseline results from LOGIC (Longitudinal Outcomes Study of Gastrointestinal Symptoms in Canada), a naturalistic study. Clin Ther. 2006;28:1726-1735; discussion 1710-1711. [PubMed] [DOI] |
| 10. | DiBonaventura M, Sun SX, Bolge SC, Wagner JS, Mody R. Health-related quality of life, work productivity and health care resource use associated with constipation predominant irritable bowel syndrome. Curr Med Res Opin. 2011;27:2213-2222. [PubMed] [DOI] |
| 11. | Longstreth GF, Thompson WG, Chey WD, Houghton LA, Mearin F, Spiller RC. Functional bowel disorders. Gastroenterology. 2006;130:1480-1491. [PubMed] |
| 12. | Lovell RM, Ford AC. Effect of gender on prevalence of irritable bowel syndrome in the community: systematic review and meta-analysis. Am J Gastroenterol. 2012;107:991-1000. [PubMed] [DOI] |
| 13. | Bryant AP, Busby RW, Bartolini WP, Cordero EA, Hannig G, Kessler MM, Pierce CM, Solinga RM, Tobin JV, Mahajan-Miklos S. Linaclotide is a potent and selective guanylate cyclase C agonist that elicits pharmacological effects locally in the gastrointestinal tract. Life Sci. 2010;86:760-765. [PubMed] [DOI] |
| 14. | Busby RW, Kessler MM, Bartolini WP, Bryant AP, Hannig G, Higgins CS, Solinga RM, Tobin JV, Wakefield JD, Kurtz CB. Pharmacologic properties, metabolism, and disposition of linaclotide, a novel therapeutic peptide approved for the treatment of irritable bowel syndrome with constipation and chronic idiopathic constipation. J Pharmacol Exp Ther. 2013;344:196-206. [PubMed] [DOI] |
| 15. | Eutamene H, Bradesi S, Larauche M, Theodorou V, Beaufrand C, Ohning G, Fioramonti J, Cohen M, Bryant AP, Kurtz C. Guanylate cyclase C-mediated antinociceptive effects of linaclotide in rodent models of visceral pain. Neurogastroenterol Motil. 2010;22:312-e84. [PubMed] [DOI] |
| 17. | Ray K. IBS: Linaclotide approved for constipation-predominant IBS. Nat Rev Gastroenterol Hepatol. 2012;9:616. [PubMed] [DOI] |
| 18. | Moher D, Liberati A, Tetzlaff J, Altman DG. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. Ann Intern Med. 2009;151:264-269, W64. [PubMed] [DOI] |
| 19. | Julian PT Higgins, Green S. Cochrane handbook for systematic reviews of interventions. Version 5.1.0 [updated March 2011]. The Cochrane Collaboration. 2011; Available from: http://www.cochrane-handbook.org. |
| 20. | Lundh A, Gøtzsche PC. Recommendations by Cochrane Review Groups for assessment of the risk of bias in studies. BMC Med Res Methodol. 2008;8:22. [PubMed] [DOI] |
| 21. | Review Manager (RevMan) [Computer program]. Version 5.2. Copenhagen: The Nordic Cochrane Centre, the Cochrane Collaboration 2012; . |
| 22. | Cochran WG. The Combination of estimates from different experiments. Biometrics. 1954;10:101-129. |
| 23. | DerSimonian R, Laird N. Meta-analysis in clinical trials. Control Clin Trials. 1986;7:177-188. [PubMed] [DOI] |
| 24. | Johnston JM, Kurtz CB, Macdougall JE, Lavins BJ, Currie MG, Fitch DA, O'Dea C, Baird M, Lembo AJ. Linaclotide improves abdominal pain and bowel habits in a phase IIb study of patients with irritable bowel syndrome with constipation. Gastroenterology. 2010;139:1877-1886.e2. [PubMed] [DOI] |
| 25. | Chey WD, Lembo AJ, Lavins BJ, Shiff SJ, Kurtz CB, Currie MG, MacDougall JE, Jia XD, Shao JZ, Fitch DA. Linaclotide for irritable bowel syndrome with constipation: a 26-week, randomized, double-blind, placebo-controlled trial to evaluate efficacy and safety. Am J Gastroenterol. 2012;107:1702-1712. [PubMed] [DOI] |
| 26. | Quigley EM, Tack J, Chey WD, Rao SS, Fortea J, Falques M, Diaz C, Shiff SJ, Currie MG, Johnston JM. Randomised clinical trials: linaclotide phase 3 studies in IBS-C - a prespecified further analysis based on European Medicines Agency-specified endpoints. Aliment Pharmacol Ther. 2013;37:49-61. [PubMed] [DOI] |
| 27. | Rao S, Lembo AJ, Shiff SJ, Lavins BJ, Currie MG, Jia XD, Shi K, MacDougall JE, Shao JZ, Eng P. A 12-week, randomized, controlled trial with a 4-week randomized withdrawal period to evaluate the efficacy and safety of linaclotide in irritable bowel syndrome with constipation. Am J Gastroenterol. 2012;107:1714-1724; quiz p.1725. [PubMed] [DOI] |
| 28. | Carson R, Tourkodimitris S, Lewis BE, Johnston JM. Effect of linaclotide on quality of life in adults with irritable bowel syndrome with constipation: Pooled results from two randomized, double-blind, placebo-controlled phase 3 trials. Gastroenterology. 2011;140:S51-S51. [DOI] |
| 29. | Carson RT, Tourkodimitris S, Lewis BE, Johnston JM. PWE-127 Two randomised, double-blind, placebo-controlled phase 3 trials of linaclotide in adults with irritable bowel syndrome: Effects on quality of life. Gut. 2012;61:A348-A349. [DOI] |
| 30. | Corsetti M, Tack J. FDA and EMA end points: which outcome end points should we use in clinical trials in patients with irritable bowel syndrome? Neurogastroenterol Motil. 2013;25:453-457. [PubMed] [DOI] |