修回日期: 2014-09-28
接受日期: 2014-10-02
在线出版日期: 2014-12-28
目的: 建立高效液相荧光法测定人血浆中多潘立酮的浓度, 考察不同多潘立酮制剂的人体药动学特性.
方法: 血浆样品中加入内标盐酸普萘洛尔溶液, 经乙醚萃取后, 采用高效液相荧光法测定人血浆中多潘立酮的浓度. 用建立的方法测定24例男性健康志愿者单剂量口服受试制剂(多潘立酮分散片)或参比制剂(多潘立酮片)后的血药浓度, 求得药动学参数, 并对2种制剂的生物等效性进行评价.
结果: 多潘立酮在质量浓度为0.1-8.0 µg/mL的范围内呈现良好的线性关系, 所建立的方法日内精密度变异标准差分别为4.9%、1.8%和7.7%; 日间精密度异标准差分别为8.1%、5.3%和6.7%, 平均提取回收率为85.6%, 平均方法回收率为96.8%, 血浆和标准血样中内标对照品在-20 ℃冰箱保存12 d、反复冻融3次后含量未见明显变化, 稳定性符合要求, 受试者单剂量口服受试片及参比片后, Cmax分别为25.71和24.88 ng/mL, Tmax分别为0.718和0.689 h, AUC(0-∞)分别为105.2和107.6 ng/(h·mL). 受试制剂与参比制剂的相对生物利用度为97.76%.
结论: 所建立的人体血浆内多潘立酮的测定方法灵敏, 无杂质干扰. 受试制剂的可信区间均落在参比制剂的可信区间范围内, 个体间无显著性差异, 制剂间也无显著性差异, 两种制剂生物等效.
核心提示: 24名健康志愿者口服两种制剂后血浆中多潘立酮的药时曲线趋势相同. 采与参比组制剂相比, 多潘立酮的相对生物利用度为97.76%. 受试制剂的个体间无显著性差异, 制剂间也无显著性差异, 两种制剂生物等效.
引文著录: 赵传勇, 丁艳芳, 梁辉, 李玲. 消化内科常用药物多潘立酮人体内药物代谢动力学影响. 世界华人消化杂志 2014; 22(36): 5746-5749
Revised: September 28, 2014
Accepted: October 2, 2014
Published online: December 28, 2014
AIM: To determine the concentration of domperidone in human plasma by high performance liquid chromatography (HPLC), and to study the pharmacokinetics of different domperidone preparations in humans.
METHODS: An HPLC-FLD method was developed to determine the concentration of domperidone in human plasma. The test formulation (domperidone dispersible tablets) and reference formulation (domperidone tablets) were given to 24 healthy male volunteers. The pharmacokinetics and bioequivalence of the test formulation and reference formulation were evaluated.
RESULTS: The calibration curve was linear within the range of 0.1-8.0 µg/mL. The method recovery was 96.8%. The relative standard deviations (RSDs) of intra-day and inter-day were less than 15%. Stability met the requirements. The Cmax, Tmax and AUC(0-∞) were 25.71 ng/mL, 0.718 h, and 105.2 ng/(h•mL), and 24.88 ng/mL, 0.689 h, and 107.6 ng/(h•mL), respectively. The relative bioavailability was 97.76%.
CONCLUSION: The method is sensitive without endogenous interference. The two kinds of preparations are bioequivalent.
- Citation: Zhao CY, Ding YF, Liang H, Li L. Pharmacokinetics of different domperidone preparations in humans. Shijie Huaren Xiaohua Zazhi 2014; 22(36): 5746-5749
- URL: https://www.wjgnet.com/1009-3079/full/v22/i36/5746.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i36.5746
多潘立酮(domperidone)是一种抗多巴胺类药物, 能够阻滞外周多巴胺受体, 具有抑制恶心和呕吐的作用, 一般用于口服和静脉注射[1-3]. 另外由于多潘立酮能够刺激脑垂体释放催乳素, 所有还具有促进乳汁分泌的作用[4,5]. 本文采用高效液相色谱法(high performance liquid chromatography, HPLC)测定了24名健康志愿者口服两种不同剂型多潘立酮后的药代动力学和生物利用度, 并进行了生物等效性分析.
24例男性健康志愿者, 年龄均在22-24岁, 随机分成2组, 每组12例. 进行双周期双交叉试验. 志愿者在给药前2 wk至试验结束期间禁止服用其他药物、烟酒且禁止剧烈运动. 受试者禁食12 h后, 温开水服用多潘立酮20 mg, 一组服用受试制剂, 另一组服用参比制剂, 2 wk后进行交叉试验. 分别在志愿者口服给药前和给药后0.08、0.25、0.50、0.75、1、2、4、8、12及24 h上臂静脉取血, 每次5 mL, 采后装入离心管内, 此离心管事先涂好肝素, 在4000 r/min的条件下离心, 时间15 min, 分离出上层血浆, -20 ℃下保存, 待分析.
受试制剂: 多潘立酮分散片(帮能)(江西汇仁药业有限公司, 规格: 10 mg/片, 批号: 20130421), 参比制剂: 多潘立酮片(吗丁啉)(西安杨森制药有限公司, 规格: 10 mg/片, 批号: 121014159), 多潘立酮对照品(中国药品生物制品检定所). L-7100高效液相色谱仪(日本日立公司), 高速微型离心机(上海昨非实验室设备有限公司), VORTEX-5旋涡混合器(上江苏海门其林贝尔仪器制造有限公司).
1.2.1 血浆中样品的提取: 先将200 μL血浆置于1.5 mL离心管内, 加入100 μL的缓冲液(磷酸盐缓冲液, pH 5.0), 涡旋混匀, 加入内标(盐酸普萘洛尔溶液)20 μL, 涡旋混匀, 加入萃取液乙醚800 μL, 涡旋混匀, 在4000 r/min的条件下离心, 时间15 min, 吸出上层有机溶液, 转移到新的离心管中, 用氮气将有机溶液挥干, 残留物用100 μL流动相复溶, 在4000 r/min的条件下离心, 时间15 min, 液相分析. 用标准曲线计算出药物在血浆中的浓度.
1.2.2 血浆内药物的分析: 色谱条件: 色谱柱: Waters C18(200 mm×4.6 mm, 5 μm), C18预柱(50 mm×4.6 mm, 5 μm); 流动相: 0.02 mol/L磷酸二氢钾-乙腈(V:V = 70:30)(用磷酸调节pH值至3.0); 流速: 1.0 mL/min; 检测波长: 荧光波长325 nm; 激发波长285 nm, 柱温: 40 ℃±2 ℃; 进样量: 20 μL.
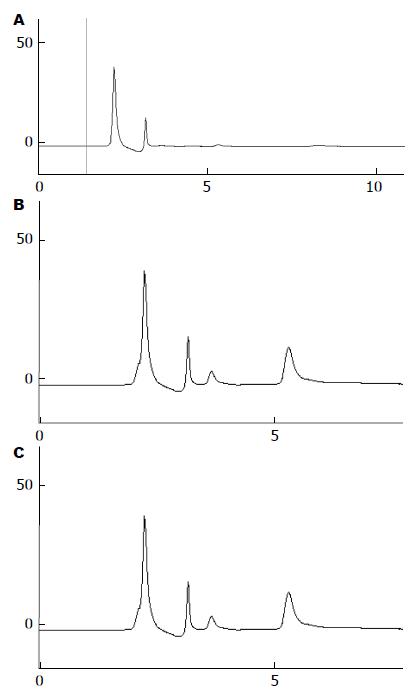
绘制标准曲线: 配制系列标准溶液, 浓度分别为0.5、1.0、2.0、4.0、8.0、16.0和32.0 μg/mL. 在空白甲醇及系列标准工作液中加入空白血浆和盐酸普萘洛尔溶液, 旋涡混匀后, 按照"1.2.1"项下操作, 高效液相色谱测定. 用峰面积与内标峰面积之比(As/Ai)对血浆内药物浓度(C)进行线性回归, 制作标准曲线, 计算出回归方程为: As/Ai = 0.068C-0.005, r = 0.9991; 多潘立酮在质量浓度为0.1-8.0 μg/mL的范围内呈现良好的线性关系(图1).
精密度: 配制高、中、低三个浓度的多潘立酮溶液, 浓度为的1.0、4.0、16.0 μg/mL. 按照"1.2.1"项下操作. 日内精密度: 三种浓度的多潘立酮溶液每个制备5份, 每份测定1次. 日间精密度: 连续5 d, 测定1次/d. 结果: 经测定, 所建立的方法日内精密度变异标准差分别为4.9%、1.8%和7.7%; 日间精密度异标准差分别为8.1%、5.3%和6.7%. 提取回收率: 取空白血浆, 分别加入低中高三个浓度的多潘立酮溶液, 使血浆中多潘立酮浓度分别为的1.0、4.0、16.0 μg/mL, 测定, 另外配制浓度为1.0、4.0、16.0 μg/mL的标准液, 直接用高效液相色谱测定, 计算在相同浓度下, 提取样品与未经提取直接进样的峰面积之比, 比值就是提取回收率, 结果所建立方法的平均提取回收率为85.6%. 方法回收率: 配制高、中、低三个浓度的多潘立酮溶液, 浓度为的1.0、4.0、16.0 μg/mL. 按照"1.2.1"项下操作, 测定药物与内标物的峰面积, 比值R = As/Ai. 将比值代入标准曲线方程计算药物浓度, 测得浓度与实际加入浓度之比即为所建立方法的方法回收率(%), 结果平均方法回收率为96.8%. 所建立方法的精密度与回收率的符符合生物样品的分析要求, 可用于人体血浆多潘立酮的含量测定.
稳定性试验: 配制高、中、低三个浓度的多潘立酮溶液, 浓度为的1.0、4.0、16.0 μg/mL. 在-20 ℃冰箱保存12 d、反复冻融3次. 按"1.2.1"项下方法处理后进样测定. 另取按"1.2.1"项下方法处理后的标准血浆样品放入4 ℃冰箱中, 10 h进样后测定. 计算稳定性. 测定结果表明, 血浆和标准血样中内标对照品的含量未见明显变化, 稳定性符合要求.
统计学处理 应用SPSS13.0软件进行统计学分析, 计量资料采用F检验, 以P<0.05为差异有统计学意义.
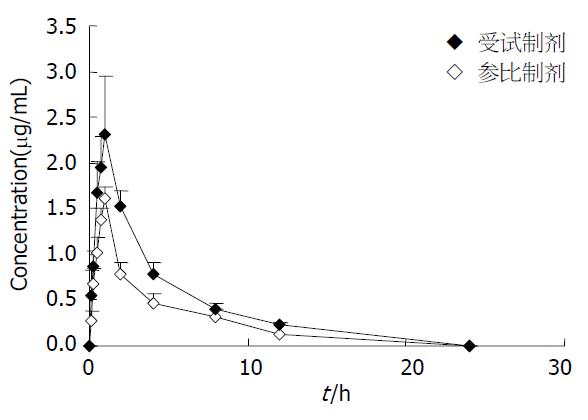
24名健康志愿者口服两种制剂后血浆中多潘立酮的药时曲线趋势相同, 如图2. 采用DAS2.0版药动学分析软件进行人体内药动学数据分析, 与参比组制剂相比, 多潘立酮的相对生物利用度为97.76%. 两种制剂的药动学参数分别如表1.
| 分组 | 单位 | 受试制剂 | 参比制剂 |
| AUC(0-t) | min.µg/mL | 105.1 | 106.3 |
| AUC(0-) | min.µg/mL | 105.2 | 107.6 |
| AUC(0-t)/AUC(0-) | 1 | 0.999 | 0.988 |
| Cmax | µg/mL | 25.71 | 24.88 |
| Tmax | h | 0.718 | 0.689 |
| T1/2 | h | 6.481 | 6.128 |
| F值 | % | 97.76 | 100.0 |
为确证两制剂吸收程度是否生物等效, 对主要药动学参数AUC(0-t)和Cmax分别进行统计分析, 由于AUC(0-t)和Cmax均不呈正态分布, 先将其进行对数转换, 然后进行方差分析(analysis of variance, ANOVA)[6].
本文将两种制剂中多潘立酮的lnAUC(0-t)、lnCmax主要参数分别作方差分析, 进行显著性检验, 结果表明, 受试制剂的可信区间均落在参比制剂的可信区间范围内, 个体间无显著性差异, 制剂间也无显著性差异, 两种制剂生物等效.
血浆样品一般有沉淀法和萃取法两种处理方式[7-11], 本实验用乙醚作萃取液, 盐酸普萘洛尔作内标, 实验结果表明, 所建立的色谱条件能充分分离多潘立酮和其内标对照品, 系统适应性实验结果表明, 所建立方法可用于多潘立酮制剂血浆样品的分析.
多潘立酮在血液中的检测方法文献报道的有很多, 包括HPLC-UV法[12,13]、液质联用法[14]、放射免疫法[15]等. 由于放射性免疫法存在操作繁琐以及较窄的线性范围, 液质联用法的费用又比较高, 本文采用高效液相色谱荧光法, 优于文献报道的其他方法.
尽管多潘立酮的临床疗效已得到广泛评价, 但很多研究样本量较小, 缺乏代表性, 且尚未明确以何种给药途径为宜. 多潘立酮是一种抗多巴胺类药物, 能够阻滞外周多巴胺受体, 具有抑制恶心和呕吐的作用, 一般用于口服和静脉注射.
刘克辛, 教授, 大连医科大学临床药理学教研室
目前市面上的多潘立酮口服剂型有很多, 包括多潘立酮片、多潘立酮口腔崩解片、多潘立酮混悬液、多潘立酮分散片、多潘立酮咀嚼片等, 销售价格也相差很大, 但是各种制剂的吸收情况并不明确, 因此找出多潘立酮的吸收效果好, 价格又的剂型就尤为重要.
目前与本文相关的研究主要包括考察相同剂型的不同厂家生产的多潘立酮片的生物等效性研究.
多潘立酮在血液中的检测方法文献报道的有很多, 包括高效液相色谱法(high performance liquid chromatography, HPLC)-UV法、液质联用法、放射免疫法等. 由于放射性免疫法存在操作繁琐以及较窄的线性范围, 液质联用法的费用又比较高, 本文采用高效液相色谱荧光法, 优于文献报道的其他方法.
多潘立酮在血液中的检测方法文献报道的有很多, 包括HPLC-UV法、液质联用法、放射免疫法等. 由于放射性免疫法存在操作繁琐以及较窄的线性范围, 液质联用法的费用又比较高, 本文采用高效液相色谱荧光法, 优于文献报道的其他方法.
本文采用HPLC测定了24名健康志愿者口服两种不同剂型多潘立酮后的药代动力学和生物利用度, 并进行了生物等效性分析, 对消化医师有一定的参考价值.
编辑: 韦元涛 电编:闫晋利
| 5. | Olausson EA, Brock C, Drewes AM, Grundin H, Isaksson M, Stotzer P, Abrahamsson H, Attvall S, Simrén M. Measurement of gastric emptying by radiopaque markers in patients with diabetes: correlation with scintigraphy and upper gastrointestinal symptoms. Neurogastroenterol Motil. 2013;25:e224-e232. [PubMed] [DOI] |
| 7. | Abdel-Rehim M. Microextraction by packed sorbent (MEPS): a tutorial. Anal Chim Acta. 2011;701:119-128. [PubMed] [DOI] |
| 8. | Abedin MZ, Narins SC, Park EH, Smith PR, Kirkwood KS. Lovastatin alters biliary lipid composition and dissolves gallstones: a long-term study in prairie dogs. Dig Dis Sci. 2002;47:2192-2210. [PubMed] |
| 10. | Dong SH, Lee J, Koh DH, Choi MH, Jang HJ, Kae SH. Pravastatin activates PPARalpha/PPARgamma expression in the liver and gallbladder epithelium of hamsters. Hepatobiliary Pancreat Dis Int. 2011;10:185-190. [PubMed] [DOI] |
| 11. | Jiang SP, Liang RY, Zeng ZY, Liu QL, Liang YK, Li JG. Effects of antireflux treatment on bronchial hyper-responsiveness and lung function in asthmatic patients with gastroesophageal reflux disease. World J Gastroenterol. 2003;9:1123-1125. [PubMed] |
| 13. | Xu DH, Lou HG, Yuan H, Jiang B, Zhou Q, Zhang ZM, Ruan ZR. Quantitative determination of domperidone in human plasma by ultraperformance liquid chromatography with electrospray ionization tandem mass spectrometry. Biomed Chromatogr. 2008;22:433-440. [PubMed] |
| 15. | Krull IS, Szulc ME, Bourque AJ, Zhou FX, Yu J, Strong R. Solid-phase derivatization reactions for biomedical liquid chromatography. J Chromatogr B Biomed Appl. 1994;659:19-50. [PubMed] [DOI] |