修回日期: 2014-05-04
接受日期: 2014-05-06
在线出版日期: 2014-07-28
目的: 研究早期肠内给予卡巴胆碱对弥漫性颅脑损伤后大鼠肠机械屏障的影响.
方法: 采用Marmarou模型制备方法造成成年雄性Wistar大鼠弥漫性颅脑损伤, 造模后成活的大鼠随机分为生理盐水组(NS组, n = 40)及卡巴胆碱组(CAR组, n = 40), 另设只切开头皮的假手术组(对照组, n = 25). 对照组自由饮水, NS组及CAR组从造模成功后2 h开始灌胃, 分别给予生理盐水及卡巴胆碱[100 μg/(kg•12 h)], 于伤后3、6、12、24、48 h活杀取材, 检测血浆中二胺氧化酶(daimine oxidase, DAO)活性、D-乳酸含量及小肠绒毛病理学改变.
结果: 成功复制弥漫性颅脑损伤大鼠模型, 弥漫性颅脑损伤后大鼠肠黏膜固有层水肿, 炎性细胞浸润, 部分黏膜上皮细胞变性、坏死、脱落, 绒毛变短, 在12 h损伤最重, 24 h肠黏膜有增高趋势, CAR组肠绒毛较NS组恢复快, 至48 h肠绒毛高度未恢复至对照组水平, 但无统计学差异. 弥漫性颅脑损伤后血浆中DAO活性及D-乳酸含量较对照组显著升高(P<0.01), 至伤后48 h未恢复至对照组水平(P<0.01). CAR组血浆中DAO活性及D-乳酸含量在伤后3-48 h低于NS组, 除3 h D-乳酸含量降低无统计学意义外均有统计学意义(P<0.05).
结论: 弥漫性颅脑损伤后早期肠内给予卡巴胆碱能减轻肠黏膜损伤, 对肠黏膜机械屏障有一定的保护作用.
核心提示: 在弥漫性颅脑损伤大鼠模型中观察到早期肠内给予卡巴胆碱能减轻肠黏膜损伤, 对肠黏膜机械屏障有一定的保护作用.
引文著录: 唐明贵, 王印华, 王宝华, 浦践一, 邱方, 李志强. 卡巴胆碱对弥漫性颅脑损伤后肠机械屏障的影响. 世界华人消化杂志 2014; 22(21): 3161-3165
Revised: May 4, 2014
Accepted: May 6, 2014
Published online: July 28, 2014
AIM: To investigate the effect of early intestinal carbachol supplementation on intestinal mucosal barrier in rats after diffuse brain injury (DBI).
METHODS: A male adult Wistar rat model of DBI was established by the Marmarou's method. Injured and survived rats were randomly divided into either a normal saline group (NS group, n = 40) or a carbachol group (CAR group, n = 40). Normal saline and carbachol [100 μg/(kg•12 h)] were intragastrically given to animals of the NS and CAR groups 2 h after injury, respectively. Meanwhile, a sham operation group (n = 25) was also included. All animals were sacrificed at 3, 6, 12, 24, 48 h after DBI to determine the activity of plasma DAO and concentration of plasma D-lactate, and to observe intestinal villus changes by microscopy.
RESULTS: DBI was reproduced successfully in rats. Edema of the lamina propria, infiltration of inflammatory cells, degeneration and necrosis of mucosal epithelial cells were most serious at 12 h after DBI induction. The height of intestinal villi had an increasing tendency from 24 h, and intestinal villous changes recovered more significantly at 48 h in the CAR group than in the control group (P > 0.05). The activity of DAO and the content of D-lactate in plasma increased obviously in rats after DBI (P < 0.01), while they did not recover to the level of the sham-operation group at 48 h (P < 0.01). Both the activity of DAO and the content of D-lactate in plasma were significantly lower in the CAR group than in the NS group, except for the content of D-lactate at 3 h after injury (P < 0.05).
CONCLUSION: Early intestinal carbachol supplementation can alleviate intestinal mucosal damage and has an appreciable protective effect on intestinal mucosal mechanical barrier in rats after DBI.
- Citation: Tang MG, Wang YH, Wang BH, Pu JY, Qiu F, Li ZQ. Effect of carbachol on intestinal mucosal barrier in rats after diffuse brain injury. Shijie Huaren Xiaohua Zazhi 2014; 22(21): 3161-3165
- URL: https://www.wjgnet.com/1009-3079/full/v22/i21/3161.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i21.3161
急性胃肠功能障碍在危重患者中发病率高, 若肠黏膜屏障破坏, 肠道内细菌及内毒素移位, 发生肠源性感染可导致全身炎症反应综合征及多脏器功能障碍(multiple organ disfunction syndrome, MODS). 既往的研究[1,2]表明重型颅脑损伤后机体应激反应较重, 肠黏膜屏障遭到破坏, 但目前能确实有效保护肠黏膜屏障的方法并不多. 卡巴胆碱是一种拟胆碱能药物, 研究表明其能促进胃肠动力、增加组织灌注、减轻炎症反应及器官功能损害[3]. 本研究将复制大鼠弥漫性颅脑损伤模型, 观察早期经胃肠道给予卡巴胆碱对肠黏膜机械屏障的影响, 为肠屏障的保护提供可能的实验依据.
成年♂Wistar大鼠159只, 由北京维通利华实验动物技术有限公司提供, 体质量350 g±20 g, 适应性饲养1 wk, 实验前12 h禁食不禁水. 弥漫性颅脑损伤后复苏成功的大鼠随机分为生理盐水组(NS组, n = 40)、卡巴胆碱组(CAR组, n = 40), 另设只切开头皮的假手术组(对照组, n = 25). 3组按伤后3、6、12、24和48 h各分为5个亚组(对照组n = 5, NS组及CAR组n = 8).
1.2.1 模型制备: 采用Marmarou模型[4]制备方法造成大鼠弥漫性颅脑损伤. 对照组自由饮水, NS组及CAR组从复苏成功后2 h开始灌胃, 分别给予生理盐水及卡巴胆碱[100 μg/(kg•12 h)], 间隔6 h一次, 保证每6 h灌胃液体量为15 mL/kg, 不足者加生理盐水.
1.2.2 DAO活性及D-乳酸检测: 于伤后3、6、12、24、48 h活杀取材. 从心尖穿刺抽血送北京304医院创伤研究室由专人用分光光度法检测DAO活性及D-乳酸含量, 检测人员对动物分组完全不知情.
1.2.3 肠绒毛病理学观察: 心尖穿刺采集完血样后立即在距回盲部5 cm处向头部取2 cm小肠进行固定、包埋、切片、HE染色. 采用HPIAS-1000彩色病理图像分析系统观测HE染色切片, 随机全盲测值, 每张切片顺次取奇数视野, 测20个小肠绒毛的高度。
统计学处理 采用SPSS16.0软件进行统计处理. 定量资料以mean±SD表示, 本研究所得的定量资料满足参数检验的前提条件, 故采用两因素成组设计方差分析处理. P<0.05为差异有统计学意义.
134只成年♂Wistar大鼠造模成功后存活80只(各亚组8只), 死亡率40.3%. NS组3、6、24 h的亚组及CAR组6、12、48 h的亚组在伤后3 h前分别有1只死亡, 且多在伤后1 h内死亡. NS组48h的亚组在取材前有1只因误吸而死亡.
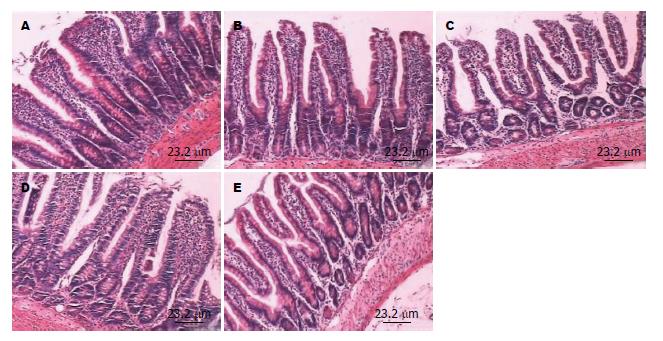
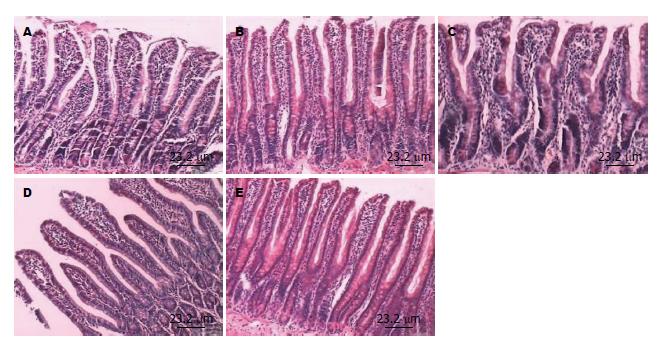
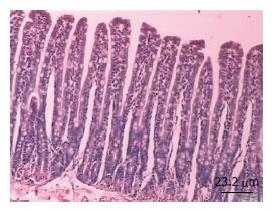
显微镜下弥漫性颅脑损伤后大鼠肠黏膜固有层水肿, 炎性细胞浸润, 部分黏膜上皮细胞变性、坏死、脱落, 绒毛变短、变宽, 在伤后12 h肠黏膜损伤最重, 但CAR组肠黏膜水肿较NS组有所减轻(图1, 图2). 24 h肠黏膜有增高趋势, CAR组较NS组恢复快, 表现为黏膜固有层肠水肿减轻, 肠绒毛变细变高, 绒毛间距变窄, 至伤后48 h未能恢复到对照组水平(图3).
与对照组比较, NS组及CAR组3-24 h肠绒毛高度明显降低, 差异有统计学意义(P<0.01), 至伤后48 h, NS组及CAR组肠绒毛高度均未恢复至对照组水平, 但CAR组与对照组差异无统计学差异(P>0.05), NS组有统计学差异(P<0.01). CAR组与NS组比较, 3-6 h肠绒毛高度无统计学差异(P>0.05), 12-48 h CAR组肠绒毛较NS组升高, 差异有统计学意义(P<0.05), 其中48 h差异显著(P<0.01)(表1).
与对照组相比, NS组及CAR组伤后3-48 h血浆DAO活性均明显升高, 差异有统计学意义(P<0.01). CAR组与NS组比较, 伤后3-48 h DAO活性低于NS组, 3 h差异有统计学意义(P<0.05), 6-48 h差异显著(P<0.01)(表2).
与对照组相比, 伤后3-48 h NS组及CAR组血浆中D-乳酸含量均明显升高, 且差异有统计学意义(P<0.01). CAR组在伤后3-48 h血浆中D-乳酸含量低于NS组, 但在3 h无统计学差异(P>0.05), 6-48 h差异有统计学意义(P<0.01)(表3).
弥漫性颅脑损伤等严重应激后可激活体内神经-内分泌系统, 为保证心、脑等重要器官的血流供应, 发生血流再分布, 胃肠道往往是最先受损伤的器官, 表现为胃肠血流减少. 因肠绒毛毛细血管攀呈极度弯曲的发夹样结构, 加上肠绒毛上皮细胞更新速度快、代谢率高, 故肠绒毛对缺血缺氧非常敏感, 胃肠缺血后肠黏膜上皮细胞易发生坏死、凋亡. 肠壁内富含黄嘌呤氧化酶, 肠道发生缺血再灌注损伤时次黄嘌呤经黄嘌呤氧化酶作用生成黄嘌呤, 释放大量活性氧自由基直接损伤肠黏膜, 胃肠黏膜屏障破坏, 通透性增加. 肠道是体内最大的细菌库, 缺血时肠蠕动减慢, 若肠黏膜屏障破坏, 肠道内细菌及内毒素发生移位, 引发全身炎症反应.
近年来研究发现中枢神经系统可通过胆碱能神经及其递质乙酰胆碱(acetylcholine, Ach)调节或对抗全身性炎症反应, 并将此称为胆碱能抗炎通路[5]. 因直接电刺激迷走神经的操作方法复杂, 组织损伤较重, 容易引起心脏抑制, 而乙酰胆碱的性质不稳定, 烟碱为剧毒, 均难以在临床应用. 而卡巴胆碱是一种人工合成的拟胆碱药物, 性质稳定, 不易被胆碱酯酶水解, 当与M和N胆碱受体结合, 具有完全拟Ach的作用, 且比Ach持久. 既往临床应用其M样作用以扩张血管、促进胃肠动力、增加腺体分泌等. 近年在烧伤模型中观察到口服卡巴胆碱可改善胃排空率、提高平均动脉压、降低胃黏膜二氧化碳分压、提高小肠黏膜血流量、降低二胺氧化酶水平, 使肠系膜细静脉舒张, 加快肠系膜微血管血流速度, 改善肠道微循环、组织灌流和脏器功能[6-8]. 在缺血再灌注模型中应用卡巴胆碱可增加肠黏膜血流量, 改善其肠道运动、吸收、屏障功能, 减轻肠黏膜病理损害[9,10]. 在缺血再灌注及脓毒症模型中均观察到卡巴胆碱能显著抑制促炎细胞因子肿瘤坏死因子-α(tumor necrosis factor-α, TNF-α)、白介素-6(interleukin-6, IL-6)等的产生和释放, 而对抗炎细胞因子IL-10和皮质醇的影响甚微[11-13], 明显减轻肠组织炎症及水肿[14]. 在临床上, 鼻饲卡巴胆碱可降低创伤和感染重症患者血清DAO、D-乳酸和内毒素水平, 改善肠积气, 降低胃肠功能评分[15]; 肌注卡巴胆碱可改善MODS患者肠道功能, 减轻炎症反应[16].
本实验成功复制弥漫性颅脑损伤大鼠模型, 在弥漫性颅脑损伤后大鼠血浆中DAO活性、D-乳酸含量均较对照组明显升高, 肠黏膜炎性细胞浸润, 黏膜水肿, 部分肠黏膜坏死、脱落, 肠绒毛横径增宽, 高度缩短, 隐窝变浅, 证实弥漫性颅脑损伤后大鼠肠黏膜机械屏障遭到严重破坏, 通透性增加. 而CAR组与NS组比较, 6-48 h血浆中DAO活性、D-乳酸含量明显低于NS组(P<0.01), 但两组至伤后48 h仍未能恢复至对照组水平. 光镜下CAR组肠绒毛损伤较NS组轻, 至伤后48 h未完全恢复至对照组水平. 以上研究提示通过胃肠道早期给予卡巴胆碱能减轻弥漫性颅脑损伤后肠黏膜损伤, 降低肠黏膜通透性, 保护肠黏膜机械屏障. 分析其机制可能与卡巴胆碱扩张血管、促进胃肠运动、改善肠道微循环、抑制炎症反应、减轻肠道组织水肿及过氧化损伤等有关. 有研究显示卡巴胆碱发挥作用可能存在一定的剂量依赖关系[17], 在本实验中未观察到卡巴胆碱对大鼠呼吸、心率的明显抑制, 但弥漫性颅脑损伤后胃肠道给予卡巴胆碱至伤后48 h血浆中DAO、D-乳酸及肠绒毛高度未能完全恢复至对照组水平, 仍需进一步实验证实卡巴胆碱的安全剂量及给药途径, 并适当延长实验观察时间.
总之, 卡巴胆碱能减轻弥漫性颅脑损伤后大鼠肠黏膜损伤, 降低肠黏膜通透性, 保护严重应激后的肠黏膜机械屏障, 为其进一步应用于临床提供实验依据.
急性胃肠功能障碍在危重患者中发病率高, 尤其是颅脑损伤者, 肠黏膜屏障破坏后肠道内细菌及内毒素容易发生移位, 发生肠源性感染可导致全身炎症反应综合征及多脏器功能障碍(multiple organ disfunction syndrome, MODS). 但目前能确实有效保护肠黏膜屏障的方法并不多. 近年来胆碱能抗炎通路的提出为肠屏障保护可能提供了一种新的选择. 本研究将复制大鼠弥漫性颅脑损伤模型, 观察早期经胃肠道给予卡巴胆碱对肠黏膜机械屏障的影响, 为肠屏障的保护提供可能的实验依据.
庹必光, 教授, 遵义医学院附属医院消化科
危重患者肠屏障保护及卡巴胆碱的胆碱能抗炎作用是近年来研究的热点, 需大量实验探讨肠屏障的保护措施及卡巴胆碱在不同患者或模型中发挥的作用及机制.
解放军总医院第一附属医院全军烧伤研究所休克与多器官障碍实验室的胡森教授、盛志勇教授等对卡巴胆碱在烧伤、缺血再灌注、脓毒症等模型中发挥的胆碱能抗炎作用做了大量研究. 我院同仁对卡巴胆碱在创伤和感染后胃肠功能障碍患者的保护也做了一些研究.
目前对卡巴胆碱在弥漫性颅脑损伤模型或患者中是否同样能发挥胆碱能抗炎作用的研究较少, 本课题旨在复制弥漫性颅脑损伤模型后探讨卡巴胆碱对肠黏膜机械屏障的影响.
本文设计合理, 指标选择得当, 研究发现卡巴胆碱对颅脑损伤后肠黏膜屏障有一定的保护作用, 有一定的临床价值.
编辑 田滢 电编 鲁亚静
| 2. | 陈 秀凯, 浦 践一, 邱 方, 程 爱国, 刘 刚. 二胺氧化酶与D-乳酸对脑损伤大鼠肠屏障功能的监测意义. 中国煤炭工业医学杂志. 2003;6:669-671. |
| 4. | Marmarou A, Foda MA, van den Brink W, Campbell J, Kita H, Demetriadou K. A new model of diffuse brain injury in rats. Part I: Pathophysiology and biomechanics. J Neurosurg. 1994;80:291-300. [PubMed] |
| 5. | Borovikova LV, Ivanova S, Zhang M, Yang H, Botchkina GI, Watkins LR, Wang H, Abumrad N, Eaton JW, Tracey KJ. Vagus nerve stimulation attenuates the systemic inflammatory response to endotoxin. Nature. 2000;405:458-462. [PubMed] |
| 10. | 邹 晓防, 林 凯, 吕 艺, 黎 君友, 陆 江阳, 胡 森, 盛 志勇. 缺血一再灌流时卡巴胆碱对大鼠肠上皮细胞的保护作用. 世界华人消化杂志. 2007;15:625-628. [DOI] |
| 12. | 姜 小国, 胡 森, 石 德光, 晋 桦, 吕 艺, 韩 翠华, 孙 丹, 盛 志勇. 卡巴胆碱对肠缺血再灌注大鼠血浆肿瘤坏死因子α和白介素-10含量的影响. 中国危重病急救医学. 2003;15:167-169. |
| 17. | Baskin WN. Advances in enteral nutrition techniques. Am J Gastroenterol. 1992;87:1547-1553. [PubMed] |