修回日期: 2013-05-15
接受日期: 2013-05-19
在线出版日期: 2013-06-28
目的: 探讨共聚焦激光内镜检查(confocal laser endoscope, CLE)在胃溃疡性病变诊断中的临床应用价值.
方法: 选取普通内镜下怀疑为恶性胃溃疡性病变的42例患者进行CLE检查及CLE引导下活检. 静脉给予10%荧光素钠溶液对胃黏膜进行荧光染色. 于病变部位采集共聚焦图像, 并在相应的病变部位分别进行靶向活检, 将其组织病理学结果与患者术后组织病理学结果比较进行统计学分析.
结果: CLE诊断38例为恶性溃疡性病变; CLE引导下靶向活检病理学结果为35例为恶性; 随访手术后组织病理学结果40例为恶性. CLE诊断胃溃疡性病变的检出率为95%; CLE靶向活检的检出率为87.50%, CLE靶向活检的组织病理学结果与手术后组织病理学结果之间差异无统计学意义(P>0.05).
结论: CLE可以实现在内镜检查的过程中体内胃黏膜组织的实时组织病理学成像, 并进行靶向活检. CLE与普通内镜相比有助于提高恶性病变检出率, 减少漏诊, 对胃溃疡性病变的良恶性鉴别具有重要的诊断价值.
核心提示: 本文选取普通内镜下怀疑为恶性胃溃疡性病变的42例患者进行共聚焦激光内镜检查(confocal laser endoscope, CLE)检查及CLE引导下活检探讨共聚焦激光内镜检查CLE在胃溃疡性病变诊断中的临床应用价值.
引文著录: 雷天霞, 孙思予, 葛楠, 王晟, 吕庆杰. 共聚焦激光内镜在胃溃疡性病变诊断中的临床应用价值. 世界华人消化杂志 2013; 21(18): 1755-1759
Revised: May 15, 2013
Accepted: May 19, 2013
Published online: June 28, 2013
AIM: To assess the clinical value of confocal laser endoscopy (CLE) in diagnosing ulcerative diseases of the stomach.
METHODS: Forty-two patients with ulcerative lesions in the stomach suspected to be malignant by conventional endoscopy were enrolled in this study and underwent CLE. Fluorescein sodium (5.5 mL of 10% solution) was administered intravenously to enable fluorescent staining of the mucosa of the stomach. Images were acquired from the lesioned areas. Targeting biopsies were performed under the guide of CLE. The detection rate of malignant ulcers was compared between histopathologic diagnosis of postoperative specimens and biopsy targeting specimens.
RESULTS: CLE diagnosed malignant ulcers in 38 patients. Histopathology of biopsy targeting specimens and postoperative specimens detected malignant ulcers in 35 and 40 patients, respectively. The detection rate of malignant ulcers by CLE was 95%, and that by histopathology of biopsy targeting specimens was 87.5%. There was no significant difference in the detection rate of malignant ulcers between histopathology of biopsy targeting specimens and postoperative specimens (P > 0.05).
CONCLUSION: CLE enables real-time histopathologic imaging of gastric mucosa in vivo at the time of endoscopic examination. Compared with conventional endoscopy, biopsy targeting can improve the detection rate of diseases and decrease missed diagnosis. CLE has significant value in diagnosing ulcerative diseases of the stomach.
- Citation: Lei TX, Sun SY, Ge N, Wang S, Lv QJ. Diagnostic value of confocal laser endoscopy in ulcerative diseases of the stomach. Shijie Huaren Xiaohua Zazhi 2013; 21(18): 1755-1759
- URL: https://www.wjgnet.com/1009-3079/full/v21/i18/1755.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v21.i18.1755
普通内镜对于消化系黏膜病变的观察只局限于黏膜表面, 难以对溃疡性病变的良恶性作出精确诊断. 对病变的活组织检查及病理诊断仍为确诊胃恶性病变的金标准, 但是恶性溃疡性病变应用普通内镜进行活检有时会得到阴性结果, 从而导致重复内镜检查和多次活检. 重复内镜检查会增加患者的痛苦, 取材次数的增加, 容易造成出血、穿孔等并发症, 而且, 常规组织病理学需要将组织标本切片、染色后进行光学显微镜下观察, 耗时较长, 可能延误恶性病变的临床诊断和治疗. 近几年出现了共聚焦激光显微镜(confocal laser microscope, LCM), 可以清楚的显示在体黏膜组织的显微结构, 将共聚焦激光内镜整合于传统电子内镜的远端头端诞生了共聚焦激光内镜(confocal laser endoscope, CLE), 其成像基本原理与LCM相似, 可以同时生成共聚焦图像和内镜图像[1,2]. 共聚焦成像系统可以在内镜检查过程中, 对体内黏膜组织进行实时组织学成像, 对病变黏膜进行靶向活检, 有助于提高恶性病变的检出率, 减少临床漏诊, 同时节省时间, 减少了常规组织学检查繁琐的过程, 为体内组织学研究提供了快速、可靠的诊断工具. 已有研究结果表明, CLE检查可以准确地预测结肠新生物的性质, 其敏感度为97.4%, 特异度为99.4%, 准确率为99.2%[1]. 本研究对普通内镜下高度怀疑为恶性胃溃疡性病变的患者进行CLE检查和靶向活检, 初步探讨CLE检查在胃溃疡性病变诊断中的临床应用价值.
选取普通内镜下高度怀疑为恶性胃溃疡性病变的42例患者进行CLE检查. 其中男36例, 女6例, 年龄48-72岁, 平均年龄58.7岁. 该42例患者临床症状分别表现为不同程度的上腹部疼痛、呕吐、呕血、黑便、近期消瘦等. 其中1例为胃癌术后3年的患者, 近期出现上腹隐痛、消瘦等症状. 所有病例均使用CLE为EC-3870FK(Pentax, Tokyo, Japan), 发射波长为488 nm的氩离子激光束扫描目标部位, 从组织表层到深层观察, 根据对比剂的分布对组织进行分析. CLE远端头端和插入镜管直径为12.8 mm, 远端头端包含一个水和气体喷嘴、两个光导束、一个辅助喷水孔道(用于局部应用对比剂)和一个2.8 mm的工作孔道. 成像平面的深度由手柄上的两个遥控按钮控制. 选用荧光素钠原液(flurescein, 20%浓度3 mL/支)静脉注射后采集共聚焦图像. 所有病例均行荧光素钠试敏. 取20%荧光素钠原液0.25 mL加入生理盐水至5 mL, 配制成1%的荧光素钠皮试液. 将剩余的20%的荧光素钠2.75 mL加生理盐水至5.5 mL配制成10%的荧光素钠溶液准备内镜检查时静脉注射.
1.2.1 检查操作: 术前准备如同常规内镜检查. 患者在检查当天禁食水, CLE检查前, 2%利多卡因胶浆15 mL口咽部局部麻醉, 同时行荧光素钠皮试. 将已配比好的1%荧光素钠溶液5 mL缓慢静脉注射, 15 min后观察结果. 患者如有血压、脉搏、呼吸和面色等全身改变为试敏阳性, 不能进行CLE检查. 如患者无过敏反应, 待内镜医师开始行CLE检查前30 s, 将10%的荧光素钠溶液5.5 mL静脉注射. 首先对普通视野下可见的溃疡性病变进行观察, 然后开启显示屏上激光发射按钮, 随之使共聚焦激光内镜头端轻柔地与目标黏膜接触, 通过内镜手柄上的按钮调整选取检查部位扫描平面的深浅, 踩脚踏板以采集图像, 将共聚焦图像及普通内镜图像保存. 每例患者检查用时约20-30 min.
1.2.2 靶向活检: CLE检查过程中, 开启显示屏上激光发射按钮, 观察到CLE发射到病变黏膜表面的蓝色激光点, 使用内镜吸引孔道将该处病变黏膜轻轻吸起, 形成一个红色的点状区域, 随后在该处进行活组织取材(活检数目为2-6块). 最后组织病理学诊断由病理学医师通过HE染色后常规光学显微镜下观察得出结果. 所有行CLE检查的患者均无穿孔、出血等并发症发生. 所有患者在确诊后均接受了手术治疗.
1.2.3 诊断标准: 根据共聚焦激光图像中显示的胃小凹及腺体的形态、细胞的大小、形态及排列、腺体周围毛细血管袢的结构形态来判断胃溃疡性病变的良恶性.
正常胃黏膜共聚焦图像显示胃小凹开口形状多为圆形(胃体)、椭圆形(贲门周围)或裂缝样(胃窦); 腺体排列规整, 柱状上皮整齐排列在基底膜上, 不存在杯状上皮细胞; 胃小凹和腺体周围的毛细血管袢形态为蜂窝状或网织状.
恶性溃疡性病变黏膜的共聚焦图像表现为: 胃小凹失去正常形态, 腺体结构破坏, 排列不规整; 细胞大小不等、结构紊乱, 着色差、呈团块状、梭状聚集; 腺体周围的毛细血管袢结构不规则或消失, 间质内对比剂着色增强.
统计学处理 对CLE下靶向活检标本与手术后标本的组织病理学资料进行分析, 经χ2检验, 计算P值. P<0.05时认为差异有统计学意义.
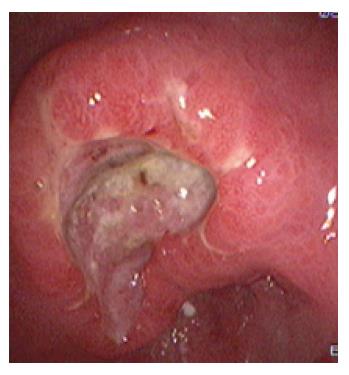
本研究入组常规胃镜检查怀疑恶性溃疡性病变的42例患者, 其病变部位在内镜视野下大致表现为溃疡形态不规则, 底部凹凸不平, 表面白苔或污秽苔, 边缘黏膜隆起(图1).
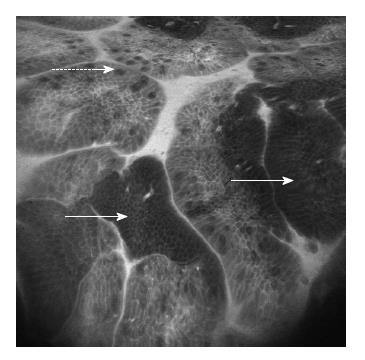
经CLE检查诊断其中有38例为恶性溃疡性病变. 其共聚焦图像中(图2)观察到病变部位失去正常胃小凹的形态结构, 且小凹之间的间隙消失, 胃小凹开口失去圆形或裂缝样形态; 细胞大小不等, 着色差, 呈团块状聚集(粗箭头所示), 散在较多杯状细胞(细箭头所示); 腺体周围看不到正常蜂窝状的毛细血管袢结构. 而正常黏膜的共聚焦图像无此表现.
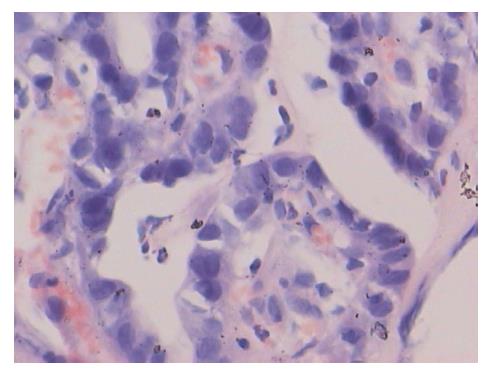
CLE下靶向活检标本的组织病理学结果35例为恶性; 随访手术后组织病理学结果40例为恶性, 包括31例腺癌和9例印戒细胞癌, 其余2例为重度慢性炎症伴中度不典型增生. 经过规律的制酸及保护胃黏膜治疗, 2 mo后随访此2例患者再次胃镜检查示溃疡病灶较前缩小, 活检检查仍确诊为慢性胃溃疡. 确诊为胃癌的组织病理学结果显示腺体形态不规则, 结构紊乱; 癌细胞的大小及形态不一致, 细胞体积变大, 核浆比例增大, 核深染(图3). 将CLE下靶向活检标本与手术后标本的组织病理学资料之间进行比较(表1).
| 恶性 | 非恶性 | 合计 | |
| 靶向活检标本组织病理学 | 35 | 7 | 42 |
| 手术后标本组织病理学 | 40 | 2 | 42 |
| 合计 | 75 | 9 | 84 |
本研究中, CLE诊断胃恶性溃疡性病变的检出率为95%(38/40); CLE靶向活检对恶性溃疡性病变的检出率为87.50%(35/40), CLE靶向活检的组织病理学结果与手术后组织病理学结果之间差异进行统计分析, 结果显示差异无统计学意义(P>0.05).
在临床上胃溃疡性病变常需要进行良恶性鉴别, 其内镜下特点分别表现为: 良性溃疡多呈圆形或椭圆形, <2 cm, 底平坦, 表面覆着黄白苔, 边缘整齐光滑; 恶性溃疡多呈不规则形, >2 cm, 底凹凸不平, 苔污秽, 边缘黏膜呈"堤坝样"隆起, 向溃疡聚集的皱襞有融合中断现象. 对于普通内镜下怀疑恶性溃疡的病变进行活检常得到阴性结果, 需要在短期内重复内镜检查并多次、多点取材, 导致出血、穿孔等并发症的发生率增高, 而且常规组织病理学检查过程耗时较长, 更有甚者根据一次阴性活检结果给予患者抑制胃酸药物治疗, 可能会延误病情.
CLE检查是一项新的内镜检查技术, 他的特点就是在内镜检查的过程中对体内胃黏膜组织进行实时组织学成像, 为体内组织学研究提供了快速可靠的诊断工具. 他平行于正常胃黏膜组织进行扫查, 通过荧光素钠对比剂的使用清楚地显示胃小凹、胃腺体、柱状上皮细胞及环绕胃小凹和腺体的蜂窝状的毛细血管袢, 与正常胃黏膜的组织病理学相一致[3,4]. 有研究表明, 对新鲜未处理的正常胃肠黏膜和癌性胃肠黏膜标本行CLE检查, 结果显示CLE检出癌变的敏感性为85.7%, 特异性为92.0%, 总的诊断精确度为89.7%[5].
本研究中, CLE诊断胃恶性溃疡性病变的检出率为95%, CLE靶向活检的检出率为87.50%, CLE靶向活检的组织病理学结果与手术后组织病理学结果之间差异无统计学意义(P>0.05), 结果显示在该内镜下靶向活检与普通内镜相比有助于提高恶性病变检出率, 减少漏诊, 并且一定程度上减少活检次数和标本数目, 从而减少活检相关的出血、穿孔等并发症的发生. 这表明该内镜技术在胃溃疡性病变诊断中有重要的临床应用价值, 为恶性病变的临床及时诊断和早期治疗带来新的方法.
值得注意的是, 共聚焦成像中图像伪像常干扰内镜诊断, 一般常见因素包括共聚焦成像窗与病变不平黏膜的不良接触、胃腔内黏液中的杂质造成图像出现黑色斑点、胃的蠕动及患者的呼吸运动等. 有报道显示, 所获得的上消化道共聚焦图像中, 由蠕动和呼吸运动造成的运动伪像占38%[6]. 但是这些伪像一般比较容易辨别. 在接触病变部位之前用生理盐水冲洗该部位, 或者断开后重新直接接触病变部位并保持稳定、仔细操作内镜等均可减少图像伪像的干扰.
由于该内镜技术尚处于初步研究阶段, 本次研究的病例数较少, 目前使用的荧光剂、氩激光束的穿透力、CLE的分辨率等许多不足之处, 故该内镜的诊断准确性还需要进一步研究证实. 目前已有研究表明使用CLE可以在活体内检测到幽门螺杆菌[7]、确诊Barrett食管[8]及相关新生物[9]、监测溃疡性结肠炎[10,11]、诊断胶原性结肠炎[12,13]及诊断结肠上皮内瘤变[14]和结直肠癌[15]. 相信随着光学纤维镜及激光扫描等技术的进步, 以及对其他对比剂的进一步应用, CLE可以逐渐完善, 实时地从分子及细胞水平诊断消化系疾病.
普通内镜对于消化系黏膜病变的观察只局限于黏膜表面, 难以对溃疡性病变的良恶性作出精确诊断. 对病变的活组织检查及病理诊断仍为确诊胃恶性病变的金标准, 但是恶性溃疡性病变应用普通内镜进行活检有时会得到阴性结果,从而导致重复内镜检查和多次活检. 重复内镜检查会增加患者的痛苦, 取材次数的增加, 容易造成出血、穿孔等并发症, 而且, 常规组织病理学需要将组织标本切片、染色后进行光学显微镜下观察, 耗时较长, 可能延误恶性病变的临床诊断和治疗.
陈其奎, 教授, 中山大学附属第二医院消化内科; 任建林, 教授, 厦门大学附属中山医院消化内科
近几年出现了共聚焦激光显微镜(confocal laser microscope, LCM), 可以清楚的显示在体黏膜组织的显微结构, 将共聚焦激光内镜整合于传统电子内镜的远端头端诞生了共聚焦激光内镜(confocal laser endoscope, CLE), 其成像基本原理与LCM相似, 可以同时生成共聚焦图像和内镜图像. 共聚焦成像系统可以在内镜检查过程中, 对体内黏膜组织进行实时组织学成像, 对病变黏膜进行靶向活检, 有助于提高恶性病变的检出率, 减少临床漏诊, 同时节省时间, 减少了常规组织学检查繁琐的过程, 为体内组织学研究提供了快速、可靠的诊断工具.
CLE可以实现在内镜检查的过程中体内胃黏膜组织的实时组织病理学成像, 并进行靶向活检. CLE与普通内镜相比有助于提高恶性病变检出率, 减少漏诊, 对胃溃疡性病变的良恶性鉴别具有重要的诊断价值.
本研究探讨了共聚焦激光内镜检查在胃溃疡性病变诊断中的临床应用价值, 科学性较好, 文献阅读较充分.
编辑: 田滢 电编:闫晋利
| 1. | Kiesslich R, Burg J, Vieth M, Gnaendiger J, Enders M, Delaney P, Polglase A, McLaren W, Janell D, Thomas S. Confocal laser endoscopy for diagnosing intraepithelial neoplasias and colorectal cancer in vivo. Gastroenterology. 2004;127:706-713. [PubMed] [DOI] |
| 2. | Goetz M, Hoffman A, Galle PR, Neurath MF, Kiesslich R. Confocal laser endoscopy: new approach to the early diagnosis of tumors of the esophagus and stomach. Future Oncol. 2006;2:469-476. [PubMed] [DOI] |
| 3. | De Palma GD. Confocal laser endomicroscopy in the "in vivo" histological diagnosis of the gastrointestinal tract. World J Gastroenterol. 2009;15:5770-5775. [PubMed] [DOI] |
| 4. | Polglase AL, McLaren WJ, Skinner SA, Kiesslich R, Neurath MF, Delaney PM. A fluorescence confocal endomicroscope for in vivo microscopy of the upper- and the lower-GI tract. Gastrointest Endosc. 2005;62:686-695. [PubMed] [DOI] |
| 5. | Hsiung PL, Hardy J, Friedland S, Soetikno R, Du CB, Wu AP, Sahbaie P, Crawford JM, Lowe AW, Contag CH. Detection of colonic dysplasia in vivo using a targeted heptapeptide and confocal microendoscopy. Nat Med. 2008;14:454-458. [PubMed] [DOI] |
| 6. | Venkatesh K, Cohen M, Abou-Taleb A, Thomas S, Taylor C, Thomson M. A new method in the diagnosis of reflux esophagitis: confocal laser endomicroscopy. Gastrointest Endosc. 2012;75:864-869. [PubMed] [DOI] |
| 7. | Ji R, Li YQ, Gu XM, Yu T, Zuo XL, Zhou CJ. Confocal laser endomicroscopy for diagnosis of Helicobacter pylori infection: a prospective study. J Gastroenterol Hepatol. 2010;25:700-705. [PubMed] [DOI] |
| 8. | Dunbar KB, Okolo P, Montgomery E, Canto MI. Confocal laser endomicroscopy in Barrett's esophagus and endoscopically inapparent Barrett's neoplasia: a prospective, randomized, double-blind, controlled, crossover trial. Gastrointest Endosc. 2009;70:645-654. [PubMed] [DOI] |
| 9. | Nguyen VX, Nguyen CC, De Petris G, Sharma VK, Das A. Confocal endomicroscopy (CEM) improves efficiency of Barrett surveillance. J Interv Gastroenterol. 2012;2:61-65. [PubMed] [DOI] |
| 10. | Gheorghe C, Cotruta B, Iacob R, Becheanu G, Dumbrava M, Gheorghe L. Endomicroscopy for assessing mucosal healing in patients with ulcerative colitis. J Gastrointestin Liver Dis. 2011;20:423-426. [PubMed] |
| 11. | Hlavaty T, Huorka M, Koller T, Zita P, Kresanova E, Rychly B, Toth J. Colorectal cancer screening in patients with ulcerative and Crohn's colitis with use of colonoscopy, chromoendoscopy and confocal endomicroscopy. Eur J Gastroenterol Hepatol. 2011;23:680-689. [PubMed] [DOI] |
| 12. | Kiesslich R, Hoffman A, Goetz M, Biesterfeld S, Vieth M, Galle PR, Neurath MF. In vivo diagnosis of collagenous colitis by confocal endomicroscopy. Gut. 2006;55:591-592. [PubMed] [DOI] |
| 13. | Zambelli A, Villanacci V, Buscarini E, Bassotti G, Albarello L. Collagenous colitis: a case series with confocal laser microscopy and histology correlation. Endoscopy. 2008;40:606-608. [PubMed] [DOI] |
| 14. | Li Z, Yu T, Zuo XL, Gu XM, Zhou CJ, Ji R, Li CQ, Wang P, Zhang TG, Ho KY. Confocal laser endomicroscopy for in vivo diagnosis of gastric intraepithelial neoplasia: a feasibility study. Gastrointest Endosc. 2010;72:1146-1153. [PubMed] [DOI] |