修回日期: 2011-06-21
接受日期: 2011-06-28
在线出版日期: 2011-09-18
目的: 系统评价替比夫定(LDT)治疗慢性乙型肝炎(CHB)的治疗效果.
方法: 应用Cochrane系统评价方法计算机检索Cochrane Library(2009年第3期)、PubMed(1966-2009.9)、EMBASE (1974-2009.9)、中国生物医学数据库(CBM, 1978-2009.9)、中国期刊全文数据库(CNKI, 1979-2009.9)和维普数据库(VIP, 1989-2009.9), 同时在临床试验注册网站及Google搜索引擎进行检索, 并追查纳入研究参考文献, 收集以LDT治疗CHB的所有随机对照试验(RCT)和交叉试验. 根据Cochrane协作网推荐的"风险评估工具"进行风险偏倚评估, 用RevMan 5.0软件进行统计学分析.
结果: 最终纳入10个RCTs, 共4 037例患者. 7篇LDT对比拉米夫定(LAM)的研究结果显示, 对于HBeAg阳性患者, LDT组较LAM组更有效提高血清HBV DNA检测不到率(RR = 1.50, 95%CI: 1.38-1.64)、ALT复常率(RR = 1.10, 95%CI: 1.05-1.16)、HBeAg转阴率(RR = 1.23, 95%CI: 1.08-1.40)和HBeAg血清转换率(RR = 1.17, 95%CI: 1.01-1.35); 对于HBeAg阴性患者, LDT组较LAM组更有效提高血清HBV DNA检测不到率(RR = 1.29, 95%CI: 1.12-1.48), 两组ALT复常率差异无统计学意义(RR = 1.08, 95%CI: 0.96-1.22). 2篇LDT对比阿德福韦酯以及1篇LDT对比治疗方案不详的常规内科治疗的研究结果均显示LDT组效果优于对照组.
结论: LDT相比其他药物治疗CHB对病毒学应答、血清学应答、生化学应答等方面指标有效, 但对于不同疗程的总体效果还需要更为大量的高质量文献提供科学的证据.
引文著录: 杨声坪, 李婧媛, 张鹏, 袁金秋, 刘雅莉. 替比夫定治疗慢性乙型肝炎疗效的系统评价. 世界华人消化杂志 2011; 19(26): 2777-2785
Revised: June 21, 2011
Accepted: June 28, 2011
Published online: September 18, 2011
AIM: To evaluate the efficacy of telbivudine in the treatment of chronic hepatitis B.
METHODS: Based on the principles and methods for Cochrane systematic reviews, we searched the Cochrane Library, PubMed, EMBASE, Chinese Bio-medicine Database, China Journal Full-text Database, VIP database, as well as websites of clinical trial registries and search engine Google. Randomized controlled trials (RCTs) or cross-over trials of telbivudine for chronic hepatitis B were included. We assessed the quality of the included trials according to the Cochrane Handbook for Systematic Reviews of Interventions Version. The Cochrane Collaboration's software RevMan 5.0 was used for meta-analysis.
RESULTS: Ten RCTs totaling 4 037 patients were included. Compared to HBeAg-positive patients treated with lamivudine, those treated with telbivudine had significantly higher rates of serum HBV DNA undetectable by PCR (RR = 1.50, 95%CI: 1.38, 1.64), ALT normalization (RR = 1.10, 95%CI: 1.05, 1.16), HBeAg loss (RR = 1.23, 95%CI: 1.08-1.40), and HBeAg seroconversion (RR = 1.17, 95%CI: 1.01-1.35). HBeAg-negative patients treated with lamivudine had a lower rate of serum HBV DNA undetectable by PCR (RR = 1.29, 95%CI: 1.12-1.48) than those treated with telbivudine.
CONCLUSION: Current evidence demonstrates that treatment with telbivudine can improve virological response, serological response and biochemical response in patients with chronic hepatitis B compared to lamivudine therapy.
- Citation: Yang SP, Li JY, Zhang P, Yuan JQ, Liu YL. Efficacy of telbivudine for chronic hepatitis B: a systematic review. Shijie Huaren Xiaohua Zazhi 2011; 19(26): 2777-2785
- URL: https://www.wjgnet.com/1009-3079/full/v19/i26/2777.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v19.i26.2777
乙型病毒性肝炎(hepatitis B, HB)是由乙型肝炎病毒(hepatitis B virus, HBV)引起的以肝脏损害为主的传染性疾病. 全世界约有20亿人感染了该病毒, 约有3.5亿人为慢性感染, 估计每年有60万人死于急性或慢性乙型肝炎[1]. 据专家估计, 目前我国有现患慢性乙肝患者2 000万人[2]. 急性乙型肝炎目前尚无特异治疗方法, 对慢性乙型肝炎(chronic hepatitis B, CHB), 国内外公认有效的药物包括干扰素类和以拉米夫定(lamivudine, LAM)为代表的核苷(酸)类似物[3], 各种药物各有优缺点. 替比夫定(telbivudine, LDT)于2006-10在美国上市, 商品名为Tyzeka, 并于2007-02以素比夫(Sebivo)为商品名在中国上市[4]. 目前针对LDT治疗CHB的疗效已进行了大量临床试验研究, 但众多临床研究较零散, 不便于临床应用, 本研究通过系统评价相关临床试验, 探讨LDT对CHB的治疗效果, 以供临床医生参考.
以 "Hepatitis B"、"HB"、" Telbivudine"、" Tyzeka"、" Sebivo"为主要检索词检索Cochrane Library(2009年第3期)、EMBASE(1974/2009-09)和PubMed(1966/2009-09), 以"乙肝"、"乙型肝炎"、"替比夫定"、"素比夫"和"素比伏"为主要检索词检索中国生物医学数据库(CBM, 1978/2009-09)、中国期刊全文数据库 (CNKI, 1979/2009-09)和维普数据库(VIP, 1989/2009-09), 根据不同数据库特点采取相应主题词检索与自由词检索结合方式进行检索. 同时在临床试验注册网站及Google搜索引擎进行检索, 并追查纳入研究参考文献. 文献检索无语种限制, 收集LDT治疗CHB的所有随机对照试验(Randomized controlled trials, RCT)和交叉试验.
1.2.1 纳入标准和排除标准: LDT治疗CHB的RCT或交叉试验. CHB患者, 性别、年龄、种族不限. 诊断标准[3]: 有乙型肝炎或HBsAg阳性史超过6 mo, 现HBsAg和/或HBV DNA仍为阳性者. 具有以下任意一条的患者将被排除: (1)合并或重复感染其他肝炎病毒和/或人类免疫缺陷病毒 (HIV); (2)合并严重失代偿性肝病和/或肝细胞癌的患者; (3)其他原发、继发病因导致的肝脏疾病.
1.2.2 分组和干预措施: 试验组为LDT, 对照组分别为接受安慰剂、不治疗、非特异性保肝治疗或LAM、阿德福韦酯(adefovir, ADV)、恩替卡韦等常规药物治疗. LDT+安慰剂对照常规药物+安慰剂的随机试验也被纳入.
1.2.3 结局测量指标: 主要测量指标: 血清HBV DNA检测不到率(PCR法)、ALT复常率. 次要测量指标: HBeAg转阴率、血清HBeAg血清学转换率、血清HBV DNA自基线下降水平、不良反应.
1.2.4 方法学质量评价与资料提取: 两名评价员独立完成文献筛选、资料提取和方法学质量评价并交叉核对, 如遇分歧通过讨论或根据第三位研究人员的意见协商解决. 遇信息不全研究通过电话或E-mail与作者联系予以补充. 采用Cochrane协作网推荐的"风险评估工具"进行风险偏倚评估, 其中RCT偏倚风险评估内容如下: (1)随机方法是否正确; (2)是否做到隐蔽分组、方法是否正确; (3)是否采用盲法; (4)有无失访或退出, 如有失访或退出时, 原因是否描述清楚, 是否采用ITT分析法; (5)选择性报告研究结果; (6)是否存在其他潜在偏倚. 每条标准依研究具体情况按"是"、"否"、"不清楚"进行评价.
统计学处理 采用Cochrane协作网提供的RevMan 5.0软件进行Meta分析, 计数资料用相对危险度(RR)作为疗效效应量, 计量资料采用均数差(MD)、标准均数差(SMD)作为疗效效应量, 二者均以95%CI表示. 首先分析纳入研究的人群, 药物使用剂量等影响临床异质性因素, 按照临床同质性和方法学同质性对各研究进行亚组分析或敏感性分析; 然后采用χ2检验分析亚组内的统计学异质性, 若亚组间无异质性(P>0.10, I2≤50%)采用固定效应模型进行Meta分析; 若存在异质性(P≤0.10, I2>50%), 则首先分析异质性原因, 确定是否能采用随机效应模型进行Meta分析. 若研究间存在明显的临床异质性, 则不进行合并, 只对其进行描述性分析.
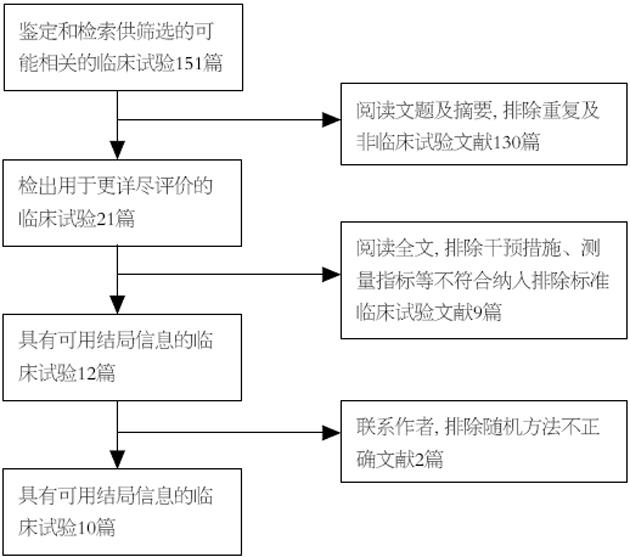
初检出151篇文献, 经阅读文题及摘要, 排除重复及非临床试验文献, 初筛纳入21篇, 进一步阅读全文, 排除干预措施、测量指标等不符合纳入排除标准临床试验文献, 初步纳入12篇[5-16], 对信息报告不清楚者与作者联系予以补充. 电话联系到两名作者[15,16], 核实其随机方法不正确排除, 其他作者均未取得联系, 最终纳入10个RCTs, 未纳入交叉试验(图1). 其中英文6篇, 中文4篇(表1). 有两个研究[9,10]通过临床试验注册平台进行注册(注册号分别为: NCT00115245、NCT00131742).
| 研究者 | n(试验组/对照组) | 年龄(岁) | 性别(男/女) | 随访时间(wk) | |||||||||
| 试验组 | 对照组 | 试验组 | 对照组 | 干预措施 | 备注 | ||||||||
| HBeAg 阳性 | HBeAg 阴性 | HBeAg阳性 | HBeAg阴性 | HBeAg阳性 | HBeAg阴性 | HBeAg阳性 | HBeAg阴性 | HBeAg阳性 | HBeAg阴性 | ||||
| Liaw等[5] | 458/463 | 222/224 | 32 | 43 | 33 | 43 | 333/125 | 174/48 | 331/112 | 177/47 | (1) | 104 | 临床Ⅲ期试验 |
| Lai等[6] | 458/463 | 222/224 | 32 | 43 | 33 | 43 | 333/125 | 174/48 | 351/112 | 177/47 | (1) | 52 | 临床Ⅲ期试验 |
| Lai等[7] | 44/19 | - | 22 | - | 34 | - | 35/9 | - | 15/4 | - | (2) | 52 | 临床Ⅱ期试验 |
| Hou等[8] | 147/143 | 20/22 | 28 | 38 | 29 | 36 | 118/29 | 17/3 | 107/36 | 19/3 | (1) | 52 | |
| Safadi等[9] | 81/81 | 41/43 | 36 | 37 | 87/35 | 95/29 | (1) | 24 | 临床Ⅲb期试验 | ||||
| Chan等[10] | 24W:45/8952W:43/42 | - | A:34, B:30, C:33 | - | A: 35/10, B: 40/4, C: 27/19 | - | (3)(4) | 24/52 | |||||
| 钟旬华等[11] | 60/60 | 60/60 | 29±8.2 | 41±10.1 | 30±8.5 | 42±9.5 | 42/19(6) | 38/22 | 40/20 | 34/26 | (1) | 52 | |
| 汤东澄等[12] | 56/52 | 29/27 | - | - | - | - | - | - | - | - | (1) | 48 | |
| 潘建华等[13] | 40/40 | - | 31±12 | - | 33±13 | - | 36/4 | - | 34/6 | - | (3) | 4/8/12/24/48 | |
| 邱绍勤等[14] | 21/9 | 20/10 | 41.45±10.98 | 48/12 | (5) | 52 | |||||||
本系统评价依据Cochrane handbook风险偏倚评估工具对纳入研究进行风险偏倚评估, 纳入研究存在不同程度的偏倚风险. 纳入研究中随机分组方法仅在4个研究中详尽报道, 大部分研究未对隐蔽分组方法进行描述(表2).
纳入研究中, 除一个研究[14]为LDT与具体方案不详的传统内科治疗对照外, 均为LDT与LAM或ADV效果比较, 纳入研究中无LDT对比安慰剂、不治疗、非特异性保肝治疗或其他常规药物的效果比较. 根据LDT对比不同药物、研究对象HBeAg情况以及不同结局测量指标对纳入的研究进行分析. 共纳入7个LDT对比LAM的研究[5-9,11,12].
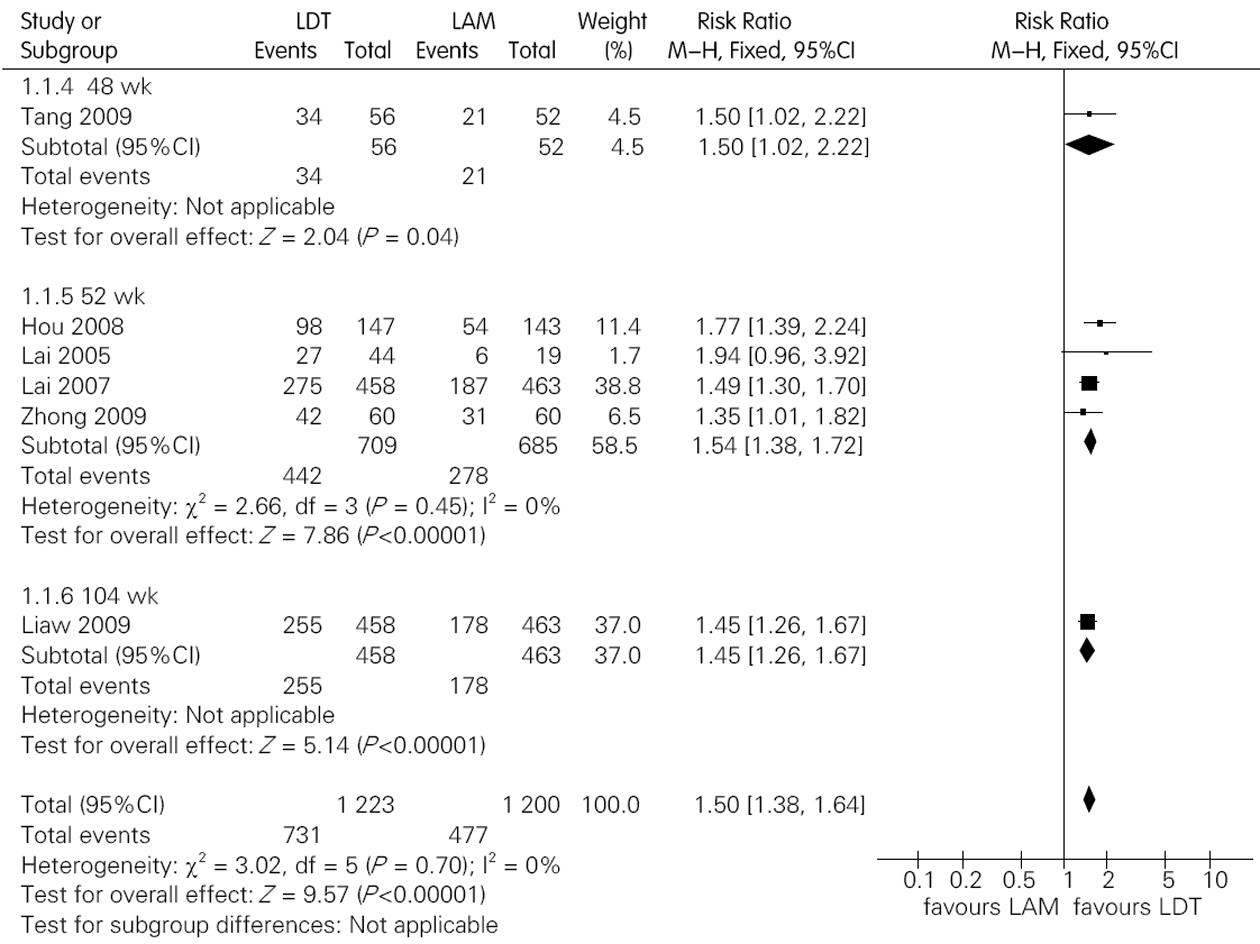
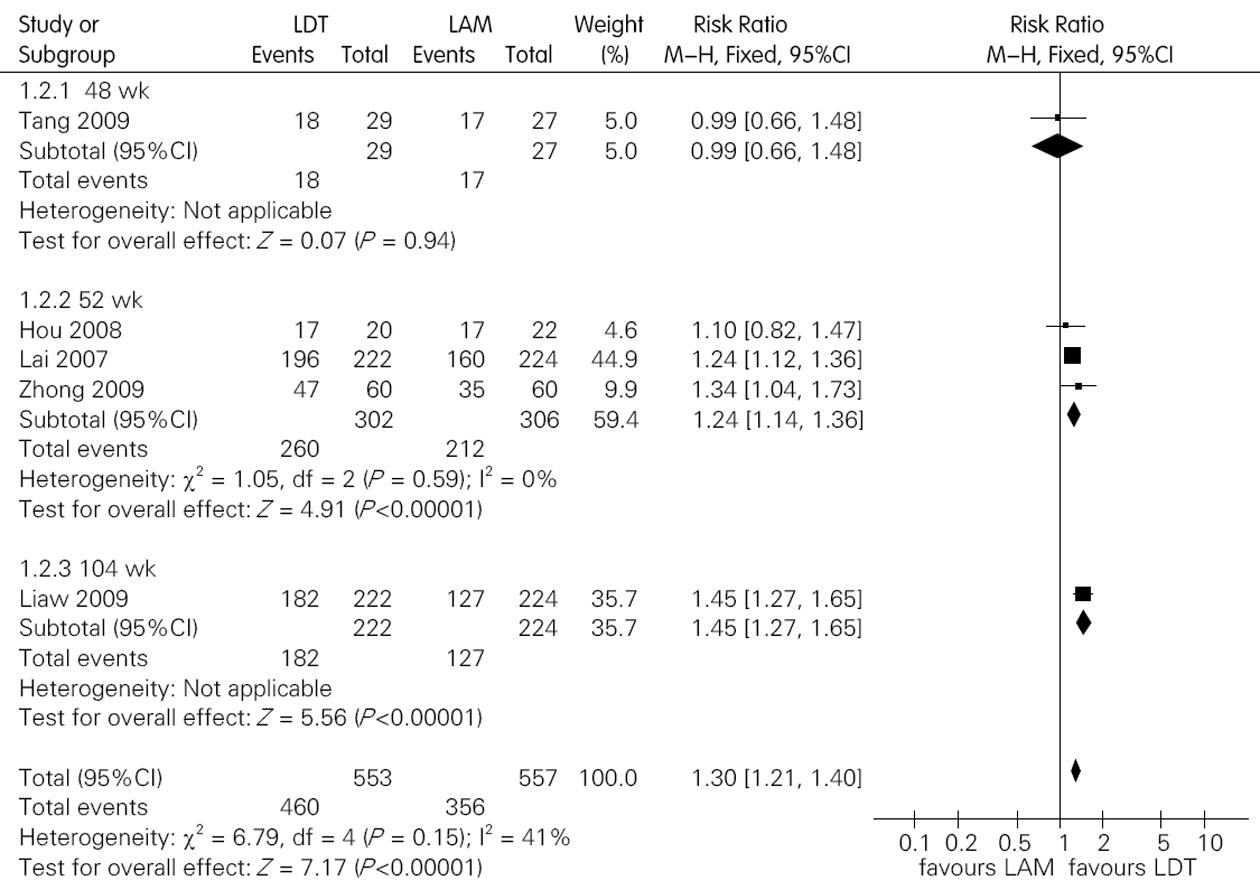
7个研究均报道了血清HBV DNA检测不到率, 其中Safadi等[9]未对HBeAg阳性和阴性分别报道, 其对24 wk疗效研究结果显示两组差异无统计学意义(RR = 1.31, 95%CI: 0.93, 1.85); 6个研究报道了HBeAg阳性患者结果; 5个研究报道了HBeAg阴性患者结果. 各研究间无统计学异质性, 合并后Mata分析结果显示对于HBeAg阳性患者和HBeAg阴性患者, LDT组的HBV DNA检测不到率均高于LAM组(图2, 3). 将方法学质量较低的研究排除[7,11,12], 进行敏感性分析, 对3个质量较高的研究进行合并, 合并后结果显示对于HBeAg阳性患者和HBeAg阴性患者, LDT组的HBV DNA检测不到率均高于LAM组(表3). 敏感性分析结果表明, 纳入3个方法学质量较低的研究并未对结果产生较大影响.
| HBeAg | 疗程(wk) | 纳入研究数 | LDT组/LAM组(n) | P值, I2值 | DNA转阴率(LDT组/LAM组) | RR值(95%CI) |
| 阳性 | 48 | 1个[12] | 56/52 | - | 60.71%/40.38% | 1.50(1.02, 2.22) |
| 52 | 4个[6-8,11] | 709/685 | 0.45, 0% | 62.34%/40.58% | 1.54(1.38, 1.72) | |
| 104 | 1个[5] | 458/463 | - | 55.60%/55.60% | 1.45(1.26, 1.67) | |
| 总疗程 | 6个 | 1 223/1 200 | 0.70, 0% | 59.77%/39.75% | 1.50(1.38, 1.64) | |
| 敏感性分析 | 3个[5,6,8] | 1 063/1 069 | 0.36, 1% | 59.08%/39.20% | 1.51(1.38, 1.65) | |
| 阴性 | 48 | 1个[12] | 29/27 | - | 差异无统计学意义 | 0.99(0.66, 1.48) |
| 52 | 3个[6,8,11] | 302/306 | 0.59, 0% | 86.09%/69.28% | 1.24(1.14, 1.36) | |
| 104 | 1个[5] | 222/224 | - | 82.00%/56.70% | 1.45(1.27, 1.65) | |
| 总疗程 | 5个 | 553/557 | 0.15, 41% | 83.18%/63.91% | 1.30(1.21, 1.40) | |
| 敏感性分析 | 3个[5,6,8] | 464/470 | 0.08, 61% | 85.13%/64.68%1 | 1.29(1.12, 1.48)1 |
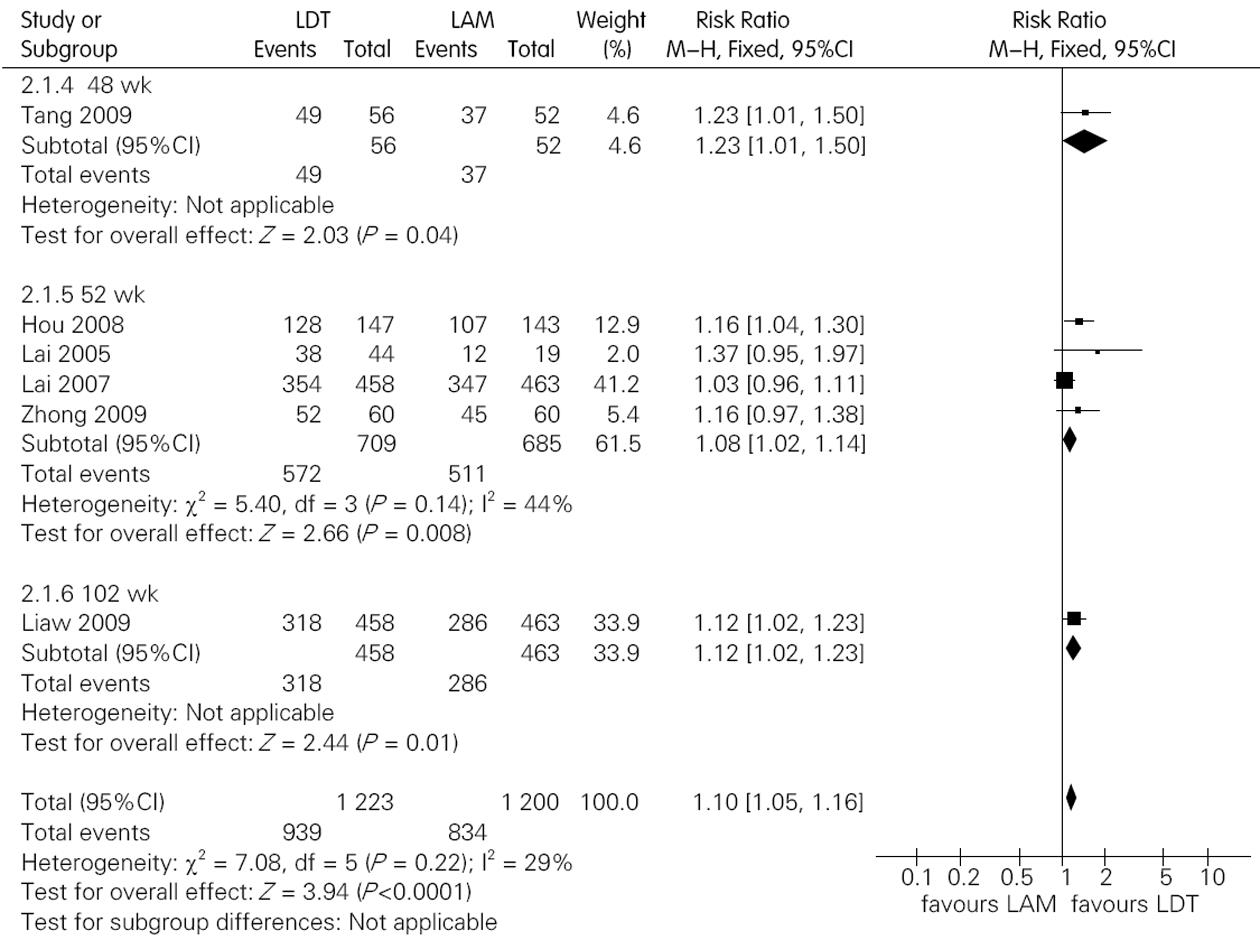
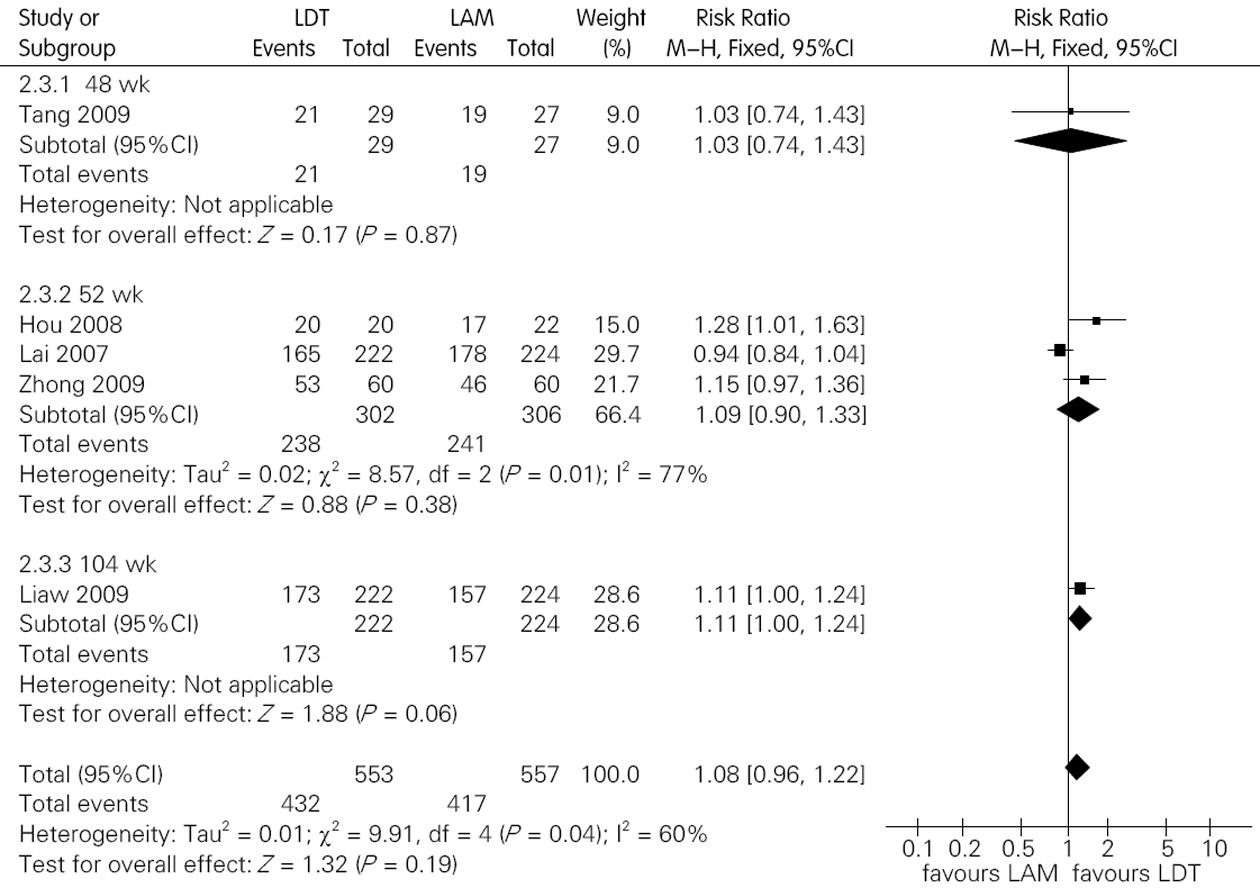
6个研究报道了ALT复常率, 其中6个研究报道了HBeAg阳性患者结果; 5个研究报道了HBeAg阴性患者结果.不同研究间无统计学异质性, Mata分析结果显示对于HBeAg阳性患者LDT组ALT复常率高于LAM组(图4), 对于HBeAg阴性患者LDT组ALT复常率与LAM组相当(图5, 表4).
| HBeAg | 疗程(wk) | 纳入研究数 | LDT组/LAM组(n) | P值, I2值 | DNA转阴率(LDT组/LAM组) | RR值(95%CI) |
| 阳性 | 48 | 1个[12] | 56/52 | - | 87.50%/71.15% | 1.23, (1.01, 1.50) |
| 52 | 4个[6-8,11] | 709/685 | 0.14, 44% | 80.67%/74.60% | 1.08, (1.02, 1.14) | |
| 104 | 1个[5] | 458/463 | - | 69.50%/61.70% | 1.12, (1.02, 1.23) | |
| 总疗程 | 6个 | 1 223/1 200 | 0.22, 30% | 76.42%/69.60% | 1.10, (1.05, 1.16) | |
| 阴性 | 48 | 1个[12] | 29/27 | - | 差异无统计学意义 | 1.03, (0.74, 1.43) |
| 52 | 3个[6,8,11] | 302/306 | 0.01, 77% | 差异无统计学意义 | 1.09, (0.90, 1.33)1 | |
| 104 | 1个[5] | 222/224 | - | 差异无统计学意义 | 1.11, (1.00, 1.24) | |
| 总疗程 | 5个 | 553/557 | 0.04, 60% | 差异无统计学意义 | 1.08, (0.96, 1.21)1 |
7个研究均报道了HBeAg转阴率. 4个研究[6-8,11]报道了52 wk疗效, 结果显示LDT组高于LAM组, 各有1个研究报道了24 wk[9]、48 wk[12]、104 wk疗效[5], 结果均显示两组差异无统计学意义. 研究试验间无统计学异质性(P = 0.58, I2 = 0%), 合并后结果显示LDT组(31.23%)高于LAM组(25.33%), 差异有统计学意义(RR = 1.23, 95%CI: 1.08, 1.40).
6个研究报道了HBeAg血清转换率. 1个研究[12]报道了48 wk疗效, 4个研究[6-8,11]报道了52 wk疗效, 结果均显示两组差异无统计学意义; 1个研究[5]报道了104 wk疗效, 结果显示LDT组高于LAM组. 研究试验间无统计学异质性(P = 0.79, I2 = 0%), 合并后结果显示LDT组(26.00%)高于LAM组(22.17%), 差异有统计学意义(RR = 1.17, 95%CI: 1.01, 1.35).
6个研究[6-9,11,12]报道了血清HBV DNA自基线下降水平. 结果均显示LDT组效果优于LAM组, 但除Safadi等[9]同时报道MD和SMD外, 其他研究均只报道MD, 故本研究未对其进行Meta分析.
共纳入2个LDT对比ADV研究, 两研究均未纳入HBeAg阴性患者. Chan等[10]同时报道了24 wk和52 wk的血清HBV DNA检测不到率(PCR法)、ALT复常率、HBeAg转阴率、HBeAg血清转换率和血清HBV DNA自基线下降水平等五个指标的疗效, 该试验分为ABC 3组, 前24 wk A组以LDT治疗, BC组以ADV治疗, 24 wk以后, AB组维持原方案, C组改为LDT治疗, 考虑24 wk后C组未经洗脱期就改用药物存在一定偏倚, 且该组LDT 28 wk的疗程于其他组用药52 wk疗程可比性较小, 故对于该试验C组, 只纳入第一阶段数据, 未对第二阶段数据纳入分析; 潘建华等[13]同时报道了4、8、12、24和48 wk的血清HBV DNA检测不到率(PCR法)、ALT复常率、HBeAg转阴率和血清HBV DNA自基线下降水平等4个指标的疗效.
Chan等[10]报道了血清HBV DNA自基线下降水平24 wk的MD、SMD和52 wk的MD, 潘建华等[13]报道了48 wk的MD, 其结果均显示LDT组效果优于ADV组, 本研究未对其进行Meta分析(表5).
| 指标 | 时间(wk) | 结果 | RR值 | 95%CI | 纳入研究 |
| HBV DNA检测不到率(PCR法) | 4 | = | 2.00 | 0.19, 21.18 | 潘建华等[13] |
| 8 | = | 1.50 | 0.26, 8.50 | 潘建华等 | |
| 12 | = | 2.00 | 0.65, 6.11 | 潘建华等 | |
| 24 | > | 2.45 | 1.56, 3.85 | 潘建华等/ Henry等[10] | |
| P = 0.36, I2 = 0% | |||||
| 48 | > | 1.59 | 1.04, 2.42 | 潘建华等 | |
| 52 | = | 1.49 | 0.96, 2.32 | Henry等 | |
| ALT复常率 | 4 | = | 1.63 | 0.76, 3.49 | 潘建华等 |
| 8 | = | 1.38 | 0.79, 2.43 | 潘建华等 | |
| 12 | = | 1.35 | 0.86, 2.12 | 潘建华等 | |
| 24 | = | 1.04 | 0.43, 1.29 | 潘建华等/ Henry等 | |
| P = 0.37, I2 = 0% | |||||
| 48 | = | 1.14 | 0.89, 1.48 | 潘建华等 | |
| 52 | = | 0.92 | 0.76, 1.12 | Henry等 | |
| HBeAg转阴率 | 4 | = | 3.00 | 0.13, 71.51 | 潘建华等 |
| 8 | = | 1.67 | 0.43, 6.51 | 潘建华等 | |
| 12 | = | 2.00 | 0.65, 6.11 | 潘建华等 | |
| 24 | = | 1.55 | 0.85, 2.84 | 潘建华等/ Henry等 | |
| P = 0.73, I2 = 0% | |||||
| 48 | = | 1.89 | 0.96, 3.72 | 潘建华等 | |
| 52 | = | 1.41 | 1.68, 2.94 | Henry等 | |
| HBeAg血清转换率 | 24 | = | 0.76 | 0.31, 1.85 | Henry等 |
| 52 | = | 1.47 | 0.67, 3.22 | Henry等 |
纳入1个[14]LDT对比常规内科治疗(具体治疗方案不详)研究, 其报道了2、4和12 wk的血清HBV DNA检测不到率(PCR法)和HBeAg血清转换率两个指标的疗效(表6).
| 指标 | 时间(wk) | 结果 | RR值 | 95%CI |
| 血清HBV DNA检测不到率(PCR法) | 2 | > | 19.00 | 1.16, 312.42 |
| 4 | > | 24.00 | 3.47, 166.23 | |
| 12 | > | 8.33 | 2.81, 24.67 | |
| HBeAg血清转换率 | 4 | = | 1.36 | 0.06, 30.64 |
| 12 | = | 0.43 | 0.03, 312.42 |
本研究基于国内外RCT对LDT治疗CHB的有效性和安全性进行定量分析. LDT对比LAM的研究结果显示, 对于HBeAg阳性患者, LDT组的血清HBV DNA检测不到率、ALT复常率、HBeAg转阴率和HBeAg血清转换率均高于LAM组; 对于HBeAg阴性患者, 血清HBV DNA检测不到率高于LAM组, ALT复常率与LAM组差异无统计学意义. LDT对比ADV仅纳入2个研究, 且方法学质量偏低, 此外, 考虑对同一研究不同报道时间点疗效的合并可能导致重复计算样本量而影响结果, 故未对其进行合并分析.
本研究共纳入10个研究, 大多数研究方法学存在局限性. 其中, 4个研究[5,6,9,10]为充分随机, 其他6个研究[6,8,11-14]未描述随机分配方法. 4个研究[5,6,9,10]实施了正确的隐蔽分组, 6个研究[6,8,11-14]隐蔽分组方法不清楚, 提示纳入试验存在选择性偏倚的可能. 6个研究采用盲法[5-10], 除Chan等[9]等描述对观察者施盲外, 其余均只描述"双盲", 未报告其施盲对象, 多认为可能是对患者和医生施盲; 4个研究[11-14]未报道是否实施盲法, 纳入试验不能确定是否存在实施偏倚. 5个研究[5,7-9,11]报道失访并采取了ITT分析, 5个研究[6,10,12-14]未报道失访情况, 不排除存在减员偏倚的可能. 9个研究[1,3-14]一个或多个测量指标报告不完整, 1个研究[6]是否选择性报告研究结果不清楚.所有研究均不清楚是否存在其他偏倚.
本研究存在一定局限性: (1)本系统评价纳入研究多采用实验室检测指标, 未报告与患者生存质量密切相关的终点指标报道, 因此该治疗方法是否能改善患者生活质量尚需进一步研究; (2)纳入研究方法学质量一般, 尤其中文研究对随机方法、隐蔽分组描述多不清晰, 影响读者对其真实性的判断; (3)入选的治疗疗程尚未统一, 虽然进行亚组分析, 但仍可能存在不同程度的偏倚和混杂因素, 但由于纳入研究用药时间不同, 因此, 无法进行整体效果分析; (4)纳入研究中只纳入LDT对比LAM、ADV等药物治疗效果比较, 无符合纳入标准的LDT对比其他药物的治疗效果比较研究.此外本研究未对各种治疗方案成本效益进行分析, 有研究表明LAM治疗方案成本效益优于LDT[18]; (5)本研究未进行发表偏倚评估, 不排除存在发表偏倚的可能.
今后的临床研究应该注意以下几点: (1)开展设计严格的长期随访的大样本RCT, 以终点指标结合实验室检测指标进行临床疗效的评价; (2)注重LDT对CHB的短期和长期疗效的研究, 并统一报道的疗程, 建议报告12、52和104 wk的随访结果; (3)明确随机分配序列产生的原则和方法并严格执行, 对随机方案做到有效的隐藏, 提高试验方法学质量; (4)严格按照CONSORT声明2010版[19]对RCT进行全面、客观报告, 提高报告质量.
目前证据表明, LDT治疗CHB对病毒学应答、血清学应答、生化学应答有效, 但对于不同疗程的总体效果还需要更为大量的高质量文献提供科学的证据.
慢性乙型肝炎感染率日趋增高, 国内外公认有效的药物包括干扰素类和核苷(酸)类似物. 近年来, 作为后者, 替比夫定已逐渐用于临床并取得一定效果. 为了客观评价其疗效和安全性, 本课题从循证医学的角度进行了该研究.
张占卿, 主任医师, 上海市公共卫生中心; 孙殿兴, 主任医师, 白求恩国际和平医院肝病科
如何通过药物治疗慢性乙型肝炎, 降低感染率和死亡率是临床亟待解决的重要问题. 目前针对替比夫定治疗慢性乙肝已进行了大量临床试验研究, 但众多临床研究较为零散, 当前尚无相关系统评价对其有效性和安全性进行客观评价.
近几年来国外的研究显示, 替比夫定治疗慢性乙型肝炎有较好的疗效, 显示出良好的应用前景. 但也有研究表明替比夫定治疗方案成本效益低于其他药物.
本项目旨在系统评价替比夫定治疗慢性乙肝的有效性及安全性. 为临床医师在治疗慢性乙肝的药物选择提供客观依据.
替比夫定和拉米夫定是目前临床上常用的抗乙肝病毒药物, 对已有的文献资料进行Meta分析很有意义, 本研究提供了有意义的信息, 研究具有新颖性.
编辑: 李军亮 电编:何基才
| 1. | 世界卫生组织. EB/OL. 2009-09. Available from: http://www.who.int/mediacentre/factsheets/fs204/zh/index.html. |
| 2. | 中华人民共和国卫生部. 2006年-2010年全国乙型病毒性肝炎防治规划. 中国实用乡村医生杂志. 2006;13:1-4. |
| 5. | Liaw YF, Gane E, Leung N, Zeuzem S, Wang Y, Lai CL, Heathcote EJ, Manns M, Bzowej N, Niu J. 2-Year GLOBE trial results: telbivudine Is superior to lamivudine in patients with chronic hepatitis B. Gastroenterology. 2009;136:486-495 PubMed DOI. |
| 6. | Lai CL, Leung N, Teo EK, Tong M, Wong F, Hann HW, Han S, Poynard T, Myers M, Chao G. A 1-year trial of telbivudine, lamivudine, and the combination in patients with hepatitis B e antigen-positive chronic hepatitis B. Gastroenterology. 2005;129:528-536 PubMed. |
| 7. | Lai CL, Gane E, Liaw YF, Hsu CW, Thongsawat S, Wang Y, Chen Y, Heathcote EJ, Rasenack J, Bzowej N. Telbivudine versus lamivudine in patients with chronic hepatitis B. N Engl J Med. 2007;357:2576-2588 PubMed DOI. |
| 8. | Hou J, Yin YK, Xu D, Tan D, Niu J, Zhou X, Wang Y, Zhu L, He Y, Ren H. Telbivudine versus lamivudine in Chinese patients with chronic hepatitis B: Results at 1 year of a randomized, double-blind trial. Hepatology. 2008;47:447-454 PubMed DOI. |
| 9. | Safadi R, Xie Q, Chen Y, Yin YK, Wei L, Hwang SG, Zuckerman E, Tia JD, Harb G, Brown NA. A randomized trial of switching to telbivudine versus continued lamivudine in adults with chronic hepatitis B: results of the primary analysis at week 24. J Hepatol. 2007;46:S196 DOI. |
| 10. | Chan HL, Heathcote EJ, Marcellin P, Lai CL, Cho M, Moon YM, Chao YC, Myers RP, Minuk GY, Jeffers L. Treatment of hepatitis B e antigen positive chronic hepatitis with telbivudine or adefovir: a randomized trial. Ann Intern Med. 2007;147:745-754 PubMed. |
| 17. | 国家食品药品监督管理局. 药物警戒快讯EB/OL. 2009-09. Available from: http://www.sda.gov.cn/WS01/CL0389/29742.html. |
| 19. | Schulz KF, Altman DG, Moher D. CONSORT 2010 statement: Updated guidelines for reporting parallel group randomised trials. J Pharmacol Pharmacother. 2010;1:100-107 PubMed DOI. |