修回日期: 2009-12-03
接受日期: 2009-12-07
在线出版日期: 2010-01-08
目的: 研究连接黏附分子C(JAM-C)在小鼠急性坏死性胰腺炎(ANP)模型胰腺、肾脏和肺脏组织中的表达.
方法: 采用雨蛙素和脂多糖联合腹腔注射的方法建立小鼠ANP模型. 模型组(ANP组)小鼠腹腔内注射雨蛙素(50 μg/kg), 连续6次, 每次间隔1 h, 在末次注射雨蛙素后, 即向小鼠腹腔内注射脂多糖(LPS)(10 mg/kg); 对照组小鼠腹腔内注射等体积生理盐水. 在末次注射3 h后, 用眼球取血法收集血液, 检测血清淀粉酶, 并取胰腺、肾脏、肺脏组织, 通过Western blot印迹杂交法检测JAM-C在这些组织上的表达.
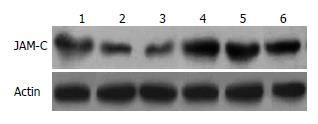
结果: JAM-C在ANP组的胰腺、肺脏和肾脏上均有着高表达, 大于生理盐水对照组3倍以上(0.608±0.133 vs 0.176±0.024, 0.718±0.148 vs 0.160±0.027, 0.654±0.085 vs 0.166±0.039, 均P<0.05).
结论: 在小鼠ANP模型中, JAM-C在胰腺、肾脏和肺脏上的表达均明显增高, 提示JAM-C在ANP发病过程中起到重要的作用.
引文著录: 胡端敏, 杨勇, 唐文. JAM-C在小鼠急性坏死性胰腺炎模型不同组织中的表达. 世界华人消化杂志 2010; 18(1): 81-83
Revised: December 3, 2009
Accepted: December 7, 2009
Published online: January 8, 2010
AIM: To investigate the expression of junctional adhesion molecule-C (JAM-C) in the pancreas, kidney and lung of mice with acute necrotizing pancreatitis (ANP).
METHODS: Mice were injected intraperitoneally with cerulein and lipopolysaccharide (LPS) to induce ANP. The ANP group was given 6 hourly injections of a supramaximal dose of cerulein (50 μg/kg). After the final cerulein injection, LPS was injected intraperitoneally at a dose of 10 mg/kg. The control group was given the same volume of normal saline solution. Three hours after the final injection, mice were sacrificed. Blood samples were taken from the mice after removing the eyeball to determine the serum amylase concentration, and the pancreas, kidney and lung specimens were removed for morphology study and Western blot to test the expression of JAM-C.
RESULTS: Western blot analysis showed a more than 3-fold increase in JAM-C expression levels in the pancreas, kidney and lung in the ANP group compared with the control group (0.608 ± 0.133 vs 0.176 ± 0.024, 0.718 ± 0.148 vs 0.160 ± 0.027, and 0.654 ± 0.085 vs 0.166 ± 0.039, respectively; all P < 0.05).
CONCLUSION: JAM-C expressed by endothelial cells contributes to the pathophysiology of acute necrotizing pancreatitis and may be used as a target for future clinical interventions.
- Citation: Hu DM, Yang Y, Tang W. Expression of JAM-C in different tissues of mice with acute necrotizing pancreatitis. Shijie Huaren Xiaohua Zazhi 2010; 18(1): 81-83
- URL: https://www.wjgnet.com/1009-3079/full/v18/i1/81.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v18.i1.81
急性坏死性胰腺炎(acute necrotizing pancreatitis, ANP)作为一种全身炎症反应性疾病, 中性粒细胞的过度激活被认为是引起胰腺炎病情加重、多器官功能衰竭以致死亡的重要原因, 接黏附分子-C(junctional adhesion molecule C, JAM-C)是近些年新发现的在血管内皮细胞上分布的细胞黏附分子, 他在中性粒细胞向炎症部位和组织损伤处的浸润和聚集过程中起重要作用[1], 故JAM-C可能参与了ANP的病情进展. 本实验通过Western blot法检测JAM-C在小鼠ANP模型胰腺、肾脏和肺脏组织中表达来探讨JAM-C在ANP的病情进展中的作用.
清洁级昆明小鼠40只, 雌雄不分, 体质量20 g±2 g, 购自苏州大学动物实验中心. 雨蛙素(cerulein)、内毒素(LPS)(Ecoli O127:B8)购自美国Sigma公司; AF1213羊抗小鼠JAM-C mAb购自美国RnD公司.
1.2.1 造模: 动物随机被分成两组: (1)对照组: 小鼠给予腹腔注射无菌生理盐水(10 mL/kg), 共注射6次, 间隔1 h; (2)ANP模型组: 即雨蛙素+内毒素组, 小鼠给予腹腔注射雨蛙素(50 μg/kg)6次, 间隔1 h, 末次注射后立即给予腹腔注射内毒素(10 mg/kg).
1.2.2 检测和观察指标: 所有小鼠均在末次注射后3 h摘眼球取血, 并断颈处死, 血液经离心后取上层血清, 存于-80 ℃冰箱中保存. 小鼠开腹后仔细分离胰腺、肾脏和肺脏组织, 一部分组织用40 g/L多聚甲醛固定24 h后石蜡包埋, 另一部分组织放入1 mL冻存管后置于液氮中保存. 小鼠血清经过稀释后通过Olympus全自动生化仪进行血清淀粉酶浓度检测. 石蜡包埋组织进行常规切片HE染色后观察各组织病理变化. Western blot分析检测黏附分子JAM-C在ANP小鼠模型胰腺、肾脏和肺脏组织上的表达.
统计学处理 采用SPSS13.0统计软件, 所有数据均用mean±SD表示. 两组数据比较时采用Mann-Whitney检验. P<0.05认为有显著性差异.
小鼠的基础血清淀粉酶远远高于人的血清淀粉酶浓度, 因此在实际测量时采取了稀释8-10倍才可测出. 血淀粉酶检测结果为对照组1 299.25 IU/L±70.27 IU/L, ANP模型组19 608.2 IU/L±1 768.98 IU/L, ANP模型组显著高于正常对照组(P<0.05).
光镜下见ANP模型小鼠胰腺水肿, 腺泡呈孤岛状, 腺细胞坏死, 细胞结构模糊不清, 胞质内空泡形成, 局部有融合性坏死灶, 坏死区有大量中性粒细胞和单核细胞浸润. 胰周脂肪坏死, 大量炎症细胞浸润, 胰腺间质内动脉痉挛, 静脉明显扩张淤血, 炎症细胞附边, 局部血管壁坏死、出血, 红细胞进入胰腺间质和淋巴管, 血管坏死区有大量中性粒细胞和单核细胞浸润. 对照组胰腺组织大致正常. ANP模型小鼠胰外组织病理学变化: 肺泡壁的毛细血管弥漫性扩张充血, 肺泡腔内有少量渗出液及红细胞和炎症细胞, 肺间质炎症细胞浸润明显; 肾小球充血, 毛细血管袢之间可见中性粒细胞和单核细胞浸润, 肾小管扩张, 积聚物增多, 肾间质轻度水肿, 对照组正常. 由此也可见, 雨蛙素联合内毒素腹腔内注射成功诱导了小鼠ANP合并多脏器损害模型.
目前的研究认为ANP时, 胰腺在胰酶异常激活所造成的损害过程中, 可以激活单核巨噬细胞, 进而造成促炎细胞因子和氧自由基的释放, 他们又可进一步导致粒细胞和内皮细胞的过度激活而释放大量的炎症介质, 这一方面可以引起胰腺微循环障碍而加重胰腺损伤, 另一方面又造成远隔脏器的损伤. 白细胞过度激活被认为是引起胰腺病情加重、多器官功能衰竭以致死亡的重要原因[2]. 其中细胞黏附分子主要作用于炎症细胞的黏附过程, 对白细胞过度激活以及ANP的发生、发展及器官功能衰竭的发生有重要意义. JAM-C是免疫球蛋白超家族成员之一, 他主要分布在白细胞、血小板、各种上皮, 及内皮细胞上. 他的配体主要是分布在各种白细胞上的整和素Mac-1(αLβ2, CD11b/CD18). Chavakis等[3]在他们的研究中发现JAM-C大量分布在血管内皮细胞上, 且主要分布在内皮细胞之间的紧密连接上, 使用JAM-C的可溶形式(sJAM-C)结合中性粒细胞上的整和素Mac-1后, 发现血管炎症明显减轻, 且白细胞渗出也明显减少, 在对腹膜炎[3]、肺炎[4]、皮肤炎症[5]、关节炎[6]等动物模型的研究中发现JAM-C增加了中性粒细胞的在炎症部位和组织损伤处的浸润和聚集. 既然ANP时存在中性粒细胞激活、游走及胰外脏器的浸润, 故JAM-C可能通过促进炎症反应过程中的炎症细胞的滚动、游走和黏附参与了ANP的病理生理进程. 本研究通过Western blot法检测JAM-C在ANP动物不同组织中的表达. 结果表明与对照组相比, JAM-C在ANP小鼠模型的肺脏、胰腺和肾脏上均有高表达(P<0.05). 这一发现和Vonlaufen等[7]通过免疫组织化学观察JAM-C在ANP小鼠模型表达结果一致. 由此可见, JAM-C在ANP的病理发展中可能起到重要作用. ANP时细胞黏附分子表达的上调及其所介导的白细胞的游出与募集是导致ANP发生与发展的关键因素之一, 既往针对细胞黏附分子的抗黏附治疗在动物实验中也取得了一定的疗效, 但总体来说并不理想[8]这可能与这些研究所涉及的黏附分子主要作用于炎症反应时白细胞和内皮细胞的黏附有关, 而由于JAM-C在内皮细胞上分布的特殊性, JAM-C主要作用在中性粒细胞通过血管内皮细胞游出过程. 于是拮抗JAM-C这些参与ANP后期细胞事件的黏附分子可能成为治疗AP的新的突破口.
ANP时细胞黏附分子表达的上调及其所介导的白细胞的游出与募集是导致ANP发生与发展的关键因素之一, 接黏附分子-C(JAM-C)是近些年新发现的在血管内皮细胞上分布的细胞黏附分子, 他在中性粒细胞向炎症部位和组织损伤处的浸润和聚集过程中起重要作用.
刘超, 副教授, 中山大学孙逸仙纪念医院肝胆胰外科.
本研究发现JAM-C在ANP组的胰腺、肺脏和肾脏上均有着高表达, 故JAM-C在ANP的病理发展中可能起到重要作用. 由于JAM-C在内皮细胞上分布的特殊性, JAM-C主要作用在中性粒细胞通过血管内皮细胞游出过程. 于是拮抗JAM-C这些参与ANP后期细胞事件的黏附分子可能成为治疗AP的新的突破口.
本文设计合理, 研究路线清晰, 研究方法可靠, 结果分析恰当, 结论可信, 但创新性一般.
编辑: 李军亮 电编:何基才
| 1. | Ody C, Jungblut-Ruault S, Cossali D, Barnet M, Aurrand-Lions M, Imhof BA, Matthes T. Junctional adhesion molecule C (JAM-C) distinguishes CD27+ germinal center B lymphocytes from non-germinal center cells and constitutes a new diagnostic tool for B-cell malignancies. Leukemia. 2007;21:1285-1293. [PubMed] [DOI] |
| 2. | Raraty MG, Connor S, Criddle DN, Sutton R, Neoptolemos JP. Acute pancreatitis and organ failure: pathophysiology, natural history, and management strategies. Curr Gastroenterol Rep. 2004;6:99-103. [PubMed] [DOI] |
| 3. | Chavakis T, Keiper T, Matz-Westphal R, Hersemeyer K, Sachs UJ, Nawroth PP, Preissner KT, Santoso S. The junctional adhesion molecule-C promotes neutrophil transendothelial migration in vitro and in vivo. J Biol Chem. 2004;279:55602-55608. [PubMed] [DOI] |
| 4. | Aurrand-Lions M, Lamagna C, Dangerfield JP, Wang S, Herrera P, Nourshargh S, Imhof BA. Junctional adhesion molecule-C regulates the early influx of leukocytes into tissues during inflammation. J Immunol. 2005;174:6406-6415. [PubMed] |
| 5. | Ludwig RJ, Zollner TM, Santoso S, Hardt K, Gille J, Baatz H, Johann PS, Pfeffer J, Radeke HH, Schön MP. Junctional adhesion molecules (JAM)-B and -C contribute to leukocyte extravasation to the skin and mediate cutaneous inflammation. J Invest Dermatol. 2005;125:969-976. [PubMed] [DOI] |
| 6. | Palmer G, Busso N, Aurrand-Lions M, Talabot-Ayer D, Chobaz-Péclat V, Zimmerli C, Hammel P, Imhof BA, Gabay C. Expression and function of junctional adhesion molecule-C in human and experimental arthritis. Arthritis Res Ther. 2007;9:R65. [PubMed] [DOI] |