修回日期: 2009-10-18
接受日期: 2009-10-19
在线出版日期: 2009-10-28
目的: 收集中英文相关随机对照试验的研究结果进行Meta分析, 对奥沙利铂联合5-FU/LV(FOLFOX) 方案的疗效进行评价.
方法: 采用Cochrane系统评价方法, 检索Cochrane Library、PubMed、EMBase、中国生物医学文献数据库(CBM)、中文期刊全文数据库, 中文科技期刊全文数据库(CSJD)等数据库, 并辅以手工检索和其他检索.
结果: 共8个随机对照试验662例患者纳入研究, 其中1个随机对照研究来自美国, 另7个均来自中国; 且8篇RCT存在偏倚的可能性均为中等程度. FOLFOX与顺铂联合5-FU/LV(PLF)方案治疗胃癌在1年生存率方面差异无统计学意义, 但在总的生存率方面有显著差异. 其OR值和95%CI分别为1.37(0.93, 2.01)、1.93(1.41, 2.66). 3/4级的不良反应中白细胞减少和恶心呕吐等治疗组轻于对照组; 在外周神经毒性反应方面, 治疗组重于对照组, 差异有统计学意义; 而血小板减少方面差异无统计学意义. 其OR值和95%CI分别为0.48(0.28, 0.83)、0.26(0.16, 0.42)、7.38(2.16, 25.23)及1.20(0.44, 3.30).
结论: FOLFOX方案总有效率优于PLF方案, 但是1年生存率并不优于对照组. 白细胞减少和恶心呕吐治疗组轻于对照组, 外周神经毒性重于对照组.
引文著录: 王娜, 关泉林, 姜雷, 周欣, 高晨, 杨含腾. 奥沙利铂、顺铂联合5-FU/LV治疗晚期胃癌的系统评价. 世界华人消化杂志 2009; 17(30): 3148-3154
Revised: October 18, 2009
Accepted: October 19, 2009
Published online: October 28, 2009
AIM: To assess the efficacy of FOLFOX chemotherapy [oxaliplatin plus 5-fluorouracil (5-FU)/leucovorin (LV)] for advanced gastric cancer through a meta-analysis of randomized controlled trials (RCTs) published worldwide in English or Chinese.
METHODS: Cochrane strategy in combination with manual search was used to identify previously published randomized controlled trials by searching Cochrane library, PubMed, EMBase, Chinese Biomedical Literature Database (CBM), China Journal Full-text Database, and Chinese Scientific Journal Full-text Database (CSJD).
RESULTS: Eight randomized controlled trials involving a total of 662 patients were studied. Of the eight trials, 7 were performed in China, and 1 in the United States. Evaluation of the methodological quality showed that the eight RCTs had a moderate risk of bias. Although no statistical difference was found in the 1-year survival rate OR = 1.37, 95% confidence interval (95%CI) = [0.93-2.01] between patients treated with oxaliplatin plus 5-FU/LV and cisplatin plus 5-FU/LV, there was a significant difference in the overall survival rate between the two groups of patients (OR = 1.93, 95%CI = 1.41-2.66). The incidences of grade 3/4 side effects such as leucopenia and nausea and vomiting were slightly lower in patients treated with oxaliplatin plus 5-FU/LV than in those treated with cisplatin plus 5-FU/LV (OR = 0.48 and 0.26, 95%CI = 0.28-0.83 and 0.16-0.42, respectively). In contrast, the incidence of peripheral neurotoxicity was higher in patients treated with oxaliplatin plus 5-FU/LV than in those treated with cisplatin plus 5-FU/LV (OR = 1.20, 95%CI = 0.44-3.30). No significant difference was noted in the incidence of thrombocytopenia between the two groups of patients (OR = 7.38, 95%CI = 2.16-25.23).
CONCLUSION: Oxaliplatin plus 5-FU/LV is superior to cisplatin plus 5-FU/LV in improving overall survival rate, but not 1-year survival rate and median survival time. The incidences of nausea and vomiting and leucopenia are lower in patients treated with oxaliplatin plus 5-FU/LV than in those treated with cisplatin plus 5-FU/LV.
- Citation: Wang N, Guan QL, Jiang L, Zhou X, Gao C, Yang HT. Cisplatin plus 5-fluorouracil/leucovorin versus oxaliplatin plus 5-fluorouracil/leucovorin in the treatment of advanced gastric cancer: a systematic review. Shijie Huaren Xiaohua Zazhi 2009; 17(30): 3148-3154
- URL: https://www.wjgnet.com/1009-3079/full/v17/i30/3148.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i30.3148
尽管胃癌的发病率在世界上的很多地区已有所下降, 但仍居恶性肿瘤发病的第2位, 且这些患者一般到晚期才得到就诊[1]. 目前胃癌切除术后患者的5年生存率为30%-60%, 手术切除是治愈的主要手段, 但对于不能手术或手术后复发转移的晚期胃癌, 化疗占有十分重要的地位. 研究表明, 联合化疗可以提高晚期胃癌患者的生活质量和总生存率. 但目前尚无标准的方案, 以往联合化疗的基本方案是5-氟尿嘧啶(5-FU)+亚叶酸钙(CF)+顺铂(DDP). 奥沙利铂化学名为反式-右旋-1, 2-环己二氨草酸铂, 是第三代铂类抗癌药物, 与顺铂、卡铂抗癌机制和耐药机制不完全相同, 与5-FU有明显的协同作用, 并且对5-FU耐药的肿瘤有效. 为比较奥沙利铂联合氟尿嘧啶和亚叶酸钙方案与顺铂联合氟尿嘧啶和亚叶酸钙方案治疗晚期胃癌的疗效与安全性, 本研究拟对这2种方案的随机对照试验的结果进行系统评价, 就其疗效和安全性及效价比进行比较研究, 为临床决策分析提供依据.
以英文关键词"leucovorin, calcium folinate, LV, Leucovorin Calcium, CF, cisplatin, DDP, CDDP, cis-platinum, neoplatin, fluorouracil, 5-FU, oxaliplatin, L-OHP, OXA, gastric cancer, stomach cancer, gastric carcinoma, stomach neoplasm, gastric tumor等"及中文关键词"亚叶酸钙, 甲酰四氢叶酸钙, 顺铂, 5-FU, 奥沙利铂, 草酸铂, 乐沙定, 胃癌, 胃肿瘤等"检索数据库PubMed(1966-2009年)、EMBase(1974-2009年)、Cochrane Library(2009年第1期). 中国生物医学文献数据库(1978-2009年)、维普中文科技期刊数据库(1989-2009年)、中国CNKI学术总库(1994-2009年)、NCCN(2009年)、ESMO(2008年)、ASCO(2009年)、SCI(1961-2009年), 获得有关文献80篇. 阅读题名、摘要, 排除综述7篇,腹腔灌注化疗的1篇, 化疗后行切除术的1篇, 其他非随机对照试验、非临床研究文献20篇. 剩余51篇查找原文, 排除未达到纳入标准的文献43篇, 最终纳入的8个研究均为随机对照试验.
1.2.1 观察对象: 纳入标准: 经病理或细胞学证实的晚期胃癌患者; 性别不限; 化疗前Kps评分≥60分, 血常规、肝肾功能、心肺功能均正常, 且有可测量的客观指标; 全部病例至少完成2个周期. 排除标准: 有化疗禁忌证; 患有胃癌合并其他疾病者; 上次化疗距现在不到1 mo者; 失访率超过20%的研究.
1.2.2 研究类型: 随机对照试验(RCT)和半随机对照试验(qRCT).
1.2.3 干预措施: 奥沙利铂联合5-FU/LV方案与顺铂联合5-FU/LV方案比较.
1.2.4 测量指标: (1)中位生存时间; (2)有效率; (3)生存率, 生活质量; (4)不良反应.
1.2.5 纳入试验的筛选: 两位研究者独立阅读所获文献题目和摘要, 在排除明显不符合纳入标准的试验后, 对可能符合纳入标准的试验阅读全文, 以确定是否真正符合纳入标准. 两位研究者交叉核对纳入试验的结果, 对有分歧而难以确定其是否纳入的试验, 通过讨论或由第三研究者决定其是否纳入.
1.2.6 质量评价: 对最后纳入文献的全文依据Cochrane评价手册5.0的文献质量评价方法进行评价, 内容包括: (1)随机方法: 随机方法正确; 随机方法不清楚; 随机方法不充分; (2)分配隐藏: 隐藏方法正确; 隐藏方法不清楚; 隐藏方法不充分; (3)盲法: 盲法正确; 盲法不清楚; 盲法不充分; (4)随访: 随访正确; 随访未描述; 随访不充分; (5)结果处理是否采用意向处理分析(ITT). 将纳入的研究分为3个等级: A(低度偏倚)所用的评价指标均正确; B(中度偏倚)有1项或1项以上指标未描述; C(高度偏倚) 有1项或1项以上指标不正确或未使用.
1.2.7 资料提取: 两位研究者按照预先设计的资料提取表, 一位研究者提取和录入资料, 另一位核对, 如遇意见不一致双方讨论解决或由第三研究者判断, 缺乏的资料通过电话或信件与作者联系予以补充. 提取的主要资料包括: (1)试验的基本情况、两组患者的基线情况和疾病状况; (2)试验设计、研究时间和随访时间、干预药物(措施)、结局测量指标、失访人数和失访处理、反应研究质量的指标.
统计学处理 采用Cochrane协作网提供的RevMan5.0统计软件进行Meta分析. 计数资料采用比值比(OR)作为疗效分析统计量; 计量资料采用加权均数差(WMD)或标准化均数差(SMD), 各效应量均以95%可信区间(CI)表示. 根据可能出现的异质性因素进行亚组分析, 并采用χ2值检验各研究间的异质性. 当亚组内各研究间有统计学同质性(P>0.1, I2<50%), 采用固定效应模型对各研究进行Meta分析; 如各研究间存在统计学异质性(P<0.1, I2>50%), 采用随机效应模型进行分析. 各亚组间有统计学同质性(P>0.05, I2<50%)采用固定效应模型计算总结果; 存在统计学异质性(P<0.05, I2>50%)采用随机效应模型计算总结果. 异质性源于低质量研究, 进行敏感性分析. 如亚组只有1项研究仍采用Meta分析相同的统计量.
纳入各研究患者的依存性以及治疗组与对照组基线相似性均较好(表1).
| 作者 | 国家 | 平均年龄(岁) | 试验组/对照组(n) | Kps评分 | 化疗疗程(每周期4 wk) | 化疗方案(试验组/对照组)及剂量(mg/m2) |
| 李智强[2] | 中国 | 54.0 | 24/25 | >60 | 4周期 | (O: 130+L: 100+F: 500)/(P: 20+L:100+F: 500) |
| 叶书成 et al[3] | 中国 | 52.8 | 56/52 | ≥70 | ≥3周期 | (O: 130+L: 200+F: 300)/(P: 80+L: 200+F: 300) |
| 冯立艳 et al[4] | 中国 | 52.6 | 26/22 | ≥60 | ≥2周期 | (O: 130+L:75+F: 500)/(P: 20+L: 75+F: 500) |
| 于桂萍 et al[5] | 中国 | 56.0 | 36/37 | ≥70 | ≥2周期 | (O: 130+L:200+F: 500)/(P: 15+L: 200+F: 500) |
| 赵予军 et al[6] | 中国 | 61.0 | 32/33 | ≥70 | ≥2周期 | (O: 130+L:100+F: 250)/(P: 15+L: 100+F: 250) |
| 文世民 et al[7] | 中国 | 54.0 | 23/23 | ≥60 | 3-4周期 | (O: 130+L:200+F: 600)/(P: 15+L: 100+F: 250) |
| 符炜 et al[8] | 中国 | 50.0 | 27/26 | ≥60 | ≥2周期 | (O: 130+L:100+F: 300)/(P: 80+L: 100+F: 300) |
| Al-Batran et al[9] | 美国 | 64.0 | 112/108 | 不清楚 | 5周期 | (O: 85+L: 200+F: 2600)/(P: 50+L: 200+F: 2000) |
本系统评价所纳入的文献存在着不同程度的方法学质量问题, 其中只有2篇[3,9]描述了具体的随机方法, 2篇[8-9]提到了随访, 1篇[9]提到了分配隐藏, 1篇[9]进行了ITT分析. 具体资料见表2.
在中位生存时间方面试验组和对照组之间无统计学差异.
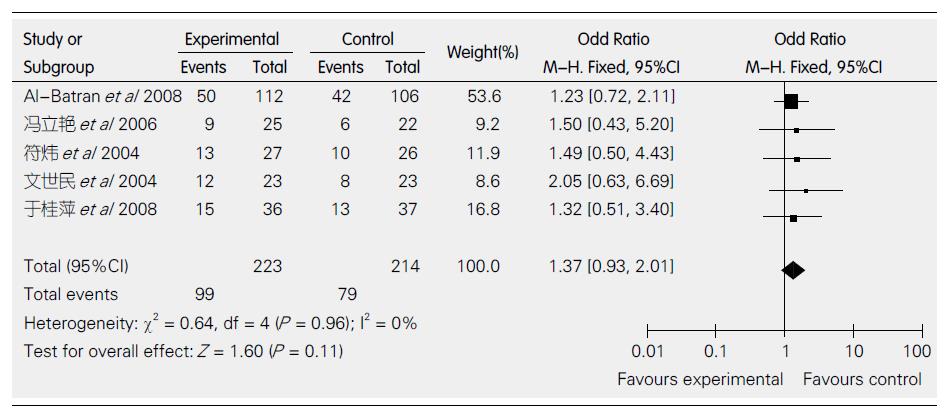
纳入各研究只有5个研究比较了1年生存率的报道, 没有远期生存率的报道. 各研究间无异质性(P = 0.96, I2 = 0%), 采用固定效应模型. 两方案在1年总生存率方面的差异无统计学意义(OR = 1.37, 95%CI: 0.93-2.01, 图1).
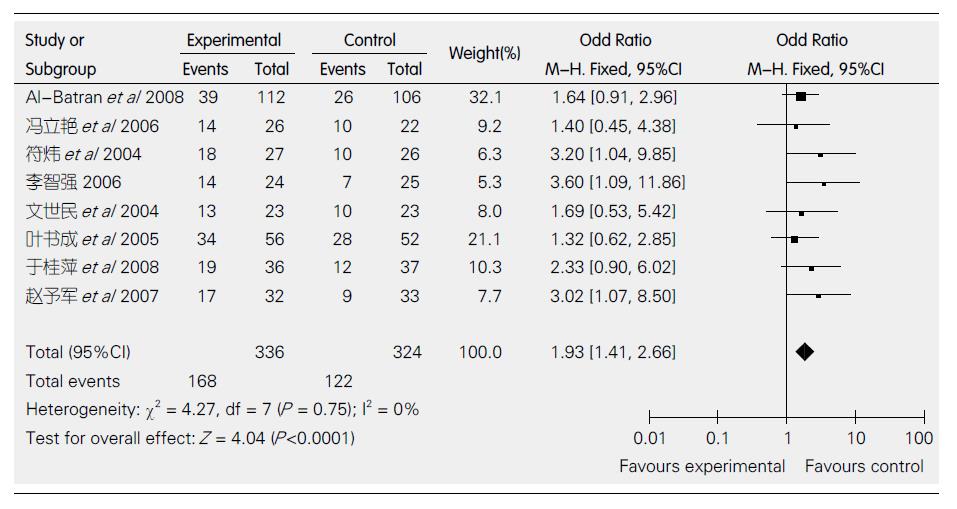
8个研究都比较了总有效率. 各研究间无异质性(P = 0.75, I2 = 0%), 采用固定效应模型. 总有效率方面的差异有统计学意义(OR = 1.93, 95%CI: 1.41-2.66, 图2).
纳入各研究均无生活质量的报道.
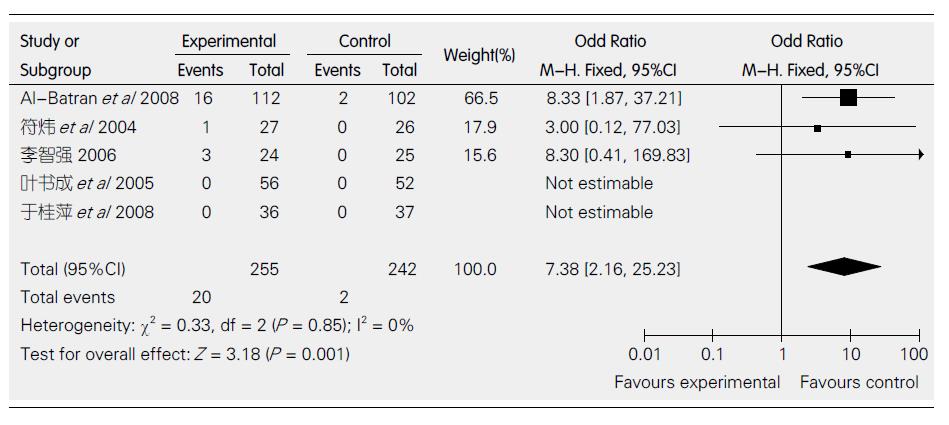
2.7.1 外周神经毒性反应: 5个研究比较了外周神经毒性反应. 各研究间无异质性(P = 0.85, I2 = 0%), 采用固定效应模型. 外周神经毒性反应方面的差异有统计学意义(OR = 7.38, 95%CI: 2.16-25.23, 图3).
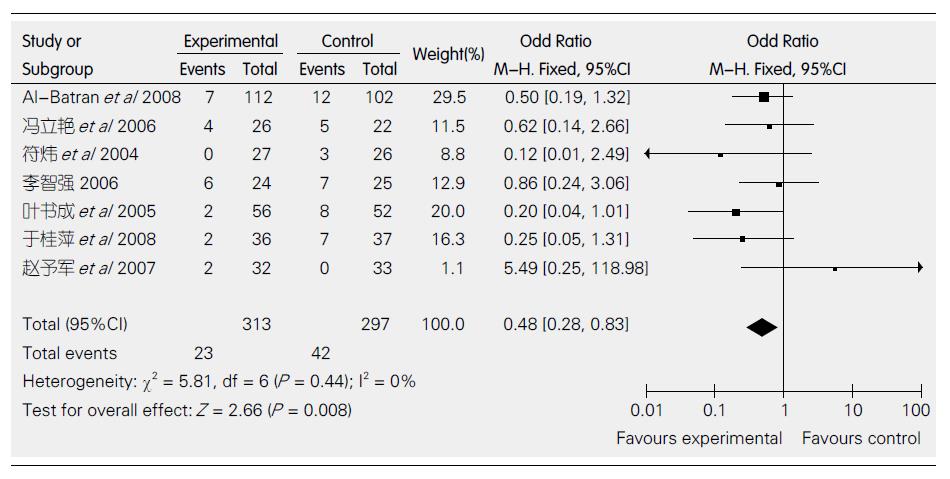
2.7.2 白细胞减少: 7个研究比较了白细胞减少. 各研究间无异质性(P = 0.44, I2 = 0%), 采用固定效应模型. 白细胞减少方面的差异有统计学意义(OR = 0.48, 95%CI: 0.28-0.83, 图4).
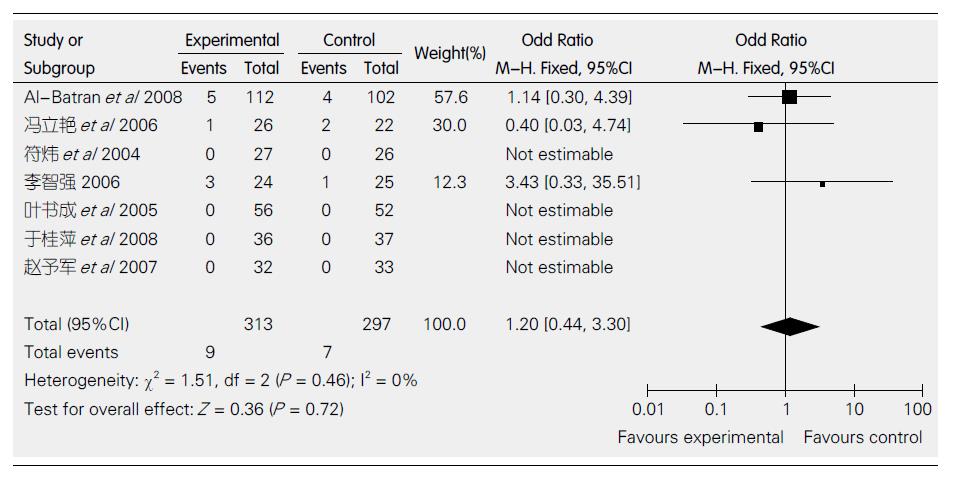
2.7.3 血小板减少: 7个研究比较了血小板减少. 各研究间无异质性(P = 0.46, I2 = 0%), 采用固定效应模型. 血小板减少方面的差异无统计学意义(OR = 1.20, 95%CI: 0.44-3.30, 图5).
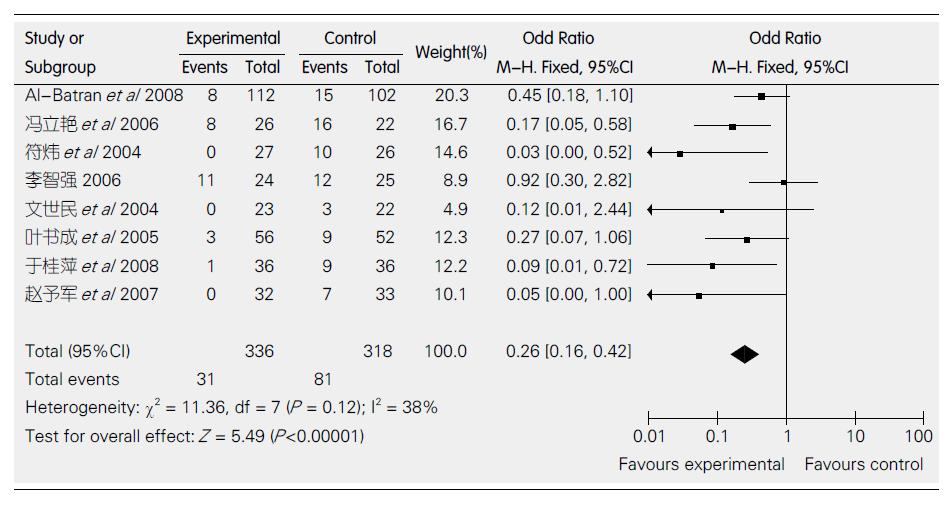
2.7.4 恶心呕吐: 8个研究都比较了恶心呕吐. 各研究间无异质性(P = 0.12, I2 = 38%), 采用固定效应模型. 恶心呕吐方面的差异有统计学意义(OR = 0.26, 95%CI: 0.16-0.42, 图6).
奥沙利铂的不良反应表现为外周神经病变、过敏反应和肝脏毒性等. 最严重的神经病变还是1级(66%), 2级(22%)的不良反应比较常见, 只有不到10%的患者出现3/4级不良反应[10]. 由纳入的文献[2-9]来看, 治疗组3/4级的不良作用中白细胞减少和恶心呕吐轻于对照组, 差异有统计学差异, 而血小板减少方面差异无统计学意义. 在外周毒性反应方面, 试验组大于对照组, 且差异有统计学意义. 因此临床治疗时应慎重, 应根据患者的个体差异制定个体化方案.
胃癌是化疗不太敏感的肿瘤, 但是由于就诊时大部分已经是进展期胃癌, 多数已失去手术机会, 手术切除率约50%, 部分患者在5年内出现原位复发或远处转移, 对不能手术或术后复发及转移的晚期胃癌, 应接受以化疗为主的综合性治疗, 争取延长生命, 提高生活质量. 5-FU是胃癌化疗的重要药物, 单独使用有效率为20%[11]. 亚叶酸钙可增加5-FU的抗癌活性. 铂类化疗药物在晚期胃癌的化疗中已被广泛地应用. 奥沙利铂是第3代铂类抗癌药物, 具有水溶性好、毒性低和抗癌谱广等特点, 剂量限制性毒性为神经系统毒性, 而顺铂主要的限制性毒性为严重的恶心、呕吐即消化系反应. 奥沙利铂的毒性较顺铂显著降低, 患者耐受性好, 同时减少了支持治疗费用, 可广泛与其他药物联用. 奥利沙铂作用强于顺铂, 与顺铂没有交叉耐药性[12], 对顺铂耐药的肿瘤细胞仍然对奥利沙铂敏感. 该研究的Meta分析结果显示: FOLFOX方案的总有效率优于PLF方案, 但是1年生存率没有统计学差异. 目前2种方案临床上应用都比较广泛, 从不良反应来考虑, FOLFOX方案其白细胞下降, 恶心、呕吐发生率均低于PLF方案; 由于晚期胃癌的患者多伴有食欲不振、恶心、呕吐, 无疑选择奥利沙铂, 其消化系毒性轻微, 更有助于提高患者的生活质量和临床受益疗效. 但由于本文所纳入的原始文献中都没有评价患者的2年生存率和5年生存率等, 只评价了1年生存率和总得有效率, 所观察的指标不足, 因此需要更多的临床试验.
本系统评价纳入的研究质量高低不等, 纳入研究对于盲法的描述都不清楚, 因此实施偏倚和测量偏倚的可能性大. 所纳入的研究中只有2篇[3,9]提到了具体的随机方法, 因此选择性偏倚的可能性大. 因此以后的研究应该叙述详细的盲法和分配隐藏的具体方法. 所纳入的文献中也只有2篇[8-9]提到了失访, 1篇[9]进行了ITT分析, 因此在一定程度上都影响了本系统评价的质量.
从方法学可以看出, 本系统评价文献搜集全面, 纳入的研究均为随机对照试验, 质量尚可. 本研究存在潜在的几个缺陷: (1)虽然该Meta分析所纳入文献质量均较高, 但是他是二次研究, 受限于原始研究固有的一些潜在偏倚. (2)纳入文献基本上来自中国, 本研究所纳入文献存在发表偏倚的可能性大. (3)各研究受试对象的基线情况完全相同可能会使合并后结果的存在潜在的偏倚. (4)纳入研究随访时间较短, 测量指标不全面, 部分终点指标如生活质量、中位生存期等无法定量评价, 各研究同样存在报道不全面的问题. (5)各研究在试验进行前均未发表protocol, 与通讯作者联系试验设计实施的具体步骤, 部分环节不清楚. 因此, 纳入研究在设计实施过程中可能存在一些潜在的偏倚.
本系统评价纳入文献存在不同程度方法学质量问题, 一定程度上降低了本系统评价结果的可靠性和全面性, 再加上纳入的原始文献的统计资料的不完整也一定程度上影响了本系统评价的结果的可靠性.
纳入研究报道不全面, 建议以后的研究都能按照CONSORTS声明的要求全面规范的报道研究结果, 晚期胃癌的预后较差, 化疗的目的是为了提高生活质量和延长患者生存期, 因此生活质量的测评是很重要的指标, 建议以后的研究都能按照统一的QOL量表评价生活质量, 本研究显示两方案对在提高患者1年生存率方面无差异, 建议以后的研究能有更长时间的随访, 两方案的远期疗效尚需要更长时间的观察. 同时, 在安全性和有效性相似的情况下, 经济性的评价是确定化疗优选方案一个重要指标, 期待以后的研究能有经济学的评价, 以期为临床决策提供更有利的证据. 本研究纳入研究7篇来自中国, 胃癌的发病在全球有着明显的地域差异, 遗传是胃癌发病的一个很重要的危险因素, 再者地域不同人群的耐药基因可能不同, 因此需要更多来自其他国家和地区的随机对照试验进一步来证实.
FOLFOX方案与常规PLF方案治疗晚期胃癌相比较, 总有效率高, 消化系不良反应小, 但在1年生存率方面无差异, 外周神经毒性方面反应重于顺铂组. 由于受纳入文献质量的限制, 本系统评价所得结论论证强度不高, 应用上述证据尚需慎重. 期待大样本、高质量的随机对照试验进一步证实.
胃癌是我国常见的恶性肿瘤之一, 居恶性肿瘤发病的第2位, 是一种严重威胁人们身体健康的疾病. 胃癌治疗早期仍以手术为主, 但对于不能手术或手术后复发转移的晚期胃癌, 化疗占有十分重要的地位.
房林, 副教授, 同济大学附属上海市第十人民医院普外科
联合化疗可以提高晚期胃癌患者的生活质量和总生存率, 但目前对于晚期胃癌仍无标准的化疗方案, 因此选择效率高、化疗不良反应少的方案是目前化疗研究热点之一, 也一直是肿瘤科医生们不断追求的目标.
本文按照严格的纳入标准, 广泛收集关于奥沙利铂联合5-FU/LV与顺铂联合5-FU/LV比较治疗晚期胃癌的原始随机对照研究, 采用Meta分析可以从统计学角度达到增大样本含量, 提高检验效能的目的, 从而得到比较可靠的结论.
本研究提示, FOLFOX方案与常规PLF方案治疗晚期胃癌相比较, 总有效率高, 由于晚期胃癌的患者多伴有食欲不振, 恶心、呕吐, 选择消化系不良反应小的奥利沙铂, 更有助于提高患者的生活质量和临床受益疗效, 值得临床进一步总结观察.
FOLFOX方案治疗胃癌有较多报道, 作者对全世界中英文相关随机对照试验研究的结果进行Meta分析, 采用Cochrane系统进行评价, 比较其与顺铂联合5-FU/LV方案疗效, 有一定应用价值.
编辑: 李军亮 电编:何基才
| 1. | Lee KH, Hyun MS, Kim HK, Jin HM, Yang J, Song HS, Do YR, Ryoo HM, Chung JS, Zang DY. Randomized, Multicenter, Phase III Trial of Heptaplatin 1-hour Infusion and 5-Fluorouracil Combination Chemotherapy Comparing with Cisplatin and 5-Fluorouracil Combination Chemotherapy in Patients with Advanced Gastric Cancer. Cancer Res Treat. 2009;41:12-18. [PubMed] [DOI] |
| 9. | Al-Batran SE, Hartmann JT, Probst S, Schmalenberg H, Hollerbach S, Hofheinz R, Rethwisch V, Seipelt G, Homann N, Wilhelm G. Phase III trial in metastatic gastroesophageal adenocarcinoma with fluorouracil, leucovorin plus either oxaliplatin or cisplatin: a study of the Arbeitsgemeinschaft Internistische Onkologie. J Clin Oncol. 2008;26:1435-1442. [PubMed] [DOI] |
| 10. | Eng C. Toxic effects and their management: daily clinical challenges in the treatment of colorectal cancer. Nat Rev Clin Oncol. 2009;6:207-218. [PubMed] [DOI] |
| 11. | Rougier P. Docetaxel delivers new management opportunities for gastrointestinal carcinomas. Anticancer Drugs. 1995;6 Suppl 4:25-29. [PubMed] [DOI] |