修回日期: 2009-01-22
接受日期: 2009-02-09
在线出版日期: 2009-05-08
目的: 了解半抗原二硝基氟苯(DNFB)结合乙型肝炎免疫球蛋白(HBIG)后对其抗体功能的影响.
方法: 常温下把HBIG(13 mg/500 µL PBS)水溶液分别与不同剂量(2、4、8 mg)的DNFB混合, 组成2、4、8 mg管, 混匀过夜后离心. 取2、4 mg管及未加DNFB的HBIG水溶液对照管, 各取半量对半稀释, 以HiTrap分子筛柱脱盐, 3个洗脱液再分别作对半系列稀释11次, 3组共组成36个标本. ELISA法检测乙肝表面抗体的效价. 取2、4 mg管的另一半分别予饱和硫酸铵沉淀后取上清, 以紫外光光度分析仪测定A340, 与加入不同剂量DNFB的5个系列浓度作内标的对照管上清相比较, 计算相应管中HBIG结合掉的DNFB量.
结果: 2、4 mg管及对照组, 经双因素方差分析及q检验, 三组间同稀释度间吸光差值(A450-A630)无差异, 而各稀释度间则有非常显著差异(P<0.01). 饱和硫酸铵沉淀结合分光光度法测定证实2、4 mg管中6.5 mg HBIG分别结合DNFB 0.67 mg和0.86 mg, 即每一个HBIG分子分别结合88.72及113.48个DNFB半抗原分子, 约占HBIG氨基酸残基的6.12%和7.86%.
结论: 免疫球蛋白(抗体)可作为半抗原DNFB免疫靶向治疗慢性病毒感染或肿瘤的一种有效载体.
引文著录: 何晓俊, 储艳秋, 蒋公羽, 戴兆云. 抗体可以作为半抗原二硝基氟苯免疫靶向治疗的载体. 世界华人消化杂志 2009; 17(13): 1350-1354
Revised: January 22, 2009
Accepted: February 9, 2009
Published online: May 8, 2009
AIM: To investigate the influence of dinitroflourobenzene (DNFB) on the antibody titer of hepatitis B immunoglobulin (HBIG).
METHODS: Three different doses (2, 4, 8 mg) of DNFB were mixed with phosphate buffer solution (PBS) of HBIG respectively, 13 mg in a volume of 500 µL PBS, while same solutions of HBIG were used as controls. The 2, 4 mg tubes and the control tubes were not precipitated except for the 8 mg tube with 10 000 r/min configuration. The 3 transparent tubes were desalted with column of Sephadex G-25 Superfine HiTrap respectively. All of the eluents of the 3 tubes were half-diluted consecutively with phosphate buffer saline (PBS) respectively to change totally into 36 samples of 2 mg group, 4 mg group and control group, with 12 in each group. The above samples were all tested for the antibody titer of HBIG using ELISA. The 2 mg tube, 4 mg tube and the control tube were all precipitated in solution of saturated (NH4)2SO4. Compared with standard curves of both quantity of DNFB and gauges of A340 in supernants made of same controlled tubes, the remaining DNFB in supernants in different tubes were all obtained respectively.
RESULTS: Except for the 8 mg group, there were no difference in the 3 groups in terms of the absorbance values (A450-A630) of HBIG in same dilution grade of any group with two-way anova (analysis of variance)(P > 0.05). However there was great difference between different dilution grades in any group with two-way anova (P < 0.01). The 6.5 mg of HBIG in the 2 mg tube and 4 mg tube were respectively combined with 0.67 mg and 0.86 mg of DNFB, meaning that each molecule of HBIG with 88.72 and 103.48 molecules of DNFB, namely 6.12% and 7.86% in residual amino acid of each molecule of HBIG combined with DNFB.
CONCLUSION: The immune globulin (antibody) might be used as a carrier for DNFB target therapy.
- Citation: He XJ, Chu YQ, Jiang GY, Dai ZY. A potential carrier for targeted therapy of DNFB hapten-induced immune. Shijie Huaren Xiaohua Zazhi 2009; 17(13): 1350-1354
- URL: https://www.wjgnet.com/1009-3079/full/v17/i13/1350.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i13.1350
半抗原是一类特殊的抗原, 他是指那些不能单独, 需与机体蛋白(载体)结合后形成完全抗原才能激发机体产生免疫的抗原. 二硝基氟苯(dinitrofluorobenzene, DNFB)是最常用的半抗原之一, 他可直接结合蛋白质, 激发机体产生细胞免疫反应[1-2], 皮肤试验可诱导红肿, 甚至水泡溃烂等变态反应, 20多年来一直作为抗过敏药物疗效评价及临床测试人体细胞免疫的标准方法. 为研究DNFB结合蛋白后对其功能的影响, 本课题组以不同剂量比的DNFB溶解到乙型肝炎免疫球蛋白(hepatitis B immunoglobulin, HBIG)溶液中, 两者混匀过夜结合后以分子筛去除游离的DNFB, 取结合了DNFB的HBIG, 以酶联免疫法(ELISA)检测该免疫球蛋白的抗体效价, 并进行了结合量测定, 从而评估DNFB结合的效应.
HBIG是上海市新兴医药公司生产的药品(批号为: 20050201-2), 100 IU/mL, 蛋白含量为130 g/L, 平均相对分子质量为160 kDa. 测定乙型肝炎表面抗体试剂盒为上海科华生物科技公司产品. 酶标测定仪由上海仪器厂出品. DNFB均为分析纯级产品. 精细脱盐柱(Sephadex G-25 Superfine HiTrap)从Amersham Biosciences公司购买. 酶标仪(Thermo labsystems, Model No. 353)为上海生化仪器厂产品. UV-240型紫外分光光度计购自日本Shimadzu株式会社. PBS为pH为8.4的磷酸钠缓冲溶液.
1.2.1 HBIG结合DNFB: 四管500 mL PBS各含13 mg HBIG, 分别加入DNFB 2、4、8及0 mg作为2 mg管、4 mg管、8 mg管和对照管. 各管标本混匀后, 置4℃结合过夜.
1.2.2 脱盐取结合物: 四管标本过夜结合后经4000 g于4℃下离心10 min, 8 mg管有少量沉淀. 溶液澄清的2 mg管、4 mg管和对照管各取半量以PBS稀释至1 mL, 以Sephadex G-25 Superfine HiTrap柱脱盐, 按说明书把无色的第一段1.5 mL丢弃, 取第二段黄色洗脱液2 mL作为DNFB结合物.
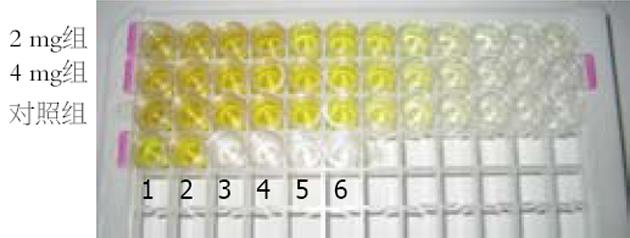
1.2.3 分组及抗体测定: 2 mg管、4 mg管、对照管的各以上脱盐结合物作为母液, 分别取50 μL以PBS进行对半倍比系列稀释至1∶1024, 加上各自未稀释的第一管, 分别制成2 mg管、4 mg管、对照组的系列稀释度溶液各12管. 各组均按由低到高的稀释度排列, 第1、2、3行分别为2 mg管、4 mg管和对照组共36个标本. 测定方法: 按试剂盒说明书测定乙肝表面抗体效价. 对以上36个标本进行顺序加样, 并同时按测定要求设立第1, 第2阳性对照, 第1, 第2阴性对照及2个空白对照, 共42个加样孔. 用酶标仪分别测定450 nm和630 nm的两个吸光值数据, 取差值进行比较. 半抗原2 mg管、4 mg管及对照组对半系列稀释与吸光值的关系.
1.2.4 HBIG结合DNFB直观及定量分析: 取澄清的2 mg管、4 mg管和对照管标本剩余的另一半溶液250 μL, 分别加入无离子水至500 μL, 各加入硫酸铵380 mg配成饱和溶液, 置4℃下1 h后 4000 g沉淀, 2 mg管、4 mg管和对照管标本沉淀. 取各管上清400 μL, 各加入无离子水1100 μL, 对照管上清标本调零, 以UV-240型紫外分光光度计测定A340. 另以同样方法制取的对照管上清400 μL共5管, 分别加入内标量DNFB 0.2 mg, 0.5 mg, 1.0 mg, 1.5 mg, 2.0 mg混匀, 寻找最大吸光峰值的波长, 再测定各管该波长的吸光度值A340, 制作标准曲线.
统计学处理 3个配伍组间及其12种不同稀释度间比较, 采用双因素方差分析(Two-way ANOVA)及q检验. 所有数据采用SPSS10.0软件进行分析.
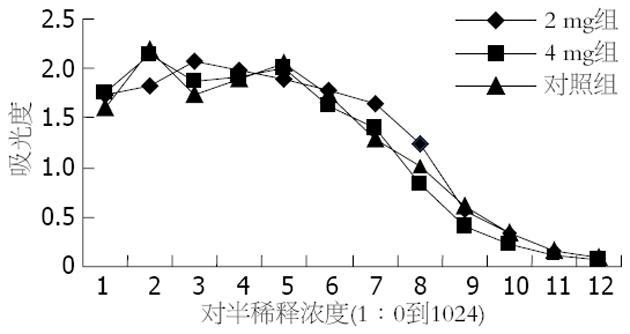
双因素方差分析及q检验, 三个配伍组间比较(F1 = 1.43, P1 = 0.262>0.05), 提示无显著差异, 而12种稀释度间比较(F2 = 117.38, P2<0.0001), 提示有非常显著差异(表1, 图1-2).
| 稀释度 | ||||||||||||
| 1∶0 | 1∶1 | 1∶2 | 1∶4 | 1∶8 | 1∶16 | 1∶32 | 1∶64 | 1∶128 | 1∶256 | 1∶512 | 1∶1024 | |
| 2 mg管 | 1.732 | 1.820 | 2.083 | 1.989 | 1.887 | 1.788 | 1.638 | 1.239 | 0.563 | 0.341 | 0.151 | 0.089 |
| 4 mg管 | 1.759 | 2.144 | 1.859 | 1.910 | 2.009 | 1.620 | 1.403 | 0.828 | 0.397 | 0.219 | 0.107 | 0.058 |
| 对照组 | 1.606 | 2.186 | 1.737 | 1.885 | 2.045 | 1.745 | 1.279 | 1.021 | 0.607 | 0.341 | 0.154 | 0.079 |
从混合了DNFB的HBIG与未混合DNFB的HBIG溶液对饱和硫酸铵沉淀的反应看, 半抗原结合免疫球蛋白, 并与他一起在水溶液中沉淀(图3).
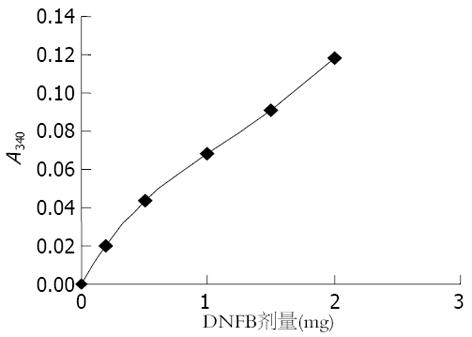
DNFB在饱和(NH4)2SO4上清液中紫外吸收最大光谱峰为340 nm. 在饱和(NH4)2SO4沉淀HBIG后, 以同样方法制作的上清液中分别加入不同内参照量的DNFB, 与所相应测出的A340值制成标准曲线(图4). 而2 mg管、4 mg管上清在A340分别为0.026及0.062. 2 mg管、4 mg管上清DNFB含量分别应为0.26 mg及0.91 mg. 以此折算, 2 mg管、4 mg管中HBIG分别结合了0.67 mg、0.86 mg的DNFB.
以DNFB外搽皮肤作为皮炎动物模型, 可用于评价抗过敏药物的疗效. 临床上也以此方法测定Ⅵ型变态反应. 长期以来, 两者均是经典方法[1-2], 原理是DNFB渗透到皮下, 与皮下的蛋白结合产生抗原性改变, 从而诱导迟发性T细胞超敏反应(DTH)[3-6]. 但DNFB作为半抗原结合蛋白质后, 对该蛋白功能是否有影响至今未见报道.
HBIG为HBsAg免疫人体后分离的免疫球蛋白, 纯度高达99%以上, 为HBsAg的多位点多克隆抗体蛋白, 由于活性测定方便, 效价与抗体活性呈线性关系, 来源又较便利, 我们就选取他作为研究目标. 我们分别以2、4、8 mg的3种不同剂量的DNFB, 加到已有PBS液稀释至500 μL的含13 mg HBIG的3管中, 并采用未加DNFB的同样HBIG溶液作对照, 除出现沉淀的8 mg管外, 其余3管均以分子筛柱去除小分子DNFB, 取其洗脱结合物经系列对半稀释, 以ELISA测定乙型肝炎表面抗体效价, 其结果经双因素方差分析(Two-way ANOVA), 3个配伍组间比较, 各组间无显著差异(P>0.05), 提示DNFB结合HBIG后, 对其功能没有任何影响. 可能是DNFB与HBIG分子内部的疏水键结合, 而不影响分子表面结合抗原的亲水键有关. 而各组中12种稀释度间比较, 有非常显著差异(P<0.01). 8 mg管出现沉淀, 提示这样的结论需在一定范围内才会成立, 同时也说明半抗原与抗体间存在相互作用, 加入的DNFB剂量过大, 可破坏HBIG溶液的稳定性, 出现浑浊而沉淀, 这与我们以往报道的大量DNFB结合HBsAg的变化相吻合[7]. 从饱和硫酸铵溶液沉淀结果及过分子筛柱时黄色的DNFB分布变化看, 有明显的半抗原实现了与HBIG的结合. 作者以饱和硫酸铵溶液沉淀HBIG, 利用内参照法, 以UV-240型紫外分光光度计定量分析证实, 2 mg管和4 mg管分别有0.67 mg及0.86 mg的DNFB实现了与DNFB的结合, 由于DNFB与免疫球蛋白分子质量比为0.0011625, 理论上讲, 这两种剂量(2、4 mg)相当于每毫克的HBIG分别结合了0.104 mg及0.132 mg的半抗原DNFB, 每一个HBIG(约含1450个氨基酸残基)分别结合了88.72及113.48个DNFB, 约占其氨基酸残基的6.12%和7.86%.
在医学上, 以与此类似的二硝基氯苯(DNCB)丙酮溶液皮肤外用诊断及治疗疾病已有20-30年的时间. 传统文献认为[2-6], DNCB外搽皮肤后即可与皮下蛋白结合, 经1 wk机体可产生针对半抗原的DTH反应. 杨国亮 et al早在20世纪80年代就以DNCB外搽法成功治愈皮肤病毒性疣, 治愈率达90%[2-5]. 除了外搽治疣外, 更常用于测定机体的非特异性细胞免疫功能, 还用于治疗斑秃[6]. 杜光辉 et al[8]以含10 mg的DNCB丙酮溶液瘤内注射治疗小鼠艾氏移植瘤, 疗效明显, 小鼠寿命延长率较单纯丙酮组, 对照组分别延长809.2%, 128.5%, 几乎已达小鼠自然寿命. Berd[9]以DNFB与自体癌瘤结合产生的DNP(二硝基酚)修饰的自体癌瘤, 作为自体疫苗治疗癌症有明显疗效, 有效率达45%, 有的同时也出现了远处肺部癌灶的好转, 病理上出现炎性细胞的浸润, 该治疗不良反应轻, 仅有个别注射处皮疹, 已申报美国专利[10]. 戴兆云 et al[11]也新近发现剂量小至1 mg的DNCB无水乙醇溶液瘤内注射治疗移植性恶性黑色素瘤小鼠, 抑瘤率也分别高达96.73%(对PBS液)、94.06%(对无水乙醇)的疗效, 肿瘤接种后1 mo时, 疗效竟是无水酒精注射法的16倍多(剥出的平均瘤重分别为0.13, 2.19 g), 特别是von et al[12]及Herrmann et al[13]更是以DNCB外搽肿瘤灶, 分别成功治愈了恶性黑色素瘤、恶性Merkel氏瘤各1例. 并观察到强大的抗瘤免疫, 看来使用很小剂量的半抗原可在一定程度上诱导打破免疫耐受. 由于抗体结合半抗原DNFB后不影响其抗体活性, 那利用结合半抗原的单抗可进行免疫靶向治疗[14], 从而激发细胞免疫, 对肿瘤及慢性感染的防治可能具有很大的实用意义.
虽然半抗原DNFB结合蛋白质的特性已发现了数十年了, 但对其结合蛋白质的化学本质仍不是很清楚. 最初我们发现DNFB结合的蛋白质没有发生共价键性结合[15-16], 提出与疏水性结合有关, 但由于当时未对结合后的沉淀物进行检测, 特别是Aleksic et al[17]对结合物的深入研究, 确认半抗原的结合, 与甲醛对蛋白的作用[18]有些相似, 实际上是共价键性结合, 这为免疫靶向治疗打下了化学基础. Lu et al发现带有半抗原结构[19-20](DNFB或FITC)的叶酸偶联物作肿瘤靶向治疗, 疗效较为突出, 甚至出现了6只小鼠移植瘤中, 2只小鼠的肿瘤完全消退, 并建立了完全的特异抗瘤免疫, 可阻断同样肿瘤的再次攻击. 所有这些为利用半抗原进行免疫靶向治疗癌症, 以及治愈像慢性乙型肝炎那样的慢性感染开拓了新的研究方向.
二硝基氟苯(DNFB)是最常用的半抗原之一, 他可直接结合蛋白质, 激发机体产生细胞免疫反应, 皮肤试验可诱导红肿, 甚至水泡溃烂等变态反应, 20多年来一直作为抗过敏药物疗效评价及临床测试人体细胞免疫的标准方法.
高春芳, 研究员, 中国人民解放军第二军医大学附属长征医院全军医学免疫诊断中心/实验诊断科.
目前研究铂类配合物的重点和热点是对现有的经典结构的改造, 如将单核的铂类配合物改为双核或多核, 增加特异性和疗效; 增加空间阻位, 防止耐药性的发生; 引入新的极性离子, 增加可溶性; 增加脂溶性, 来改变用药途径, 等等. 以此达到高效、低毒、水溶性好、选择性高、与顺铂无交叉耐药性、可口服的新型铂类.
Lu et al发现带有半抗原结构(DNFB或FITC)的叶酸偶联物作肿瘤靶向治疗, 疗效较为突出, 甚至出现了6只小鼠移植瘤中, 2只小鼠的肿瘤完全消退, 并建立了完全的特异抗瘤免疫, 可阻断同样肿瘤的再次攻击.
免疫球蛋白(抗体)可作为半抗原DNFB免疫靶向治疗慢性病毒感染或肿瘤的一种有效载体.
本研究总体设计合理, 方法可靠, 结论明确, 具有较好的学术价值.
编辑: 李军亮 电编:何基才
| 1. | 中华人民共和国卫生部药政局编. 新药(西药)临床前研究指导原则汇编. 北京: 人民卫生出版社 1993; 135-136. |
| 2. | 杨 国亮, 王 侠生. 现代皮肤病学. 上海: 上海医科大学出版社 1996; 61-78. |
| 3. | Buckley DA, Du Vivier AW. The therapeutic use of topical contact sensitizers in benign dermatoses. Br J Dermatol. 2001;145:385-405. [PubMed] [DOI] |
| 4. | Gibbs S. Topical immunotherapy with contact sensitizers for viral warts. Br J Dermatol. 2002;146:705. [PubMed] [DOI] |
| 5. | Gibbs S, Harvey I, Sterling J, Stark R. Local treatments for cutaneous warts: systematic review. BMJ. 2002;325:461. [PubMed] [DOI] |
| 9. | Berd D. Contribution of dead cells to the immunogenicity of an autologous, hapten-modified melanoma vaccine. Vaccine. 2003;21:795-797. [PubMed] [DOI] |
| 10. | Berd D, inventor; Thomas Jefferson University, assignee. Composition comprising tumor cells and extracts and method of using thereof. 2002;October 1. |
| 12. | von Nida J, Quirk C. Successful treatment of in-transit melanoma metastases using topical 2-4 dinitrochlorobenzene. Australas J Dermatol. 2003;44:277-280. [PubMed] [DOI] |
| 13. | Herrmann G, Groth W, Krieg T, Mauch C. Complete remission of Merkel cell carcinoma of the scalp with local and regional metastases after topical treatment with dinitrochlorbenzol. J Am Acad Dermatol. 2004;50:965-969. [PubMed] [DOI] |
| 14. | Lu Y, Low PS. Targeted immunotherapy of cancer: development of antibody-induced cellular immunity. J Pharm Pharmacol. 2003;55:163-167. [PubMed] [DOI] |
| 15. | Dai ZY, Chu YQ, Wu B, Wu L, Ding CF. Investigation of non-covalent complexes of glutathione with common amino acids by electrospray ionization mass spectrometry. Acta Pharmacol Sin. 2008;29:759-771. [PubMed] [DOI] |
| 16. | Wu B, Chu YQ, Dai ZY, Ding CF. Interaction between cytochrome c and the hapten 2,4-dinitro-fluorobenzene by electrospray ionization mass spectrometry. Chin J Chem Phys. 2008;21:217-220. [DOI] |
| 17. | Aleksic M, Pease CK, Basketter DA, Panico M, Morris HR, Dell A. Investigating protein haptenation mechanisms of skin sensitisers using human serum albumin as a model protein. Toxicol In Vitro. 2007;21:723-733. [PubMed] [DOI] |
| 18. | Metz B, Kersten GF, Hoogerhout P, Brugghe HF, Timmermans HA, de Jong A, Meiring H, ten Hove J, Hennink WE, Crommelin DJ. Identification of formaldehyde-induced modifications in proteins: reactions with model peptides. J Biol Chem. 2004;279:6235-6243. [PubMed] [DOI] |
| 19. | Lu Y, You F, Vlahov I, Westrick E, Fan M, Low PS, Leamon CP. Folate-targeted dinitrophenyl hapten immunotherapy: effect of linker chemistry on antitumor activity and allergic potential. Mol Pharm. 2007;4:695-706. [PubMed] [DOI] |
| 20. | Lu Y, Xu LC, Parker N, Westrick E, Reddy JA, Vetzel M, Low PS, Leamon CP. Preclinical pharmacokinetics, tissue distribution, and antitumor activity of a folate-hapten conjugate-targeted immunotherapy in hapten-immunized mice. Mol. Cancer Ther. 2006;5:3258-3267. [PubMed] [DOI] |