修回日期: 2007-01-10
接受日期: 2007-01-23
在线出版日期: 2007-04-08
目的: 研究白花蛇舌草总黄酮(flavonoids from Hedyotis diffusa willd., FHD)抑制人肝癌细胞SMMC-7721的靶基因调控.
方法: 分别提取人正常肝细胞、人肝癌SMMC-7721细胞和FHD作用后的SMMC- 7721细胞的总RNA, 逆转录合成单链、双链cDNA后, 体外转录合成生物素标记的cRNA与人HO4基因表达谱芯片杂交, 扫描杂交芯片图像, 利用软件获得FHD抗肝癌的靶基因, 对靶基因进行生物信息学分析.
结果: 共找到20条FHD抑制肝癌细胞的有效靶基因, 即给予FHD后, 通过上调或下调, 这些显著异常表达的基因被恢复至正常水平. 其中, 癌基因pim-1(Hs.81170)、rel(Hs.858)、ras(Hs.204354)、fos(Hs.25647)、myc (Hs.79070)、met(Hs.285754)以及编码Bcl-2相关蛋白的基因(Hs.227817)被显著下调; 成纤维细胞生长因子(Hs.284244)、胰岛素样生长因子1受体(Hs.239176)、胰岛素样生长因子结合蛋白(Hs.1516)、G蛋白偶联受体(Hs.23016)、酪氨酸蛋白磷酸化酶(Hs.227777)、转录因子12(Hs.21704)、转录因子CP2(Hs.154970)等与细胞生长相关的信号转导分子被显著下调; 细胞因子IL-1(Hs.1722)被显著下调; 丝裂原活化的蛋白激酶(MAPK)信号传导通路成员MAP2K6(Hs.118825)和MAP3K12(Hs.211601)被显著上调; 抑癌基因NF-2(Hs.902)被显著上调; 编码T细胞活化共刺激信号分子的TNFSF9(Hs.1524)、TNFSF7(Hs.99899)基因被显著上调. 这些基因均与肝癌的发生、发展密切相关.
结论: FHD抑制SMMC-7721细胞的作用由多条靶基因协同, 并通过胞内、胞外信号转导途径协调完成.
引文著录: 张硕, 宋衍芹, 周三, 倪同尚, 岳旺. 白花蛇舌草总黄酮抑制人肝癌细胞的靶基因调控. 世界华人消化杂志 2007; 15(10): 1060-1066
Revised: January 10, 2007
Accepted: January 23, 2007
Published online: April 8, 2007
AIM: To investigate the target gene regulation during the inhibition of human hepatoma cell line SMMC-7721 induced by favonoids from Hedyotis diffusa willd. (FHD).
METHODS: The total RNA was extracted from normal human hepatic cells, SMMC-7721 cells and FHD-treated SMMC-7721 cells, and synthesized into double strand cDNA templates. Transcription of cRNA probe with biotin labeling was performed, and then the obtained cDNA was hybridized with human HO4 gene profile. Cy3 dye was detected with Scan array 5000, and the image information was converted into numeric data. Clusting analysis was performed with IMAGNE Ⅳ software.
RESULTS: Twenty target genes were found to be involved in the FHD-induced inhibition of human hepatoma cells. After FHD treatment, these genes were either up-regulated or down-regulated. Among these genes, oncogenes such as pim-1 (Hs.81170), rel (Hs.858), ras (Hs.204354), fos (Hs.25647), myc (Hs.79070), met (Hs.285754) and Bcl-2-related protein A1 (Hs.227817) were down-regulated; some genes related with cell signal transduction during tumor developing process, such as fibroblast growth factor 2 (Hs.284244), insulin-like growth factor 1 receptor (Hs.239176), insulin-like growth factor-binding protein 4 (Hs.1516), G protein-coupled receptor (Hs.23016), protein tyrosine phosphatase type IVA (Hs.227777), transcription factor 12 (Hs.21704), transcription factor CP2 (Hs.154970), were down-regulated; cytokine interleukin-1 (Hs.1722) was also down-regulated; mitogen-activated protein kinase kinase 6 (Hs.118825) and mitogen-activated protein kinase kinase kinase 12 (Hs.211601), the members of MAPK signal transduction pathway, were up-regulated; NF-2 (Hs.902), the anti-oncogene was up-regulated; the genes which encode the T-cell activation co-stimulatory signal molecules such as TNFSF9 (Hs.1524) and TNFSF7 (Hs.99899) were also up-regulated. All the above genes were closely related with the occurrence and development of hepatoma.
CONCLUSION: FHD inhibits SMMC-7721 cells by co-regulation of various genes, which are involved in the intracellular and extracellular signal transduction pathways.
- Citation: Zhang S, Song YQ, Zhou S, Ni TS, Yue W. Target gene regulation involved in the inhibitory effect of favonoids from Hedyotis diffusa willd. on human hepatoma cell line SMMC-7721. Shijie Huaren Xiaohua Zazhi 2007; 15(10): 1060-1066
- URL: https://www.wjgnet.com/1009-3079/full/v15/i10/1060.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v15.i10.1060
白花蛇舌草(Hedyotis diffusa willd.)是茜草科耳草属植物, 广泛分布于亚热带地区, 在中国云南、广西、广东、福建、浙江、江苏等地均有生长. 研究表明, 其具有抗菌、增强免疫、抗肿瘤、抗衰老等作用[1]. 经药物化学分析, 其中的主要成分为蒽醌类、环烯醚萜苷类、甾醇类、黄酮类等[2]. 近年来, 我们对其抗癌作用展开研究, 发现黄酮类成分在体内、体外实验中对肝癌细胞表现出显著的抑制作用. 为了探讨白花蛇舌草总黄酮(FHD)抗肝癌的机制, 我们采用基因芯片技术研究其抑制人肝癌细胞SMMC-7721的靶基因调控.
白花蛇舌草经成都中医药大学药学院中药鉴定教研室鉴定后, 由药物化学教研室提取FHD(经检测, 其纯度为85.63%), 经500 mL/L乙醇溶解, RPMI1640(Gibco)稀释至1000 mg/L, 0.22 μm滤膜过滤除菌; 人肝癌细胞SMMC-7721瘤株, 由四川大学华西医学中心肿瘤研究所提供; 人正常肝叶组织, 由成都中医药大学附属医院提供; ExpressChipTM基因芯片系统的人HO4基因芯片(为包含3360个点的寡核苷酸基因芯片, 基因列表见网址: http://www.mergen-ltd.com), 由美国Mergen公司提供.
设肝正常细胞组、肿瘤细胞组和给药组. 获得正常肝叶组织后, 采用"原位两步灌注法"体外灌注分离肝组织[3-5]. 前灌流液为含EDTA、无Ca2+和Mg2+的Hanks液500 mL, 其中300 mL灌流后丢弃, 另200 mL循环灌流, 灌速为80-100 mL/min, 时间约10-15 min; 第二步灌流液为0.05%胶原酶液, 循环灌速为50-70 mL/min, 时间约10 min. 灌流结束后, 用剪刀划破肝包膜, 剔除大块纤维结缔组织, 收集细胞悬液, 置37 ℃条件下消化10-15 min. 用RPMI1640培养液终止消化, 纱布过滤2次, 反复离心3次获取肝细胞, 以RPMI1640稀释, 按1×108/L接种于培养瓶中, 设为肝正常细胞组.
将人肝癌细胞SMMC-7721接种于培养瓶, 37 ℃培养18 h使细胞贴壁, 分别设给药组和肿瘤细胞组, 给药组加入FHD溶液, 使其终浓度为100 mg/L; 肿瘤细胞组不加药. 各组细胞设定、加药完成后, 于50 mL/L CO2, 37 ℃条件下继续培养48 h. 根据TRIzol Reagent(Life Technologies Inc)的步骤提取总RNA, 通过10 g/L琼脂糖电泳检验质量, 并使用UV分光光度计测RNA的浓度和纯度, 浓度须达到要求的10-20 μg量, 其吸光度A260/A280比值须不低于1.7.
根据cDNA Synthesis kit(Roche Inc)操作说明进行单链cDNA、双链cDNA的合成, 再根据MEGAscriptTM transcription kit (Amibion Inc)操作说明进行生物素标记. 使用TSATM(Tyramide Signal Amplification) Detection System(NEN Life Science)检验验证. 根据ExpressChipTM DNA Microarray System试剂盒操作说明进行HO4芯片杂交. 将标记生物素的cRNA交联在玻片上, 与Streptavidin-HRP联接, 加入Cy3荧光染料, 聚集在HRP周围, 放大信号, 洗涤. 用ScanArray5000和ScanArray Microarray Analysis System进行图像扫描. 使用QuantiArray Quantitative Microarray Analysis软件(GSL Lumonics)将扫描的图像信息转化为数据, 进行标准化, 使用IMAGENE Ⅳ进行差异分析. 肝癌细胞(C)与肝正常细胞(N)基因表达丰度比值Ratio≥2或≤0.5, 且给药后肝癌细胞(T)与肝正常细胞(N)基因表达丰度比值Ratio接近1时, 所对应的基因为有效靶基因.
在倒置显微镜下观察, 肿瘤细胞组细胞始终保持大小均匀, 为多角形, 呈铺展状, 细胞膜完整, 细胞核淡染, 核质均匀, 核膜轮廓清晰, 核仁明显. 给药组细胞经FHD作用48 h, 经HE染色, 呈现出典型的细胞凋亡特征: 细胞皱缩为圆形, 体积缩小, 核深染, 染色质浓缩, 固缩核呈团状、环状及新月状, 细胞质浓缩; 透射电镜下可见部分细胞出现染色质边集、浓缩, 在核膜下形成小团块及胞质起泡, 凋亡小体形成.
该基因芯片包括空白点96个(每个点阵含24个), 阴性对照点8个(每个点阵含2个), 阳性对照点88个(每个点阵含22个), 并且这些阳性对照点存在不同的稀释度. 从所得的结果看, 空白点与阴性对照点的杂交信号很低, 阳性对照点很强, 并且存在饱和点与不饱和点, 有力证明了数据的可靠性.
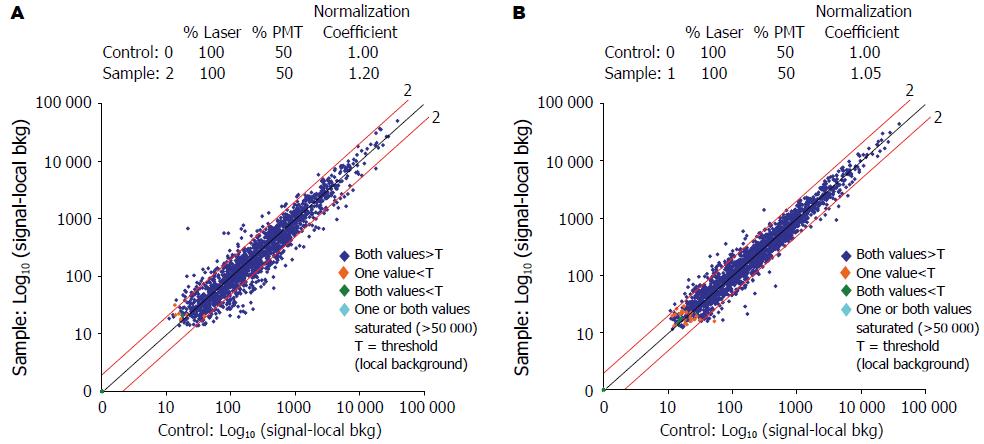
分别将肝癌细胞与肝正常细胞、给药后的肝癌细胞与肝正常细胞基因芯片谱做对比分析, 所得的散点图如图1所示, 每个点代表一个基因, 点的横坐标为基因在肝正常细胞的丰度值, 图1A纵坐标为基因在肝癌细胞的丰度值, 图1B纵坐标为基因在给药后的肝癌细胞的丰度值. 在三条45°斜线内的点表示基因在两张芯片的丰度值之比在0.5-2之间, 越接近中间对角线的点比值越接近1, 表示基因在两张芯片上差异越小, 越偏离中间对角线的点表示基因在两张芯片上差别越大, 在两条标记为"2"的斜线以外的点, 表示该点在两张芯片的比值大于2或者小于0.5, 提示基因的表达存在显著差异. 根据数据分析, 共找到20条FHD抑制肝癌细胞的有效靶基因(表1, 表2). 其中, Hs.1722, Hs.227777, Hs.284244, Hs.79070, Hs.858, Hs.21704, Hs.204354, Hs.23016, Hs.227817, Hs.1516, Hs.81170, Hs.25647, Hs.285754, Hs.154970, Hs.239176基因在人肝癌细胞SMMC-7721中表达显著升高; Hs.211601, Hs.99899, Hs.118825, Hs.902, Hs.1524基因在SMMC-7721中表达显著下降; 给予FHD后, 上述基因恢复至正常水平.
| Accession | Gene description | Ratio | |
| C/N | T/N | ||
| Hs.1722 | Interleukin 1 alpha | 5.0 | 1.0 |
| Hs.227777 | Protein tyrosine phosphatase type IVA, member 1 | 4.3 | 1.0 |
| Hs.284244 | Fibroblast growth factor 2 (basic) | 3.7 | 1.0 |
| Hs.79070 | V-myc avian myelocytomatosis viral oncogene homolog | 3.4 | 1.0 |
| Hs.858 | V-rel avian reticuloendotheliosis viral oncogene homolog B (nuclear factor of kappa light polypeptide gene enhancer in B-cells 3) | 3.1 | 1.0 |
| Hs.21704 | Transcription factor 12 (HTF4, helix-loop-helix transcription factors 4) | 3.1 | 1.0 |
| Hs.204354 | Ras homolog gene family, member B | 2.9 | 1.0 |
| Hs.23016 | G protein-coupled receptor | 2.6 | 1.0 |
| Hs.227817 | Bcl2-related protein A1 | 2.3 | 1.0 |
| Hs.1516 | Insulin-like growth factor-binding protein 4 | 2.22 | 1.0 |
| Hs.81170 | Pim-1 oncogene | 2.1 | 1.0 |
| Hs.25647 | V-fos FBJ murine osteosarcoma viral oncogene homolog | 2.1 | 1.0 |
| Hs.285754 | Met proto-oncogene (hepatocyte growth factor receptor) | 2.1 | 1.0 |
| Hs.154970 | Transcription factor CP2 | 2.0 | 1.0 |
| Hs.239176 | Insulin-like growth factor 1 receptor | 2.0 | 1.0 |
| Accession | Gene description | Ratio | |
| C/N | T/N | ||
| Hs.211601 | Mitogen-activated protein kinase kinase kinase 12 | 0.45 | 1.0 |
| Hs.99899 | Tumor necrosis factor (ligand) superfamily, member 7 | 0.39 | 1.0 |
| Hs.118825 | Mitogen-activated protein kinase kinase 6 | 0.36 | 1.0 |
| Hs.902 | Neurofibromin-2 (bilateral acoustic neuroma) | 0.24 | 1.0 |
| Hs.1524 | Tumor necrosis factor (ligand) superfamily, member 9 | 0.20 | 1.0 |
肿瘤的形成是一个多因素、多途径相互作用的复杂过程, 往往涉及到多个基因的变化或参与. 通过各种干预手段调控肿瘤相关基因的表达已经发展为一种新的肿瘤治疗手段[6].
癌基因(oncogene)是人类或动物细胞固有的一类基因, 在正常细胞中, 他们不表达或者仅有限度地表达, 对细胞无害, 其表达产物在细胞正常代谢及信号传导中起到必不可少的调节作用, 此时称之为原癌基因. 在某些因素作用下, 癌基因发生结构改变或调控异常, 其表达异常升高, 造成细胞的癌变. 本研究结果显示, FHD可将SMMC-7721多个癌基因的表达下调至正常水平, 他们包括pim-1(Hs.81170), rel(Hs.858), ras(Hs.204354), fos(Hs.25647), myc(Hs.79070), met(Hs.285754)以及编码Bcl-2相关蛋白的基因(Hs.227817). 这些基因编码的蛋白分别涉及细胞生长因子、丝氨酸蛋白激酶类蛋白、酪氨酸蛋白激酶类(TPK)、G蛋白和信号传导类蛋白、转录因子等, 均参与细胞生长分化信息的传递与细胞的增殖分化. 他们的异常表达可造成细胞增殖分化的失控. 大量研究表明, myc在原发性肝癌中普遍高表达[7]; 这些基因分别也在其他肿瘤中有异常高表达, 如ras基因在肺癌、卵巢癌、结肠癌中存在异常激活[8-9]; met, ras, myc, Bcl-2基因在胃癌中有异常高表达[10]. FHD对以上癌基因表达的下调作用可能是其体内抗肝癌的机制之一.
细胞的生长增殖直接受到复杂的信号传导网络的调节. 这些信号传导过程涉及多种信号传导分子的参与, 包括各种生长因子及其受体、酪氨酸蛋白激酶类、丝氨酸蛋白激酶类、各种转录因子等. 如前所述, 原癌基因的表达产物就是参与细胞生长信息传递的一些信号调节蛋白, 而癌基因的致癌作用亦最终通过这些信号传导通路实现. 因此, 生长增殖的信号传导异常, 是导致细胞无限生长的直接原因. 本研究结果表明, FHD不但直接抑制癌基因的表达, 而且对多种与细胞生长增殖密切相关的信号传导分子的表达有显著的下调作用. FHD对成纤维细胞生长因子(Hs.284244)、胰岛素样生长因子1受体(Hs.239176)、胰岛素样生长因子结合蛋白(Hs.1516)、G蛋白偶联受体(Hs.23016)、酪氨酸蛋白磷酸化酶(Hs.227777)、转录因子12(Hs.21704)、转录因子CP2(Hs.154970)等与细胞生长相关的信号转导分子均有显著的下调作用. 这表明, FHD可以通过下调细胞生长过程的多个信号传导分子靶点抑制肝癌细胞的异常生长.
细胞因子(cell factors, CF)在肿瘤的发生和发展中的作用具有双重性. 有些细胞因子直接或间接地杀死肿瘤(如: IFN-γ), 有些细胞因子能促进肿瘤生长(如IL-1和IL-6). 本研究中, FHD对细胞因子IL-1(Hs.1722)有显著下调作用. 已有研究表明, IL-1及其相应受体的过度表达均在多种细胞恶变中起重要作用, 肿瘤细胞的生长依赖于他们的异常分泌[11]. IL-1还能通过诱导血管生成而促进肿瘤生长和转移[12-13]. FHD可使肝癌细胞IL-1的表达显著下降. 对IL-1合成的下调可能是FHD抑制肝癌生长以及转移的重要机制之一.
研究结果还显示, FHD对丝裂原活化的蛋白激酶(MAPK)信号传导通路的几个成员也有显著影响. MAPK通路是细胞增殖、分化等多个信号传递途径的交汇点. MAPK是激酶链在细胞质中的最后一个激酶, 他平时位于胞质, 一旦被激活则被迅速转运到细胞核内, 或直接激活转录因子, 或激活其他蛋白激酶, 启动、关闭一些特定基因的转录, 对刺激信号做出必要的反应. 本研究中, FHD对MAP2K6(Hs.118825)和MAP3K12(Hs.211601)均有显著的上调作用. MAP2K6编码的蛋白是外界因素诱导的MAPK通路的分子之一, 在细胞周期阻滞和细胞凋亡过程中均需要MAP2K6的激活[14]. 我们在相关实验中发现, FHD可以将肿瘤细胞周期阻滞在G0-G1期. 我们推测, 对MAP2K6的表达上调可能是FHD引起肝癌细胞周期阻滞的主要分子基础.
抑癌基因(tumor suppressor gene)是人类正常基因组的成员, 其功能是诱导细胞的终末分化, 维持基因的稳定和负调节细胞的生长分化, 阻止细胞发生癌变. 细胞癌变不仅涉及癌基因的异常激活, 也涉及抑癌基因的失活. NF-2基因是一种重要的抑癌基因, 最初的研究发现, 神经纤维瘤等多种中枢神经系统肿瘤的发生是由于这一基因的失活造成的[15]. 后来在恶性黑色素瘤、恶性间皮瘤、乳腺癌、肺癌中也发现了NF-2的异常缺失或转录异常[16-17]. 该蛋白的表达异常不但使肿瘤细胞生长增殖失控, 而且使细胞具有高转移性[18-19]. 通过转基因技术将这一基因的表达恢复升高能够抑制肿瘤细胞的增殖[20]. 因此, 调节NF-2基因及其蛋白的表达可能是治疗肿瘤的有效途径. 本研究中, 人肝癌细胞经FHD作用后, NF-2(Hs.902)是表达上调最显著的基因之一. 这表明, FHD具有上调抑癌基因表达的作用, 这可能是FHD抗肝癌作用的又一重要基础.
抗肿瘤免疫中, T细胞是主要的效应细胞, 他不但可以直接杀伤肿瘤细胞, 而且可以通过分泌多种细胞因子调节其他免疫细胞的功能; 而在肿瘤的发生、发展过程中, 肿瘤细胞可以通过一系列机制逃避机体的免疫攻击, 从而使T细胞缺乏足够的共刺激信号而不能激活, 这是肿瘤细胞免疫逃逸的重要机制之一. 本研究中, TNFSF9(Hs.1524)和TNFSF7(Hs.99899)所编码的蛋白均为T细胞活化的共刺激信号分子. TNFSF9编码的蛋白为4-1BBL, 是肿瘤坏死因子(TNF)家族的成员之一[21]. 4-1BB为4-1BBL的特异性的配体, 他在T细胞有大量表达. 研究表明, 4-1BBL/4-1BB的结合是T细胞激活的共刺激信号, 他可以促进T细胞的增殖, 增强细胞毒性T细胞的杀伤作用, 延长T细胞的生存时间[22-24]. 最近的研究发现, 4-1BBL在肿瘤细胞上也有表达, 与其配体结合后, 他一方面可以促进肿瘤细胞释放细胞因子IL-8, 另一方面, 肿瘤表面表达的4-1BBL可以作为一种共刺激分子, 激活T细胞上产生大量IFN-γ. IL-8是一种趋化因子, 他可以诱导多种免疫细胞向局部迁移, 对局部的免疫反应有促进作用[25]; 而IFN-γ是一种抗肿瘤细胞因子, 他不但对肿瘤细胞有直接的杀伤作用, 而且可以激活多种免疫细胞. 以上研究提示, 提高4-1BBL的表达是一种提高机体抗肿瘤免疫的有效途径. 同样, TNFSF7编码的蛋白为CD70, 也是一种T细胞活化的共刺激信号, 可以增强T细胞的增殖和杀伤功能、延长记忆性T细胞的存活时间, 提高机体的抗肿瘤免疫功能[26-27]. 最近的研究已经证明, 通过转基因技术使癌细胞表达CD70后, 可以提高机体T细胞免疫功能从而有效地抑制肿瘤细胞的生长[28]. 本研究结果显示, FHD对TNFSF9和TNFSF7基因的表达均有显著的上调作用, 其中, TNFSF9的提高尤为明显, 是表达上调最显著的基因之一. 这提示, FHD可以促进肿瘤细胞表面共刺激分子的表达, 使其可以有效地激活T淋巴细胞, 增强免疫系统对肝癌细胞的敏感性.
总之, FHD通过调控多个靶基因抑制人肝癌细胞, 包括: 显著下调多种癌基因、多种与肿瘤生长增殖密切相关的信号传导分子及细胞因子IL-1的表达; 显著上调MAP2K6, MAP3K12, TNFSF9, TNFSF7和以NF-2为代表的抑癌基因的表达. 这反映了FHD抗肝癌多向性、多靶点的作用特点, 也从基因水平为揭示其机理提供了依据.
白花蛇舌草是一种具有突出抗癌作用的中药, 在临床中广泛应用. 但对其有效成分的研究及基于确切成分的作用机制的研究鲜见报道. 本文作者已发现: 其所含的黄酮类成分对肝癌表现出显著的抑制作用. 本研究将重点从基因调控角度揭示其黄酮类成分抗肝癌的分子靶点.
基因芯片技术的出现, 极大地提升了研究抗癌药物的视野和效率. 药物对于肿瘤、机体的作用及其机制, 可以通过基因的差异表达谱, 得到更全面、更深入的解释. 而基因芯片高通量筛选的优势非常适合中药多靶点、多环节的作用特点. 基因芯片技术, 正在成为研究中药抗癌靶点的重要手段.
大量报道表明: 癌基因、抑癌基因以及与肿瘤增殖、免疫逃逸机制密切相关的信号传导分子、细胞因子的异常表达是肿瘤发生、发展的重要基础. 通过干预手段调控肿瘤相关基因的表达已经发展为一种新的肿瘤治疗手段. 而采用中药成分纠正肿瘤相关基因的异常表达, 可望成为肿瘤治疗的一个方向.
目前, 多数对白花蛇舌草抗癌作用的研究主要停留在粗提物的水平, 缺乏对确切成分的深入研究, 对其抗癌分子机制, 也缺乏系统、清晰的认识. 本研究采用基因芯片技术, 通过比较基因差异表达谱, 探查出白花蛇舌草总黄酮抑制人肝癌的20条有效靶基因, 为深入开展机制研究, 指明了方向.
本研究发现白花蛇舌草总黄酮成分可将15条显著高表达的基因和5条显著低表达的基因恢复至正常的表达水平. 这些基因与肝癌的发生、发展密切相关. 这为将白花蛇舌草总黄酮开发为更安全有效的抗癌新药提供了重要的实验依据.
靶基因: 指在生物技术攻关中针对的基因. 在基因芯片技术中, 用于芯片点样的是靶基因. 靶基因可分为染色体DNA(或基因组DNA) 、cDNA(或人工合成DNA). 目前, 以cDNA的研究为主, 因为cDNA是染色体上编码蛋白质的DNA序列, 有医疗和其他领域的研究价值和商业价值.
白花蛇舌草作为抗肿瘤中药在肝癌的临床治疗中有一定的疗效, 但有关其机制, 尤其是对其作用的分子靶点的研究报道尚不多见. 本文应用基因芯片技术, 比较了正常肝、肝癌细胞和白花蛇舌草总黄酮作用后的肝癌细胞三组间的基因表达谱, 总结了受白花蛇舌草总黄酮作用下调的15个基因和上调的5个基因, 为进一步探索白花蛇舌草抑癌的分子机制提供了方向.
编辑: 张焕兰 电编:张敏
| 3. | Seglen PO. Preparation of isolated rat liver cells. Methods Cell Biol. 1976;13:29-83. [PubMed] [DOI] |
| 4. | Ismail T, Howl J, Wheatley M, McMaster P, Neuberger JM, Strain AJ. Growth of normal human hepatocytes in primary culture: effect of hormones and growth factors on DNA synthesis. Hepatology. 1991;14:1076-1082. [PubMed] [DOI] |
| 5. | Dorko K, Freeswick PD, Bartoli F, Cicalese L, Bardsley BA, Tzakis A, Nussler AK. A new technique for isolating and culturing human hepatocytes from whole or split livers not used for transplantation. Cell Transplant. 1994;3:387-395. [PubMed] |
| 6. | Tisdale JF, Wilson DR. Clinical applications of gene therapy. Curr Opin Mol Ther. 2003;5:456-457. [PubMed] |
| 7. | 王 征旭, 胡 桂芳. 肝癌差异表达基因研究进展. 国外医学·外科学分册. 2002;29:82-85. |
| 11. | Suganuma M, Okabe S, Kurusu M, Iida N, Ohshima S, Saeki Y, Kishimoto T, Fujiki H. Discrete roles of cytokines, TNF-alpha, IL-1, IL-6 in tumor promotion and cell transformation. Int J Oncol. 2002;20:131-136. [PubMed] |
| 12. | Voronov E, Shouval DS, Krelin Y, Cagnano E, Benharroch D, Iwakura Y, Dinarello CA, Apte RN. IL-1 is required for tumor invasiveness and angiogenesis. Proc Natl Acad Sci U S A. 2003;100:2645-2650. [PubMed] [DOI] |
| 13. | Saijo Y, Tanaka M, Miki M, Usui K, Suzuki T, Maemondo M, Hong X, Tazawa R, Kikuchi T, Matsushima K. Proinflammatory cytokine IL-1 beta promotes tumor growth of Lewis lung carcinoma by induction of angiogenic factors: in vivo analysis of tumor-stromal interaction. J Immunol. 2002;169:469-475. [PubMed] [DOI] |
| 14. | Wang X, McGowan CH, Zhao M, He L, Downey JS, Fearns C, Wang Y, Huang S, Han J. Involvement of the MKK6-p38gamma cascade in gamma-radiation-induced cell cycle arrest. Mol Cell Biol. 2000;20:4543-4552. [PubMed] [DOI] |
| 15. | Trofatter JA, MacCollin MM, Rutter JL, Murrell JR, Duyao MP, Parry DM, Eldridge R, Kley N, Menon AG, Pulaski K. A novel moesin-, ezrin-, radixin-like gene is a candidate for the neurofibromatosis 2 tumor suppressor. Cell. 1993;72:791-800. [PubMed] [DOI] |
| 16. | Kley N, Seizinger BR. The neurofibromatosis 2 (NF2) tumour suppressor gene: implications beyond the hereditary tumour syndrome? Cancer Surv. 1995;25:207-218. [PubMed] |
| 17. | Bianchi AB, Hara T, Ramesh V, Gao J, Klein-Szanto AJ, Morin F, Menon AG, Trofatter JA, Gusella JF, Seizinger BR. Mutations in transcript isoforms of the neurofibromatosis 2 gene in multiple human tumour types. Nat Genet. 1994;6:185-192. [PubMed] [DOI] |
| 18. | Lallemand D, Curto M, Saotome I, Giovannini M, McClatchey AI. NF2 deficiency promotes tumorigenesis and metastasis by destabilizing adherens junctions. Genes Dev. 2003;17:1090-1100. [PubMed] [DOI] |
| 19. | McClatchey AI, Saotome I, Mercer K, Crowley D, Gusella JF, Bronson RT, Jacks T. Mice heterozygous for a mutation at the Nf2 tumor suppressor locus develop a range of highly metastatic tumors. Genes Dev. 1998;12:1121-1133. [PubMed] [DOI] |
| 20. | Fraenzer JT, Pan H, Minimo L, Smith GM, Knauer D, Hung G. Overexpression of the NF2 gene inhibits schwannoma cell proliferation through promoting PDGFR degradation. Int J Oncol. 2003;23:1493-1500. [PubMed] [DOI] |
| 21. | Alderson MR, Smith CA, Tough TW, Davis-Smith T, Armitage RJ, Falk B, Roux E, Baker E, Sutherland GR, Din WS. Molecular and biological characterization of human 4-1BB and its ligand. Eur J Immunol. 1994;24:2219-2227. [PubMed] [DOI] |
| 22. | Shuford WW, Klussman K, Tritchler DD, Loo DT, Chalupny J, Siadak AW, Brown TJ, Emswiler J, Raecho H, Larsen CP. 4-1BB costimulatory signals preferentially induce CD8+ T cell proliferation and lead to the amplification in vivo of cytotoxic T cell responses. J Exp Med. 1997;186:47-55. [PubMed] [DOI] |
| 23. | Kim J, Choi SP, La S, Seo JS, Kim KK, Nam SH, Kwon B. Constitutive expression of 4-1BB on T cells enhances CD4+ T cell responses. Exp Mol Med. 2003;35:509-517. [PubMed] [DOI] |
| 24. | Salih HR, Kosowski SG, Haluska VF, Starling GC, Loo DT, Lee F, Aruffo AA, Trail PA, Kiener PA. Constitutive expression of functional 4-1BB (CD137) ligand on carcinoma cells. J Immunol. 2000;165:2903-2910. [PubMed] [DOI] |
| 25. | Eckmann L, Jung HC, Schürer-Maly C, Panja A, Morzycka-Wroblewska E, Kagnoff MF. Differential cytokine expression by human intestinal epithelial cell lines: regulated expression of interleukin 8. Gastroenterology. 1993;105:1689-1697. [PubMed] [DOI] |
| 26. | Yamada S, Shinozaki K, Agematsu K. Involvement of CD27/CD70 interactions in antigen-specific cytotoxic T-lymphocyte (CTL) activity by perforin-mediated cytotoxicity. Clin Exp Immunol. 2002;130:424-430. [PubMed] [DOI] |
| 27. | Arens R, Schepers K, Nolte MA, van Oosterwijk MF, van Lier RA, Schumacher TN, van Oers MH. Tumor rejection induced by CD70-mediated quantitative and qualitative effects on effector CD8+ T cell formation. J Exp Med. 2004;199:1595-1605. [PubMed] [DOI] |
| 28. | Cormary C, Gonzalez R, Faye JC, Favre G, Tilkin-Mariamé AF. Induction of T-cell antitumor immunity and protection against tumor growth by secretion of soluble human CD70 molecules. Cancer Gene Ther. 2004;11:497-507. [PubMed] [DOI] |