修回日期: 2003-12-01
接受日期: 2003-12-16
在线出版日期: 2004-04-15
目的: 筛选与克隆丙型肝炎病毒(HCV)NS3反式激活基因1的反式激活基因, 了解其可能存在的调节功能线索.
方法: 应用抑制性消减杂交(SSH)技术及生物信息学(bioin-formatics)技术筛选并克隆NS3TP1反式激活的新型靶基因. 以NS3TP1表达质粒pcDNA3.1(-)-NS3TP1转染HepG2细胞, 以空载体pcDNA3.1(-)为平行对照, 制备转染后的细胞裂解液, 提取mRNA并逆转录为cDNA, 经Rsa I酶切后, 将实验组cDNA分成两组, 分别与两种不同的接头衔接, 再与对照组cDNA进行两次消减杂交及两次抑制性聚合酶链反应(PCR), 将产物与pGEM-Teasy载体连接, 构建cDNA消减文库, 并转染大肠杆菌进行文库扩增, 随机挑选克隆PCR扩增后进行测序及同源性分析.
结果: 成功构建人NS3TP1反式激活基因差异表达的cDNA消减文库. 文库扩增后得到68个阳性克隆, 进行菌落PCR分析, 均得到200-1 000 bp插入片段. 随机挑选其中36个插入片段测序, 并通过生物信息学分析获得其全长基因序列, 结果共获得23种编码基因, 其中3个为未知功能的新基因.
结论: 筛选到的cDNA全长序列, 包括一些与细胞生长调节、物质代谢、免疫及细胞凋亡密切相关的蛋白编码基因, 推测了NS3TP1可能存在的调控机制的线索.
引文著录: 纪冬, 成军, 王建军, 刘妍, 杨倩, 党晓燕, 王春花. 应用抑制性消减杂交技术克隆和筛选丙型肝炎病毒NS3蛋白反式激活基因1的反式调节基因. 世界华人消化杂志 2004; 12(4): 843-846
Revised: December 1, 2003
Accepted: December 16, 2003
Published online: April 15, 2004
AIM: To clone and identify human genes transactivated by human gene 1 transactivated by hepatitis C virus NS3 protein (NS3TP1) by constructing a cDNA subtractive library with suppression subtractive hybridization (SSH).
METHODS: Suppression subtractive hybridization and bioinformatics were used for screening and cloning of the target genes transactivated by NS3TP1 protein. The mRNA was isolated from HepG2 cells transfected pcDNA3.1(-)-NS3TP1 and pcDNA3.1(-) empty vector, respectively, and SSH method was employed to analyze the differentially expressed cDNA sequence between the two groups. After restriction enzyme Rsa I digestion, small sizes cDNAs were obtained. Then tester cDNA was divided into two groups and ligated to the specific adaptor 1 and adaptor 2, respectively. Tester cDNA was hybridized with driver cDNA twice and underwent polymerase chain reaction (PCR) twice, and then was subcloned into pGEM-Teasy plasmid vectors to set up the subtractive library. Amplification of the library was carried out with E. coli strain DH5. The cDNA was sequenced and analyzed in GenBank with Blast search after PCR.
RESULTS: The subtractive library of genes transactivated by NS3TP1 was constructed successfully. The amplified library contained 68 positive clones. Colony PCR showed that these clones contained 200-1000 bp inserts. Sequence analysis was performed in 36 clones, ramdomly, and the full length sequences were obtained with bioinformatics method. Altogether 23 coding sequences were obtained, which consisted of 20 known and 3 unknown ones.
CONCLUSION: The obtained sequences may be target genes transactivated by NS3TP1. among which some genes coding proteins involve in cell cycle regulation, metabolism, immunity and cell apoptosis. This finding brings some new clues for studying the biological functions of NS3TP1.
- Citation: Ji D, Cheng J, Wang JJ, Liu Y, Yang Q, Dang XY, Wang CH. Screening and cloning of the target genes transactivated by human gene 1 transactivated by hepatitis C virus NS3 protein using suppression subtractive hybridization. Shijie Huaren Xiaohua Zazhi 2004; 12(4): 843-846
- URL: https://www.wjgnet.com/1009-3079/full/v12/i4/843.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v12.i4.843
丙型肝炎病毒(HCV)非结构蛋白3(NS3)具有丝氨酸蛋白酶、三磷酸核苷酶 (NTPase) 和解旋酶 (Helicase) 的功能, 在HCV多聚蛋白的成熟和病毒复制过程中发挥重要作用, 并且对于宿主多种基因具有反式激活作用, 影响细胞的功能, 诸如细胞增生、凋亡, 甚至是HCV的致癌作用[1-2]. 我室对NS3反式激活基因进行筛选和克隆化研究, 发现了NS3蛋白上调一些基因的表达, 并且包括一些未知功能基因, 其中之一命名为NS3TP1, 利用生物信息学技术确定其开放读码框架(ORF), 并对其进行了克隆化研究, 顺利得到了NS3TP1基因编码序列. 为了解其细胞内功能, 我们利用抑制性消减杂交技术构建NS3TP1作用于肝母细胞瘤细胞系HepG2细胞的反式调节cDNA消减文库, 筛选差异表达的基因片段, 并应用生物信息学进行分析, 为了解NS3TP1的功能、进一步探讨HCV发病及致癌机制提供新的研究方向.
HepG2细胞及感受态大肠杆菌DH5为本室保存, pcDNA3.1(-)真核表达载体购自Invitrogen公司; FuGENE6 转染试剂购自Roche公司, mRNA Purification试剂盒购自Amersham Pharmacia Biotech公司, PCR-Select cDNA Subtraction试剂盒、50×PCR Enzyme Mix、Advantage PCR Cloning试剂盒购自Clontech公司, High Pure PCR Product Purification试剂盒购自Boehringer Mannheim公司, T7、SP6通用引物及pGEM-Teasy载体购自Promega公司.
NS3TP1真核表达质粒pcDNA3.1(-)-NS3TP1由本室构建. 用FuGENE6转染试剂将2 g pcDNA3.1(-)-NS3TP1及pcDNA3.1(-)空载体分别转染35 mm平皿HepG2 细胞, 48 h后收获细胞.
使用mRNA Purification试剂盒, 直接提取转染了重组表达质粒及空载体的HepG2细胞mRNA, 经琼脂糖凝胶电泳及分光光度计进行定性定量分析.
采用Clontech公司的PCR-Select cDNA Subtraction Kit, 常规SSH方法按说明书进行: 以转染了重组表达质粒及空载体的HepG2 细胞mRNA为模板逆转录合成双链cDNA(dscDNA), 并分别标记为Tester和Driver, dscDNA经RsaⅠ(一种识别4碱基序列的内切酶)消化, 产生相对较短的平端片段, 纯化酶切产物. 将Tester的dscDNA分为两份, 分别连接试剂盒提供的特殊设计的寡核苷酸接头Adaptor 1和Adaptor 2, 然后与过量的Driver dscDNA进行杂交; 合并两种杂交产物后再与Driver dscDNA作第2次杂交; 然后将杂交产物做选择性PCR扩增, 使Tester dscDNA中特异性表达或高表达的片段得到特异性扩增.
扩增产物与pGEM-Teasy载体连接, 转化DH5感受态细菌, 在含氨苄青霉素的LB/X-gal/IPTG培养板上, 37 ℃培养18 h. 共得到68个白色菌落, 以pGEM-Teasy载体多克隆位点两端T7/SP6引物进行菌落PCR扩增, 证明含有插入片段后(200-1 000 bp), 随机挑选其中个36个克隆增菌, 测序(上海申友公司), 并且应用生物信息学将测得序列GenBank数据库进行同源性分析.
NS3TP1真核表达质粒pcDNA3.1(-)-NS3TP1经测序及酶切鉴定均正确.
使用高质量的mRNA是保证cDNA高产量的前提. 紫外分光检测显示, 转染了pcDNA3.1(-)-NS3TP1质粒及空载体的HepG2 细胞mRNA分别为4.84 g和6.13 g, A260/A280 = 1.92. 2.0%琼脂糖凝胶电泳见mRNA为大于0.5 kb清晰慧尾片状条带.
dscDNA与接头连接效率的高低是决定抑制性消减杂交成败的最关键步骤. 将连接有adaptor l和adaptor 2的两组dscDNA分别用不同的特异性引物(看家基因甘油三磷酸脱氢酶G3PDH引物)进行28个循环扩增, 产物用2.0%琼脂糖凝胶电泳鉴定. 结果显示两组dscDNA扩增产物浓度相当, 说明dscDNA已与接头高效率连接.
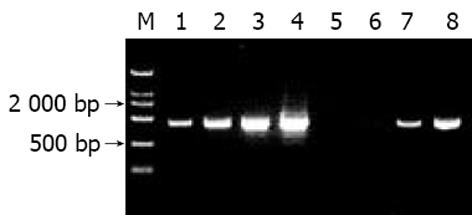
分别取1 L抑制性及非抑制性PCR产物为模板, 用看家基因G3PDH引物进行PCR扩增, 分别在18、23、28、33次循环结束时从体系中吸取5 L进行电泳鉴定. 结果显示: 与非抑制性PCR产物相比, 抑制性PCR产物中G3PDH基因产物大大减少, 说明所构建的消减文库具有很高的消减效率(图1).
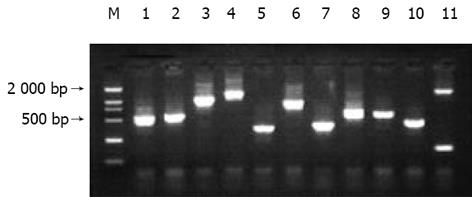
杂交产物经两轮PCR扩增后, 菌落PCR扩增结果显示为200-1000 bp大小不等的插入片段, 所获得的68个克隆中几乎均含有插入片段, 这些条带可能代表差异表达的基因片段(图2).
挑选其中36个克隆测序, 与GenBank数据库进行初步比较. 有33个与已知基因的部分序列高度同源(97%-100%), 3个克隆未检索到任何对应的相似序列, 可能代表了某些新基因, 详细结果见表1.
| 同源蛋白名称 | 同源克隆数 | 同源性(%) |
| 核糖体蛋白 | 9 | 98-100 |
| CDC28蛋白激酶 | 3 | 99-100 |
| 皮肤T细胞淋巴瘤肿瘤抗原HD-CL-08 | 2 | 99-100 |
| 真核翻译延长因子 | 2 | 99-100 |
| 胰岛素样生长因子结合蛋白 | 2 | 97-100 |
| 5-微管蛋白 | 1 | 100 |
| RAS癌基因家族RAB10 | 1 | 100 |
| 纤维结合素 | 1 | 100 |
| 白蛋白 | 1 | 100 |
| 线粒体单倍体 | 1 | 100 |
| 细胞色素C氧化酶亚单位IV亚型1(COX4I1) | 1 | 100 |
| 真核翻译起始因子3 | 1 | 100 |
| 肝丙酮酸脱氢酶 | 1 | 100 |
| ATP合酶、H+转运、线粒体F1复合体 | 1 | 99 |
| -2巨球蛋白 | 1 | 99 |
| 膜整合溶酶体/后期核内体蛋白 | 1 | 99 |
| 凋亡抑制子(IEX-1L) | 1 | 99 |
| 蛋白二硫化物异构酶相关蛋白 | 1 | 99 |
| 甲状腺激素受体相互作用蛋白3(TRIP3) | 1 | 98 |
| 蛋白激酶WEE1 | 1 | 97 |
| 新基因序列 | 3 | |
| 克隆总计 | 36 |
HCV NS3蛋白为一多功能蛋白, 近年研究表明他对多种基因具有反式激活作用[3-4], 为了解NS3在丙肝发病机制中的作用, 我室构建出HCV NS3反式激活基因差异表达的cDNA消减文库, 并发现了一些新基因, 其中一个命名为NS3TP1, GenBank 收录AY116969. 对其进行克隆化研究, 反应产物经测序完全符合计算机分析结果, 表明我们顺利得到了NS3TP1编码序列. NS3TP1的ORF长度为1 932个核苷酸(nt), 编码642个氨基酸残基(aa)[5]. 为进一步研究NS3TP1这一新基因的功能, 明确 HCV NS3在丙型肝炎发病机制中的作用, 我们构建NS3TP1基因真核表达载体pcDNA3.1(-)-NS3TP1, 利用抑制性消减杂交技术[6] (suppression subtractive hybridization, SSH)筛选并克隆NS3TP1反式激活的靶基因, 推测其在体内可能存在功能的线索.
SSH方法是近年发展起来的一项新的基因克隆技术, 与传统的方法比较, 具有实验周期短、易操作、可靠性高、假阳性率低等特点, 能有效地分离扩增低丰度特异表达的基因, 可以在较短的时间内获得较理想的实验结果[7]. 我们将真核表达载体pcDNA3.1(-)-NS3TP1, 转染肝母细胞瘤细胞系HepG2, 并以转染空白载体的相同细胞系作为对照, 以2种转染的细胞系中提取的mRNA为起始材料, 应用SSH方法成功地构建了NS3TP1反式激活相关基因差异表达的cDNA消减文库, 挑选36个克隆测序分析, 主要包括两种类型的序列, 即已知功能的基因序列和未知功能的基因序列. 在本次实验中共获得3个差异表达的未知序列, 对其基因结构和功能正在研究之中.
在已知功能基因序列中, 主要包括以下几种类型: (1)细胞内结构与细胞生长相关蛋白, 如线粒体蛋白、核糖体蛋白、纤维结合素、5-微管蛋白、真核翻译起始因子、真核翻译延长因子等, 在细胞生长、分化、黏附中起重要作用. (2)参与细胞内代谢的蛋白基因, 如白蛋白在各种物质代谢中起运输作用, 并且是维持血浆胶体渗透压的重要物质. 肝丙酮酸脱氢酶参与了三羧酸循环等的代谢. 细胞色素C氧化酶是线粒体呼吸链的终末酶, 他是一个多亚单位的酶复合体, 功能是将电子从细胞色素c传递到分子氧, 并且为线粒体内膜提供一部分的电化学梯度. 复合体由线粒体及核编码的共13个亚单位组成, 线粒体编码的亚单位是电子转运体并且有质子泵活性, 而核编码的亚单位功能尚不清楚, 但他们可能发挥了对于复合体的调控作用. 本实验筛选到的细胞色素c氧化酶IV亚型1(COX4I1)属于核编码的亚单位, 位于NOC4基因的3'-端, 并且与之共用一个启动子. 这很可能说明了HCV NS3蛋白涉及到了线粒体的呼吸链, 改变了细胞的正常的能量代谢. (3)参与信号转导途径, 影响HCV与宿主细胞的相互反应, 导致肝硬化、肝癌等病理改变. 如CDC28蛋白激酶属于细胞周期素依赖性激酶(CDK)家族, 是细胞由G1期到S期、G2期到M期所必需, 影响着细胞分裂的过程[8], 近年研究认为CDK在慢性肝炎向肝细胞癌(HCC)的转换过程中具有十分重要的意义[9]. 蛋白激酶WEE1为一种细胞周期调节蛋白, 主要通过阻断M期启动因子(MPF), 包括cdc2 激酶和细胞周期蛋白B, 特异性的调控细胞G2/M的转换, 抑制细胞的有丝分裂. 既往研究发现, WEE1激酶的活性和水平在S期均升高, 在细胞进入M期时则很快下降[10], 研究者认为这种现象可能是由于当DNA的复制被阻断时, WEE1激酶的降解就被抑制, 在进入DNA复制期间有一种因子可以使WEE1激酶保持持续的高水平直至进入M期, 推测这种因子即c-Fos/AP-1[11]. 王建军 et al[12]研究发现了HCV核心蛋白可以上调WEE1基因的表达, 而本研究则说明了HCV NS3也可以上调WEE1基因. RAS癌基因家族RAB10为RAS样小分子量的GTP结合蛋白, 主要负责真核细胞内的膜运输. 癌基因RAS可以与RAF超家族结合, 从而启动MAPK信号转导途径[13], HCV NS3与RAS家庭成员相互作用的关系还需进一步的研究. 凋亡抑制子IEX-1L, Wu et al[14]于1998年克隆出来, 他们运用mRNA差异性展示技术发现了与早期即刻反应基因IEX-1同源的基因[15], 但他在IEX-1编码区211位点上有111个核苷酸的插入, 故将之命名为IEX-1L, 认为他是IEX-1未经过剪切的形式, 包含了IEX-1全部的内含子. IEX-1L可以保护细胞免于由Fas或肿瘤坏死因子(TNF)介导的凋亡, 并且还发现用干扰素(IFN)处理JurKat细胞时, NF-kappaB的细胞存活功能是通过IEX-1L来完成的, 因为他是惟一的核因子(NF-kappaB)蛋白调节基因. 本实验得到NS3TP1可以反式激活IEX-1L, 提示了NS3蛋白与IFN治疗HCV时的耐药有关. (4)肝外组织相关性基因. 如甲状腺激素受体相互作用蛋白3(TRIP3)、胰岛素样生长因子结合蛋白、皮肤T细胞淋巴瘤肿瘤抗原, 可能与HCV所致自身免疫性损伤有关, 但具体意义尚待进一步研究.
通过对NS3TP1的上述反式激活基因的分析, 我们发现他与体内物质代谢、信号转导、凋亡关系密切, 在病毒感染后肝细胞恶性变方面有一定的作用, 而且还与肝外组织有关, 这可能与HCV所致肝外疾患有一定的关系. NS3TP1是正常人体存在的基因, 在病毒蛋白NS3的存在下其功能被进一步激活. 关于其在体内与各种活性因子的具体调节机制, 仍需进行详细的实验来研究. 对新基因的研究及其功能的确定是分子生物学领域一项很具有挑战性的工作, NS3TP1抑制性消减文库的建立为研究其功能提供了理论依据, 并为HCV感染慢性化机制提供了新的研究方向.
编辑: N/A
| 1. | 刘 妍, 成 军, 牟 劲松, 陆 荫英, 王 建军, 李 克, 王 琳, 张 玲霞. 丙型肝炎病毒非结构蛋白NS3反式激活SV40病毒早期启动子的研究. 解放军医学杂志. 2003;28:44-46. |
| 2. | Yoshida H, Kato N, Shiratori Y, Lan KH, Ono-Nita SK, Feng Z, Shiina S, Omata M. Poor association of TT virus viremia with hepatocellular carcinoma. Liver. 2000;20:247-252. [PubMed] [DOI] |
| 3. | 牟 劲松, 刘 妍, 成 军. 丙型肝炎病毒非结构蛋白NS3及其对信号转导途径的影响. 国外医学. 流行病学传染病学分册. 2002;29:342-345. |
| 4. | 牟 劲松, 刘 妍, 王 刚, 成 军, 段 惠娟, 李 克, 陆 荫英, 王 琳, 王 惠芬. 应用抑制性消减杂交技术克隆丙型肝炎病毒非结构蛋白NS3反式激活的相关基因. 世界华人消化杂志. 2003;11:399-403. [DOI] |
| 5. | 纪 冬, 成 军, 王 建军, 刘 妍, 杨 倩, 王 春花, 党 晓燕. 丙型肝炎病毒非结构蛋白NS3反式激活基因1的克隆化研究. 胃肠病学和肝病学杂志. 2003;12:237-240. |
| 6. | Libíková H, Pogády J, Wiedermann V, Breier S. Search for herpetic antibodies in the cerebrospinal fluid in senile dementia and mental retardation. Acta Virol. 1975;19:493-495. [PubMed] |
| 7. | Deng HB, Parekh HK, Chow KC, Simpkins H. Increased expression of dihydrodiol dehydrogenase induces resistance to cisplatin in human ovarian carcinoma cells. J Biol Chem. 2002;277:15035-15043. [PubMed] [DOI] |
| 8. | Russo GL, van den Bos C, Sutton A, Coccetti P, Baroni MD, Alberghina L, Marshak DR. Phosphorylation of Cdc28 and regulation of cell size by the protein kinase CKII in Saccharomyces cerevisiae. Biochem J. 2000;351:143-150. [DOI] |
| 10. | Michael WM, Newport J. Coupling of mitosis to the completion of S phase through Cdc34-mediated degradation of Wee1. Science. 1998;282:1886-1889. [PubMed] [DOI] |
| 11. | Kawasaki H, Komai K, Ouyang Z, Murata M, Hikasa M, Ohgiri M, Shiozawa S. c-Fos/activator protein-1 transactivates wee1 kinase at G(1)/S to inhibit premature mitosis in antigen-specific Th1 cells. EMBO J. 2001;20:4618-4627. [PubMed] [DOI] |
| 13. | 纪 冬, 成 军. 乙型肝炎和丙型肝炎病毒对MKP蛋白信号转导影响的研究. 胃肠病学和肝病学杂志. 2003;12:200-202. |
| 14. | Wu MX, Ao Z, Prasad KV, Wu R, Schlossman SF. IEX-1L, an apoptosis inhibitor involved in NF-kappaB-mediated cell survival. Science. 1998;281:998-1001. [DOI] |
| 15. | Kondratyev AD, Chung KN, Jung MO. Identification and characterization of a radiation-inducible glycosylated human early-response gene. Cancer Res. 1996;56:1498-1502. [PubMed] |