修回日期: 2003-07-01
接受日期: 2003-07-16
在线出版日期: 2004-01-15
目的: 应用抑制性消减杂交(SSH)技术及生物信息学技术筛选并克隆丙型肝炎病毒(HCV)非结构蛋白5A(NS5A)反式激活新型靶基因.
方法: 以HCV NS5A表达质粒pcDNA3.1(-)-NS5A转染HepG2细胞, 以空载体pcDNA3.1(-)为平行对照, 提取mRNA并进行SSH分析. 对于所获基因片段序列分析表明, 其中之一为新型基因片段, 与GenBank中注册的已知功能基因序列没有同源性, 利用表达序列标签(EST)序列的搜索和比对, 进行电子拼接, 根据基因起始密码子的Kozak规则和终止密码子下游保守的多聚腺苷酸信号序列, 确定新型基因序列. 从HepG2细胞提取总RNA, 以逆转录多聚酶链反应(RT-PCR)技术扩增获得该新基因的全长序列, 并测序证实, 命名为NS5ATP7, 在GenBank中注册, 注册号为AF529368.
结果: NS5ATP5基因的编码序列全长为894个核苷酸(nt), 编码产物由297个氨基酸残基(aa)组成.
结论: HCV NS5A反式激活新型靶基因NS5ATP5的筛选与克隆, 为进一步研究HCV NS5A反式激活作用的分子生物学机制和探索新型治疗技术奠定了基础.
引文著录: 张健, 刘妍, 成军, 王琳, 邵清, 梁耀东, 刘敏. 丙型肝炎病毒非结构蛋白NS5A反式激活基因NS5ATP7的克隆. 世界华人消化杂志 2004; 12(1): 82-85
Revised: July 1, 2003
Accepted: July 16, 2003
Published online: January 15, 2004
AIM: To screen and clone the target genes transactivated by nonstructural protein 5A (NS5A) of hepatitis C virus (HCV) using suppression subtractive hybridization (SSH) technique and bioinformatics technique.
METHODS: The mRNA was isolated from HepG2 cells which were transfected with pcDNA3.1(-)-NS5A and pcDNA3.1(-) empty vector, respectively, and SSH method was employed to analyze the differentially expressed DNA sequence between the two groups. The obtained sequences were searched for homologous DNA sequence from GenBank, one of which was a new gene with unknown function. The new gene with no homology with known genes in this database was confirmed and electric polymerase chain reaction (PCR) was conducted for the cloning of the full-length cDNA for the new gene and in conjunction with Kozak role and the exist of polyadenyl signal sequence. The reverse transcription PCR (RT-PCR) was used to amplify the new gene, named NS5ATP7, from the mRNA of HepG2 cells. The sequence for the NS5ATP7 gene was deposited into GenBank, and the accession number was AF529368.
RESULTS: The full-length DNA sequence for the NS5ATP7 gene was of 894 nucleotides (nt), and its coding product consisted of 297 amino acid (aa) residues.
CONCLUSION: These results will pave the way for the study of the molecular mechanism of the transactivating effects of NS5A protein of HCV and the development of new therapy for chronic hepatitis C.
- Citation: Zhang J, Liu Y, Cheng J, Wang L, Shao Q, Liang YD, Liu M. Cloning and identification of human gene 7 transactivated by nonstructural protein 5A of hepatitis C virus. Shijie Huaren Xiaohua Zazhi 2004; 12(1): 82-85
- URL: https://www.wjgnet.com/1009-3079/full/v12/i1/82.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v12.i1.82
丙型肝炎病毒(HCV)的感染, 不仅能够引起急慢性病毒性肝炎, 且与肝脏纤维化(liver cirrhosis, LC)和肝细胞癌(hepatocellular carcinoma, HCC)的发生密切相关. 值得注意的是, HCV感染具有较高的慢性化比例, 有时高达80%以上. 目前我国一般人群的感染率达3.2%, 因而具有很大的危害性[1-14]. 丙型肝炎病毒是单股正链RNA病毒, 全长约9 500个核苷酸, 含有一个大的开放读码框架(ORF), 编码3 010-3 033个氨基酸残基的多肽前体, 多肽前体至少被加工为10种结构蛋白和非结构蛋白. 其中, HCV非结构蛋白5A(NS5A)基因(位于6 258-7 601 bp之间)编码的56 kD的NS5A蛋白(448 aa)除了参与HCV多蛋白的成熟和RNA的复制过程外, 还具有多种生物学功能. 目前, 不同磷酸化形式的NS5A蛋白具有反式激活作用是国内外学者关于NS5A生物学功能研究的热点. NS5A蛋白是一种作用很强的转录激活因子, 能够影响细胞信号转导途径, 激活多种病毒及细胞基因启动子, 调控着细胞基因的转录, 推测NS5A蛋白的这种反式激活作用, 可能是HCV感染与肝细胞癌发生发展密切相关的重要分子生物学机制[15,16].
本研究利用抑制性消减杂交技术(suppression subtractive hybridization, SSH), 对于表达HCV NS5A载体转染的HepG2细胞进行研究, 阐明了NS5A蛋白反式激活作用的部分靶基因, 同时我们结合生物信息学技术(bioinformatics)克隆了NS5A蛋白反式激活作用的新靶基因, 即HCV NS5A蛋白反式激活基因7(NS5ATP7), 从而为HCV NS5A反式激活作用的研究提供新的方向.
HepG2细胞及感受态大肠杆菌DH5α为本室保存, pcDNA3.1(-)真核表达载体购自Invitrogen公司; Lipofectamine PLUS 转染试剂购自Gibco公司, mRNA Purification试剂盒购自Amersham Pharmacia Biotech, PCR-Select cDNA Subtraction试剂盒, 50×PCR Enzyme Mix、Advantage PCR Cloning试剂盒购自Clontech, High Pure PCR Product Purification试剂盒购自Boehringer Mannheim公司, T7、SP6通用引物及pGEM-T vector载体购自Promega公司. 丙型肝炎病毒非结构蛋白NS5A真核表达质粒pcDNA3.1(-)-NS5A由本室构建[17]. DNA测序由上海博亚公司完成.
1.2.1 消减杂交文库的建立及克隆分析: 分别将pcDNA3.1(-)-NS5A及pcDNA3.1(-)空载体转染HepG2细胞, 48 h后提取mRNA, 以此mRNA为模板逆转录合成双链cDNA(dscDNA), 并分别标记为Tester和Driver, 经Rsa I(一种识别4碱基序列的内切酶)消化后将Tester cDNA分为两份, 分别连接特殊设计的寡核苷酸接头Adapter 1和Adapter 2, 与过量的Driver cDNA进行2次消减杂交和2次抑制性PCR, 使Tester cDNA中特异性表达或高表达的片段得到特异性扩增. 扩增产物与pGEM-T载体连接, 转化DH5α感受态细菌, 在含氨苄青霉素的LB/X-gal/IPTG培养板上, 37 ℃培养18 h. 挑取白色菌落, 增菌, 以pGEM-T载体多克隆位点两端T7/SP6引物进行菌落PCR扩增, 证明含有插入片段后(2 00-1 000 bp)测序. 对于每一条基因片段的序列提交GenBank进行同源基因序列的搜索, 确认所得基因片段的独特性, 然后依据GenBank数据库中的同源基因片段进行电子拼接, 根据Kozak规则和终止密码子下游的多聚腺苷酸信号序列, 确定完整的编码基因序列.
1.2.2 新基因的PCR扩增与序列分析: 根据电子拼接序列的新基因序列, 设计新基因特异性引物, 利用转染了pcDNA3.1(-)-NS5A的HepG2细胞来源的mRNA, 经过逆转录多聚酶链反应(RT-PCR)扩增与克隆技术, 获得阳性克隆并进行序列分析.
使用高质量的mRNA是保证cDNA高产量的前提. 紫外分光检测显示, 转染了真核表达质粒及空载体的HepG2 细胞mRNA分别为4.54 g和4.23 g, A260/A 280= 1.7. 10 g/L琼脂糖凝胶电泳见 mRNA为大于0.5 kb清晰慧尾片状条带.
dscDNA两端连接效率检测结果显示两组dscDNA已与接头高效率连接. 消减效率的鉴定结果显示: 与未消减组PCR产物相比, 消减组PCR产物中看家基因甘油三磷酸脱氢酶G3PDH基因产物大大减少, 说明所构建的消减文库具有很高的消减效率. 对差异表达基因片段进行菌落PCR扩增, 结果显示为200-1 000 bp大小不等的插入片段. 挑选克隆测序, 并与GenBank数据库进行初步比较.
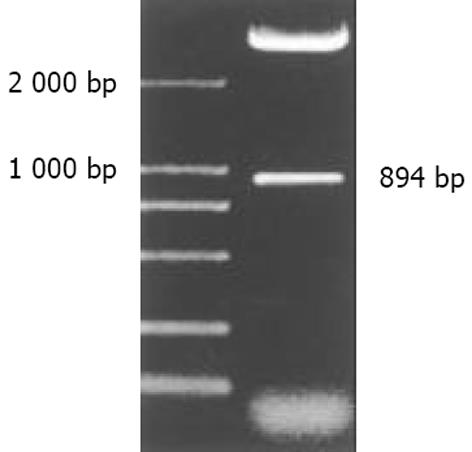
利用美国国立卫生院(NIH)国立医学图书馆(NLM)国立生物工程中心(NCBI)建立的核苷酸序列数据库(GenBank)及其同源基因序列的搜索(BLASTN), 发现其中的1个克隆序列与GenBank中注册的已知功能基因序列没有同源. 电子拼接推定该基因的开放读码框架, 设计引物, 从表达HCV NS5A蛋白的HepG2细胞提取总RNA后, 进行RT-PCR, 扩增出约1 000 bp片段(图1), 经过测序克隆出全长基因片段, 获得HCV NS5A蛋白反式激活作用的新型靶基因, 命名为NS5ATP7. 新基因的开放读码框架(ORF)长度为894个核苷酸, 编码产物由297个氨基酸残基组成(图2). 新基因的核苷酸序列被GenBank收录, 收录号为AF529368.
HCV基因组的翻译是在有关酶的作用下合成一个长约 3 011氨基酸的多蛋白前体, 然后在宿主信号肽酶和病毒编码的蛋白酶作用下裂解为各种蛋白, 即: 结构蛋白C、E1、E2、p7, 和非结构蛋白NS2、NS3、NS4A、NS4B、NS5A和NS5B[18-23]. NS5A是非结构蛋白的一种, 哺乳动物细胞表达的HCV NS5A位于HCV多蛋白的羧基末端, 是丝氨酸磷酸化蛋白质, 依磷酸化程度的不同而产生两种分子量不同的多肽p56和p58, 分子量分别为56 kD和58 kD, p58被认为是p56的超级磷酸化产物, 目前认为NS5A蛋白是在细胞蛋白激酶作用下发生磷酸化修饰后发挥生物调节作用的[24]. 不同磷酸化形式的NS5A蛋白具有反式激活作用是目前关于NS5A生物学功能研究的热点. 研究发现, NS5A片段转录激活作用最强的位点定位于2 135和2 331 aa之间. NS5A的转录激活区域包括两个酸性氨基酸区(2 143-2 184, 2 220-2 273 aa)和一个脯氨酸富集区(2 282-2 327 aa). 酸性氨基酸区的酸性氨基酸残基的数量与NS5A的反式激活活性相关, 两个酸性氨基酸区是NS5A的转录激活作用的核心区域, 因此酸性氨基酸区2的一些氨基酸的突变可明显影响NS5A的转录激活作用, 但是这些突变更多的是引起蛋白二级结构的改变. 最近的研究表明缺失N-末段146个氨基酸残基和DNA结合区域在GAL4(一种酵母细胞转录激活因子)的HCV NS5A蛋白可强烈的激活酵母和哺乳动物细胞的转录活性. 结合到GAL4 DNA结合区域的全长的HCV NS5A蛋白并没有激活转录的作用. 尽管已有明确证据显示NS5A蛋白全长定位于细胞质内, 在细胞核内仍可以检测到NS5A的N-末段的具有功能性核定位信号(nucleic localization signal, NLS)序列,即PPRKKRVV(354-362 aa), 因此NS5A蛋白具有核信号转导功能, 这就提示这部分结构可进入细胞核内并成为转录激活因子的一部分. Gong et al 研究发现, NS5A能够反式激活核转录因子NF-B及STAT3, 在细胞炎症反应、肿瘤发生及转移过程中起重要作用. 通过反式激活作用, NS5A还可抑制细胞周期调节基因p21WAF1的表达, 抑制p53介导的对转录的反式激活作用和细胞凋亡作用. 此外, 由于NS5A表现出对抗干扰素α(IFNα)的治疗效应而引起人们广泛的关注, NS5A能够与肝细胞中的IFN刺激蛋白-双链RNA依赖的激酶(PKR)相互作用, 抑制PKR的功能, 从而下调IFN刺激的抗病毒效应. 位于NS5A蛋白中央包括一段干扰素敏感决定区(ISDR), 该区被认为是介导NS5A与IFNα诱导的双链RNA依赖的蛋白激酶结合的部位, 后者是IFNα诱导的早期细胞内抗病毒合成反应. 同时NS5A显示出诱导CXC趋化因子、白介素-18(IL-18), 可抵消IFNα抗病毒效应.
本研究建立了真核表达载体pcDNA3.1(-)-NS5A, 转染肝母细胞瘤细胞系HepG2, 以转染空白载体的肝母细胞瘤细胞系HepG2作为对照, 将2种转染的细胞系中提取的mRNA做为起始材料, 应用SSH方法成功地构建了HCV NS5A反式激活相关基因差异表达的cDNA消减文库, 挑选90个克隆测序, 并与GenBank数据库进行同源性比较分析, 结果主要包括2种类型, 第一种是已知基因的序列, 与GenBank中数据高度同源, 其中包括已知的看家基因序列和与细胞生长调节密切相关的基因序列, 第二种是未知基因序列, 共获得15个差异表达的未知序列[6]. 对其中的一个未知功能基因序列, 我们采用生物信息学方法进行电子拼接分析, 获得了其全长基因序列, 被GenBank收录. 本项研究中发现的HCV NS5A蛋白反式激活的新靶基因, 命名为NS5ATP7, 为研究HCV NS5A蛋白的反式激活作用及其作用机制提供了新的研究方向和思路.
编辑: N/A
| 2. | Sakamuro D, Furukawa T, Takegami T. Hepatitis C virus nonstructural protein NS3 transforms NIH 3T3 cells. J Virol. 1995;69:3893-3896. [PubMed] |
| 3. | Ray RB, Lagging LM, Meyer K, Ray R. Hepatitis C virus core protein cooperates with ras and transforms primary rat embryo fibroblasts to tumorigenic phenotype. J Virol. 1996;70:4438-4443. [PubMed] |
| 4. | 刘 妍, 成 军. 丙肝病毒致肝细胞癌的分子生物学机制. 国外医学. 流行病学传染病学分册. 2000;27:10-13. |
| 5. | Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M. Isolation of a cDNA clone derived from a blood-borne non-A non-B viral hepatitis genome. Science. 1989;244:359-362. [PubMed] [DOI] |
| 6. | Kuo G, Choo QL, Alter HJ, Gitnick GL, Redecker AG, Purcell RH, Miyamura TJ, Dienstag L, Alter MJ, Stevens CE. An assay for circulating antibodies to a major etiologic virus of human non-A non-B hepatitis. Science. 1989;244:362-364. [PubMed] [DOI] |
| 7. | Assy N, Minuk GY. A comparison between previous and present histologic assessments of chronic hepatitis C viral infections in humans. World J Gastroenterol. 1999;5:107-110. [PubMed] [DOI] |
| 8. | Huang F, Zhao GZ, Li Y. HCV genotypes in hepatitis C patients and their clinical significance. World J Gastroenterol. 1999;5:547-549. [PubMed] [DOI] |
| 9. | Deng ZL, Ma Y, Yuan L, Teng PK. The importance of hepatitis C as a risk factor for hepatocellular carcinoma in Guangxi. World J Gastroenterol. 2000;6:75-79. |
| 10. | Song ZQ, Hao F, Min F, Ma QY, Liu GD. Hepatitis C virus infection of human hepatoma cell line 7721 in vitro. World J Gastroenterol. 2001;7:685-689. [PubMed] |
| 11. | Zhang LF, Peng WW, Yao JL, Tang TH. Immunohistochemical detection of HCV infection in patients with hepatocellular carcinoma and other liver diseases. World J Gastroenterol. 1998;4:64-65. [PubMed] [DOI] |
| 12. | Yang JM, Wang RQ, Bu BG, Zhou ZC, Fang DC, Luo YH. Effect of HCV infection on expression of several cancer associated gene products in HCC. World J Gastroenterol. 1999;5:25-27. [PubMed] [DOI] |
| 13. | Cheng J. Progress in gene therapy for liver diseases. J Gastroenterol Hepatol. 1999;14:A261. |
| 14. | 王 琳, 李 克, 成 军, 陆 荫英, 张 健, 刘 妍, 王 刚, 洪 源, 王 贺, 芮 莉莉. 筛选与克隆丙型肝炎病毒NS5A蛋白结合蛋白基因. 解放军医学杂志. 2003;28:50-52. |
| 16. | Sato C. Effects of hepatitis C virus proteins on the interferon-stimulated signal transduction. Nippon Rinsho. 2001;59:1271-1276. [PubMed] |
| 17. | 刘 妍, 董 菁, 成 军, 夏 小兵, 李 克, 王 琳, 施 双双, 段 惠娟, 杨 继珍. 乙肝病毒X基因在真核细胞中的表达及反式激活SV40病毒早期启动子的研究. 解放军医学杂志. 2001;26:404-406. |
| 18. | 成 军, 钟 彦伟, 施 双双, 王 刚, 董 菁, 夏 小兵, 杨 继珍, 陈 菊梅. HCV非结构蛋白NS5A人源单链抗体可变区基因的筛选与鉴定. 中华微生物和免疫学杂志. 2000;20:567. |
| 19. | 钟 彦伟, 成 军, 施 双双, 杨 继珍, 董 菁, 夏 小兵, 李 克, 刘 妍, 陈 菊梅. 丙型肝炎病毒非结构蛋白NS5A人源单链抗体的筛选与表达. 中华中西医杂志. 2001;2:97-99. |