修回日期: 2022-09-26
接受日期: 2022-11-24
在线出版日期: 2022-12-28
临床报道多因素可致肛周坏死性筋膜炎(perianal necrotizing fasciitis, PNF), 但直肠恶性肿瘤作为一种极其罕见的诱发因素往往容易被外科医师所忽视, 通过本文案例以期为此类复杂性疾病提供临床诊治经验.
老年男性患者因"右侧肛旁肿痛伴发热3 d"入院, 行相关检查后诊断为: (1)PNF; (2)直肠肿物; (3)肛周脓肿, 行清创术后确诊肿物为直肠腺癌, 根据患者病情予再次清创干预及抗生素调整, 后续行结肠造口术及肠癌根治术, 随访3 mo患者恢复良好.
通过此例患者的诊疗经过, 临床应高度重视PNF的发病因素, 避免因漏诊误诊而延误病情. 对于直肠恶性肿瘤伴PNF患者, 早期诊断十分重要, 确诊后仍建议优先治疗处于急症期的PNF, 再对直肠恶性肿瘤进行综合治疗, 这对于患者预后具有重要意义.
核心提要: 肛周坏死性筋膜炎(perianal necrotizing fasciitis, PNF)早期诊断困难、病情变化迅速且死亡率高, 直肠恶性肿瘤导致PNF十分罕见, 如何平衡和选择两种危重疾病的治疗方案值得探讨. 本文通过报道1例直肠腺癌并发PNF患者的诊疗过程, 以期为临床实践提供指导.
引文著录: 陈光华, 王燕, 张如洁, 冷冬玲, 李璐. 直肠恶性肿瘤并发肛周坏死性筋膜炎患者1例. 世界华人消化杂志 2022; 30(24): 1095-1100
Revised: September 26, 2022
Accepted: November 24, 2022
Published online: December 28, 2022
Perianal necrotizing fasciitis (PNF) has been reported to be caused by multiple factors, but rectal malignant tumors, as an extremely rare predisposing factor, are often easily overlooked by surgeons.
An elderly male patient was admitted due to "right perianal swelling and pain with fever for 3 d" and was diagnosed with PNF, rectal mass, and perianal abscess. The mass was diagnosed as rectal adenocarcinoma after debridement. According to the patient's condition, re-debridement intervention and antibiotic adjustment were given, followed by colostomy and radical resection of the adenocarcinoma. The patient recovered well after 3 mo of follow-up.
The present case suggests that high attention should be paid to etiological factors of PNF in clinical practice to avoid delayed treatment due to missed diagnosis and misdiagnosis. For patients with rectal malignant tumors and PNF, early diagnosis is very important, and it is still recommended to give priority to the treatment of PNF in the acute phase after diagnosis, followed by comprehensive treatment of rectal malignant tumors, which is of great significance for the prognosis of patients.
- Citation: Chen GH, Wang Y, Zhang RJ, Leng DL, Li L. Rectal malignant tumor complicated with perianal necrotizing fasciitis: A case report. Shijie Huaren Xiaohua Zazhi 2022; 30(24): 1095-1100
- URL: https://www.wjgnet.com/1009-3079/full/v30/i24/1095.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v30.i24.1095
肛周坏死性筋膜炎(perianal necrotizing fasciitis, PNF)是一种主要累及于皮下筋膜、会阴部及肛周软组织大面积坏死的急性细菌感染性疾病. PNF早期难以诊断且病情变化迅速, 可在数小时内出现严重并发症甚至发生多器官功能衰竭而导致死亡. 临床报道多种诱因可导致PNF, 但直肠恶性肿瘤作为一种极其罕见的诱发因素往往容易被外科医师所忽视, 生长迅速的癌细胞易向解剖结构复杂的直肠旁间隙侵袭, 进一步导致严重感染形成PNF. 直肠恶性肿瘤和PNF均是肛肠科一类预后不佳、诊断困难、治疗棘手的疾病, 当两者同时出现时, 如何精确地诊断以及选择最佳治疗方案对提高患者生存率显得尤为重要.
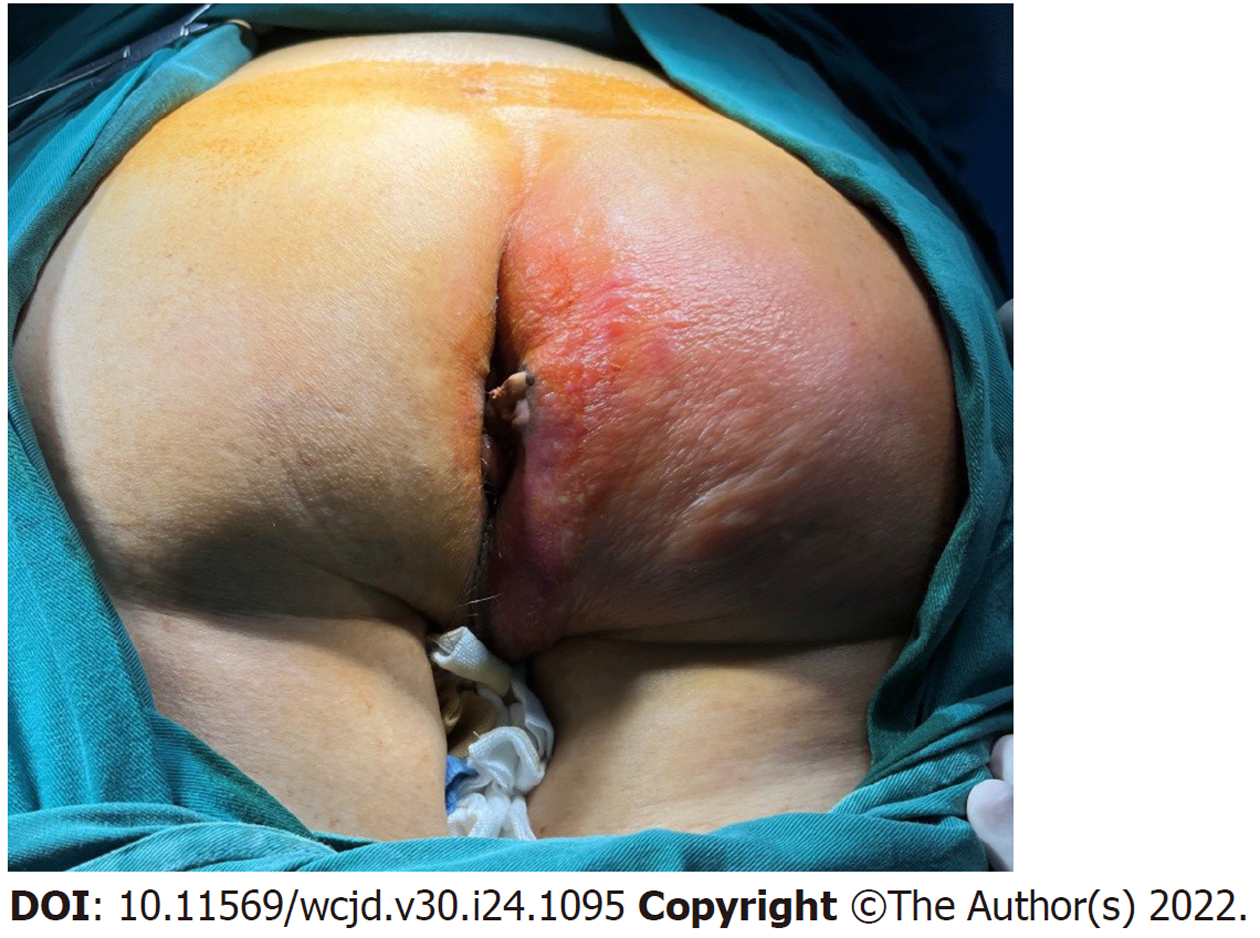
患者男, 71岁, 因"右侧肛旁肿痛伴发热3 d"急诊入院. 患者3 d前发现右侧肛旁红肿疼痛, 体温高至38 ℃, 于当地医院予抗感染治疗(具体不祥), 效果不显, 上述症状逐渐加重, 右侧臀部破溃流脓性分泌物和稀便, 伴有恶臭味, 遂来我院就诊. 近年来排便困难, 大便偶夹有粘液脓血, 近一月来体重下降8 kg. 既往体健. 查体: T38 ℃, P82次/分, R19次/分, BP82/62 mmHg. 专科检查(膝胸位): 右侧肛周皮肤及阴囊根部可见大范围红肿, 边界弥漫不清, 皮温灼热, 指压疼痛加剧. 3点位距肛门4 cm可见一破溃口, 有褐色稀便流出, 伴恶臭味. 距肛缘约5 cm可触及凹凸不平肿物, 环直肠一圈, 质地硬, 上界未触及, 肠腔变窄, 仅能容食指通过(图1).
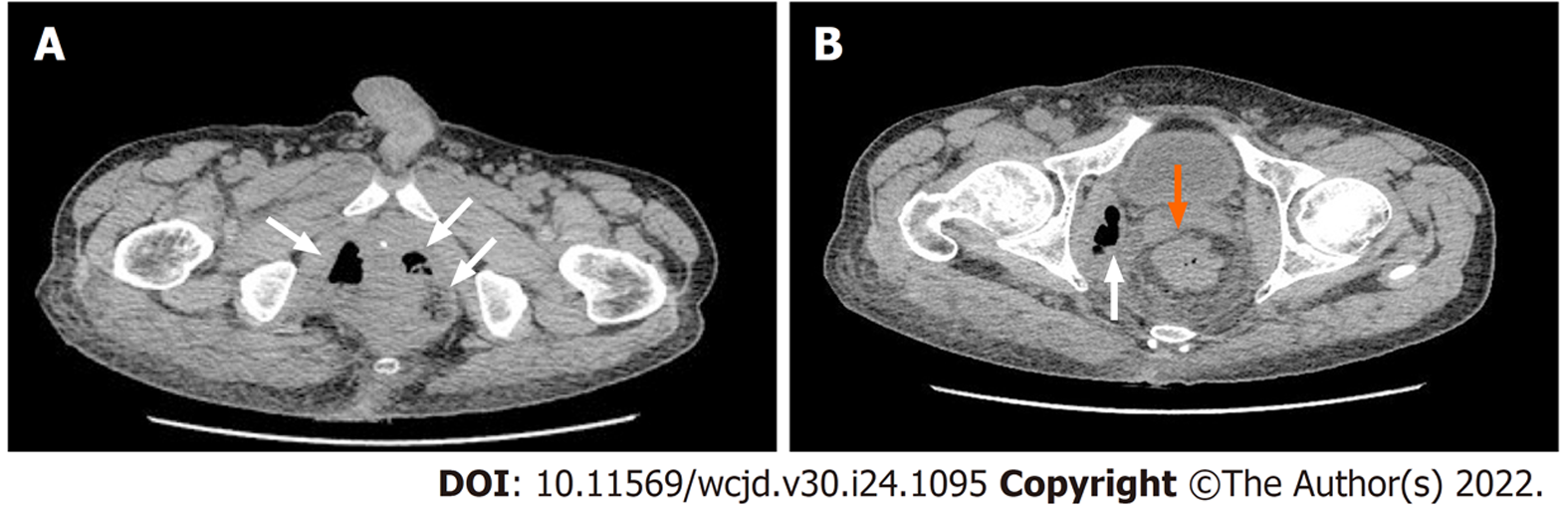
实验室检验: 炎症指标(白细胞21.34×109, 中性粒细胞百分比90.6%, C反应蛋白101 mg/L, 超敏C反应蛋白65.5 mg/L, 血沉30.0 MM/H), 血生化(血红蛋白79 g/L, 总蛋白48.3 g/L, 白蛋白26.7 g/L, 血钾3.2 mmol/L, 血钙1.83 mmol/L), 肿瘤指标(癌胚抗原6.73 ng/mL, 细胞角蛋白21 3.45 ng/mL), 血糖7.00 mmol/L; 全胸腹CT平扫示: 骶前间隙片及盆腔筋膜.
片絮状增厚, 括约肌间隙见斑片状密度增高影及气体, 括约肌及肛提肌肿胀增厚, 部分边界模糊, 右侧坐骨直肠窝条片絮状密度增高影及气体影延伸至会阴部、臀后部. 直肠壁不规则增厚. 肛瘘伴坏死性筋膜炎改变(图2). 本病应与气性坏疽、非梭状芽孢杆菌蜂窝织炎、丹毒等肛周感染性疾病相鉴别. 气性坏疽主要由产气荚膜梭菌引起的广泛肌肉坏死, 病灶处可见特有的血性水泡, 疼痛剧烈, X线可表现为大量的皮下气肿形成; 非梭状芽孢杆菌蜂窝织炎主要是涉及皮下疏松结缔组织的细菌感染, 致病菌多为金黄色葡萄球菌, 并且单用抗生素治疗有效, 当伴有皮肤淋巴管受累时称之为丹毒, 两者预后良好, 不难与本病鉴别. 入院诊断: (1)PNF; (2)直肠肿物; (3)肛周脓肿.
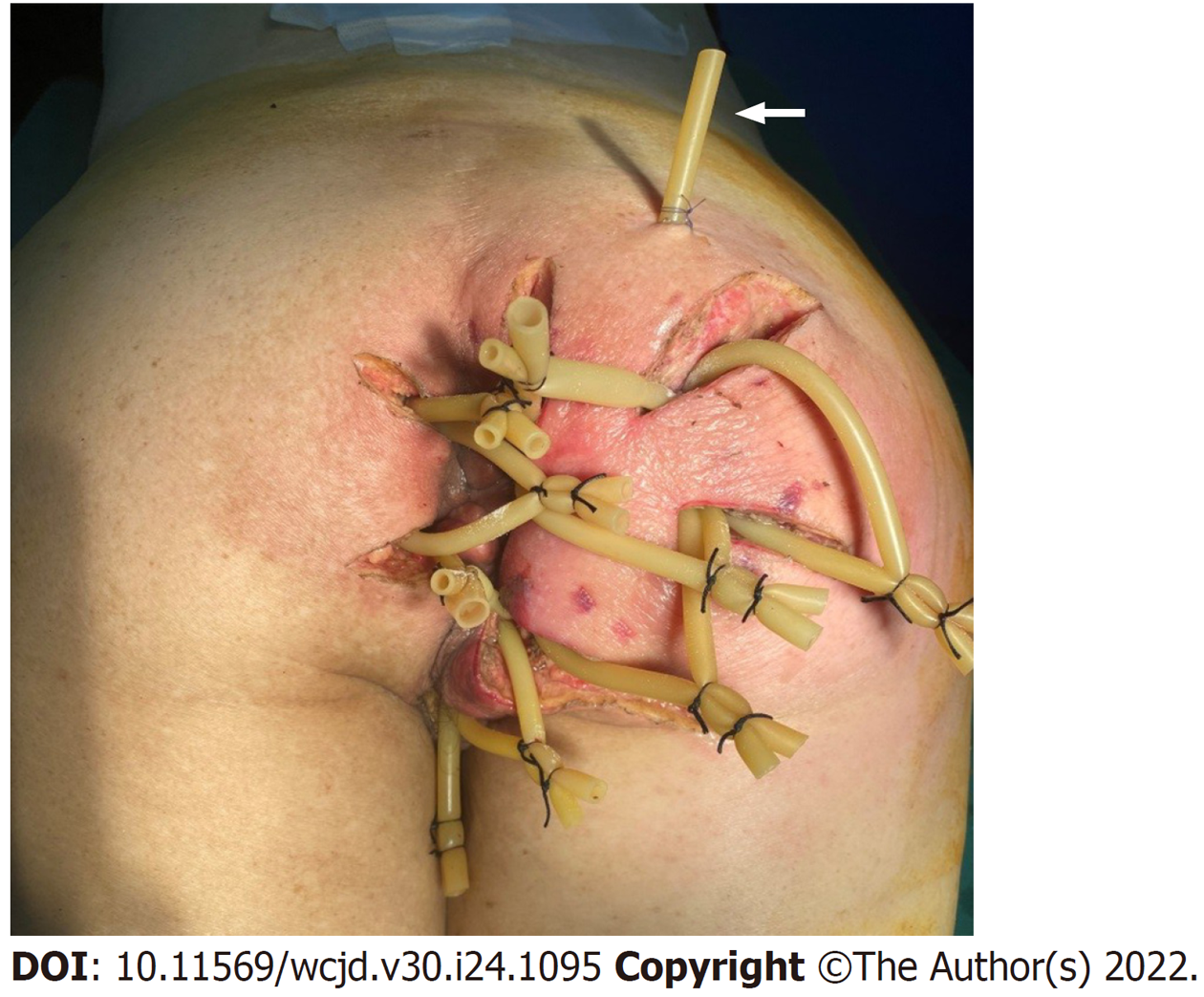
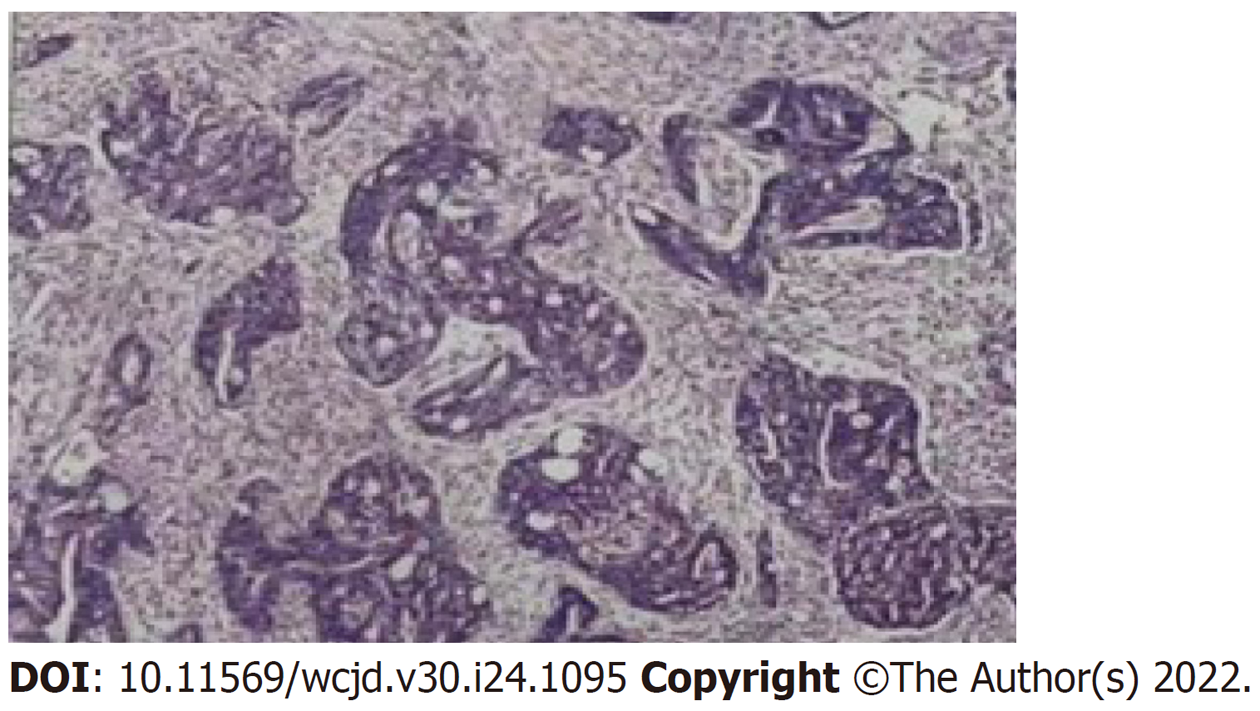
完善必要检查后, 入院6 h内立即行急诊清创术, 根据臀周红肿范围做多个放射状切口, 清除坏死的筋膜与脂肪直至正常组织, 各切口间以硅胶管贯穿引流, 右侧坐骨直肠窝深处置入蕈状引流管(图3). 术中发现右侧坐骨直肠窝内存有大量粪便, 冲洗后在直肠、坐骨直肠窝深处分别留取菜花样组织标本(病理诊断示: 直肠腺癌, 图4). 坏死筋膜及脓液行细菌培养, 提示感染菌为大肠埃希杆菌, 药敏结果显示对氨基糖苷类、第三代头孢菌素类、硝咪唑类、大环内酯类等敏感; 血培养阴性. 予头孢哌酮舒巴坦联合甲硝唑以抗感染治疗, 纠正低蛋白血症, 补充血容量, 纠正水电解质平衡紊乱等对症支持治疗. 术后诊断: (1)PNF; (2)直肠恶性肿瘤; (3)肛周脓肿. 术后创面换药: 早晚两次碘伏/生理盐水1:1混合液、生理盐水、甲硝唑氯化钠溶液依次冲洗创面及引流管以抑制厌氧菌的生长保持肛周清洁, 发现坏死组织及时清理.
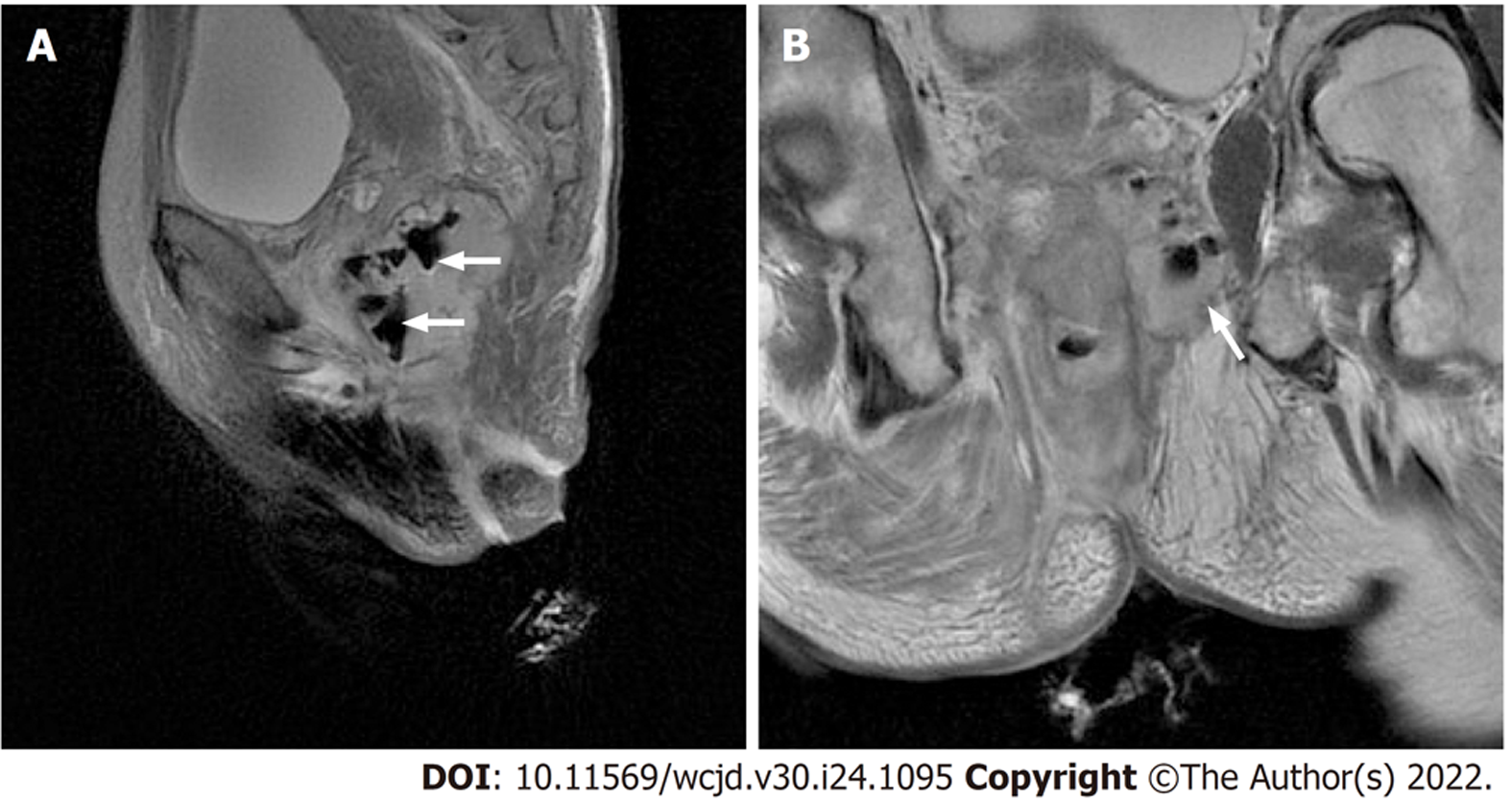
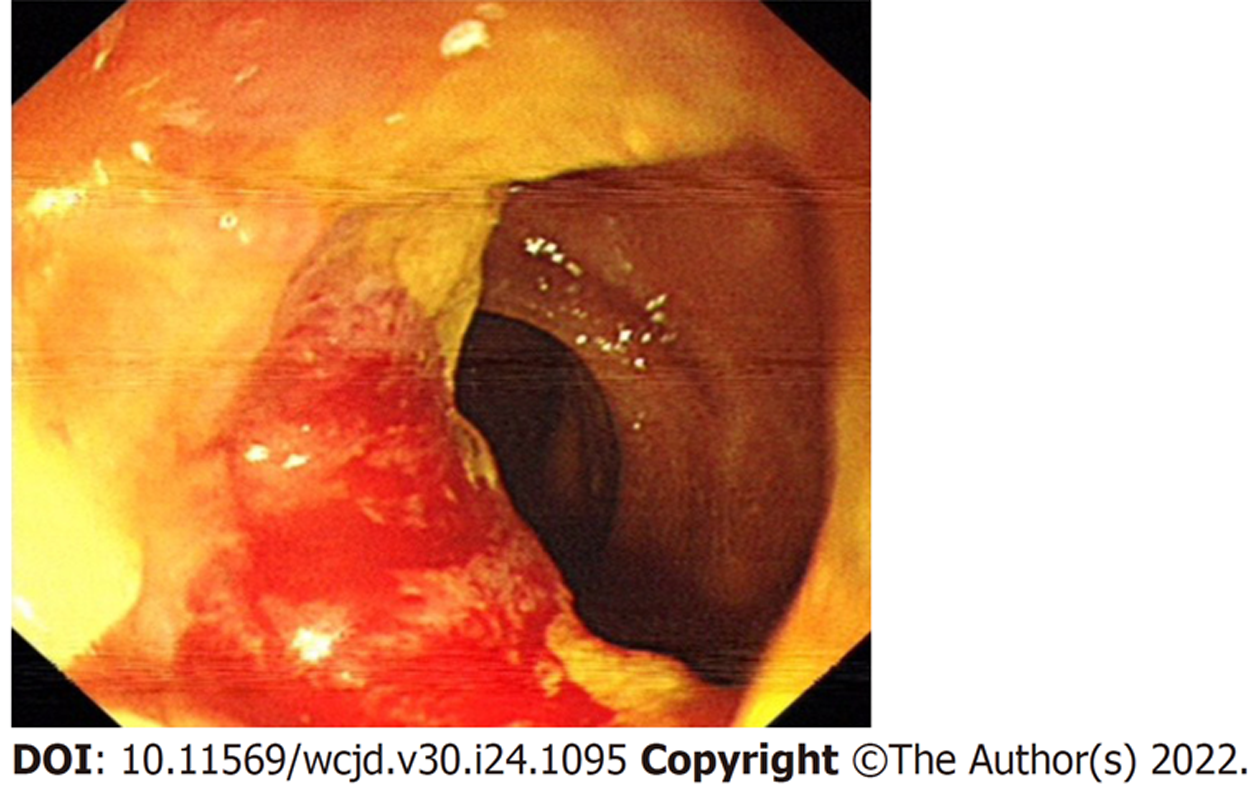
术后12 d患者再次出现发热, 体温高至39.3 ℃, 全身乏力, 大便伴有较多粘液脓血. 急查各项指标与检查: 中性粒细胞百分比79.9%, C反应蛋白54.7 mg/L, 超敏C反应蛋白78.6 mg/L, 血清淀粉样蛋白A 325.1 mg/L. 肛周磁共振示: 直肠中上段管壁明显不规则增厚, 管腔变窄. 直肠周围间隙可见多发大小不等脓腔, 向上突破肛提肌, 以直肠左侧间隙、左侧坐骨直肠窝、左侧会阴部为主, 内见散在气体(图5). 遂再次行清创术, 处理左侧骨盆直肠间隙及坐骨直肠窝深处脓腔并置入蕈状引流管, 并调整抗生素为亚胺培南西司他丁钠联合甲硝唑, 余治疗同前. 术后第6天再次复查肛周磁共振示: 与前次MRI对照, 肛周脓腔明显较前缩小. 患者感染逐渐控制, 为排除肠道上段累及情况并了解肿瘤全貌, 行结肠镜检查示: 直肠见连续性大片状糜烂灶, 并可见出血, 距肛门口10 cm明显狭窄(图6). 为保持创面清洁予行结肠造口术, 待患者身体条件允许后拟行直肠癌根治性手术. 目前肛周创面愈合良好.
(1)PNF; (2)直肠腺癌; (3)肛周脓肿.
根据病情变化行两次清创术后, 患者肛周创面愈合良好; 后续行结肠造口术及肠癌根治术, 随访3 mo患者精神状态可, 无恶寒发热, 无明显不良反应.
PNF是由多种微生物参与的引起肛周组织爆发性感染的危重病症, 在1833年首次由Fournier提出并报道, 所以又名为Fournier坏疽[1]. 有研究显示男女发病比例为10:1, 主要好发于(50-60)岁的中年男性, 其中男性发病率为1.6/100000[2]. 不同的成像技术可辅助诊断PNF, 如磁共振成像(magnetic resonance imaging, MRI)、电子计算机断层扫描(computed tomography, CT)、x线、超声等, 其中临床上以MRI和CT最为常用. MRI通常被认为是较为精确的影像技术, 在检测软组织感染方面优于其他成像模式, 但在急诊状态下, 耗时是MRI的一大局限, 且并非所有医院均配备有MR扫描仪, 临床医生需要在最短时间内了解疾病信息, CT是较为合适的选择[3]. CT能够识别筋膜受累和其他肌肉骨骼感染, 是识别感染源和描绘疾病范围的有效工具, 已有研究证明CT在识别疾病范围方面比平片x线或超声具有更高的特异性, 其影像上可变现为皮下气体形成、软组织弥漫性肿胀、积液等改变, 对于每位患者的不同情况, 适当考虑胸腹部、骨盆至双下肢的计算机断层扫描, 不仅可以了解病灶在不同解剖间隙的受累情况, 还有助于识别局部或远处的恶性肿瘤[4-6]. 本文病例借助CT不仅辅助诊断了直肠肿瘤, 还明确了病灶的播散途径, 通过CT对病灶的追踪, 为手术较为彻底的清创提供了重要的导航作用.
根据病灶的播散规律及人体解剖组织特性, 感染通常沿筋膜平面和邻近软组织传播. 肛周生殖器和会阴区存在几个主要的筋膜平面, 包括Buck筋膜、dartos筋膜和Colles筋膜. Buck筋膜起源于阴茎的冠状沟, 附于阴茎肌肉的表面; Colles筋膜(也称为会阴浅筋膜)通过耻骨上支横向固定, 它与泌尿生殖膈下筋膜向后融合并向前延伸, 形成包裹阴囊和阴茎的dartos筋膜, 再向前腹壁延续则形成Scarpa筋膜. 当Colles筋膜被发生于肛门直肠的感染所穿透, 感染可扩散坐骨直肠间隙向前、向后或向上发展. 由于dartos筋膜是Colles筋膜的直接延伸, Scarpa筋膜又是dartos筋膜的延伸, 因此, 感染若不控制可向前自由扩散到阴囊和腹壁; 若病灶向后进展, 可至臀大肌深浅筋膜, 甚至进一步蔓延至下肢筋膜. 如果病灶进入骶前间隙、膀胱后间隙及骨盆直肠间隙时, 感染可累及腹膜后间隙至上腹部水平, 甚至可渗入腹膜腔[7]. 当至深筋膜平面时, 致病菌就更易通过静脉通道和淋巴管迅速传播, 导致感染性休克和器官衰竭甚至死亡[8]. 由于PNF是一种侵袭性强、扩展迅速、死亡率高的软组织感染性疾病, 细菌在筋膜层面可通过静脉通道和淋巴管迅速扩散, 一次清创较难完全处理干净, 往往需要进行多次清创引流术, 干预的时机与死亡率直接相关, 积极的手术干预是治疗PNF成功的关键. 本例患者感染源来自肛门直肠, 肿瘤穿破肠壁至由右侧坐骨直肠窝、括约肌间感染, 向下延伸至会阴部和臀后部, 向上突破肛提肌到达直肠旁间隙, 由于病情复杂感染进一步发展, 遂予行二次清创术, 积极的手术干预延长了患者的生存期.
文献报道与坏死性筋膜炎有关的危险因素包括糖尿病、高血压、酗酒、高龄、肝硬化、慢性肾病、结核病、心脏瓣膜病、脑卒中、恶性肿瘤等[9,10]. 其中糖尿病是PNF最常见的诱感因素, 高糖的环境使得周围神经和血管易发生病变, 形成缺氧条件, 促使厌氧菌的繁殖与生长, 破坏了免疫细胞的调节功能进而加重了感染, 延缓了创面的愈合, 因此对于有合并糖尿病的患者控制血糖犹为关键[11]. 恶性肿瘤作为一种罕见的诱发因素, 有文献报道在10%的恶性肿瘤患者中常被忽视, 导致诊治延缓而加重病情[12]. 因此建议所有PNF患者均应进行直肠指检, 详细询问有无癌症病史或家族史, 再借助实验室、影像学检查以及组织活检, 以降低癌症漏诊的可能性. 本文病例中直肠恶性肿瘤为原发疾病, 为PNF发病的关键因素, 应引起临床高度重视, 总结分析: (1)患者近年来体重明显下降且伴有排便习惯、大便性质的改变, 可知直肠恶性肿瘤早已出现, 为PNF的发病诱因; (2)术中发现右侧坐骨直肠窝内有大量粪便, 且在直肠壁、坐骨直肠窝顶端可触及大片质硬、菜花样肿物, 考虑癌组织穿透肠壁形成肠瘘, 造成严重感染而致PNF形成. 尽管目前因直肠癌放化疗导致的穿孔已被证实[13], 但表现为直肠癌自发性穿孔形成PNF的报告实属罕见. 有研究显示一旦形成穿孔, 致病菌可沿着阻力最小的筋膜平面快速侵入, 最常累及的是泌尿生殖道和会阴组织[14]; (3)患者为老年男性, 免疫力低下、营养状况差, 加速了PNF的形成[15].
和其他PNF病例相比, 与直肠癌相关的PNF的治疗显得更为复杂, 也是临床医生面临的挑战. 有报道显示与恶性肿瘤相关的PNF的死亡风险至少为20%-40%, 其中包括年龄>60岁、营养状况差、存在外周血管疾病、伴败血症或休克、就诊或治疗延迟(>48 h)都是预后不良指标[16]. Yoshino等[17]描述了1例晚期直肠癌合并重度Fournier坏疽患者, 并为其进行了结肠造口术加会阴清创术, 术后50天行根治性全盆腔脏器切除术与骶骨切除术,术后患者无严重并发症. Bruketa等[7]回顾性分析了23例直肠癌合并PNF的患者, 发现直肠癌作为诱发因素导致的PNF中占了全部发病因素的1.47%-16.6%, 并且短期预后中总体生存率为74%, 死亡率为13%. Celik等[18]报告了1例继发于结直肠肿瘤穿孔的下肢坏死性筋膜炎患者, 进行了筋膜切开术及Hartmann术, 并指出在充分开窗引流后, 结肠造口术是下一步治疗合理的选择, 一旦NF得到控制, 应切除原发灶. 由于需处理急性的PNF, 对直肠癌的治疗有一定的延迟, 加上直肠癌穿孔引起的炎症反应有助于促进癌细胞播散, 直肠癌诱导的PNF患者预后可能更差. 本文病例中直肠癌作为一种既存疾病, 治疗上先予处理情况紧急危重的PNF, 当PNF病情得到控制并稳定后再行直肠癌治疗.
PNF是外科医生必须意识到的一种具有挑战性的危重病症, 尽早的诊断、积极的手术清创、经验性广谱抗生素的应用可能是提高生存率的关键. 直肠恶性肿瘤诱发导致PNF在临床上及为罕见, 相关的癌症诊断常常被漏诊, 使治疗延误使导致预后较差, 因此临床医生必须保持高度的警惕性, 尤其是当患者伴有直肠恶性肿瘤时, 如何恰当地处理两者治疗的缓急显得至关重要.
学科分类: 胃肠病学和肝病学
手稿来源地: 江西省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C, C
D级 (一般): 0
E级 (差): 0
科学编辑: 张砚梁 制作编辑:张砚梁
| 1. | Zingaro MD, Boni A, Vermandois JAR, Paladini A, Lepri E, Ursi P, Cirocchi R, Turco M, Gaudio G, Nogara A, Mearini E. Fournier's Gangrene and Intravenous Drug Abuse: an Unusual Case Report and Review of The Literature. Open Med (Wars). 2019;14:694-710. [PubMed] [DOI] |
| 2. | Wongwaisayawan S, Krishna S, Haroon M, Nisha Y, Sheikh A. Fournier gangrene: pictorial review. Abdom Radiol (NY). 2020;45:3838-3848. [PubMed] [DOI] |
| 3. | Carbonetti F, Cremona A, Carusi V, Guidi M, Iannicelli E, Di Girolamo M, Sergi D, Clarioni A, Baio G, Antonelli G, Fratini L, David V. The role of contrast enhanced computed tomography in the diagnosis of necrotizing fasciitis and comparison with the laboratory risk indicator for necrotizing fasciitis (LRINEC). Radiol Med. 2016;121:106-121. [PubMed] [DOI] |
| 4. | Gupta N, Zinn KM, Bansal I, Weinstein R. Fournier's gangrene: ultrasound or computed tomography? Med Ultrason. 2014;16:389-390. [PubMed] |
| 6. | Singh A, Ahmed K, Aydin A, Khan MS, Dasgupta P. Fournier's gangrene. A clinical review. Arch Ital Urol Androl. 2016;88:157-164. [PubMed] [DOI] |
| 7. | Bruketa T, Majerovic M, Augustin G. Rectal cancer and Fournier's gangrene - current knowledge and therapeutic options. World J Gastroenterol. 2015;21:9002-9020. [PubMed] [DOI] |
| 8. | Myers CM, Miller JJ, Davis WD. Skin and Soft Tissue Infections: A Case of Necrotizing Fasciitis. Adv Emerg Nurs J. 2019;41:322-329. [PubMed] [DOI] |
| 9. | Liu TJ, Tai HC, Chien KL, Cheng NC. Predisposing factors of necrotizing fasciitis with comparison to cellulitis in Taiwan: A nationwide population-based case-control study. J Formos Med Assoc. 2020;119:18-25. [PubMed] [DOI] |
| 10. | 钟 洁, 刘 小孙. 坏死性筋膜炎诊治分析及研究进展. 中国急救复苏与灾害医学杂志. 2018;13:955-958. |
| 12. | Mann AJ, Reinoso DB, Genuit T, Jimenez J. Fournier's Gangrene in the Setting of Underlying Carcinoma: A Case Report and Review of the Literature. Cureus. 2020;12:e10317. [PubMed] [DOI] |
| 14. | Karam C, Badiani S, Berney CR. COVID-19 collateral damage: delayed presentation of a perforated rectal cancer presenting as Fournier's gangrene. ANZ J Surg. 2020;90:1483-1485. [PubMed] [DOI] |
| 15. | Al-Qurayshi Z, Nichols RL, Killackey MT, Kandil E. Mortality Risk in Necrotizing Fasciitis: National Prevalence, Trend, and Burden. Surg Infect (Larchmt). 2020;21:840-852. [PubMed] [DOI] |
| 16. | Ioannidis O, Kitsikosta L, Tatsis D, Skandalos I, Cheva A, Gkioti A, Varnalidis I, Symeonidis S, Savvala NA, Parpoudi S, Paraskevas GK, Pramateftakis MG, Kotidis E, Mantzoros I, Tsalis KG. Fournier's Gangrene: Lessons Learned from Multimodal and Multidisciplinary Management of Perineal Necrotizing Fasciitis. Front Surg. 2017;4:36. [PubMed] [DOI] |
| 17. | Yoshino Y, Funahashi K, Okada R, Miura Y, Suzuki T, Koda T, Yoshida K, Koike J, Shiokawa H, Ushigome M, Kaneko T, Nagashima Y, Goto M, Kurihara A, Kaneko H. Severe Fournier's gangrene in a patient with rectal cancer: case report and literature review. World J Surg Oncol. 2016;14:234. [PubMed] [DOI] |
| 18. | Celik SU, Senocak R. Necrotizing fasciitis of the lower extremity secondary to a perforated rectosigmoid tumor. Indian J Cancer. 2021;58:603-607. [PubMed] [DOI] |