修回日期: 2021-11-26
接受日期: 2021-12-17
在线出版日期: 2022-01-08
简短炎症性肠病问卷(the short inflammatory bowel disease questionnaire, SIBDQ) 广泛用于评估炎症性肠病(inflammatory bowel disease, IBD)患者的健康相关生活质量.
引进SIBDQ量表并评估其信效度.
根据Brislin模型的翻译-回译流程得到中文版SIBDQ(SIBDQ-C). 对2020-06/2021-06就诊于广州中医药大学第一附属医院、中山大学第一附属医院IBD患者进行测评; 使用克朗巴赫系数、分半信度和重测信度检验量表的信度, 使用验证性因子分析评价其结构效度.
共发放问卷113份, 最终回收112份.SIBDQ-C的Cronbach's α为0.90, 折半系数为0.86; 量表四个维度间的Spearman相关系数在0.61到0.77之间; 验证性因子分析的近似误差方根、非范拟合指数、比较拟合指数、拟合优度指数分别为0.08、0.93、0.97、0.92; 不同粪便形态患者的SIBDQ-C总分及各维度得分均有统计学差异(P<0.05).
SIBDQ-C具有良好的信度及效度, 可以用于临床测量我国IBD患者的生活质量.
核心提要: 简短炎症性肠病问卷(the short inflammatory bowel disease questionnaire, SIBDQ) 被广泛用于评估炎症性肠病(inflammatory bowel disease, IBD)患者的健康相关生活质量.本研究对SIBDQ进行汉化并通过收集临床资料证实了其良好的信度及效度, 可用于临床测量我国IBD患者生活质量.
引文著录: 张诗静, 罗建峰, 彭彬, 侯江涛, 徐谦, 陈丽霞, 李辉标, 刘诗颖, 钟嘉敏, 何镇帆, 陈新林. 简短炎症性肠病生活质量问卷的信效度评价. 世界华人消化杂志 2022; 30(1): 17-23
Revised: November 26, 2021
Accepted: December 17, 2021
Published online: January 8, 2022
The short inflammatory bowel disease questionnaire (SIBDQ) is a widely used assessment tool to measure the health-related quality of life of patients with inflammatory bowel disease (IBD).
To translate and validate the SIBDQ in Chinese IBD patients.
A simplified Chinese version of SIBDQ (SIBDQ-C) was obtained according to Brislin's translation and back-translation procedure. The patients with IBD were measured in the First Affiliated Hospital of Guangzhou University of Chinese Medicine and the First Affiliated Hospital of Sun Yat-Sen University between June 2020 and June 2021. Cronbach's α, split-half reliability, and intraclass correlation coefficient (ICC) were used to test the reliability of the SIBDQ-C. Confirmatory factor analysis was used to evaluate its structural validity.
A total of 113 patients with IBD were enrolled, and 112 were eventually included for analysis. Cronbach's α of the SIBDQ-C was 0.90, and split-half coefficient was 0.86. ICCs of the four dimensions ranged from 0.61 to 0.77. Confirmatory factor analysis showed that root mean square error of approximation, non-normed fit index, comparative fit index, and goodness-of-fit index were 0.08, 0.93, 0.97, and 0.92, respectively. There were significant differences in the SIBDQ-C score and the scores of four dimensions in patients with different fecal characters (P < 0.05).
The SIBDQ-C has good reliability and validity, which can be used to measure the quality of life of patients with IBD in mainland China.
- Citation: Zhang SJ, Luo JF, Peng B, Hou JT, Xu Q, Chen LX, Li HB, Liu SY, Zhong JM, He ZF, Chen XL. Reliability and validity of the Chinese version of the short inflammatory bowel disease questionnaire. Shijie Huaren Xiaohua Zazhi 2022; 30(1): 17-23
- URL: https://www.wjgnet.com/1009-3079/full/v30/i1/17.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v30.i1.17
炎症性肠病(inflammatory bowel disease, IBD)是一种胃肠道慢性、非特异性、复发性炎症疾病, 包括克罗恩病(Crohn's disease, CD)和溃疡性结肠炎(ulcerative colitis, UC). 目前, 我国IBD患病率是亚洲最高的[1,2]. IBD尚无根治方法, 且疾病反复发作, 严重影响患者的生活质量. 健康相关生活质量量表被临床医生视为重要的结局指标. 陈新林等[3]评估和比较IBD疾病特异性的健康相关生活质量工具, 指出对于成年IBD患者, 简短版炎症性肠病生活质量问卷(short inflammatory bowel disease questionnaire, SIBDQ)具有良好的测量特性, 在全球范围内被广泛使用. 然而, 未见文献报道SIBDQ的中文版的翻译工作和测量性能评价. 本研究对SIBDQ进行汉化并对评价其信效度, 为临床医生测量我国IBD患者生活质量提供可靠的工具.
1.1.1 研究对象: 本研究获得广州中医药大学第一附属医院伦理委员会批准(编号: ZYYECK[2019]160). 2020-06/2021-06, 纳入广州中医药大学第一附属医院、中山大学第一附属医院就诊的炎症性肠病患者, 对其进行问卷调查. 对于疾病稳定的患者, 在1-4周后重新发放中文版SIBDQ(SIBDQ-C), 以评估量表的重测信度[4]. 纳入标准: (1)参照2018年《炎症性肠病诊断与治疗的共识意见》[5]中推荐的标准, 符合UC或CD诊断标准的病人; (2)年龄在(16-75)岁; (3)能正常沟通交流, 单独或在他人帮助下能够完成问卷; (4)自愿签署知情同意书. 排除标准: 并发其他对生活质量有严重影响的疾病, 如癌症、心脏病等的患者.
1.1.2 研究工具: 调查问卷包括基本人口学资料、SIBDQ-C量表、布里斯托尔大便量表. (1)基本人口学资料包括性别、年龄、婚姻状况和文化程度; (2)翻译得到的SIBDQ-C量表与原版具有相同的条目数量及维度结构.量表共有10个条目, 分为四个不同的维度: 肠道症状、心理功能、社会功能和全身症状. 其中肠道症状维度由条目4、6和9组成, 社会功能维度包括条目2和3, 心理功能维度由条目5、8和10组成(其中条目8为反向条目), 全身症状由条目1和7组成.所有条目均以7分李克特量表评分作为反应选项, 范围从1分(所有时间)到7分(完全没有). SIBDQ-C的总分范围从10到70, 得分越高, 生活质量越高; (3)布里斯托尔大便量表(bristol stool form scale, BSFS)是Lewis等人[6]为评估粪便形态研发的量表. 该量表的有效性和可靠性已经得到验证并在临床实践和研究中广泛使用[7,8]. BSFS将大便类型分为7个分类: 最硬(类型1)到最软(类型7). 1型和2型被认为是硬便(以及其他指示便秘的症状), 3、4、5型是理想型大便(指示正常大便形态), 而6型和7型被认为是稀烂/液体大便(以及其他指示腹泻的症状). 本研究使用BSFS量表评估患者粪便形态以研究区分度和评估参与重测患者的病情变化情况.
1.2.1 量表的汉化: SIBDQ是一种广泛使用的工具, 用于评估炎症性肠病患者的健康相关生活质量[9-13]. 在获得SIBDQ作者授权后, 根据Brislin模型[14]对原始版本的SIBDQ进行翻译和回译工作. 首先, 原始版本的SIBDQ由两位具有专业英语水平的研究者单独翻译成中文. 在不改变原量表的原始含义的基础上, 双方对有争议部分进行讨论并修改, 形成SIBDQ-C的初稿. 然后由两名未接触过原始量表的双语胃肠道疾病医师将SIBDQ-C回译成英文, 并将回译后的英文版本进行校对整合. 最后由研究小组对回译后得到的英文版量表与原始量表进行语义偏差的对比, 最终形成SIBDQ-C.
1.2.2 资料收集: 调查采用电子问卷的形式进行资料收集. 问卷内容由研究者录入问卷星后通过网络向患者发放. 为了让研究人员熟知调查的目的和意义, 熟悉和掌握资料收集的要求和方法, 确保资料的准确性和可靠性, 对参与调查的研究人员进行调查前培训. 在进行问卷调查前, 先向患者进行解释, 阐明此次调查的研究目的, 获得患者同意后, 开始调查研究. 患者通过研究者提供电子设备进行自行填写. 问卷填写完毕后, 研究者进行人工排查, 剔除无效问卷(信息不完整, 填写时间少于10秒).
统计学处理 采用Microsoft Office Excel 2016建立数据库, 由两名研究者核对数据以避免研究过程中数据错误. 采用SPSS 25.0统计软件和AMOS 21.0软件进行统计分析. 计量资料且服从正态分布采用均数±标准差(mean±SD)描述, 非正态分布用中位数和四分位间距描述; 计数资料使用频数及百分比描述. (1)SIBDQ-C的信度分析包括: 采用克朗巴赫(Cronbach's α)系数和分半信度系数评估其内部信度. 采用组内相关系数(intraclass correlation coefficient, ICC)评估SIBDQ-C的重测信度. ICC<0.4表示重测信度差, ICC>0.7表示重测信度好[4]; (2)SIBDQ-C的效度分析包括: ①采用各条目得分与其所属维度得分的Spearman相关系数评价量表的聚合效度、判别效度, 相关系数大则表明量表的内容效度好. ②采用AMOS 21.0软件进行验证性因子分析, 计算拟合度指标χ2/df、近似误差方根(RMSEA)、非范拟合指数(NFI)、比较拟合指数(CFI)和拟合优度指数(GFI); (3)SIBDQ-C的区分度分析: 比较UC及CD患者的总分及其各维度得分, 比较不同粪便形态患者的SIBDQ-C总分及其各维度得分, 评价量表的区分度. P≤0.05为差异有统计学意义.
一共发放问卷113份, 去除1份无效问卷(信息不完整), 最终得到有效问卷112份.受试者平均年龄(38.94±13.59)岁, 其中69例UC患者, 43例为CD患者, 其他人口学特征见表1. 选取40例病情稳定患者进行重测.
| IBD(n = 112) | UC(n = 69) | CD(n = 43) | 重测患者(n = 40) | |
| 性别(%) | ||||
| 男 | 72(64.3) | 46(66.7) | 26(60.5) | 30(75.0) |
| 女 | 40(35.7) | 23(33.3) | 17(39.5) | 10(25.0) |
| 年龄(mean±SD) | 38.9±13.6 | 44.6±12.9 | 29.8±9.0 | 38.0±14.1 |
| 婚姻状况(%) | ||||
| 未婚 | 73(65.2) | 58(84.1) | 15(34.9) | 26(65.0) |
| 已婚 | 39(34.8) | 11(15.9) | 28(65.1) | 14(35.0) |
| 文化程度(%) | ||||
| 初中及以下 | 17(15.2) | 11(15.9) | 6(14.0) | 7(17.5) |
| 高中、中专 | 30(26.8) | 21(30.4) | 9(20.9) | 11(27.5) |
| 大专 | 22(19.6) | 13(18.8) | 9(20.9) | 8(20.0) |
| 大学本科 | 37(33.0) | 19(27.5) | 18(41.9) | 12(30.0) |
| 研究生及以上 | 6(5.4) | 5(7.2) | 1(2.3) | 2(5.0) |
SIBDQ-C的Cronbach's α为0.90, 4个维度的Cronbach's α分别为肠道症状0.77、全身症状0.74、心理功能0.56、社会功能0.90. 分半信度: 采用前后分半, 计算两半量表得分的系数, 本量表分半信度为0.86. 本量表的ICC系数(表2)分别为总量表0.94, 肠道症状0.89, 全身症状0.88, 心理功能0.75, 社会功能0.88, 说明SIDBQ-C的重测信度良好.
| 维度 | 首测得分 | 复测得分 | ICC | P值 |
| 总量表 | 50.60±10.94 | 49.90±10.16 | 0.94 | <0.01 |
| 肠道症状 | 16.35±3.84 | 15.73±3.73 | 0.88 | <0.01 |
| 全身症状 | 9.85±3.02 | 10.13±3.02 | 0.88 | <0.01 |
| 心理功能 | 14.60±2.62 | 14.35±2.89 | 0.75 | <0.01 |
| 社会功能 | 9.98±2.97 | 9.53±3.05 | 0.88 | <0.01 |
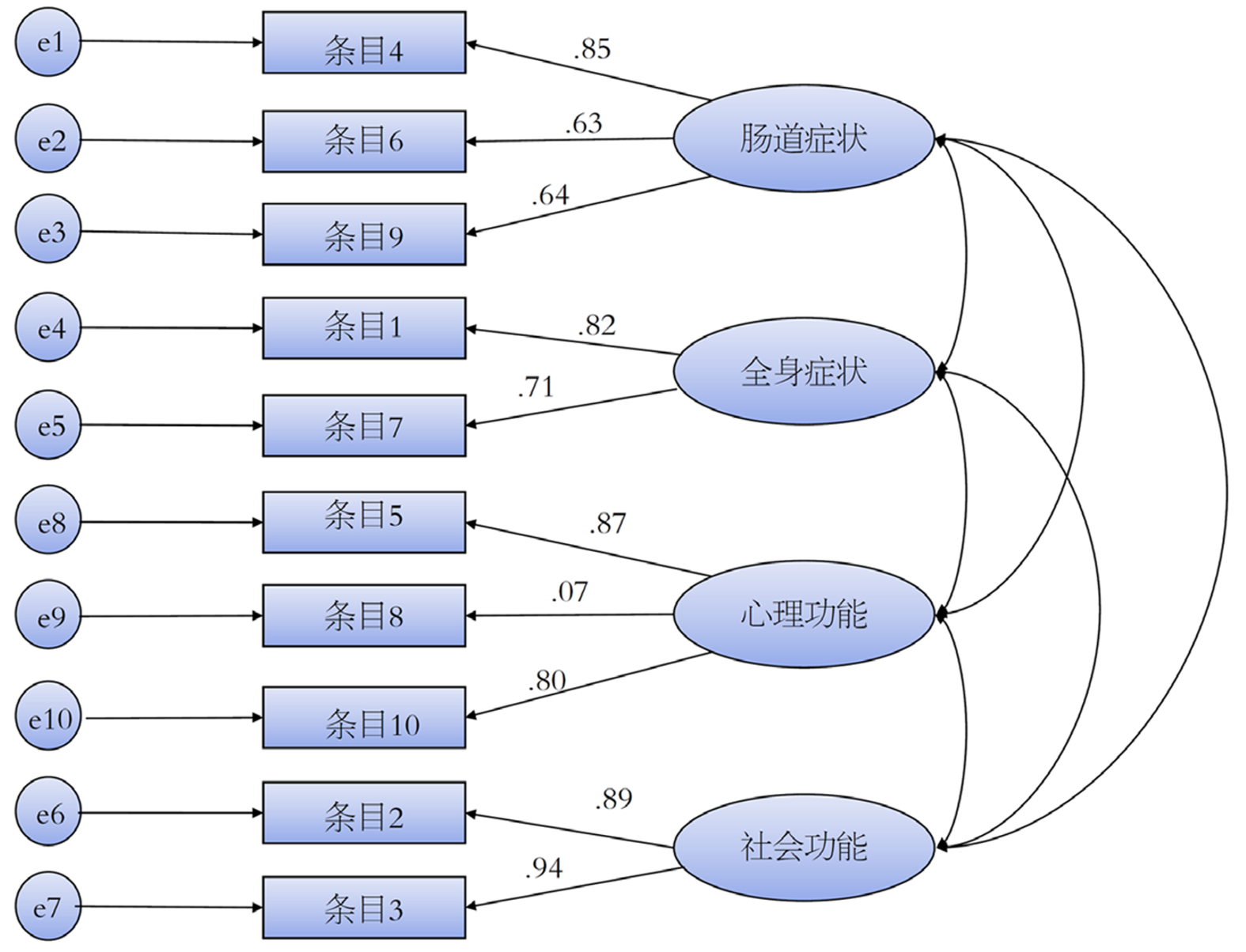
SIBDQ-C各维度之间Spearman相关系数0.61-0.74, 各维度与总分之间的Spearman相关系数为0.83-0.89(表3), 说明量表的内容效度好. 量表各条目与所属的维度相关系数最高, 且均>0.4, 提示量表具有良好的聚合效度和判别效度(表4). 对中文版SIDBQ拟合因子模型, 结果如图1所示, 各条目与各维度(潜在变量)的因子负荷均大于0.60, 每个条目对应潜变量的解释率较大. 拟合度指标χ2/df、RMSEA、NFI、CFI、GFI分别为1.78、0.08、0.93、0.97、0.92.
UC及CD患者的总得分及其各维度得分差异均无统计学意义. 不同粪便形态的患者的总分及其各维度得分均有统计学差异(P<0.05), 腹泻患者SIBDQ-C的总分和各维度得分均低于正常或便秘患者, 表明其生活质量更差(表5).
| 总分 | 肠道症状 | 全身症状 | 心理功能 | 社会功能 | |
| 疾病分类 | |||||
| UC(n = 69) | 47.77±11.44 | 15.39±3.99 | 9.28±2.94 | 13.75±3.05 | 8.94±3.31 |
| CD(n = 43) | 47.26±12.63 | 15.84±3.80 | 9.49±3.17 | 14.19±3.38 | 8.35±3.12 |
| t值 | -0.05 | -0.59 | 0.94 | -0.25 | 0.36 |
| P值 | 0.94 | 0.56 | 0.35 | 0.80 | 0.72 |
| 粪便形态 | |||||
| 硬便 | 54.33±15.50 | 16.00±5.00 | 10.67±3.01 | 16.33±4.51 | 11.33±3.05 |
| 正常大便 | 51.21±9.93 | 16.90±3.24 | 9.63±2.93 | 14.63±2.95 | 10.07±2.84 |
| 稀便 | 38.97±11.18 | 12.83±3.79 | 6.81±3.05 | 11.67±3.55 | 7.67±2.69 |
| F值 | 17.11 | 16.71 | 11.10 | 8.93 | 11.10 |
| P值 | <0.0001 | <0.0001 | <0.0001 | <0.0001 | <0.0001 |
生活质量是一个多维概念, 被视为潜在变量, 包括幸福感和角色功能的身体、社会和心理方面[15]. 评估IBD患者的健康相关生活质量是医疗管理和临床决策的重要组成部分, 在过去十年中, 国内评估IBD患者生活质量的量表迅速增加. 炎症性肠病生活质量问卷(IBDQ)是国内使用最为广泛的量表, 但是包含32个条目, 涵盖疾病相关症状评估、全身症状评估、心理功能评估和社会功能评估4个方面[16], 测评需要花费较多时间, 在一定程度上增加了被测试者的负担. 而SIBDQ由于测量耗时少, 且具有良好的信度、效度, 已经被多国学者翻译并修正且推广使用. 英国[9]、德国[10]、美国[11]、西班牙[12]和葡萄牙语版[13]的SIBDQ的被证实具有良好的信度、效度. 随着我国IBD患者的患病率逐年增加, 临床试验及科研研究的需求增加, 因此需要翻译和验证中文版SIBDQ以便临床使用.
接受测量的患者均可在10分钟内完成SIBDQ-C, 测试者可快速计算临床评分, 可见SIBDQ-C具有良好的可操作性. SIBDQ-C具有高内部一致性和高重测性. 中文版SIBDQ的Cronbach's α系数为0.90, 高于量表研发作者报告的0.78[17]及葡萄牙版本的0.80[13], 与德国版本的0.84较为接近[10], 说明该量表具有很好的内部一致性. 各个维度Cronbach's α均在0.61-0.77之间, 说明各个维度下, 条目测量内容的一致性较好.
SIBDQ-C在少数IBD患者中进行了重复评估. 在临床情况不变的情况下, 重复评估的结果显示可重复和一致性. 肠道症状、全身症状、社会功能维度的ICC均大于0.8, 心理功能ICC为0.73, 高于原版的0.65, 葡萄牙语版本的0.69(CI 0.50-0.82), 及德语版本的0.60. 这可能重测间隔时间较短有关, 本次评价间隔时间最短6天, 最长24天, 间隔6-8的病例数占所有复测病例数的75%. 根据Hernaez[18]建议的划分标准, 依然在可接受范围内, 本次研究重测ICC均大于0.7, SIBDQ-C仍然是可靠的测量工具.
验证性因子分析结果显示, SIBDQ-C具有良好的结构效度. NFI、CFI、GFI均大于0.90, 并且χ2/df小于2. 虽然RMSEA大于0.05, 但小于0.1, 在可接受范围内. 通过4个维度得分与总得分的相关分析显示心理功能为显著相关, 其余3个维度都与量表总分存在高度相关性.
本研究中采用的BSFS量表经循证验证, 信效度良好, 可以根据患者的粪便形态进行评分, 无创、简单易行且不增加患者痛苦和经济负担. 结果显示, SIBDQ-C可以较好的区分患者腹泻和便秘状态. 因此, SIBDQ-C不仅是一种有效的健康生活质量测量方法, 也是一种可靠和一致的测量方法.
本研究存在一定的不足之处. 重测的样本量偏小, 研究者推荐重测样本量应大于50[19], 且重测间隔时间短, 被调查者可能存在记忆效应. 本研究暂未对SIBDQ-C进行校标效度评价, 且本研究仅纳入广州市双中心的IBD患者作为研究对象, 在今后的研究中, 应纳入更多地区的患者进行研究并进行校标效度评价, 以期全面评价量表普适性.
综上所述, SIBDQ-C是测量IBD患者健康相关生活质量的一种简单、有效、可靠的测量工具, 可以被应用于临床实践和科学研究.
感谢广州中医药大学第一附属医院脾胃病科及中山大学附属第一医院消化内科医务人员在本研究开展中给与的帮助.
简短炎症性肠病问卷(the short inflammatory bowel disease questionnaire, SIBDQ)广泛用于评估炎症性肠病(inflammatory bowel disease, IBD)患者的健康相关生活质量, 但未见文献报道SIBDQ的中文版的翻译工作和测量性能评价.
旨在汉化SIBDQ量表并评估其信效度.
通过评估中文版SIBDQ量表, 为临床医生引进可靠的测量IBD患者生活质量的工具.
根据标准的翻译-回译流程得到中文版SIBDQ (SIBDQ-C). 收集并分析2020-06/2021-06就诊于广州中医药大学第一附属医院、中山大学第一附属医院IBD患者的临床信息, 评价SIBDQ-C的信效度.
SIBDQ-C的Cronbach's α高于其他语言版本; 量表四个维度间的Spearman相关系数提示各个维度下, 条目的内容一致性较好; 验证性因子分析显示SIBDQ-C具有良好的结构效度.
SIBDQ-C具有良好的测量特性并适用于测量我国IBD患者的生活质量.
本研究发现SIBDQ-C适用于测量中国IBD患者的生活质量, 未来可通过多中心研究并进行校标效度评价, 以期全面评价量表普适性.
学科分类: 胃肠病学和肝病学
手稿来源地: 广东省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): B, B
C级 (良好): 0
D级 (一般): 0
E级 (差): 0
科学编辑: 张砚梁 制作编辑:张砚梁
| 1. | Kaplan GG. The global burden of IBD: from 2015 to 2025. Nat Rev Gastroenterol Hepatol. 2015;12:720-727. [PubMed] [DOI] |
| 2. | Ng SC, Kaplan GG, Tang W, Banerjee R, Adigopula B, Underwood FE, Tanyingoh D, Wei SC, Lin WC, Lin HH, Li J, Bell S, Niewiadomski O, Kamm MA, Zeng Z, Chen M, Hu P, Ong D, Ooi CJ, Ling KL, Miao Y, Miao J, Janaka de Silva H, Niriella M, Aniwan S, Limsrivilai J, Pisespongsa P, Wu K, Yang H, Ng KK, Yu HH, Wang Y, Ouyang Q, Abdullah M, Simadibrata M, Gunawan J, Hilmi I, Lee Goh K, Cao Q, Sheng H, Ong-Go A, Chong VH, Ching JYL, Wu JCY, Chan FKL, Sung JJY. Population Density and Risk of Inflammatory Bowel Disease: A Prospective Population-Based Study in 13 Countries or Regions in Asia-Pacific. Am J Gastroenterol. 2019;114:107-115. [PubMed] [DOI] |
| 3. | Chen XL, Zhong LH, Wen Y, Liu TW, Li XY, Hou ZK, Hu Y, Mo CW, Liu FB. Inflammatory bowel disease-specific health-related quality of life instruments: a systematic review of measurement properties. Health Qual Life Outcomes. 2017;15:177. [PubMed] [DOI] |
| 4. | Terwee CB, Bot SD, de Boer MR, van der Windt DA, Knol DL, Dekker J, Bouter LM, de Vet HC. Quality criteria were proposed for measurement properties of health status questionnaires. J Clin Epidemiol. 2007;60:34-42. [PubMed] [DOI] |
| 5. | 吴 开春, 梁 洁, 冉 志华, 钱 家鸣, 杨 红, 陈 旻湖, 何 瑶. 炎症性肠病诊断与治疗的共识意见(2018年, 北京). 中华消化杂志. 2018;38:292-311. [DOI] |
| 6. | Lewis SJ, Heaton KW. Stool form scale as a useful guide to intestinal transit time. Scand J Gastroenterol. 1997;32:920-924. [PubMed] [DOI] |
| 7. | Degen LP, Phillips SF. How well does stool form reflect colonic transit? Gut. 1996;39:109-113. [PubMed] [DOI] |
| 8. | Blake MR, Raker JM, Whelan K. Validity and reliability of the Bristol Stool Form Scale in healthy adults and patients with diarrhoea-predominant irritable bowel syndrome. Aliment Pharmacol Ther. 2016;44:693-703. [PubMed] [DOI] |
| 9. | Jowett SL, Seal CJ, Barton JR, Welfare MR. The short inflammatory bowel disease questionnaire is reliable and responsive to clinically important change in ulcerative colitis. Am J Gastroenterol. 2001;96:2921-2928. [PubMed] [DOI] |
| 10. | Rose M, Fliege H, Hildebrandt M, Körber J, Arck P, Dignass A, Klapp B. [Validation of the new German translation version of the "Short Inflammatory Bowel Disease Questionnaire" (SIBDQ)]. Z Gastroenterol. 2000;38:277-286. [PubMed] [DOI] |
| 11. | Lam MY, Lee H, Bright R, Korzenik JR, Sands BE. Validation of interactive voice response system administration of the Short Inflammatory Bowel Disease Questionnaire. Inflamm Bowel Dis. 2009;15:599-607. [PubMed] [DOI] |
| 12. | López-Vivancos J, Casellas F, Badia X, Vilaseca J, Malagelada JR. Validation of the spanish version of the inflammatory bowel disease questionnaire on ulcerative colitis and Crohn's disease. Digestion. 1999;60:274-280. [PubMed] [DOI] |
| 13. | Roseira J, Sousa HT, Marreiros A, Contente LF, Magro F. Short Inflammatory Bowel Disease Questionnaire: translation and validation to the Portuguese language. Health Qual Life Outcomes. 2021;19:59. [PubMed] [DOI] |
| 14. | Jones PS, Lee JW, Phillips LR, Zhang XE, Jaceldo KB. An adaptation of Brislin's translation model for cross-cultural research. Nurs Res. 2001;50:300-304. [PubMed] [DOI] |
| 15. | Bullinger M, Quitmann J. Quality of life as patient-reported outcomes: principles of assessment. Dialogues Clin Neurosci. 2014;16:137-145. [PubMed] [DOI] |
| 16. | Guyatt G, Mitchell A, Irvine EJ, Singer J, Williams N, Goodacre R, Tompkins C. A new measure of health status for clinical trials in inflammatory bowel disease. Gastroenterology. 1989;96:804-810. [PubMed] [DOI] |
| 17. | Irvine EJ, Zhou Q, Thompson AK. The Short Inflammatory Bowel Disease Questionnaire: a quality of life instrument for community physicians managing inflammatory bowel disease. CCRPT Investigators. Canadian Crohn's Relapse Prevention Trial. Am J Gastroenterol. 1996;91:1571-1578. [PubMed] |
| 18. | Hernaez R. Reliability and agreement studies: a guide for clinical investigators. Gut. 2015;64:1018-1027. [PubMed] [DOI] |
| 19. | Elting LS, Bodey GP. Is a picture worth a thousand medical words? A randomized trial of reporting formats for medical research data. Methods Inf Med. 1991;30:145-150. [PubMed] [DOI] |