修回日期: 2020-08-04
接受日期: 2020-09-28
在线出版日期: 2020-10-28
细菌感染是增加肝硬化患者病死率的主要原因之一, 失代偿期肝硬化比代偿期肝硬化更容易发生感染. 肝硬化中最常见和威胁生命的感染是自发性细菌性腹膜炎, 其次是尿路感染、肺炎、心内膜炎以及皮肤和软组织感染. 然而, 除了自发性细菌性腹膜炎外, 其他感染发生率较低, 认识也少.
本文报道我院1例肝硬化失代偿期自发性腹膜炎反复发作, 最终发生感染性心内膜炎(infective endocarditis, IE)的病例, 经过积极手术治愈.
肝硬化合并IE预后较差, 早期发现、并及时干预, 以提高生存率. 在肝硬化患者出现反复发作的细菌性腹膜炎, 并存在不能解释的胸闷、呼吸困难等症状, 或者原因不明的反复发热症状, 应考虑到合并IE的可能.
核心提要: 感染性心内膜炎(infective endocarditis, IE)为心脏内膜表面的微生物感染, 伴赘生物形成. 慢性肝病增加了IE的易感性, 但因为其体征和症状可能会被肝病引起的全身表现恶化所混淆, 除非强烈怀疑IE, 否则极易漏诊. 如肝硬化病人出现不明原因的长期发热或败血症、难以解释的顽固性腹水, 则需要高度警惕IE可能.
引文著录: 项艺, 王曦, 梅雪灿, 韩怡, 孔德润. 失代偿期肝硬化合并感染性心内膜炎瓣膜穿孔1例. 世界华人消化杂志 2020; 28(20): 1048-1052
Revised: August 4, 2020
Accepted: September 28, 2020
Published online: October 28, 2020
Bacterial infection is one of the main reasons for increased mortality of patients with cirrhosis, and patients with decompensated cirrhosis is more likely to be infected than those with compensated cirrhosis. The most common and life-threatening infection in cirrhosis is spontaneous bacterial peritonitis, followed by urinary tract infections, pneumonia, endocarditis, and skin and soft tissue infections. However, except spontaneous bacterial peritonitis, the incidence of other infections is low and little is known on them.
This paper reports a patient with recurrent spontaneous peritonitis in the decompensated stage of liver cirrhosis at our hospital, who eventually developed infective endocarditis (IE) that was cured by surgery.
The prognosis of cirrhosis complicated with IE is poor. Early detection and timely intervention can improve survival rate. In cirrhotic patients with recurrent bacterial peritonitis and unexplained chest tightness, dyspnea, or unexplained recurrent fever, the possibility of IE should be considered.
- Citation: Xiang Y, Wang X, Mei XC, Han Y, Kong DR. Decompensated cirrhosis with valve perforation due to infective endocarditis: A case report. Shijie Huaren Xiaohua Zazhi 2020; 28(20): 1048-1052
- URL: https://www.wjgnet.com/1009-3079/full/v28/i20/1048.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v28.i20.1048
感染性心内膜炎(infective endocarditis, IE)为心脏内膜表面的微生物感染, 伴赘生物形成. 慢性肝病增加了IE的易感性, 但因为其体征和症状可能会被肝病引起的全身表现恶化所混淆, 除非强烈怀疑IE, 否则极易漏诊[1]. 如肝硬化病人出现不明原因的长期发热或败血症、难以解释的顽固性腹水, 则需要高度警惕IE可能.
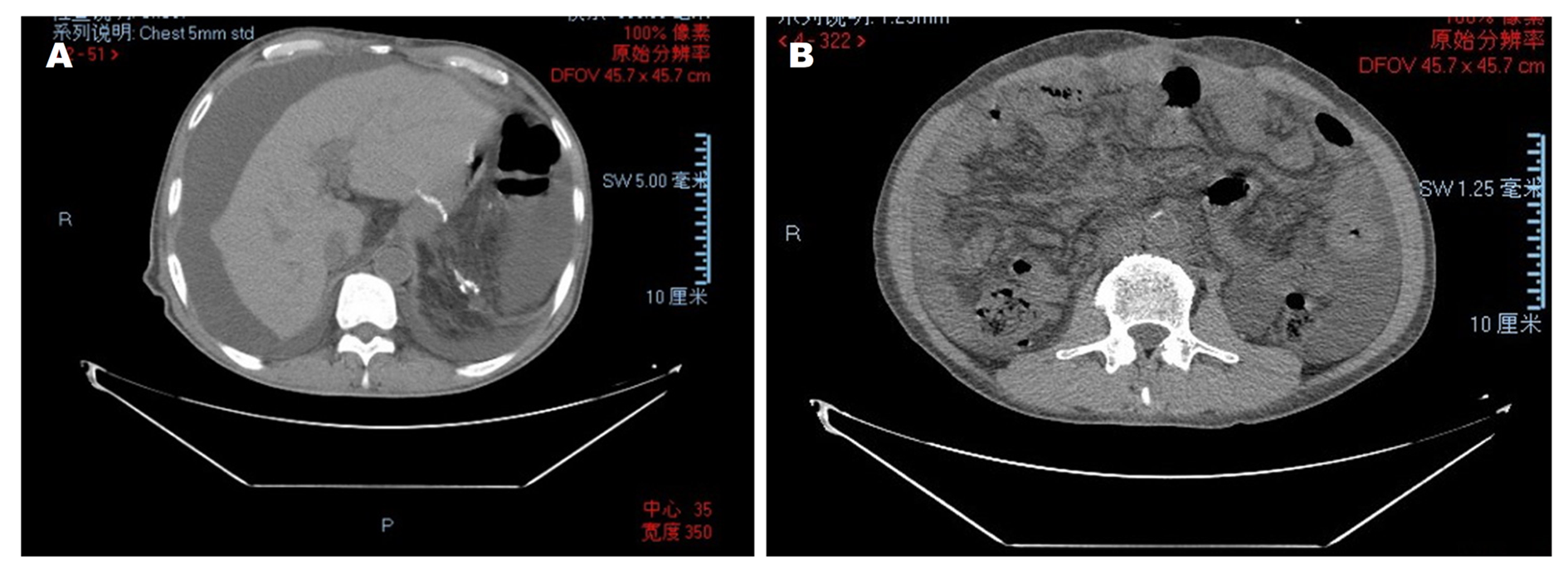
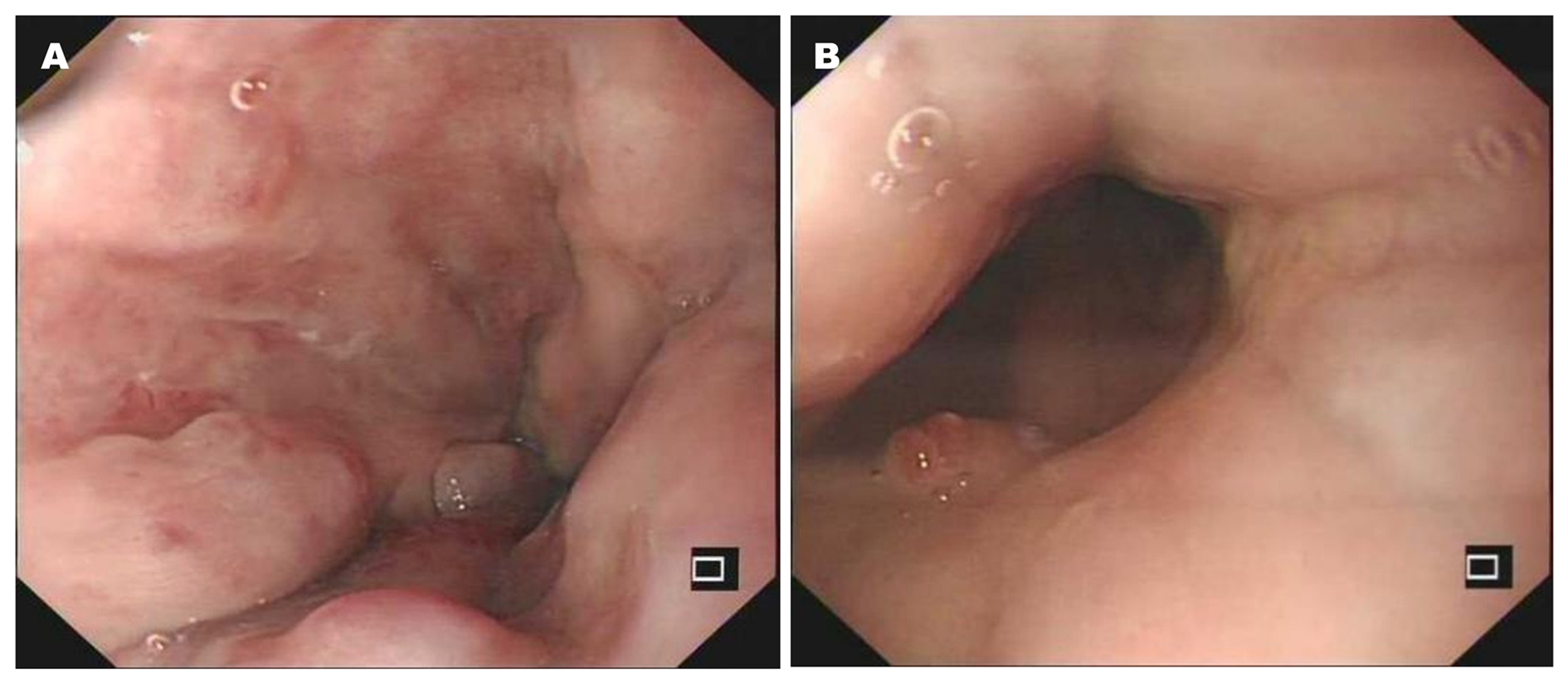
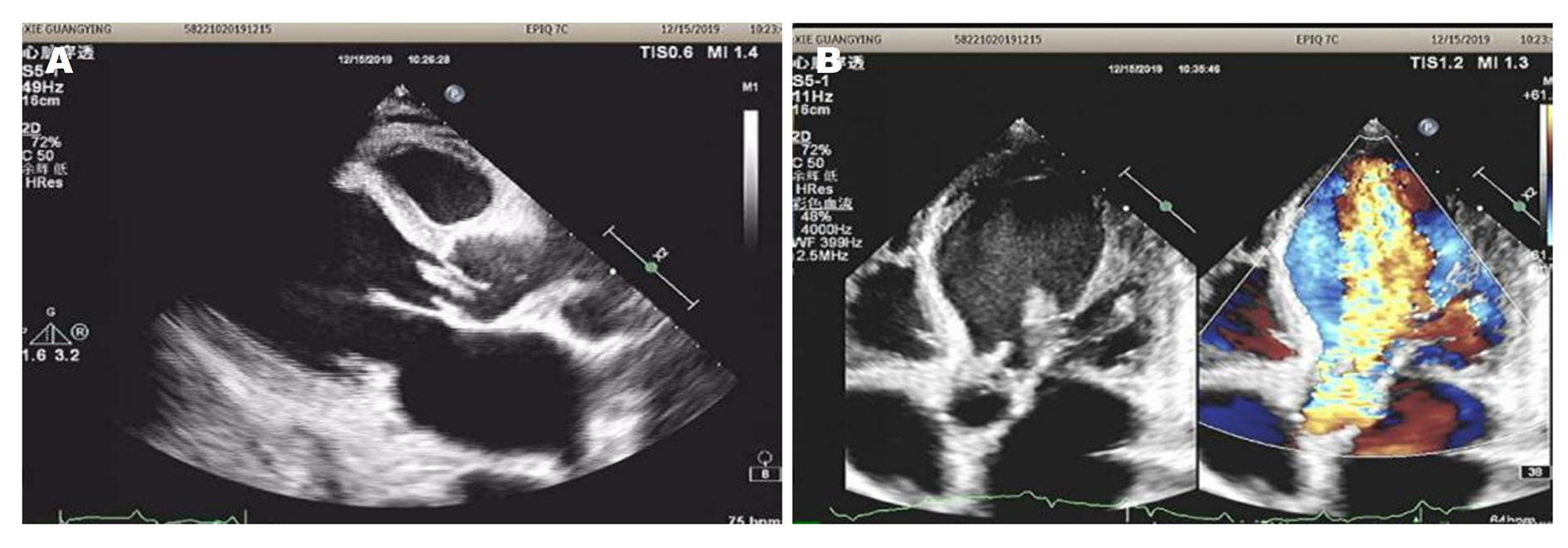
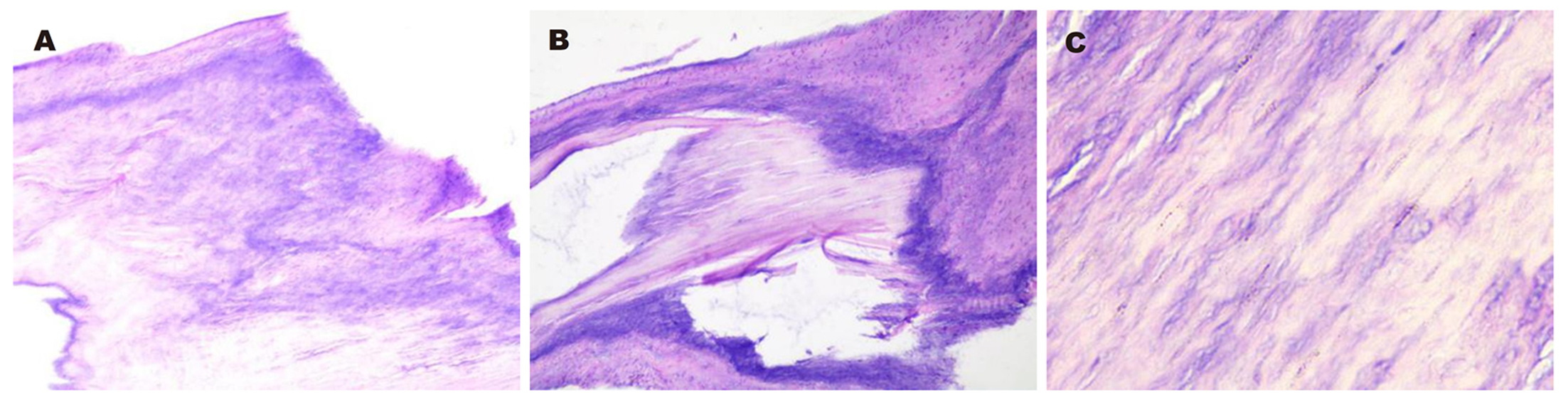
男性, 55岁. 因"腹痛腹胀伴发热1月余"于2019-12-12入院, 1月余前患者受凉后出现腹胀腹痛, 伴发热, 体温最高38.5 ℃, 就诊当地医院, 予以抗感染等对症治疗后症状好转, 后仍间断发热, 腹胀较前明显加重, 伴双下肢水肿, 予以对症治疗后症状缓解不明显. 遂就诊我科, 胸、腹、盆腔CT平扫诊断肝硬化, 腹、盆腔大量积液, 积液量较上次检查增加; 网膜浑浊, 考虑腹膜炎(图1). 胃镜提示食管残留曲张静脉, 择期内镜下治疗(图2). 按照自发性腹膜炎、肝硬化失代偿期, 予以抗感染、利尿、输蛋白等处理, 腹胀及双下肢浮肿缓解出院. 既往有酒精性肝硬化伴食管静脉曲张病史7年, 于2018-04-10因消化道出血在全麻下行"肠黏连松懈+全胃切除+食道-食管-空肠Roux-en-Y吻合+脾切除术", 既往行食管静脉曲张套扎治疗2次(具体不详); 查体: 体温36.9 ℃, 脉搏97次/分, 呼吸20次/分, 血压104/37 mmHg, 体重70 kg. 皮肤巩膜轻度黄染, 有肝掌蜘蛛痣, 心律齐, 各瓣膜区未闻及病理性杂音, 双肺呼吸音清, 两肺未闻及干湿性啰音, 腹膨隆, 质软, 无压痛反跳痛, 肝肋下未及, 脾缺如, 移动性浊音可疑, 肠鸣音不亢, 双下肢中度水肿. 辅助检查: 血常规: WBC 6.49 × 109/L, N 52.70%, Hb 68 g/L, RBC 3.19 × 1012/L, PC 281 × 109/L; BNP 2157.32 pg/mL; 肝功能: TP 60.9 g/L, A 26.3 g/L, A/G 0.76, STB 26.52 μmol/L, CB 6.66 μmol/L, UCB 19.86 μmol/L, Cr 45.0 μmol/L; cTnI 0.100 ng/mL. 止凝血(六项): PT-SEC 17.5s, PT-% 60.00%, PT-INR 1.42, APTT_SE 45.2s, AT-Ⅲ 44.0%, D-D 5.30 μg/mL, FDP 15.12 μg/mL. 胸(腹)水生化: CL 121.8 mmol/L, G 7.92 mmol/L, P 5.3 g/L, LDH 38 U/L; 腹水常规: 颜色淡黄色,透明度微浑, pH值7.0, 李凡他试验阴性, WBC 129.00 × 106/L, 单个核细胞绝对值103.0 × 106/L, 单个核细胞百分比79.80%, 多个核细胞绝对值26.0 × 106/L, 多个核细胞百分比20.2%; ECG: (1)窦性心律; (2)室性早搏(成对); (3)ST-T改变; (4)低电压. 入院辅检示心律失常、肌钙蛋白升高, 完善超声心动图: 提示主动脉瓣赘生物形成伴穿孔, 建议经食管TEE检查, 主狭(轻度)主闭伴中重度瓣口返流, 肺动脉高压(中度)少量, 轻中度二尖瓣返流, 轻度三尖瓣返流, 心包积液, 肺动脉高压中度, LA: 5.54 LVD: 7.25 EF: 59%(图3). 诊断: (1) IE; (2)主动脉瓣赘生物伴穿孔; (3)肝硬化失代偿期(酒精性); (4)门静脉高压; (5)门静脉血栓形成; (6)脾术后; (7)胃术后; (8)贫血; (9)肾错构瘤(可能); (10)肾上腺肿瘤(腺瘤可能). 当日患者诉胸闷加重, 可能与主动脉瓣膜异常有关, 主动脉瓣膜赘生物形成伴穿孔, 转入心脏外科, 于2020-01-14在全麻下行主动脉瓣机械瓣膜置换术(21#Regent双叶进口机器瓣). 术中视野可见: 主动脉瓣无冠瓣脱垂, 其上可见絮状漂浮物, 主动脉瓣整体增厚. 术前血培养阴性, 肝功能: A 32.8 g/L, A/G 1.00, STB 46.38 μmol/L, CB 12.46 μmol/L, UCB 33.92 μmol/L, AST 48 U/L, LDH 571 U/L, CKMB 52 U/L, Cr 53.7 μmol/L. 术中送病理示: (主动脉瓣)镜检示瓣膜纤维组织黏液样变性(图4). 术后1 wk后复查心脏彩超示: 主动脉瓣置换术后改变, 主动脉不增宽, 置换主动脉瓣形态活动正常, 据CW Doppler测及主动脉瓣跨瓣压差为38 mmHg, Doppler测及轻度主动脉瓣反流.
IE性赘生物、主动脉瓣狭窄伴有关闭不全、主动脉瓣赘生物伴穿孔、肺动脉高压中度、贫血、肝硬化、脾术后、胃术后(胃大切).
首先予以抗感染等对症治疗后症状好转, 后仍间断发热, 腹胀较前明显加重, 伴双下肢水肿, 予以对症治疗后症状缓解不明显.患者诉胸闷加重, 可能与主动脉瓣膜异常有关, 主动脉瓣膜赘生物形成伴穿孔, 转入心脏外科, 于2020-01-14在全麻下行主动脉瓣机械瓣膜置换术(21#Regent双叶进口机器瓣). 术中视野可见: 主动脉瓣无冠瓣脱垂, 其上可见絮状漂浮物, 主动脉瓣整体增厚.术中送病理示: (主动脉瓣)镜检示瓣膜纤维组织黏液样变性(图4).
术后常规营养支持, 于术后16 d康复出院, 术后随访3 mo无特殊.
现行的Duke标准是在1994年提出的诊断标准基础上经过多次修改的, 是诊断IE的金标准[2,3]. 据修改后的Duke标准, 本例患者心脏彩超发现主动脉瓣赘生物形成、穿孔, 伴发热, 术中可见主动脉瓣上絮状漂浮物, 主动脉瓣整体增厚, 病理回报: (主动脉瓣)镜检示瓣膜纤维组织黏液样变性, 诊断IE.
细菌感染在肝硬化病例中很常见, 病死率是普通人群的3.75倍[4]. IE越来越被认为是一种与健康相关的疾病, 通常与慢性疾病如肾功能衰竭、糖尿病或癌症有关[5]. 最近, 肝硬化已被列入IE的危险因素, 其发展与免疫系统的损伤有关, 免疫系统随着时间的推移而恶化, 并与疾病的进展有关. 与肝硬化感染相关的危险因素是严重肝功能衰竭、静脉曲张出血、低腹水蛋白水平和既往自发性细菌性腹膜炎发作[6]. 肝脏在抵御细菌感染方面起着重要作用, 而肝硬化则会增加对感染的易感性, 这里有许多不同的原因, 如黏膜屏障功能障碍, 免疫球蛋白和补体成分的相对缺乏, 以及网状内皮系统的功能障碍等[7]. 肝硬化患者容易发生细菌感染, 原因是细菌移位(门静脉高压症、肠道微生物群改变和屏障完整性)和免疫功能障碍(由于与肠道细菌的长期相互作用而精疲力竭, 免疫细胞脾脏聚集, 肝脏营养因子合成受损)引起的慢性炎症[4,8]. 炎症反应后的组织破坏会影响瓣膜和瓣膜周围组织, 使瓣膜组织变弱, 最后演变为撕裂或穿孔, 导致瓣膜返流(图3, Video 1和Video 2). 细菌清除率降低以及肠黏膜的结构和功能改变导致对细菌及其衍生产物的通透性增加. 这有利于细菌易位, 从而增加感染的易感性, 特别是自发性细菌性腹膜炎. C3和C4的缺乏, 巨噬细胞Fcγ受体介导的抗体包被细菌清除的损害, 以及单核细胞人类白细胞抗原DR表达的下调, 也可能是导致这种防御变化的原因[9]. 本例患者自发性细菌性腹膜炎的反复发作, 肝功能差, 即使感染消退后也会严重影响预后.
肝硬化感染经常产生菌血症, 可能发展为心内膜炎, 及时诊断和治疗这些菌血症可以预防不可逆的瓣膜损伤, 如瓣膜穿孔[7]. 在Hung等[5]的研究中, 在近10%的IE中观察到肝硬化病史, 而在肝硬化患者中有45%的IE是医院获得性IE, 这明显高于没有肝硬化的心内膜炎患者. 肝硬化患者发生IE的风险很高, 临床医生应重视肝硬化患者的IE, 而IE的主要病变是引起栓塞和破坏的瓣膜和(或)瓣膜周围组织的赘生物, 导致一系列瓣膜及瓣膜周围病变, 瓣膜损伤(穿孔或撕裂)和瓣膜周围(脓肿)是微生物和炎症细胞释放的蛋白水解酶破坏细胞外基质的后果[10]. 肝硬化在严重的细菌感染中可能会出现非特异性的临床症状, 使得细菌性心内膜炎早期诊断变得困难, 且肝硬化合并IE预后较差, 早期发现、并及时干预, 有利于提高患者生存率. 本文的报道以期提高临床医生对该病的认识与重视. 本例出现间断发热、腹水及双下肢浮肿加重, 按照肝硬化自发性腹膜炎治疗疗效差, 特别是心功能不全症状的出现, 提示心脏累及损害, 由此进一步抽丝剥茧诊断IE. 文献认为, 慢性肝病是IE不良预后的独立预测因素, 有肝病的IE患者的长期死亡风险增加了大约2.5倍, 进一步提该患者其预后不良[1].
心脏手术是IE治疗的重要手段之一, 特别在瓣膜关闭不全、持续性脓毒症或严重栓塞引起的顽固性心力衰竭的情况下, 应该立即手术[11]. 在普通人群中, 25%-30%的急性期患者和20%-40%的感染后期患者接受手术, 其10年存活率可达到61%[12]. 虽然肝硬化合并IE接受心脏换瓣手术可能有更高的风险性, 但Allaire等[13]发现, 肝硬化术后病死率在10%以下. 本例患者的诊治过程也是一个例证.
肝硬化合并IE预后较差, 早期发现、并及时干预, 以提高生存率. 在肝硬化患者出现反复发作的细菌性腹膜炎, 并存在不能解释的胸闷、呼吸困难等症状, 或者原因不明的反复发热症状, 应考虑到合并IE的可能.
学科分类: 胃肠病学和肝病学
手稿来源地: 安徽省
同行评议报告学术质量分类
A级 (优秀): 0
B级 (非常好): 0
C级 (良好): C
D级 (一般): D, D, D
E级 (差): E
编辑: 刘继红 制作编辑:张砚梁
| 1. | de Isla LP, Zamorano JL, Almería C, Rodrigo JL, Piedra I, Aubele A, Mataix L, Herrera D, Macaya C. Endocarditis infecciosa en pacientes con hepatopatía crónica: valoración clínica y pronóstica [Infective endocarditis in patients with chronic liver disease: clinical and prognostic assessment]. Revista espanola de cardiologia. 2003;56:794-800. [DOI] |
| 2. | Büchi A, Hoffmann M, Zbinden S, Atkinson A, Sendi P. The Duke minor criterion "predisposing heart condition" in native valve infective endocarditis - a systematic review. Swiss Med Wkly. 2018;148:w14675. [PubMed] [DOI] |
| 3. | Li JS, Sexton DJ, Mick N, Nettles R, Fowler VG, Ryan T, Bashore T, Corey GR. Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis. 2000;30:633-638. [PubMed] [DOI] |
| 4. | Allaire M, Ollivier-Hourmand I, Garioud A, Heng R, Dao T, Cadranel JD. Infectious endocarditis in the case of cirrhosis: where do we stand? Eur J Gastroenterol Hepatol. 2018;30:1406-1410. [PubMed] [DOI] |
| 5. | Hung TH, Hsieh YH, Tseng KC, Tsai CC, Tsai CC. The risk for bacterial endocarditis in cirrhotic patients: a population-based 3-year follow-up study. Int J Infect Dis. 2013;17:e391-e393. [PubMed] [DOI] |
| 6. | Bunchorntavakul C, Chamroonkul N, Chavalitdhamrong D. Bacterial infections in cirrhosis: A critical review and practical guidance. World J Hepatol. 2016;8:307-321. [PubMed] [DOI] |
| 7. | Ruiz-Morales J, Ivanova-Georgieva R, Fernández-Hidalgo N, García-Cabrera E, Miró JM, Muñoz P, Almirante B, Plata-Ciézar A, González-Ramallo V, Gálvez-Acebal J, Fariñas MC, Bravo-Ferrer JM, Goenaga-Sánchez MA, Hidalgo-Tenorio C, Goikoetxea-Agirre J, de Alarcón-González A; Spanish Collaboration on Endocarditis Group-Grupo de Apoyo al Manejo de la Endocarditis en España (GAMES); Spanish Network for Research in Infectious Diseases (REIPI). Left-sided infective endocarditis in patients with liver cirrhosis. J Infect. 2015;71:627-641. [PubMed] [DOI] |
| 8. | Jalan R, Fernandez J, Wiest R, Schnabl B, Moreau R, Angeli P, Stadlbauer V, Gustot T, Bernardi M, Canton R, Albillos A, Lammert F, Wilmer A, Mookerjee R, Vila J, Garcia-Martinez R, Wendon J, Such J, Cordoba J, Sanyal A, Garcia-Tsao G, Arroyo V, Burroughs A, Ginès P. Bacterial infections in cirrhosis: a position statement based on the EASL Special Conference 2013. J Hepatol. 2014;60:1310-1324. [PubMed] [DOI] |
| 9. | Pleguezuelo M, Benitez JM, Jurado J, Montero JL, De la Mata M. Diagnosis and management of bacterial infections in decompensated cirrhosis. World J Hepatol. 2013;5:16-25. [PubMed] [DOI] |
| 10. | Iung B. [Infective endocarditis. Epidemiology, pathophysiology and histopathology]. Presse Med. 2019;48:513-521. [PubMed] [DOI] |
| 11. | Habib G, Lancellotti P, Antunes MJ, Bongiorni MG, Casalta JP, DelZotti F, etal. 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by:European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). Eur Heart J. 2015;36:3075-3128. |
| 13. | Allaire M, Cadranel JF, Bureau C, Zerkly S, Thévenot T, Garioud A. Severe liver failure rathan cirrhosis is associated with mortality in patients with infectious endocarditis: a retrospective case control study. Eur J Gastroenterol Hepatol. 2018;. |