修回日期: 2019-01-14
接受日期: 2019-01-29
在线出版日期: 2019-03-08
胃肠道功能与失眠关系密切, 脑肠轴理论的提出为调理胃肠功能治疗失眠提供新的思路. 通过分析脑肠轴影响脑功能的神经、内分泌、免疫及肠道菌群系统, 结合针灸的调节效应及脑肠轴与胃肠道和失眠关系的传统理论依据, 探讨基于脑肠轴理论调理胃肠在针灸治疗失眠中应用的可行性.
核心提要: 脑肠轴是沟通胃肠道与脑之间的重要途径, 通过分析针灸调理胃肠, 对脑肠轴四条作用通路的影响, 探讨针灸调节脑肠轴功能治疗失眠的可行性, 力求为针灸治疗失眠提供新思路.
引文著录: 刘涛, 刘维红. 基于脑肠轴理论探讨调理胃肠在针灸治疗失眠中的应用. 世界华人消化杂志 2019; 27(5): 324-329
Revised: January 14, 2019
Accepted: January 29, 2019
Published online: March 8, 2019
Gastrointestinal function is closely related to insomnia. The brain-gut axis theory provides a new way to regulate gastrointestinal function in the treatment of insomnia. By analyzing the nervous, endocrine, immune, and intestinal flora systems of the brain-gut axis that affects brain function as well as the regulatory effect of acupuncture and the traditional theoretical basis for the relationship of the brain-gut axis with the gastrointestinal tract and insomnia, we discuss the feasibility of acupuncture treatment of insomnia by regulating the gastrointestinal tract based on the brain-gut axis theory.
- Citation: Liu T, Liu WH. Application of gastrointestinal regulation in acupuncture treatment of insomnia based on the brain-gut axis theory. Shijie Huaren Xiaohua Zazhi 2019; 27(5): 324-329
- URL: https://www.wjgnet.com/1009-3079/full/v27/i5/324.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v27.i5.324
失眠是指由于入睡困难或维持障碍导致睡眠质量不能满足机体需要, 进而产生日间瞌睡、情绪障碍甚至出现机体疾病的一种主观体验[1]. 流行病学调查显示, 全球范围内约有12.1%的人患有失眠相关症状[2], 长期的睡眠障碍不仅会造成生理上的损害(糖尿病、肥胖等), 还会引起焦虑、抑郁等心理问题[3,4]. 研究发现[5], 在失眠导致的诸多躯体和精神症状中, 胃肠道功能异常最常见, 高达36.17%. 国外研究人员发现[6]约68%的功能性消化不良患者伴有睡眠障碍, 国内学者调查发现[7]睡眠异常在功能性消化不良、上腹疼痛综合征、餐后饱胀不适综合征、肠易激综合征的发生率分别为71.1%、45.3%、61.9%、26.6%. 这些研究有力证实了胃肠道与失眠的密切关系, 近年国际专家学者提出了"脑肠轴"这一概念, 将胃肠道功能与失眠的相关性研究推至一个新的高度. 传统医学在失眠的治疗上亦重视胃肠与大脑的关系, 甚至形成了"胃不和则卧不安"这一中医理论. 现代基础研究[8]亦发现针刺足三里、中脘调理胃肠能够明显促进大鼠胃溃疡的愈合, 并延长睡眠时间. 笔者主要基于脑肠轴理论, 探讨针灸调理胃肠道功能治疗失眠的可行性, 以期为针灸治疗失眠的临床应用提供系统客观的证据支持.
《素问·逆调论》中提出"胃不和则卧不安", 是对现代"脑肠轴"理论最早的中医理论阐释. "人有逆气不得卧......是阳明之逆也......阳明者, 胃脉也, 胃者, 六腑之海, 其气亦下行. 阳明逆不得从其道, 故不得卧". 此处之"胃", 并不单指胃腑, 而是包括胃、大肠、小肠等, 如《灵枢·本输》云: "大肠属上, 小肠属下, 足阳明胃脉也. 大肠小肠, 皆属于胃, 是足阳明也". 脑为元神之府, 总司五脏之神志, 主宰人身之寤寐. 脑与胃肠从经络循行、脏腑功能、病理变化三个方面相互联系, 相互影响.
从经络循行来看, 胃经经脉"起于鼻, 交頞中......过客主人, 循发际, 至额颅", 其经别"循胫骨外廉, 上络头项, 合诸经之气"; 大肠经经脉"从缺盆上颈贯颊, 入下齿中", 其经别"上循臂, 乘肩髃, 上曲颊伤齿......入耳, 合于宗脉"; 小肠经经脉"从缺盆循颈上颊, 至目锐眦, 却入耳中......至目内眦, 斜络于颧". 由此看出, 胃经、大肠经、小肠经均与脑在经络分布上有密切联系.
从脏腑功能来看, 胃为"仓廪之官", 主受纳和腐熟水谷, 小肠为"受盛之官", 主泌别清浊, 吸收精微, 大肠为"传导之官", 主传化糟粕. 三者功能相辅相成, 气调血和, 水谷精微才能上荣于脑, 维持机体正常的生命活动, 正如《素问·六节脏象论》云: "五味入口, 藏于肠胃, 味有所藏, 以养五气, 气和而生, 津液相成, 神乃自生".
从病理变化来看, 胃、大肠、小肠功能失调常可导致脑部活动异常. 《灵枢·经脉》曰"胃足阳明之脉......是动则病......闻木声则惕然而惊, 心欲动, 独闭户塞牖而处. 甚则欲上高而歌, 弃衣而走", 《素问·厥论》云: "阳明之厥, 则癫疾欲走呼......妄见而妄言", 均说明胃肠经络受邪, 可沿经脉循行上传于脑引起神志病变. 《伤寒论》记载"阳明病, 脉迟, 食难用饱, 饱则微烦, 头眩, 必小便难"(第195条), "阳明病, 其人多汗, 以津液外出, 胃中燥, 大便必硬, 硬则谵语"(第214条), 说明胃肠腑病变, 邪气亦可上犯于脑.
由上可知, 胃肠与大脑功能活动密切相关, 脑肠轴理论是对中医"胃不和则卧不安"的现代的、科学的阐释, 亦说明传统医学的理论认识对现代临床研究及应用仍具有重要的指导意义.
脑肠轴是指通过中枢或外周神经系统将胃肠道与大脑联系起来的神经-内分泌网络, 具有双向调节的作用[9]. 大脑中枢神经系统可以通过脑肠轴将信号冲动下传来调节胃肠道功能, 而胃肠道功能异常亦会影响中枢或外周系统的相关神经活动[10], 这种通过脑肠轴联结的神经-内分泌网络与胃肠道的双向调控作用又称为脑肠互动[11]. 研究发现由胃肠道传至大脑的信息主要是通过神经、内分泌、免疫及肠道菌群四条信息传导通路进行的[12].
脑肠轴对胃肠道与神经系统的双向调控作用主要是通过肠神经系统、自主神经系统及中枢神经系统三个层次来实现的[13]. 胃肠感觉信号通过肠神经系统、迷走神经传入纤维和脊髓传入神经元传至脑内的孤束核、弓状核和丘脑中心[12], 其中迷走神经是将胃肠信息传至大脑的主要通路[14]. 在神经传导通路中, γ-氨基丁酸(γ-aminobutyric acid, GABA)和谷氨酸(Glu)是参与冲动传导的重要神经递质, 对睡眠节律的调节起着决定性作用[15]. GABA作为抑制性神经递质, 有研究证实在原发性失眠患者脑内含量明显低于正常人[16]. Glu可以通过兴奋Orexin神经元以及胆碱能神经元来提高大脑皮层的觉醒状态[17]. 人类肠道细菌亦可以产生GABA、Glu[18], 通过血脑屏障、迷走神经影响中枢神经系统内的GABA、Glu[19], 进而影响睡眠节律.
脑肠肽(brain-gut peptide, BGP)是一种具有激素与神经递质双重功能的小分子多肽, 既存在于中枢神经系统, 也存在于胃肠道内, 对脑肠系统活动起着重要的调控作用. 胃泌素(gastrin, GAS)、生长抑素(somatostatin, SS)和褪黑素(melatonin, MT)均属于BGP, 对胃肠黏膜有保护作用, 同时对睡眠也产生重要影响[20]. GAS主要是由胃肠道细胞分泌的多肽类激素, 同时也存在于中枢神经系统的延髓迷走神经背核[21]. SS广泛存在于下丘脑和胃肠道内, 是重要的睡眠因子之一, 其含量减少会导致促觉醒机制发生障碍, 延长睡眠时间[22]. 此外, SS可以作用于结肠环形肌细胞来抑制胃酸和胃肠激素的分泌, 从而减缓胃肠运动, 延长胃排空时间. MT是参与调控睡眠-觉醒周期的重要物质[23], 可以抑制调节昼夜节律等人体生命活动的下丘脑-垂体-肾上腺轴(hypothalamic-pituitary-adrena, HPA), 降低应激时血液皮质醇浓度, 进而改善睡眠[24]. MT还可以抑制胃酸分泌, 保护胃黏膜, 促进胃肠道运动.
胃肠道是人体最大的免疫器官, 约70%的淋巴组织附于肠道黏膜, 起到黏膜免疫、保护机体的作用[25]. 肿瘤坏死因子(tumor necrosis factor, TNF-α)是由活化的巨噬细胞和单核细胞生成的能够引起溃疡形成的烈性介质, 在胃肠黏膜的损伤中发挥重要作用. 白介素-25(interleukin-25, IL-25)可以诱导细胞因子及聚集嗜酸性粒细胞, 促进趋化因子的活性, 破坏细胞因子间的动态平衡, 与应激性胃溃疡的发生密切相关[26]. 基础研究证实当大鼠被剥夺快速动眼睡眠时, 血浆中的TNF-α、IL-25等免疫因子含量显著增加[27]. 睡眠剥夺、过度进食等实验干预措施均可引起动物非快速眼动睡眠时间延长, 同时伴有TNF-α水平的升高.
肠道菌群是脑肠轴的核心通路, 可以直接分泌小分子物质通过血脑屏障作用于大脑或间接通过参与神经、内分泌、免疫的调节对大脑功能产生影响[28]. 肠道菌群可生成多种细胞因子与趋化因子如IL-1, 通过血脑屏障进入脑血管与脑细胞中的IL-1受体结合产生前列腺素, 进而调节脑的功能和活动[29]. 此外, 肠道菌群可产生并调控神经递质如GABA[30]、5-羟色胺(Serotonin, 5-HT)、多巴胺[31]等, 通过肠道菌群-肠道神经系统-迷走神经-脑[32]这一信息传导通路影响大脑功能. 肠道菌群还可刺激肠道内分泌细胞分泌激素直接作用于脑, 如调节肠嗜铬细胞分泌5-HT, 进而调节大脑的情绪活动[33].
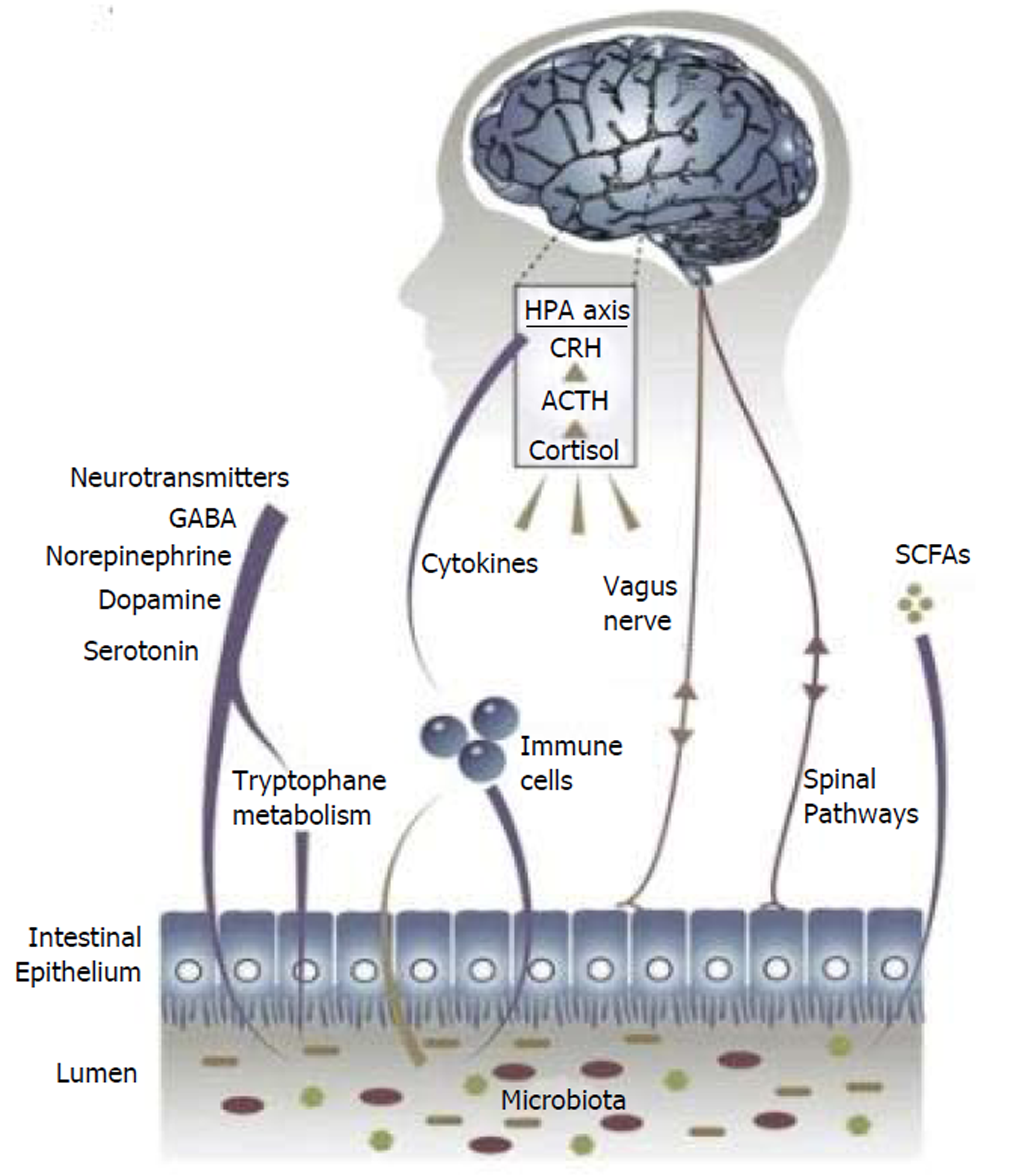
如图1所示, 脑肠轴在胃肠道与大脑的交互作用中起着重要的调节作用, 主要通过神经、内分泌、免疫、肠道菌群等通路发挥其功能, 其中肠道菌群是核心通路, 直接或间接参与其他三条通路的调节活动. 胃肠道与脑的互动关系, 正是通过脑肠轴借助于神经-内分泌-免疫网络系统以及肠道菌群来实现的[34].
针灸治疗失眠具有明显优势, 但基于脑肠轴理论通过调理胃肠来实现治愈失眠的相关研究较少. 笔者建议从以下四个方面入手.
2.5.1 针灸调节神经通路: 临床研究发现[35]针刺足三里可明显提高下丘脑内GABA含量, 改善机体免疫能力, 因而起到安神镇静的作用. 动物实验亦证实[36]电针能同时调节失眠大鼠脑内的GABA、Glu含量及GABAA受体活性, 使神经抑制作用占优势地位, 延长睡眠时间, 改善睡眠质量.
2.5.2 针灸调节内分泌通路: 针刺足三里、中脘能够明显改善应激性溃疡大鼠的失眠状态, 其机制可能是针灸效应通过神经内分泌网络同时作用于中枢和外周, 降低GAS含量, 提高SS和MT水平, 调节脑肠轴以恢复神经内分泌系统的动态平衡, 在修复溃疡的同时, 产生一定的抗应激作用, 从而降低应激时血液皮质醇浓度, 改善睡眠状态[37]. 针刺效应还可以刺激大脑相关核团中的神经元产生神经冲动, 刺激BGP中GAS的释放, 进而介导针灸对胃肠道功能的调节作用[38,39]. 研究证实失眠伴有胃肠道疾病患者的SS水平明显高于正常[40-42], 而针刺足三里、太冲或中脘穴可显著降低SS含量[43,44]. 此外, 针刺足三里、中脘可以明显升高大鼠血清和下丘脑中的MT水平, 降低胃溃疡损伤指数, 减少胃黏膜充血, 并缓解大鼠焦虑状态, 改善睡眠质量[37].
2.5.3 针灸调节免疫通路: 大量研究[45,46]证实针灸对胃肠道的运动和分泌具有良好的调节作用, 例如增加血清分泌型免疫球蛋白的含量, 增强胃肠道局部免疫, 有效保护胃肠黏膜的完整性和屏障作用[47]. 针刺足三里、中脘等腧穴不仅可以降低TNF-α和IL-25在血清和脑组织中的含量, 缩小溃疡面积和降低胃黏膜损伤指数, 并且能够缩短睡眠诱导时间, 进而提高溃疡率的愈合并改善睡眠状态[48].
2.5.4 针灸调节肠道菌群通路: 现代研究发现[49], 针灸足三里、关元穴可以促进溃疡性结肠炎小鼠肠道菌群多样性的恢复, 并证实针灸调节脑肠轴可能是缓解溃疡性结肠炎小鼠焦虑样行为的重要机制.
综上所述, 脑肠轴是沟通胃肠道与脑之间联系的桥梁, 是实现临床调理胃肠治疗失眠的基础. 针灸调理胃肠, 进而调节脑肠轴功能, 为针灸治疗失眠提供了新思路. 《灵枢·海论》云: "夫十二经脉者, 内属于脏腑, 外络于肢节", 经络系统将人体的五脏六腑、气血阴阳联系贯通, 生理上相互依存, 病理上相互影响. 胃经、肠经分别络属于体内相应脏腑, 其循行、病候又与脑密切相关, 间接证实了胃肠道疾病与脑之间的联系, 为脑肠相关理论提供了可靠依据, 为探讨针灸调理胃肠治疗失眠提供了可行性理论依据. 目前, 有关针灸调理胃肠治疗失眠的作用机制尚未完全明确, 脑肠轴在其中发挥的作用有待深入研究. 因此, 笔者认为在研究胃肠道与脑之间的重要关系的过程中, 应遵循传统的"step by step"循证医学研究模式, 先进行文献研究、观察性研究和小型随机对照试验研究(randomized controlled trail, RCT), 进而在大量可靠的研究证据基础上再进行高质量的大样本多中心RCT研究, 以期为临床针灸治疗失眠提供最佳的优化方案.
学科分类: 胃肠病学和肝病学
手稿来源地: 天津市
同行评议报告分类
A级 (优秀): 0
B级 (非常好): B
C级 (良好): C, C
D级 (一般): D
E级 (差): 0
编辑: 崔丽君 电编:张砚梁
| 1. | Bastien CH. Insomnia: Neurophysiological and neuropsychological approaches. Neuropsychol Rev. 2011;21:22-40. [PubMed] [DOI] |
| 2. | Soldatos CR, Allaert FA, Ohta T, Dikeos DG. How do individuals sleep around the world? Results from a single-day survey in ten countries. Sleep Med. 2005;6:5-13. [PubMed] [DOI] |
| 3. | Rains JL, Jain SK. Oxidative stress, insulin signaling, and diabetes. Free Radic Biol Med. 2011;50:567-575. [PubMed] [DOI] |
| 4. | Janszky I. Insomnia is associated with risk of future cardiovascular events irrespective of comorbidities. Evid Based Med. 2016;21:107. [PubMed] [DOI] |
| 6. | Fass R, Fullerton S, Tung S, Mayer EA. Sleep disturbances in clinic patients with functional bowel disorders. Am J Gastroenterol. 2000;95:1195-2000. [PubMed] [DOI] |
| 11. | Mertz HR. Overview of functional gastrointestinal disorders: dysfunction of the brain-gut axis. Gastroenterol Clin North Am. 2003;32:463-476. [PubMed] [DOI] |
| 12. | Holzer P, Farzi A. Neuropeptides and the microbiota-gut-brain axis. Adv Exp Med Biol. 2014;817:195-219. [PubMed] [DOI] |
| 14. | Forsythe P, Bienenstock J, Kunze WA. Vagal pathways for microbiome-brain-gut axis communication. Adv Exp Med Biol. 2014;817:115-133. [PubMed] [DOI] |
| 15. | Julio-Pieper M, O'Connor RM, Dinan TG, Cryan JF. Regulation of the brain-gut axis by group III metabotropic glutamate receptors. Eur J Pharmacol. 2013;698:19-30. [PubMed] [DOI] |
| 16. | Plante DT, Jensen JE, Schoerning L, Winkelman JW. Reduced γ-aminobutyric acid in occipital and anterior cingulate cortices in primary insomnia: a link to major depressive disorder. Neuropsychopharmacology. 2012;37:1548-1557. [PubMed] [DOI] |
| 17. | Schwartz MD, Kilduff TS. The Neurobiology of Sleep and Wakefulness. Psychiatr Clin North Am. 2015;38:615-644. [PubMed] [DOI] |
| 18. | Dinan TG, Stilling RM, Stanton C, Cryan JF. Collective unconscious: how gut microbes shape human behavior. J Psychiatr Res. 2015;63:1-9. [PubMed] [DOI] |
| 19. | Boonstra E, de Kleijn R, Colzato LS, Alkemade A, Forstmann BU, Nieuwenhuis S. Neurotransmitters as food supplements: the effects of GABA on brain and behavior. Front Psychol. 2015;6:1520. [PubMed] [DOI] |
| 24. | Zhong LY, Yang ZH, Li XR, Wang H, Li L. Protective effects of melatonin against the damages of neuroendocrine-immune induced by lipopolysaccharide in diabetic rats. Exp Clin Endocrinol Diabetes. 2009;117:463-469. [PubMed] [DOI] |
| 25. | Joscelyn J, Kasper LH. Digesting the emerging role for the gut microbiome in central nervous system demyelination. Mult Scler. 2014;20:1553-1559. [PubMed] [DOI] |
| 26. | 张 永梅, 徐 青. IL-25的研究进展. 细胞与分子免疫学杂志. 2008;24:1034-1036. [DOI] |
| 27. | Yehuda S, Sredni B, Carasso RL, Kenigsbuch-Sredni D. REM sleep deprivation in rats results in inflammation and interleukin-17 elevation. J Interferon Cytokine Res. 2009;29:393-398. [PubMed] [DOI] |
| 29. | Wang Y, Kasper LH. The role of microbiome in central nervous system disorders. Brain Behav Immun. 2014;38:1-12. [PubMed] [DOI] |
| 30. | Bravo JA, Forsythe P, Chew MV, Escaravage E, Savignac HM, Dinan TG, Bienenstock J, Cryan JF. Ingestion of Lactobacillus strain regulates emotional behavior and central GABA receptor expression in a mouse via the vagus nerve. Proc Natl Acad Sci USA. 2011;108:16050-16055. [PubMed] [DOI] |
| 31. | Matsumoto M, Kibe R, Ooga T, Aiba Y, Kurihara S, Sawaki E, Koga Y, Benno Y. Impact of intestinal microbiota on intestinal luminal metabolome. Sci Rep. 2012;2:233. [PubMed] [DOI] |
| 32. | Powley TL, Wang XY, Fox EA, Phillips RJ, Liu LW, Huizinga JD. Ultrastructural evidence for communication between intramuscular vagal mechanoreceptors and interstitial cells of Cajal in the rat fundus. Neurogastroenterol Motil. 2008;20:69-79. [PubMed] [DOI] |
| 33. | Gershon MD, Tack J. The serotonin signaling system: from basic understanding to drug development for functional GI disorders. Gastroenterology. 2007;132:397-414. [PubMed] [DOI] |
| 34. | Dinan TG, Cryan JF. The Microbiome-Gut-Brain Axis in Health and Disease. Gastroenterol Clin North Am. 2017;46:77-89. [PubMed] [DOI] |
| 37. | 马 佳佳, 闫 亚南, 关 翰宇, 付 晨露, 李 婧婷, 薛 婷, 王 旒靖, 邵 一轩, 熊 敏, 葛 东宇, 董 瑞娟, 马 惠芳. 针刺对应激性胃溃疡模型大鼠血清和下丘脑中GAS、SS和MT表达的影响. 环球中医药. 2018;11:486-491. [DOI] |
| 39. | 虞 意华, 金 肖青, 俞 迈红, 龚 仕金, 刘 秉宇, 李 莉. 针灸对老年严重脓毒症患者胃肠功能及胃肠激素影响的临床研究. 中华中医药学刊. 2015;33:1953-1956. [DOI] |
| 40. | 张 超, 王 景杰, 卢 王, 唐 华, 陈 慧群, 王 庆莉, 刘 莉, 黄 裕新. 失眠伴便秘型肠易激综合征患者睡眠特征及胃动素、生长抑素的临床观察. 胃肠病学和肝病学杂志. 2009;18:735-737. [DOI] |
| 41. | 张 海燕, 鲁 格兰, 朱 冬梅, 张 津, 林 思远, 耿 文飞. 厌食和睡眠障碍儿童血清胃动素、生长抑素、Ghrelin水平变化及临床意义. 临床儿科杂志. 2010;28:659-661. [DOI] |
| 43. | 刘 美荣, 肖 瑞飞, 彭 芝配, 左 和宁, 朱 克, 王 思明. 针刺"足三里"、"太冲"穴对腹泻型肠易激综合征大鼠胃肠激素的影响. 针刺研究. 2012;37:363-368. [DOI] |
| 45. | Jin Y, Zhao Q, Zhou K, Jing X, Yu X, Fang J, Liu Z, Zhu B. Acupuncture for Functional Dyspepsia: A Single Blinded, Randomized, Controlled Trial. Evid Based Complement Alternat Med. 2015;2015:904926. [PubMed] [DOI] |
| 46. | Da N, Wang X, Liu H, Xu X, Jin X, Chen C, Zhu D, Bai J, Zhang X, Zou Y, Hu G, Zhang J. The Effectiveness of Electroacupuncture for Functional Constipation: A Randomized, Controlled, Clinical Trial. Evid Based Complement Alternat Med. 2015;2015:670963. [PubMed] [DOI] |
| 47. | Li G, Li S, Wang B, An L. The effect of electroacupuncture on postoperative immunoinflammatory response in patients undergoing supratentorial craniotomy. Exp Ther Med. 2013;6:699-702. [PubMed] [DOI] |