修回日期: 2015-09-30
接受日期: 2015-10-13
在线出版日期: 2015-11-18
食管颗粒细胞瘤在临床上较少见, 大部分为孤立性结节且多无特异性临床症状, 多在胃镜检查时被发现. 对于食管颗粒细胞瘤仅依据组织学诊断不能确定肿瘤的良恶性. 随着内镜技术的广泛应用, 肿瘤的发现率及治疗方式在不断改变. 本文报道经内镜下切除食管颗粒细胞瘤2例, 并查阅相关文献进行复习.
核心提示: 食管颗粒细胞瘤多无特异性临床症状, 经常被误诊, 术前确诊率极低, 即使术后病理确诊为良性病变, 肿瘤仍存在复发或转移的可能, 临床医师应对确诊病例做好密切的随访.
引文著录: 刘婉, 朱海航, 徐永居, 卜平. 内镜下切除食管良性颗粒细胞瘤2例. 世界华人消化杂志 2015; 23(32): 5250-5254
Revised: September 30, 2015
Accepted: October 13, 2015
Published online: November 18, 2015
Granular cell tumors of the esophagus are rare and mostly isolated lesions, many of which have no clinical symptoms and are usually accidentally discovered during annual endoscopic examination. Benign and malignant GCTs have similar histopathology, and there are no clear histological diagnostic criteria for the differentiation of benign and malignant tumors. With the wide application of endoscopic techniques, the detection rate of esophageal GCTs and treatment strategy have greatly changed. Here we report two cases of benign GCTs of the esophagus and reviewed the literature.
- Citation: Liu W, Zhu HH, Xu YJ, Bo P. Endoscopic resection of benign esophageal granular cell tumors: Report of two cases. Shijie Huaren Xiaohua Zazhi 2015; 23(32): 5250-5254
- URL: https://www.wjgnet.com/1009-3079/full/v23/i32/5250.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i32.5250
颗粒细胞瘤(granular cell tumors, GCTs)是一种非常少见的软组织肿瘤, 可发生于全身各个部位, 约有8%的GCTs发生于消化系, 近1/3的消化系颗粒细胞瘤发生在食管, 以食管下段为主要发生部位. 现总结本院近期内镜下切除食管GCTs 2例, 结合国内外文献进行学习, 就食管GCTs的诊疗做一讨论.
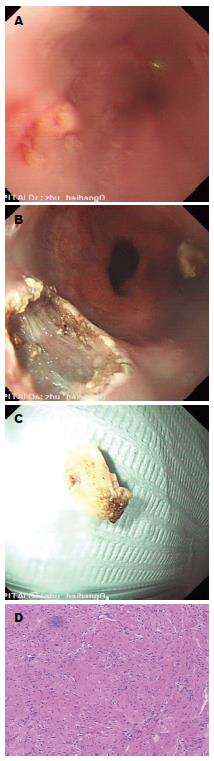
病例1, 刘某, 男, 44岁, 因胸骨后不适于2015-03-09行电子胃镜检查, 见距门齿40 cm处食管下段近前壁隆起性病变, 大小约0.7 cm×0.7 cm, 黏膜光滑淡黄(图1A), 移动性好, 门诊拟"食管间质瘤"收入院. 入院后完善相关检查, 无手术禁忌, 行内镜黏膜下剥离术(endoscopic submucosal dissection, ESD), 常规麻醉后, Q260J内镜进镜至贲门食管侧可见食管前壁隆起性病变, 约0.6 cm×0.7 cm大小, 沿病变基部数点注射1:10000肾上腺素生理盐水靛胭脂液总量约10 mL, 病变处明显抬举隆起, 应用hook刀沿标记之外0.5 cm左右切开黏膜, 找见肿块黏膜下剥离, 最后用圈套器摘除(图1B), 以肽夹夹闭. 切除完整标本送病理检查, 病灶标本约0.6 cm×0.8 cm大小(图1C)送检. 标本HE染色: 组织被覆鳞状上皮, 其下可见呈巢状、器官样排列分布的细胞, 细胞浆丰富、红染(图1D). 免疫组织化学结果: S100(+), NSE(+), CD56(+), Syn(-), CgA(-), Desmin(-), SMA(-), H-caldesmon(-).
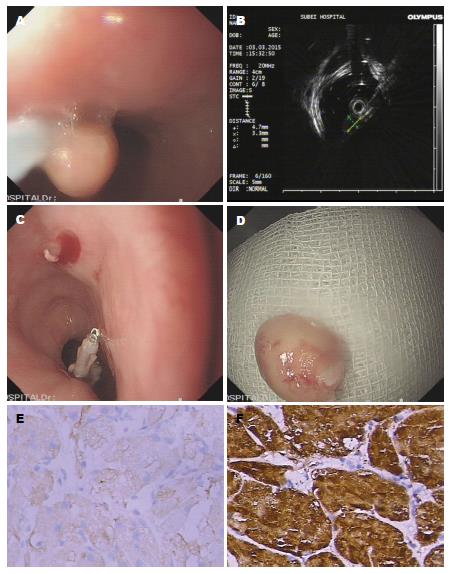
病例2, 昌某某, 女, 56岁, 因时有反酸、嗳气不适于2015-03-03行胃镜检查见距门齿约30 cm处食管可见一小隆起, 约0.7 cm×0.8 cm, 表面光滑(图2A). 超声胃镜提示低回声团块, 回声均匀, 向腔内突出, 边界清楚, 起源于黏膜肌层(图2B). 无手术禁忌, 行内镜黏膜切除术(endoscopic mucosal resection, EMR), 常规麻醉后见食管距门齿30 cm处一0.6 cm×0.7 cm半球状隆起, 表面光滑, 中央无溃疡形成, 无黏膜桥形成, 再将圈套器置于病灶基底部后, 收紧圈套钢丝, 通以高频电流, 强度约为45-50 W, 分次凝切, 切下后创面无渗血(图2C), 予钛夹3枚夹闭创面; 息肉以五爪钳收住后随镜取出(图2D)后送检. HE染色: 组织被覆鳞状上皮, 上皮下见增生的组织样细胞, 胞浆丰富、颗粒状. 免疫组织化学: 组织样细胞S-100(+)(图2E)、NSE(+)(图2F); SMA、Desmin、CD117、Dog-1均(-).
因形态学上发现肿瘤组织与神经有密切联系, 免疫组织化学及电镜也证实瘤细胞来源于雪旺细胞. 但极少数颗粒细胞瘤胞浆内可见肌丝、密体及微饮泡, 免疫组织化学染色瘤细胞Desmin、Actin阳性, 其亦可来源于平滑肌细胞; 本组2例结合病理及免疫组织化学符合雪旺细胞学说来源.
食管GCTs好发于40岁左右的女性, 多无特异性症状, 仅在胃镜检查时被发现, 真正表现为进食梗阻、出血而就诊的多因肿瘤较大, 且占GCTs的级少数; 食管GCTs常表现为上腹痛、反酸、嗳气、胸闷等不典型症状, 即使将食管GCT完整的摘除, 患者不适仍可能存在, 可能其内脏的感觉系统受到永久的损害, 本组两例患者1例表现为胸骨后不适, 1例表现为反酸、嗳气, 均不具有特异性.
食管GCTs内镜下多为直径在0.5-2.0 cm黏膜下隆起性结节, 多为单发, 亦可见多发结节, 多发GCTs常见于国外报道; 表面光滑, 少数病例出现黏膜过度增生、粗糙或伴糜烂、黏膜桥形成. 黏膜呈淡黄色, 有学者认为淡黄色颗粒结节是GCTs的特征性表现, 但也有黏膜灰白色、正常食管黏膜颜色的颗粒细胞瘤被确诊[1], 本组两例患者术前内镜观察1例表现为淡黄色, 另1例黏膜色泽于食管黏膜颜色相同, GCTs外观并不具有特征性变现, 术前误诊率较高, 这有待于大量文献的总结报道.
超声内镜(endoscopic ultrasound, EUS)主要为低回声、均质回声结节, 也有回声不均质的, 但是内部回声并不影响肿瘤的病理特征[2];起源于黏膜层及黏膜肌层的GCTs肿瘤边界尚清楚, 起源于黏膜下层的肿瘤境界不清, 浸润至肌层, 边界是否清楚与肿瘤的生长方式及起源有关, 有部分瘤体超声内镜下显示的起源层次与实际切除时不相符合, 部分瘤体在超声内镜下的数量与实际不符[1,2]. 根据EUS灰度值的不同, 可将其与其他肿瘤进行鉴别[3], EUS-FNA能获得组织学标本, 但有潜在的瘤体破裂和转移可能, 本组第2例患者超声胃镜提示食管隆起病灶处为低回声、均质回声团块, 边界清楚, 起源于黏膜肌层, 行EMR术即能完整切除瘤体, 而第1例患者术前未能行EUS检查, 对于手术存在一定的困难, 我们认为术前常规行EUS检查, 可以明确肿瘤的起源, 更有助于手术方式的选择.
组织学镜下细胞排列成巢状或条索状, 巢间见少量纤维组织分隔, 胞体较大, 胞质丰富, 充满嗜伊红颗粒; 核小、居中、大小一致, 常深染, 少数核增大、异型, 但这并不代表恶性; PSA染色阳性, 并耐淀粉酶消化; 间质稀少, 有时细胞巢间或肿瘤组织周围可见灶状淋巴细胞浸润. 本文两例与以往文献报道有相同的内镜下表现.
电镜下异染色质散在于核内, 核仁明显, 位于核的中央; 胞浆内充满大量由单层膜包绕形成的自噬泡, 亦可见小泡融合的多泡体; 瘤细胞巢周或细胞间见基板围绕, 少数颗粒细胞瘤的瘤细胞可见角小体或轴索样结构, 亦有超微结构显示细胞质内可见angulated小体, 少数瘤细胞内见肌丝、密体及微饮泡.
GCTs阳性表达一些神经特异性标记, 如S-100、NSE、MBP、vimentin等, 而一些肌源性、组织细胞源性及上皮源性等免疫组织化学为阴性, 其中S-100蛋白和NSE是神经嵴来源肿瘤两种较为可靠的标记, 特别是S-100在瘤细胞胞浆和胞核均表达; 本组两例患者均S-100(+)、NSE(+), 与既往文献报道相一致.
GCTs诊疗的难点是鉴别良性颗粒细胞瘤(benign granular celltumor, BGCT)与恶性颗粒细胞瘤(malignant granuIar celltumor, MGCT), MGCTs极少见, 发生率约为2%; 消化系内MGCTs更是极其罕见. 恶性颗粒细胞瘤直径多>2 cm, 瘤体>5 cm是一个潜在恶性的临床指标, 也有肿瘤直径小于1cm后经病理证实为恶性的报道. 病理学被认为是鉴别肿瘤良恶性的金标准, 但BGCTs和MGCTs在病理组织学上表现相似, 目前尚无统一的鉴别良恶性GCTs的标准. 应用最广泛的是Fanburg-Smith等提出恶性者5个判断指标: 瘤细胞变梭形, 空泡状核并有大核仁, 核分裂象(≥2个/10 HPF), 肿瘤性坏死, 高核质比和多形性; 符合3个或3个以上的被视为组织学恶性; 但有少数病例按照上述标准不能诊断为恶性, 而临床已出现复发或转移. 因此有学者提出将核分裂象的诊断指标改为≥5个/50 HPF, 以便更确切地反映肿瘤的核分裂活动. 有报道P53的表达、Ki-67阳性细胞数的多少与肿瘤的恶性潜能相关, 良性及无复发GCTs的Ki-67增殖指数较低[1]. 在MGCTs中, 大肿块、快速增殖、肿瘤性坏死和临近组织的侵犯或转移及早期局部复发、局部引流区域出现肿大淋巴结时被认为比病理学更有力的证据; 而多发性病例似乎并不具有更高的恶性风险. 通过EUS确认肿瘤有无浸润肌层及其以外的各层, 对于鉴别良恶性有重要的意义, 但对于早期无浸润表现的MGCTs, 仍不能识别.
BGCTs有恶变可能,目前大多数学者主张进行积极的治疗. 术前EUS可帮助明确病变起源和性质, 并根据起源及病变大小选择合适的治疗方法. 对直径<2 cm、位于黏膜层的食管GCTs首选内镜治疗, 大部分随访未发现肿瘤的复发及转移. 对多发的或侵及肌层的,此类GCTs多为恶性, 既往多采取手术治疗, 近年来通过内镜黏膜下隧道肿瘤切除术、内镜全层切除术[4,5]可达到与外科完整切除肿瘤的效果; 同时双镜联合即内镜与胸腔镜联合手术微创治疗食管GCTs也越来越受到人们的重视, 内镜下治疗食管GCTs显得越来越重要. 但对于发生转移的MGCT, 外科手术仍是主要的治疗手段. MGCT术后局部复发率高达50%, 转移率68%, 最常见的转移部位为区域淋巴结和肺, 平均生存期为2.5年, 化疗和放疗并不能改善MGCT的临床病程. 对于具有潜在恶性的GCT, 应定期随访, 以尽早发现其局部复发和转移, 提高患者的生存质量.
颗粒细胞瘤(granular cell tumors, GCTs)是一种非常少见的软组织肿瘤, 消化系统的GCTs更为罕见, 多发生在食管的下段, 外科手术治疗创伤较大, 本文对发现的2例食管下段GCT采用内镜下治疗, 效果显著.
姜春萌, 教授, 大连医科大学附属第二医院消化科
病理被认为是诊断肿瘤良恶性的金标准, 但是少数GCT病例依照病理不能诊断为恶性, 而临床却出现复发或转移. 张明等认为P53的表达、Ki-67阳性细胞数的多少与肿瘤的恶性潜能相关, 良性及无复发GCTs的Ki-67增殖指数较低, 这有助于鉴别肿瘤的良恶性.
本文的创新处在于系统的总结了食管颗粒细胞瘤的诊治现状, 有助于临床医师全面的了解食管颗粒细胞瘤的诊断与治疗.
对食管颗粒细胞瘤良恶性的鉴别, 在依据病理诊断的基础上, 可完善P53、Ki-67免疫化学化学、超声内镜(endoscopic ultrasound, EUS)检查, 全面的评估病情, 指导患者随访, 预防肿瘤的恶变.
EUS灰度值: EUS图像是一种二维灰阶图像, 图像中有丰富的灰度信息, 黑-灰-白-连续变化的灰度值量化为256个灰度级, 灰度值的范围为0-255, 表示亮度从深到浅, 对应图像中的颜色为从黑到白.
本文报道了2例少见疾病-食管颗粒细胞瘤, 并且进行了详细的讨论和文献回顾, 具有良好的临床示范作用.
编辑: 郭鹏 电编: 闫晋利
| 3. | Seo SW, Hong SJ, Han JP, Choi MH, Song JY, Kim HK, Lee TH, Ko BM, Cho JY, Lee JS. Accuracy of a scoring system for the differential diagnosis of common gastric subepithelial tumors based on endoscopic ultrasonography. J Dig Dis. 2013;14:647-653. [PubMed] |
| 5. | Xu MD, Cai MY, Zhou PH, Qin XY, Zhong YS, Chen WF, Hu JW, Zhang YQ, Ma LL, Qin WZ. Submucosal tunneling endoscopic resection: a new technique for treating upper GI submucosal tumors originating from the muscularis propria layer (with videos). Gastrointest Endosc. 2012;75:195-199. [PubMed] [DOI] |