修回日期: 2015-07-13
接受日期: 2015-07-24
在线出版日期: 2015-09-28
腹膜假性黏液瘤在国内外报道中罕见, 早期症状、体征无明显特异性, 后期呈慢性消耗表现, 与恶性肿瘤腹腔内转移表现相似, 但一般情况大多较好, 病程进展缓慢, 且无特异性检查手段, 易被漏诊、误诊, 绝大多数患者是在手术中或手术后行病理检查才得以确诊, 这就要求临床医师提高警惕, 并为患者做出正确的诊治.
核心提示: 腹膜假性黏液瘤罕见, 早期无明显特异性症状及体征, 后期与恶性肿瘤腹腔内转移表现相似, 且无特异性检查手段, 易被漏诊、误诊, 绝大多数患者是在手术中或手术后行病理检查才得以确诊, 要求临床医师提高警惕, 做出正确的诊治.
引文著录: 张海玲, 陶丽华, 包文霞, 严苏. 腹膜假性黏液瘤1例及文献复习. 世界华人消化杂志 2015; 23(27): 4452-4456
Revised: July 13, 2015
Accepted: July 24, 2015
Published online: September 28, 2015
Pseudomyxoma peritonei (PMP) is a rare clinical entity. Early PMP has no specific symptoms and signs. The clinical manifestations of PMP are very similar to those of intra-abdominal carcinomatosis, such as chronic wasting. The general condition of most PMP patients is good. PMP develops slowly and is often misdiagnosed clinically due to the lack of specific examinations. The vast majority of patients were diagnosed by pathological examination in or after surgery. Clinicians should raise their awareness of this disease to avoid misdiagnosis.
- Citation: Zhang HL, Tao LH, Bao WX, Yan S. Pseudomyxoma peritonei: A case report and literature review. Shijie Huaren Xiaohua Zazhi 2015; 23(27): 4452-4456
- URL: https://www.wjgnet.com/1009-3079/full/v23/i27/4452.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i27.4452
腹膜假性黏液瘤(pseudomyxoma peritonei, PMP)是以腹腔大量弥漫性胶冻样黏液形成伴腹膜、网膜或脏器表面黏液种植为特征的临床少见肿瘤性疾病, 胶冻样物质为假性黏液蛋白, 又称PMP综合征、假性黏液瘤性腹水或假性腹水. PMP发病率低且缺乏特异性临床表现和检查手段, 因此, 首诊误诊率高. 现将诊治的1例病例报道如下.
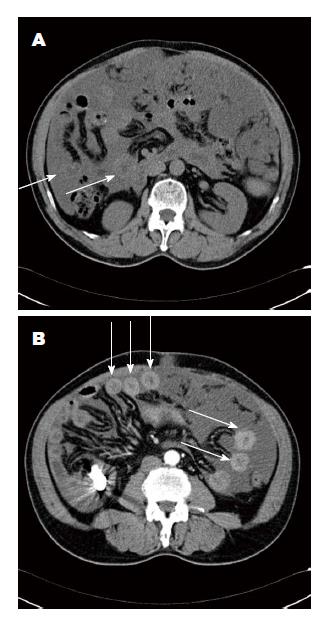
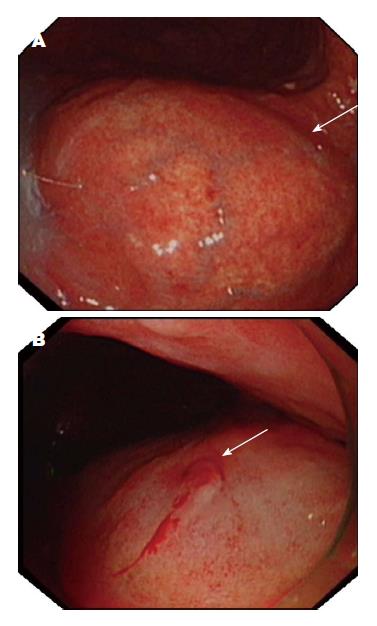
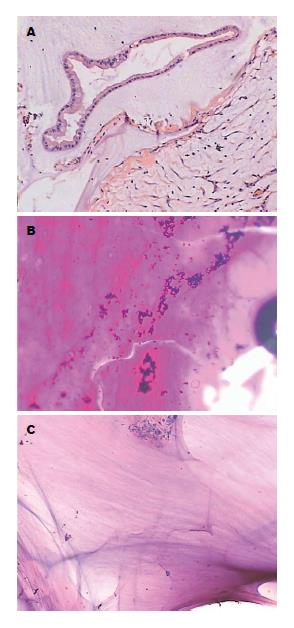
患者男性, 61岁, 因"左下腹胀痛4 d"于2014-10-14入住苏州大学附属第一医院消化内科. 患者入院前4 d无明显诱因下感左下腹胀痛, 无恶心呕吐, 无腹泻, 无发热寒战, 纳差, 睡眠可, 二便正常, 近4 mo体质量下降约7.5 kg, 遂至苏州大学附属第一医院消化内科门诊就诊(2014-10-09), 门诊胸腹盆计算机断层扫描(computed tomography, CT)检查(图1)示腹腔见多发囊性低密度影, 边界清晰, 向周围呈缝样生长, 突向纵膈及脐内, 范围广泛, 增强后囊内未见明显强化, 囊壁稍强化; 另腹腔内见多量液性低密度影, 其余未见明显异常. 影像诊断: 腹腔多发囊性病变, 腹腔积液, 考虑腹腔恶性黏液瘤可能性大, 结核不除外, 建议进一步检查, 结合临床. 门诊胃镜(2014-10-10)检查(图2A)示: 贲门下胃底处见一巨大黏膜下隆起, 表面光滑; 胃窦前壁可见一小息肉, 大小约0.5 cm×0.5 cm, 表面发红. 镜下诊断: (1)贲门胃底隆起性病变(性质待定); (2)胃窦息肉. 建议行超声内镜进一步检查. 为进一步诊治收住苏州大学附属第一医院消化内科. 入院查体: 体温: 36.3 ℃, 脉搏: 72次/分, 呼吸: 18次/分, 血压: 131/78 mmHg, 心肺未见明显异常. 全腹略膨隆, 未见腹壁静脉曲张及肠形蠕动波, 左下腹可触及一大小约15 cm×10 cm的肿块, 质硬、囊实性感、表面光滑、活动度较差、边界清楚、无触压痛, 叩之实音, 移动性浊音阴性. 辅助检查: 血常规(2014-10-15): 白细胞(white blood cell, WBC)4.9×109/L, 血小板(platelet, PLT)52×109/L(↓), 红细胞(red blood cell, RBC)4.47×1012/L, 血红蛋白(hemoglobin, Hb)134 g/L; 肿瘤全套(2014-10-15): 癌胚抗原(carcino-embryonic antigen, CEA): 54.91 ng/mL(↑), 糖类抗原(cancer antigen, CA)724: 21.19 U/mL(↑), CA125: 38.1 U/mL(↑), CA199: 311.93 U/mL(↑); 乙型肝炎两对半(2014-10-15): 乙型肝炎表面抗体23.085 mIU/mL(↑), 乙型肝炎核心抗体1.388 PEIU/L(↑), 乙型肝炎E抗体0.333 PEIU/mL(↑); 尿常规、粪常规、血凝常规、结核抗原IgG抗体、肝肾功能、心电图无明显异常. 腹部B超示: 腹腔积液, 腹腔内混合回声, 考虑囊腺瘤可能. 2014-10-16行超声胃镜示: 贲门下胃底处见一大小约8 cm×6 cm左右的低回声团块, 内见条索状高回声, 用19 G针行细针抽吸(fine needle aspiration, FNA)(图2B), 共穿刺3针, 脱落细胞送检, 病理(C201409970)示: (贲门下胃底穿刺涂片)见黏液, 未见明显异型细胞. 后转入外科并于2014-10-29在全麻下行剖腹探查术, 术中见腹腔内多发囊性肿块, 腹腔黏连, 经周围组织纱布保护后剥离黏连组织肿块完整取出, 剖开肿块可见大量黄色胶冻样液体. 尽可能清除腹腔黏液物质并彻底清洗腹腔后关腹, 与患者及家属沟通建议同时行腹腔内化疗, 患者及家属考虑后拒绝化疗, 欲自行中药治疗. 术后予充分引流, 患者好转后出院. 术后病理(1432224)结果(图3)示: 腹膜假性黏液瘤. 术后1 mo复查肿瘤四项: CEA: 52.38ng/mL(↑), CA724: 30.34U/mL(↑), CA125: 30.1 U/mL, CA199: 417.86 U/mL(↑). 随访半年, 以肿瘤指标CEA、CA199、CA125、CA724和腹盆腔CT作为监测方法, 肿瘤指标1 mo检查1次, CT每2 mo检查1次, 均未见明显进展. 现患者一般情况可, 继续随访中.
PMP是由Rokitansky等于1842年首次报道, 1884年Werth首次提出PMP这一命名[1]. PMP在临床上是一种罕见的疾病, 年发病率约为1/100万或10000例剖腹手术中有2例[2], 女性发病率较高, 男女之比1:(3-4), 多见于中年及老年患者. PMP的组织来源存在诸多争论, 但阑尾黏液肿瘤是其原发病灶已被广泛接受[3]. PMP是一种低度恶性病变疾病, 进展较缓慢, 很少发生淋巴结转移或血转移, 局限于腹腔, 最终导致腹腔弥漫性组织黏连、挤压腹腔脏器形成各种并发症而死亡[4]. PMP的生物学行为较广泛, 可从良性到恶性. 根据Ronnett等[5]报道PMP分为3型: (1)即偏向于良性病变的腹膜腺黏液病(disseminated peritoneal adenomucinosis, DPAM); (2)偏恶性的腹膜黏液癌病(peritoneal mucinous carcinomatosis, PMCA); (3)兼有DPAM和PMCA特征的混合型(peritoneal mucinous carcinomatosis with intermediate or discordant features, PMCA-I/D). DPAM的5年和10年生存率分别为75%和68%, PMCA和PMCA-I/D的5年和10年生存率分别为50%和21%.
PMP临床症状缺乏特异性、病程较长, 主要表现为腹痛、腹胀、消瘦等, 查体腹部可触及包块, 易致误诊, 常由腹部影像学检查或外科手术偶然发现, 通常其在出现症状后5-35年后才被明确诊断. 肿瘤指标如CEA、CA199等在多数PMP患者中可见升高, 可起到辅助诊断作用[6]. 影像学检查具有一定的特征, 可降低术前误诊率, 有助于了解病变范围、指导手术和监测复发. 腹部B超是常用的检查方法, 典型者表现为不动性同声的腹水, 伴因邻近腹膜种植的外在压迫所致的肝、脾缘的"扇形"显像, 这种回声特征与低回声区相间. 目前CT被广泛用于明确诊断和了解病变范围, 表现为: (1)腹盆腔内囊实性密度肿块, 密度均匀, CT值近似水或略高, 边缘强化; 多囊, 囊壁大多厚度一致; (2)胶冻样腹水, 大量密度不均匀腹水, 脏器表面形成贝壳样压迹, 肠管受压向腹腔中心移位; (3)腹膜浸润, 大网膜和肠系膜增厚、密度增高、结节状浸润、网格样改变, 严重时大网膜呈一大块软组织密度影位于肠管前方, 形成较为特征的网膜样改变[7]. B超引导下腹水穿刺细胞学检查可确诊, 但阳性率不高, 由于胶冻样黏液不易抽出并且抽出物中仅含有少量的细胞和大量的黏液素, 缺乏特异的细胞学表现. 腹腔镜或剖腹探查及术后活组织检查可明确诊断. 本例患者首发症状为腹部胀痛伴有消瘦遂就医, 查体左下腹触及一包块, 由腹部CT检查发现, 肿瘤指标CEA、CA199、CA125、CA724均升高, 超声胃镜下行FNA, 病理见黏液未见异型细胞, 最终行剖腹探查术才明确诊断. 这要求临床医师提高警惕, 作出正确诊断, 及早干预治疗.
目前手术治疗是最主要的手段之一, 术中尽可能切除所有病灶, 阑尾应切除送病检, 必要时可重复手术. 无论是病灶局限、弥漫播散还是肿瘤复发的PMP患者, 都主张减瘤术和肿瘤细胞减灭术(cytoreductive surgery, CRS). Sugarbaker[8]提倡根治手术和辅助治疗, 需切除受累的腹膜和脏器, 根治切除合并辅助性腹腔内和全身化疗可取得较好的效果. CRS可清除宏观肿瘤, 围手术期腹腔内化疗(preoperative intraperitoneal chemotherapy, PIC)可清除微观残余病变, 两者联合可使10年生存率从20%-30%上升至70%以上[9,10]. 在法国, 有适应症的条件下, CRS联合腹膜内化疗是PMP治疗的金标准. PMP预后与组织学的类型、手术、放化疗的效果等有密切关系. Elias等[11]研究指出腹膜肿瘤种植的范围和完整的CRS比病理组织学分级对患者的预后影响更大. 因此, 我们可根据患者的病变范围及CRS的手术效果来粗略的评估患者的预后. 此外, 肿瘤指标可预测CRS后生存时间以及复发的风险. Taflampas等[12]调查指出CEA、CA125、CA199 3项均正常与3项均升高相比, 完整的CRS的几率会从97%降至50%. 因此肿瘤指标与腹盆腔CT同样可评估手术效果及预后, PMP患者的5年存活率为53%-75%, 死因主要为肠道功能异常、肠梗阻和感染. 早发现、早治疗对本病有利, 手术治疗很有必要. 本例患者四十余年前因阑尾炎已行阑尾切除, 本次手术行CRS术, 与患者及家属沟通建议同时行腹腔内化疗, 患者及家属考虑后拒绝化疗, 欲自行中药治疗, 手术后患者恢复可, 以肿瘤指标CEA、CA199、CA125、CA724和腹盆腔CT监测是否复发,术后随访半年, 未见PMP复发, 现患者一般情况可, 继续随访中.
腹膜假性黏液瘤非常少见, 无特异性症状、体征, 且无特异性检查手段, 临床上易误漏诊. 本病属低度恶性疾病, 局限于腹腔, 易复发, 可形成各种并发症缩短患者生存期, 如何给予患者更好的治疗并延长患者生存期一直困扰着广大医务工作者.
迟雁, 副教授, 北京大学第一医院
腹膜假性黏液瘤通常在症状出现后5-35年才被明确诊断, 易延误治疗, 致患者生存期明显缩短, 目前的研究表明术后给予化疗可延长患者生存期, 故细胞减灭术联合腹腔化疗或全身化疗可能成为最佳治疗方法.
腹膜假性黏液瘤在临床上罕见, 国内外公开报道病例少, 临床医师缺乏经验. 早发现、早治疗可提高患者生存率, 目前对于本病的治疗国内外文献报道均主张手术联合局部或全身化疗, 复发时可重复手术.
本文报道了1例罕见的腹膜假性黏液瘤并复习了国内外文献讨论其起源、诊断、治疗、预后等方面, 得出本病最终确诊靠术中或术后病理检查的结果, 并且还探讨了手术方式及监测方法.
术中应在组织纱布的保护下尽可能完整取出包块, 避免其破裂造成腹腔种植, 尽可能切除所有病灶和阑尾并送病检, 这将为临床医师判断其来源和作出正确的诊治提供重要的依据.
减瘤术: 指对手术无法完全切除的原发性肿瘤行大部分切除, 目的为了减轻肿瘤的负荷, 以便能用其他的治疗手段(化疗、放疗、生物治疗等)来控制手术后残存的瘤灶; 细胞减灭术: 完整切除肿瘤, 清除肉眼可见转移灶; 围手术期腹腔内化疗: 手术前后一定时期内腹腔内注入化疗药物以清除微观残余病灶.
本例报道对腹膜假性黏液瘤这类临床少见病的诊治有一定的临床指导意义, 能提高对该病的诊疗经验.
编辑: 郭鹏 电编: 都珍珍
| 1. | Werth R. Pseudomyxoma peritonei. Archives of Gynecology and Obstetrics. 1884;24:100-118. |
| 2. | Bevan KE, Mohamed F, Moran BJ. Pseudomyxoma peritonei. World J Gastrointest Oncol. 2010;2:44-50. [PubMed] [DOI] |
| 3. | Smeenk RM, van Velthuysen ML, Verwaal VJ, Zoetmulder FA. Appendiceal neoplasms and pseudomyxoma peritonei: a population based study. Eur J Surg Oncol. 2008;34:196-201. [PubMed] |
| 4. | Touloumis Z, Galyfos G, Kavouras N, Menis M, Lavant L. Aggressive pseudomyxoma peritonei: a case report with an unusual clinical presentation. Case Rep Oncol Med. 2013;2013:926963. [PubMed] [DOI] |
| 5. | Ronnett BM, Yan H, Kurman RJ, Shmookler BM, Wu L, Sugarbaker PH. Patients with pseudomyxoma peritonei associated with disseminated peritoneal adenomucinosis have a significantly more favorable prognosis than patients with peritoneal mucinous carcinomatosis. Cancer. 2001;92:85-91. [PubMed] |
| 6. | Alexander-Sefre F, Chandrakumaran K, Banerjee S, Sexton R, Thomas JM, Moran B. Elevated tumour markers prior to complete tumour removal in patients with pseudomyxoma peritonei predict early recurrence. Colorectal Dis. 2005;7:382-386. [PubMed] |
| 7. | 谭 国强, 吴 标, 兰 勇, 张 朝桐, 龙 晚生, 胡 茂清, 梁 启堂, 蔡 小琴. 腹膜假性粘液瘤的CT诊断与鉴别诊断. 中国CT和MRI杂志. 2007;5:37-39. |
| 8. | Sugarbaker PH. Pseudomyxoma peritonei. Cancer Treat Res. 1996;81:105-119. [PubMed] |
| 9. | Youssef H, Newman C, Chandrakumaran K, Mohamed F, Cecil TD, Moran BJ. Operative findings, early complications, and long-term survival in 456 patients with pseudomyxoma peritonei syndrome of appendiceal origin. Dis Colon Rectum. 2011;54:293-299. [PubMed] [DOI] |
| 10. | Yan TD, Bijelic L, Sugarbaker PH. Critical analysis of treatment failure after complete cytoreductive surgery and perioperative intraperitoneal chemotherapy for peritoneal dissemination from appendiceal mucinous neoplasms. Ann Surg Oncol. 2007;14:2289-2299. [PubMed] |
| 11. | Elias D, Gilly F, Quenet F, Bereder JM, Sidéris L, Mansvelt B, Lorimier G, Glehen O. Pseudomyxoma peritonei: a French multicentric study of 301 patients treated with cytoreductive surgery and intraperitoneal chemotherapy. Eur J Surg Oncol. 2010;36:456-462. [PubMed] [DOI] |
| 12. | Taflampas P, Dayal S, Chandrakumaran K, Mohamed F, Cecil TD, Moran BJ. Pre-operative tumour marker status predicts recurrence and survival after complete cytoreduction and hyperthermic intraperitoneal chemotherapy for appendiceal Pseudomyxoma Peritonei: Analysis of 519 patients. Eur J Surg Oncol. 2014;40:515-520. [PubMed] [DOI] |