修回日期: 2015-03-27
接受日期: 2015-04-02
在线出版日期: 2015-06-18
胰腺假性囊肿(pancreatic pseudocyst, PPC)是胰腺的一种常见囊性疾病. 超声内镜引导下经胃、十二指肠穿刺置管引流术是治疗PPC的有效、安全、首选方法, 现以被临床广泛认可并应用. 然而, 同时发生于胰头及胰体尾部者甚少, 通过对本病例的探讨, 以提高对超声内镜引导下经胃、十二指肠穿刺置管引流术治疗PPC的认识.
核心提示: 应用此方法治疗胰腺假性囊肿(pancreatic pseudocyst)时应具备预见其可能的并发症以及处理并发症的能力, 术前结合有效的影像学检查, 制定合理的个体化治疗方案, 术后加强护理, 可降低该治疗方法并发症的发生率. 此外, 该方法的适应症为一相对标准而非绝对标准, 应该具体情况具体分析.
引文著录: 卢庆威, 秦鸣放, 孙向宇. 超声内镜下经胃、十二指肠穿刺内引流治疗胰腺假性囊肿1例. 世界华人消化杂志 2015; 23(17): 2839-2842
Revised: March 27, 2015
Accepted: April 2, 2015
Published online: June 18, 2015
Endoscopic ultrasound (EUS) guided transgastric or transpapillary pancreatic pseudocyst (PPC) drainage is safe and effective in treating PPC and can therefore be a preferred therapeutic approach, which is now replacing other conventional therapies. However, pseudocysts existing simultaneously in the head and the body and tail of the pancreas are uncommon, and this paper presents such a case to improve the awareness of the approach in treating PPC.
- Citation: Lu QW, Qin MF, Sun XY. A case of endoscopic ultrasound guided transgastric and transpapillary pancreatic pseudocyst drainage. Shijie Huaren Xiaohua Zazhi 2015; 23(17): 2839-2842
- URL: https://www.wjgnet.com/1009-3079/full/v23/i17/2839.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i17.2839
胰腺假性囊肿(pancreatic pseudocyst, PPC)是指在胰腺内或周围异常存留的体液经纤维组织包裹形成的囊腔, 囊壁由腹膜、网膜或炎性纤维结缔组织构成, 腔内含有胰液或丰富胰酶, 囊壁内无胰腺上皮细胞衬, PPC约占胰腺囊性疾病的75%-80%[1,2], 常多继发于慢性胰腺炎而急性胰腺炎较为罕见[3]. 外科手术曾经是治疗PPC的经典方法, 但是存在创伤大、并发症多的缺点. 过去常采用外科手术及经皮引流术, 近年来随着内镜技术的发展, 超声内镜(endoscopic ultrasonography, EUS)具有创伤小、并发症少、死亡率低等优点, 正逐步取代传统引流术及外科手术, 成为治疗PPC的主要方法[4]. PPC多发生在胰体、尾部, 80%为单发, 罕有与胰管相通[5], 胰头、胰体尾部同时发生假性囊肿的病例报道甚少, 针对天津市南开医院微创外科中心收治的1例胰头-胰体尾假性囊肿患者的临床表现、治疗方法、治疗后并发症及预后等方面进行报告, 并结合相关文献进行讨论, 以提高对EUS引导下经消化系穿刺置管引流术治疗PPC的认识.
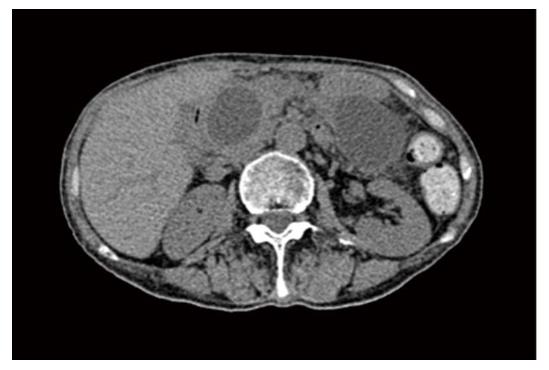
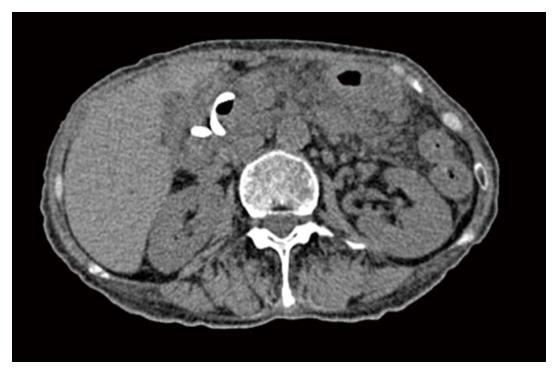
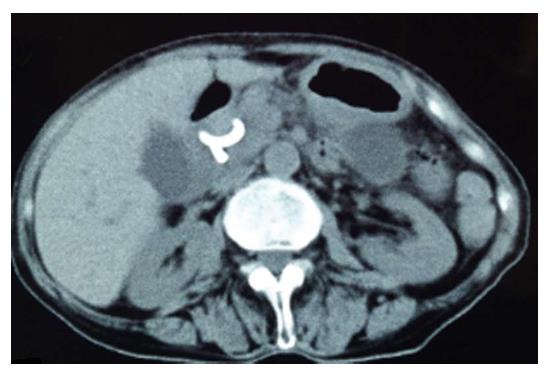
杨某, 女, 70岁, 患者主因间断上腹疼痛不适2年, 伴进食后腹胀4 mo余入院. 2年前无明显诱因间断出现上腹疼痛不适, 于外院诊断为慢性胰腺炎, 期间给予内科输液治疗. 2 mo前出现进食后腹胀不适, 为求诊治到天津市南开医院微创外科中心就诊, 查上腹部计算机断层扫描(computed tomography, CT)提示: 胰腺炎伴周围渗出、相邻胃及十二指肠壁较厚; 胰头、胰尾区低密度灶, 边界较清晰, 假性囊肿形成首考, 大者约4.8 cm×4.1 cm; 胰管轻度扩张(图1). 尿淀粉酶: 37 U/L. 予以抗炎、抑酸、补充肠外营养等治疗, 同时经讨论决定行EUS引导下胰体尾-胃, 胰头-十二指肠内引流术. 大致方法如下: 进入胃内后, 利用EUS的胃镜视野观察胃壁情况, 选择囊肿在胃内压迹隆起最明显且无大血管处. 采用针刀电凝、电切胃壁, 液体流出后放入导丝, 用弓形刀适当扩大胃壁切口, 沿导丝放入10F"双猪尾形"塑料支架(Cook公司, 美国), 继续进镜至十二指肠下段, 行胰管选择性插管造影, 见囊腔与主胰管相通, 直接将导丝经主胰管插至囊腔内, 沿导丝再置入10F"双猪尾形"塑料支架. 前后分别见囊液经支架流入胃及十二指肠内, 再通过X线显示支架引流位置, 最后EUS显示支架等号样位于囊肿内, 退镜前,观察胃肠壁局部无出血. 术后穿刺引流液送检化验, 淀粉酶: 10929 U/L. 经上述治疗患者症状较前明显好转, 术后第6天因胰体尾-胃引流支架意外脱落致患者突发呕血、便血, 急诊行数字减影血管造影(digital subtraction angiography, DSA)+介入栓塞术, 止血成功. 复查上腹部CT示: PPC内引流术后, 胰头周围结构欠清晰, 胰腺尾部低密度灶(图2). 经补充悬浮红细胞、抗感染等治疗后患者出院. 70 d后入院复查上腹部CT示: PPC内引流术后, 胰头周围结构欠清晰, 胰腺尾囊肿较前增大, 壁变薄, 边界清晰(图3). 由于经胃-胰体尾部引流支架脱落, 引流时间短, 未达到治疗目的, 患者复发胰体尾部假性囊肿. 因患者无明显临床症状, 拔出引流支架后予以抗炎补液治疗3 d后出院.
对于PPC的治疗有多种方法, 如常规内科治疗: 禁食, 抑制胰酶、抑制胃酸、改善胰腺微循环、纠正水电解质紊乱、早期应用广谱抗菌素、营养支持等. 此外还有外科手术, 如B超引导下经皮穿刺置管外引流术, 胃囊肿吻合内引流术, 囊肿空肠Roux-en-Y内引流术, EUS引导下经胃肠壁囊肿置管引流术等, 后者因具有创伤小、并发症少、死亡率低、疗效佳等优点, 正逐步取代外科手术及传统经皮穿刺引流术, EUS引导下经胃肠壁囊肿置管引流术是近20年发展起来治疗PPC最新技术, 目前此方法已成为PPC的重要临床治疗手段并获得良好疗效[6]. 值得注意的是, 采用该方法时要明确其适应证: 囊肿直径>6 cm, 囊肿已形成6 wk以上[7], 囊肿壁与胃肠道壁之间的最短距离<1 cm, 即使囊肿未突入胃腔造成压迫, 也可行EUS引导下经胃肠壁囊肿置管引流术. 对于巨大PPC应适当延长治疗时机, 待囊壁无残余坏死胰腺组织附着时进行内引流效果更好[8]. 个人认为, 内科治疗效果不明显, 即便囊肿直径<6 cm反复发作的单个囊肿, 根据具体情况也可采用此方法, 例如本病例. 多发性囊肿, 合并慢性胰腺炎及胰管狭窄, 假性囊肿有较厚的分隔, 出现出血、感染、破裂、压迫等并发症, 邻近血管有动脉瘤形成则为引流禁忌[9]. 在拔除支架的时机选择上, 应在囊肿完全消失以及腹痛、腹胀症状完全缓解后拔除支架, 大部分国内文献主张支架存留时间应超过3 mo[10]. 在随访期间, 如果出现腹痛、发热等症状, 或CT显示囊肿减小不明显甚至增大, 应明确是否发生支架堵塞或移位, 及时更换支架. 当然该方法的并发症也难以避免, 如穿孔、出血、感染, 了解并预见可能的并发症以及具有处理并发症的能力显得尤为重要, 上述病例可能因体位改变引起引流支架脱落而致出血, 所以术后应尽量减少活动. 此外, 可在术前行磁共振胰胆管造影(magnetic resonance cholangiopancreatography, MRCP)或内窥镜逆行胰胆管造影术(endoscopic retrograde ccholangiopancreatography, ERCP)检查, 以了解PPC的部位、形态、大小及与主胰管的关系, 有利于决定恰当的治疗方案, 同时也降低了该治疗方法并发症的发生率.
总之, 临床上在治疗PPC中应根据具体情况, 采取相应措施, 制定合理的个体化治疗方案. EUS引导下经胃肠壁囊肿置管引流术是治疗PPC的首选方法[11], 具有微创、痛苦小、围手术期短及并发症少等优点, 值得应用和推广.
胰腺假性囊肿(pancreatic pseudocyst, PPC)是继发于急、慢性胰腺炎或胰腺损伤后的常见并发症, 当出现各种并发症时应及时处理. 超声内镜(endoscopic ultrasonography, EUS)引导下胃肠壁穿刺置管引流术正逐步取代传统引流术及外科手术, 成为PPC治疗的主要方法.
任粉玉, 教授, 延边大学附属医院消化内科
与传统手术相比, 借助EUS, 可以准确确定囊壁与胃肠壁的距离, 在其间选择最佳穿刺点, 也可以清楚显示穿刺及置管的全过程, 避免意外发生.
临床上, 胰头、胰体尾部同时发生假性囊肿的病例报道甚少, 结合此病例提高了对EUS引导下胃肠壁穿刺置管引流术治疗PPC的认识.
EUS引导下经胃肠壁穿刺置管引流术治疗PPC具有创伤小, 安全性高和疗效确切等优点, 相信随着EUS技术的不断发展, 此方法将成为治疗PPC的首选方法, 具有广阔的应用前景.
本文结合国内外报道对EUS下经胃、十二指肠穿刺内引流治疗PPC进行了详尽的分析, 具有良好的临床指导意义.
编辑: 韦元涛 电编:都珍珍
| 2. | Palanivelu C, Senthilkumar K, Madhankumar MV, Rajan PS, Shetty AR, Jani K, Rangarajan M, Maheshkumaar GS. Management of pancreatic pseudocyst in the era of laparoscopic surgery--experience from a tertiary centre. Surg Endosc. 2007;21:2262-2267. [PubMed] [DOI] |
| 3. | Talukdar R, Sundaram M, Nageshwar Reddy D. Endoscopic vs surgical drainage of pancreatic pseudocysts. Gastroenterology. 2014;146:319-320. [PubMed] [DOI] |
| 4. | 秦 鸣放, 王 震宇, 王 庆, 勾 承月, 李 宁. 超声内镜引导下穿刺引流治疗胰腺假性囊肿. 中华腔镜外科杂志(电子版). 2012;5:33-36. |
| 6. | Inui K, Yoshino J, Okushima K, Miyoshi H, Nakamura Y, Watanabe S, Takashima T, Nakazawa S, Hattori T. EUS-guided one-step drainage of pancreatic pseudocysts: experience in 3 patients. Gastrointest Endosc. 2001;54:87-89. [PubMed] [DOI] |
| 7. | Habashi S, Draganov PV. Pancreatic pseudocyst. World J Gastroenterol. 2009;15:38-47. [PubMed] [DOI] |