修回日期: 2015-03-09
接受日期: 2015-03-18
在线出版日期: 2015-05-08
胃癌转移一般以腹腔脏器为主, 较少侵及中枢神经系统. 本文报道了胃癌术后脑膜转移1例, 探讨了胃癌术后脑膜转移的临床特点、治疗方法及预后转归, 并重点探讨胃癌术后脑膜转移的诊断要点.
核心提示: 胃癌术后脑膜转移常以神经系统症状起病, 临床表现缺乏特异性, 因此较易被误诊, 增强磁共振和脑脊液检查是检出该病较为敏感和有效的方法. 及早明确诊断, 进行积极处理是该病的治疗基础.
引文著录: 乔振国, 陈易, 汪立峰, 祝建红. 胃癌术后脑膜转移1例. 世界华人消化杂志 2015; 23(13): 2189-2192
Revised: March 9, 2015
Accepted: March 18, 2015
Published online: May 8, 2015
The metastasis of gastric cancer is mainly seen in abdominal organs, and the central nervous system is infrequently affected. This paper reports a case of meningeal metastasis of gastric cancer after surgery. We also discuss the clinical characteristics, treatment methods and prognosis of meningeal metastasis of gastric cancer after surgery.
- Citation: Qiao ZG, Chen Y, Wang LF, Zhu JH. Meningeal metastasis of gastric cancer after surgery: A case report. Shijie Huaren Xiaohua Zazhi 2015; 23(13): 2189-2192
- URL: https://www.wjgnet.com/1009-3079/full/v23/i13/2189.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v23.i13.2189
胃癌转移途径以淋巴转移和腹腔种植转移为主, 本例患者胃癌术后2年余以头痛为主要症状起病, 通过脑脊液细胞学检查诊断脑膜转移, 期间多次行胸腹盆计算机断层扫描(computed tomography, CT)平扫+增强、胃镜及病理检查, 未见明显肿瘤复发或转移表现. 为使临床医师拓宽思路, 减少误诊, 现将1例胃癌术后脑膜转移的临床资料分析报告如下.
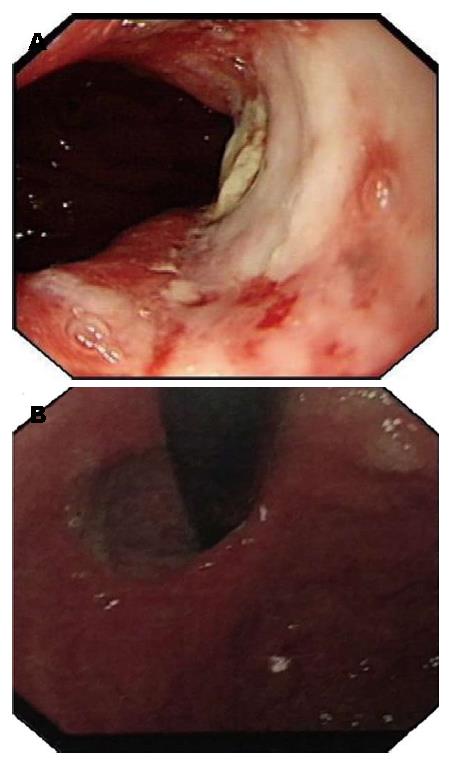
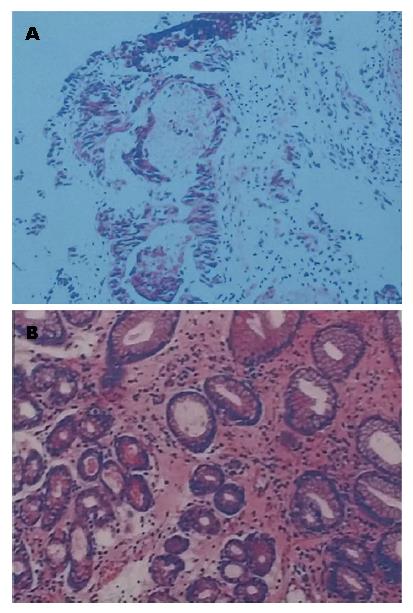
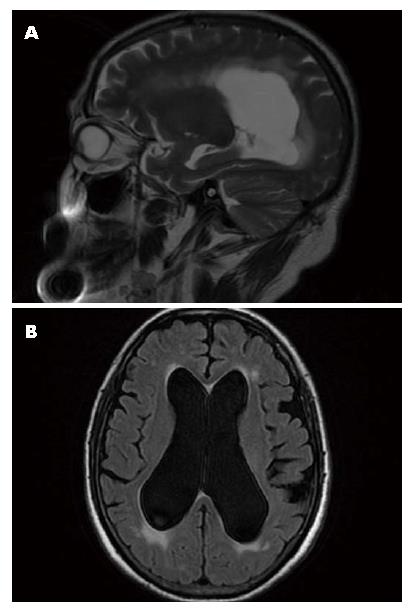
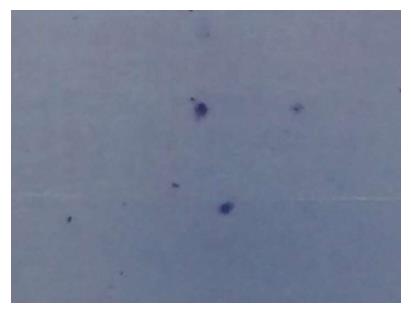
患者, 男性, 68岁, 2009-07因纳差、乏力和消瘦查胃镜示: 贲门癌, 胃窦黏膜隆起(图1A), 病理示: (贲门胃窦)腺癌(图2A). 遂于2009-07-30行"近端胃癌根治术+脾脏切除术", 术中探及肿瘤侵及全层, 两切端未见癌累及, 淋巴结见癌转移(3/13), 另见癌结节, 术后病理示: 贲门中低分化腺癌. 免疫组织化学染色结果: CK20、CK均(+), Ki-67约30%(+), CK7、Her-2、S-100、syn均(-). 手术过程顺利, 患者恢复良好. 术后行FOLFOX方案(奥沙利铂+5-氟尿嘧啶+亚叶酸钙)静脉化疗6个周期, 过程顺利, 末次化疗时间为2010-01-07. 后患者定期随访复查, 于2010-01-06、2010-03-10、2011-06-16查癌胚抗原(carcinoembryonic antigen, CEA)分别为: 1.46、0.98、20.64 ng/mL. 2011-06-16查胸腹盆CT平扫+增强示: 胃癌术后改变, 脾脏缺如, 肝右叶海面状血管瘤, 两肺未见明显异常; 胃镜示: 残胃吻合口炎. 2011-08-29患者因"胃癌术后2年余, 头痛20余天"入院, 主要为双颞部及额部胀痛, 伴头晕、恶心呕吐, 曾有数次双眼外翻, 呼之不应发作, 无明显肢体抽搐及二便失禁, 并有纳差、乏力. 体格检查: 生命体征平稳, 神志清楚, 颈项稍强直, 双侧瞳孔等大等圆, 对光反射灵敏, 四肢肌力5级, 双侧病理征未引出. 辅助检查: CEA>100 ng/mL, 胸腹盆CT平扫+增强示: 胃癌术后改变, 考虑肝右叶血管瘤, 脾脏未见显示; 右上肺尖段钙化结节. 胃镜示: 残胃吻合口炎(图1B), 胃镜病理示: (食道-胃吻合口黏膜)轻度慢性浅表性炎(图2B). 头颅磁共振成像(magnetic resonance imaging, MRI)+磁共振血管造影(magnetic resonance angiography, MRA)+增强示: 脑积水, 双额叶小缺血灶(图3). 患者2011-09-01行腰椎穿刺, 测压>400 mmH2O, 留10 mL脑脊液送检查, 脑脊液外观: 无色透明; 脑脊液潘氏试验: 阴性; 脑脊液糖半定量: (1-5滴)阳性; 脑脊液白细胞计数: 20×106/L, 脑脊液红细胞计数: 0×106/L; 脑脊液生化: 氯: 112.6 mmol/L; 蛋白: 0.38 g/L; 糖: 2.42 mmol/L; 腺苷脱氨酶: 1.1 U/L; 乳酸脱氢酶: 44 U/L. 脑脊液脱落细胞检查: 见核大异型细胞(图4). 临床诊断: 胃癌术后脑膜转移, 予加强脱水降颅压, 对症止痛支持治疗, 患者病情进展迅速, 于2011-09-02出现昏迷, 家属放弃进一步诊治, 自动出院, 患者于2011-09-03死亡.
脑膜转移癌又称脑膜癌病(meningeal carcinomatosis, MC), 是恶性肿瘤由原发病灶向颅内转移, 侵犯脑膜从而发生的一种严重病变, 是恶性肿瘤致死的重要原因之一. MC绝大多数为颅外恶性肿瘤转移所致, 其中以乳腺癌、肺癌、恶性淋巴瘤、恶性黑色素瘤居多.胃癌脑膜癌病较少见, 约占全部MC的0.19%左右[1]. MC的主要症状有头痛、恶心呕吐、脑膜刺激征等, 由于其临床表现缺乏特异性, 因此极易被误诊. 另一方面, MC未形成实体肿瘤, 故患者常缺乏定位体征, 且常规影像学检查如脑CT及MRI平扫多正常, 增强MRI是检出MC较为敏感和有效的方法[2], 本例患者头颅MRI检查提示脑积水, 对该病的诊断有一定价值. 脑脊液检查是诊断MC的常用手段[3], 大部分患者脑脊液压力升高, 本例患者测压>400 mmH2O, 而脑脊液细胞学检查对该病诊断往往起到关键作用, Collie等[4]报道41例脑膜转移瘤中常规脑脊液细胞学检查的阳性率为85%, 本例患者脑脊液脱落细胞检查找到核大异型细胞, 为诊断提供了重要依据. 胃癌转移途径以淋巴转移和腹腔种植转移为主, 血行转移较为少见. 其中淋巴转移通常按淋巴引流顺序, 即由近及远, 由浅及深的规律转移, 故胃癌转移一般以腹腔脏器为主, 较少侵及中枢神经系统[3]. 本例患者胃癌术后2年余以MC的主要症状起病, 通过脑脊液细胞学检查诊断脑膜转移, 期间多次行胸腹盆CT平扫+增强、胃镜及病理检查, 未见明显肿瘤复发或转移表现, 在临床上极为罕见. 但该患者2011-06-16、2011-09-01日查CEA分别为: 20.64 ng/mL、>100 ng/mL, 较前进行性升高, 高度提示可能病情进展. MC预后极差, 治疗效果不佳, 目前的治疗方法属姑息性, 包括全身化疗、鞘内注射、局部放射治疗等. 多数患者经过治疗后可改善神经系统症状、提高生活质量[5]. 本例患者确诊后病情迅速恶化, 短期出现昏迷、死亡. 因此, 对于消化系肿瘤患者, 如出现不明原因的头痛、呕吐、眼底水肿、癫痫发作、视力丧失、听力及前庭功能障碍、四肢无力、偏瘫、大小便失禁等症状, 颅脑CT或MRI未见明显占位, 且排除颅内原发疾病、中枢神经系统感染时, 即使患者无原发肿瘤症状且未见明显腹腔转移, 亦应高度警惕MC可能. 尽早行头颅MRI增强或腰椎穿刺检查, 及时明确诊断并予相应治疗, 以期改善患者症状, 延长生存期.
胃癌术后脑膜转移临床罕见, 早期难发现, 容易误诊, 治疗效果及预后均极差.
王刚, 副研究员, 哈尔滨医科大学附属第一医院胰胆外科(普外二科)
脑膜癌病预后极差, 治疗效果不佳, 目前全身化疗、鞘内注射、局部放射治疗等均属姑息性治疗, 因此, 对该病的治疗尚需多方合作以积累更多资料及更深入的研究.
胃癌术后脑膜转移罕见, 国内外公开报道少, 报道的焦点主要是脑膜癌病的诊断与鉴别诊断要点.
本例患者胃癌术后2年余以脑膜癌病起病, 期间定期体检未见明显肿瘤复发或转移表现. 临床医师应加强对该疾病的认识, 重视相关检查的诊断价值.
对于消化系肿瘤患者, 如出现不明原因的神经系统症状, 临床医师应警惕脑膜癌病可能. 尽早行相应检查, 及时明确诊断并予积极治疗, 以期改善患者预后.
本文报道了1例胃癌术后脑膜转移的病例, 对指导临床工作具有重要的参考意义.
编辑: 郭鹏 电编: 都珍珍
| 1. | Giglio P, Weinberg JS, Forman AD, Wolff R, Groves MD. Neoplastic meningitis in patients with adenocarcinoma of the gastrointestinal tract. Cancer. 2005;103:2355-2362. [PubMed] [DOI] |
| 3. | Oh SY, Lee SJ, Lee J, Lee S, Kim SH, Kwon HC, Lee GW, Kang JH, Hwang IG, Jang JS. Gastric leptomeningeal carcinomatosis: multi-center retrospective analysis of 54 cases. World J Gastroenterol. 2009;15:5086-5090. [PubMed] [DOI] |
| 4. | Collie DA, Brush JP, Lammie GA, Grant R, Kunkler I, Leonard R, Gregor A, Sellar RJ. Imaging features of leptomeningeal metastases. Clin Radiol. 1999;54:765-771. [PubMed] [DOI] |