修回日期: 2014-10-09
接受日期: 2014-11-04
在线出版日期: 2014-12-08
原发性十二指肠肿瘤(primary tumors of the duodenum, PTD)分为良性和恶性肿瘤, 以恶性肿瘤为多, 十二指肠各段均可发生, 但相对于胃肠道其他部位的肿瘤, PTD的发病率较低, 治疗以外科手术切除为主, 且多行根治性胰十二指肠切除术. 近年来, 随着医学影像技术的不断提高和内镜微创技术的发展, 尤其是十二指肠镜、胶囊内镜、超声内镜、经内镜逆行胰胆管造影(endoscopic retrograde cholangio-pancreatography, ERCP)及腹腔镜技术的发展, PTD的早期发现和检出率增高, 其诊断和治疗也取得了新的进展, 微创治疗和局部切除等损伤较小的手术方式越来越受到临床医师的重视. 本文着重就PTD的临床分类、病理分型及外科诊治进展进行介绍, 以利于更好地诊断和治疗十二指肠肿瘤.
核心提示: 本文结合最新文献及作者临床经验阐述了原发性十二指肠肿瘤(primary tumors of the duodenum)诊断和治疗的进展. 其诊断纤维十二指肠镜及气钡双重上消化道造影为首选检查方法, 其治疗良性肿瘤首选局部切除术和节段性十二指肠切除术, 也可选择内镜下肿瘤切除术, 恶性肿瘤首选胰十二指肠切除术.
引文著录: 王凤山, 高正杰, 刘永锋. 原发性十二指肠肿瘤的诊治进展. 世界华人消化杂志 2014; 22(34): 5221-5227
Revised: October 9, 2014
Accepted: November 4, 2014
Published online: December 8, 2014
Compared to tumors from other parts of the gastrointestinal tract, primary tumors of the duodenum are uncommon. Both benign tumors and malignancies are possible, although the majority are malignancies. The treatment of choice is surgical resection, mostly pancreaticoduodenectomy. With the development of endoscopy microsurgery and medical imaging technology, especially the advent of gastroduodenal fiberscopy, capsule endoscopy, endoscopic ultrasonography (EUS), endoscopic retrograde cholangio-pancreatography (ERCP) and laparoscopy, more duodenal neoplasms have been detected in recent years. Some advances have been achieved in the diagnosis and treatment of duodenal tumors. Endoscopic and segmental resections play a more and more important role in the management of duodenal tumors. In this paper, we describe the clinical features, pathological patterns, diagnosis and treatment of primary duodenal tumors.
- Citation: Wang FS, Gao ZJ, Liu YF. Recent advances in diagnosis and treatment of primary duodenal tumors. Shijie Huaren Xiaohua Zazhi 2014; 22(34): 5221-5227
- URL: https://www.wjgnet.com/1009-3079/full/v22/i34/5221.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i34.5221
原发性十二指肠肿瘤(primary tumors of the duodenum, PTD)指发生于十二指肠各段的良恶性肿瘤, 分为原发性十二指肠良性肿瘤(primary benign tumors of the duodenum, PBTD)和原发性十二指肠恶性肿瘤(primary malignant tumors of the duodenum, PMTD), 但不包括Vater壶腹及胆总管末端的肿瘤. 国内报道PTD占小肠肿瘤的13%-36%[1,2], 国外统计PTD占小肠肿瘤的比率为18.4%-52.0%[3-7]. PTD好发于中年人, 多位于十二指肠降部及水平部, 最常见于乳头部[8]. 病理类型良性肿瘤以腺瘤为多, 恶性肿瘤以腺癌为多. 因十二指肠在解剖和生理上都具有特殊性, 缺乏早期特异性临床表现, 易延误诊断. 诊断主要根据临床表现、上消化道造影、胃十二指肠镜及多层螺旋CT(multislice CT, MSCT)、磁共振成像(magnetic resonance imaging, MRI)等辅助检查手段. 治疗方法以外科手术切除为首选, 具体根据肿瘤的性质、位置及浸润范围选择个体化的治疗. 而早期诊断和治疗对于患者的生存质量及预后有重要意义.
PTD发病率较低, 起病隐匿, 早期缺乏典型临床表现, 缺乏大宗病例研究. 参考相关文献, 总结其临床特点, 其常见的临床症状有: (1)消化系非特异性症状: 包括腹痛、恶心、厌食等类似于消化系炎症和溃疡症状; (2)体质量下降及贫血: 是十二指肠肿瘤的常见症状, 尤其见于病史较长和恶性肿瘤晚期患者; (3)黄疸: 多见于十二指肠降部而肿瘤较大者, 尤见于乳头区肿瘤阻塞胆胰管开口者, 常伴有腹痛; (4)消化系出血: 以粪便隐血阳性和黑便为多见, 少见呕血病例; (5)恶心、呕吐等肠梗阻症状: 多见于肿瘤生长较快, 体积较大, 致肠腔阻塞者或恶性肿瘤浸润生长, 突破浆膜者; (6)腹部包块: 临床少见, 多见于浆膜面肿瘤, 体积大, 向腔外生长者. 临床以腹痛、黄疸、黑便、体质量下降最为多见. 上腹部疼痛的出现率约为66%, 消化系梗阻40%, 消化系出血24%, 体质量下降54.4%, 黄疸48.1%[5,9,10].
内镜检查为诊断PTD的首选方法, 最好用十二指肠镜, 不仅可镜下肉眼观察肿瘤的大小、位置、形态特征, 最主要的是可以取活组织病理检查以确诊. 随着十二指肠镜的广泛应用, PTD的诊断率明显提高, 国内报告一般在80%左右[14]. 但内镜受本身盲区等因素的影响, 不易发现十二指肠水平部和升部的肿瘤, 或观察不满意, 常需结合十二指肠气钡双重造影来提高诊断率. 近年来随着内镜技术的发展, 胶囊内镜的临床应用相继开展并走向成熟. 胶囊内镜为无创性检查方法, 患者易接受, 顺应性良好, 并发症少, 适用于不明原因的消化系出血病例, 尤其是合并心脑血管疾病不易接受十二指肠镜检查的老年患者[15,16]. Maieron等[17]通过多中心回顾分析发现78.4%的检查全段小肠显像良好, 推荐胶囊内镜作为隐性出血或缺铁性贫血患者的常规检查.
胃肠道造影检查, 尤其是十二指肠低张气钡双重造影检查, 有助于了解肠腔狭窄情况及黏膜病变, 易发现十二指肠3、4段的肿瘤, 准确率可达85.6%[1,18,19]. 结合十二指肠镜可提高诊断的准确率, 但不易了解肠腔外及十二指肠球后的病变情况, 结合CT检查也可以提高诊断率. 李惠民等[20]报告低张十二指肠造影联合CT诊断十二指肠肿瘤的特异性为90.9%.
MSCT作为一种微创检查, 易于被患者接受, 其诊断的敏感性要高于胃肠道造影检查, 对判断肿瘤性质及与周围组织器官的关系、有无淋巴结转移等有重要价值, 有助于肿瘤定性[21], 并可为手术方案提供依据, 还可行三维重建, 能多角度、更直观地显示肿瘤形态、范围、周围结构及脏器情况, 此点优于十二指肠镜. 有学者报告其对腺瘤和腺癌诊断的准确性为69%、对良恶性间质瘤的准确性为80%、对脂肪瘤的准确性为100%[22].
MRI可以直接显示十二指肠乳头部肿瘤的形态和信号特征, MRCP可以清楚的显示肿瘤引起胆管扩张的形态与程度. 随着MRI及MRCP技术日渐成熟, 如低张力和动态增强技术的应用, 能清楚地显示早期癌瘤结节和十二指肠壁的增厚情况. 二者联合检查, 能够提高诊断符合率, 具有成功率高、无创伤性、无并发症的优点, 尤其适用于梗阻性黄疸患者的检查, 可作为十二指肠乳头癌的首选检查方法[23].
近年来应用彩色多普勒超声检查十二指肠肿瘤越来越受到重视, 不仅可观察腔内病变, 同时可判断周围脏器有无浸润、受浸程度及胆管有无梗阻等间接征象. 有学者报告腹部超声对PTD诊断的符合率为86.4%, 误诊率为13.5%[24], 具有很广泛的应用价值, 可作为一种无创性检查方法应用于十二指肠肿瘤的筛查诊断.
十二指肠腔内超声或超声内镜(endoscopic ultrasonography, EUS)可有效地对十二指肠黏膜下病变及腔外组织器官进行观察, 可发现早期局限性病变及其他检查不易定性的病变. 尤其是可以通过EUS引导下的细针穿刺对黏膜下病灶及周围可疑病灶进行穿刺取细胞学检查以明确病变性质. 有研究[25-27]报告EUS引导下细针穿刺进行细胞病理学检查可使诊断总体准确率达到90%.
ERCP在国内开展应用将近40余年, 随着操作技术的不断改进、内镜及相关附属器械的发展, 成功率不断提高, 在PTD的诊断中具有重要的作用, 尤其适用于乳头部肿瘤合并梗阻性黄疸的患者. 任旭等[28]对32例梗阻性黄疸的患者行ERCP检查, 并与超声、CT对比, 其定位诊断率分别为93.7%、87.5%、81.3%, 定性诊断率分别为90.6%、62.5%、56.3%, 显示ERCP对梗阻性黄疸的病因诊断明显优于超声和CT, 对其他疾病的鉴别诊断具有重要意义. 同时ERCP还具有治疗作用, 可内镜下行胆管引流术、胆管支架或十二指肠支架置入术. 近年来随着ERCP技术的不断成熟和完善, 已作为十二指肠乳头肿瘤的首选检查, 联合内镜超声可大大提高诊断的准确性. 刘全达等[29]研究报告超声结合ERCP检查, 可使乳头区肿瘤的检出率达到100%.
数字减影腹腔动脉造影有助于对血管丰富的十二指肠肿瘤做出诊断, 可显示肿瘤大体轮廓, 尤其是在肿瘤破裂, 急性出血时, 可同时行栓塞治疗, 对于高龄老年患者, 对其他检查不易耐受者, 此方法为一种重要选择.
PET-CT适用于其他检查不易确定肿瘤性质的病例, 对肿瘤晚期患者, 易发现局部淋巴结及全身其他器官转移情况[30]. 国内有报道[31]8例行PET-CT检查的患者中, 7例提示肠壁增厚、肠腔狭窄, 4例提示占位性病变和周围淋巴结肿大, 1例提示肝脏和腹腔淋巴结转移, 结合CT检查能够提高确诊率. 由于检查价格昂贵, 不易被患者所接受, 目前应用局限.
总之本病发病率低, 诊断主要依靠临床表现、内镜检查、十二指肠低张双重造影的辅助检查. 早期诊断对本病的治疗和预后有重要意义. 近年来随着医学影像技术的发展和人民健康意识的提高, 本病的早期诊断率有所提高. 因此必须提高对本病的警惕和认识, 为此一般认为: (1)年龄在50岁以上, 出现上腹部隐痛不适, 伴有消瘦、黄疸, 不能明确诊断者; (2)波动性黄疸伴有胆胰管扩张, 胆囊增大而无结石或胰头部无占位性病变者; (3)不明原因的反复消化系出血而胃镜无阳性发现者; (4)有不典型消化性溃疡症状伴胆道或十二指肠梗阻者; 凡具有上述征象之一者应高度怀疑本病, 并及时行相应检查, 以早期明确诊断. 本病早期缺乏特异性临床表现, 误诊率高, 主要与胃十二指肠炎、消化性溃疡、黄疸型肝炎、胆石症、胆道感染、胰头癌等. 误诊的主要原因为: (1)早期缺乏特异性表现, 中晚期临床表现复杂多样; (2)本病常合并其他疾病, 并发症表现掩盖了原发病情; (3)医生警惕性差, 满足于常见病的诊断; (4)临床应用辅助检查单一, 局限性较大; (5)十二指肠间质瘤常位于黏膜下, 向腔外生长, 内镜活检常为阴性.
十二指肠肿瘤无论是良性或恶性, 一经确诊, 以手术治疗为首选. 手术方式需根据肿瘤部位、大小、浸润范围、有无转移及患者身体状况等因素综合考虑, 由于解剖位置的特殊性, 十二指肠肿瘤的手术难度较大. 近年来, 随着对十二指肠肿瘤的认识提高和纤维内镜的广泛应用, 早期诊断率逐渐提高, 使得本病的手术方式逐渐增多.
十二指肠大部分位于腹膜后, 与胰腺的关系密切, 因此十二指肠的肿瘤, 尤其是恶性肿瘤易侵及胰头, PD术不仅能完整地切除肿瘤, 还能彻底清扫肝十二指肠韧带及胰周的淋巴结, 从而获得更好的疗效, 是目前最有希望的根治性手术和标准的治疗方法[32,33]. 该术式自1909年由Kuasch首例成功实行以来, 获得了满意效果, 该术式适用于十二指肠各段的恶性肿瘤. PD术后常见的并发症主要是胰瘘、胆瘘、出血、感染等, 胰瘘是最严重的并发症, 也是导致患者术后早期死亡的主要原因, 近年来随着抗生素的应用、重症监护水平和营养支持技术的提高, 围术期并发症发生率和死亡率显著降低[10,34-36].
该术是PD术的改良术式, 其区别在于保留了全胃、幽门、十二指肠球部, 因此最大限度地保留了胃功能, 能够预防术后倾倒综合征和改善患者营养状况. 自1978年Traverso和Langmire报道将其应用于治疗十二指肠肿瘤以来, 得到了广泛应用, 适应证不断扩大, 适用于未侵犯胃窦、幽门、第5、6组淋巴结的十二指肠肿瘤患者[37], 疗效与PD术相似, 尤适用于早期癌, 无淋巴结转移患者和良性肿瘤患者, 手术创伤相对较小, 提高了患者生存质量.
近年来腹腔镜技术和器械发展越来越完善, 其在腹部外科疾病治疗中的应用也越来越广泛, 而腹腔镜胰十二指肠切除术仍被认为是腹腔镜手术中难度最大、最复杂的手术, 并有越来越多的成功报道[38-42]. 较常规开腹手术具有创伤小、痛苦轻、恢复快的优点, 是十二指肠肿瘤微创治疗的重要组成部分. 但由于对术者的临床经验及器械要求较高, 目前尚未能广泛开展, 但随着技术经验的提高和器械的发展, 相信该术式会被患者和医务人员逐步接受.
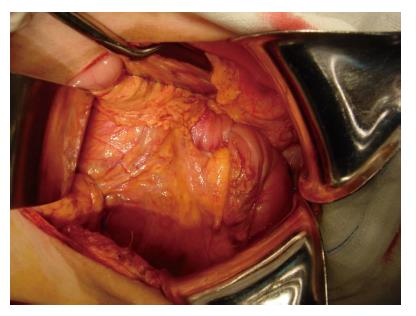
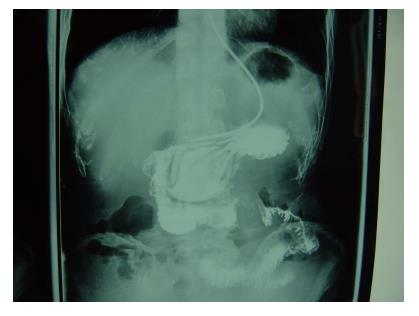
适用于病变范围小、界限清楚、未浸透浆膜的早期病例和癌前病变, 或者全身状况差、高龄、不能耐受根治性切除的患者, 尤其是十二指肠第3、4段的良性肿瘤[14,45], 也适用于低度恶性肿瘤和早期十二指肠乳头癌及晚期十二指肠癌的姑息性切除. 缺点是对恶性肿瘤切除不彻底, 术后易复发. 分为保留十二指肠乳头近端的十二指肠切除术、胃十二指肠切除术、包括十二指肠乳头区在内的节段性十二指肠切除术[46,47]以及十二指肠第3、4段切除. 根据病变部位、范围及性质选择相应的节段性切除术. 我们有4例十二指肠第3段癌的病例实施了十二指肠节段切除, 其中1例合并肠套叠, 手术效果满意(图1, 2).
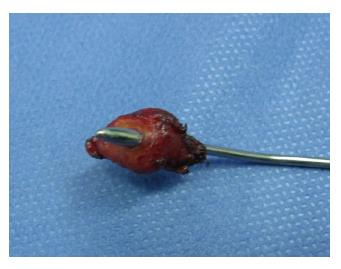
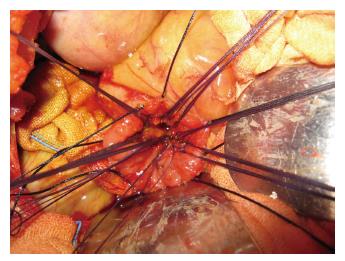
适用于良性肿瘤、类癌、不典型增生患者, 肿瘤直径<3 cm者, 以及T1期十二指肠乳头癌患者和经EUS评估TNM分期为T2N0M0以下者均适宜局部切除术. 对于高龄、重度黄疸、全身情况差得患者作为姑息性切除短期内可提高生活质量, 是一种在某些特定条件下治疗十二指肠肿瘤有效方法[48-52], 并应严格掌握适应证[27], 要能达到切缘无瘤细胞残留. 我们也曾对多例年老体弱的十二指肠乳头癌患者实施十二指肠乳头局部切除(图3, 4), 取得比较满意的结果.
近年来应用内镜技术对十二指肠肿瘤进行治疗是外科治疗的重要进展, 其操作的安全性和有效性已成为共识. 主要适用于良性肿瘤、癌前病变、一些早期恶性肿瘤以及无法手术切除的恶性肿瘤的姑息治疗, 以缓解症状提高生活质量. 主要包括十二指肠良性肿瘤内镜切除、内镜黏膜切除、内镜黏膜下剥除术、内镜下乳头切除术, 术前应用EUS活检并评估肿瘤性质、大小、浸润深度及结构层次, 以决定能否行内镜切除[53-58], 对于晚期恶性肿瘤还可内镜下置入支架解除梗阻症状.
化疗、辅助化疗以及中医中药治疗, 均可部分改善十二指肠恶性肿瘤患者症状[61], 尚需要进一步研究.
十二指肠良性肿瘤预后较好, 恶性肿瘤总体预后差, 受肿瘤的浸润深度、有无淋巴结转移及手术方式影响而不同. 行根治性手术患者预后相对较好, 目前缺乏大宗随访资料. 总的5年生存率在27%左右[1,14,62], 有报道十二指肠癌PD和SR术后1、3、5年生存率分别为100.0%、67.7%、41.6%和100.0%、60.0%、0.0%; 接受根治性手术中早期患者较中晚期患者中位生存期长[63-65].
PTD临床少见, 因缺乏特异性临床表现, 早期诊断不易, PMTD预后差, 早期诊断和治疗能够显著提高生存率. 因此临床医生应提高对该病的认识和警惕性, 对早期的非特异性消化系症状及时行相关检查, 能够提高早期诊断率. 纤维十二指肠镜及气钡双重对比上消化道造影检查为首选检查方法. 治疗良性肿瘤首选局部切除和节段性十二指肠切除术, 也可选择内镜下肿瘤切除术, 恶性肿瘤首选胰十二指肠切除术, 对于高龄、一般状况差不易耐受PD术者可选择姑息性手术或旁路手术, 以解除症状, 改善生活质量. 但具体治疗方式仍以根据肿瘤性质、部位、浸润深度、有无转移及患者全身状况决定. 内镜下肿瘤切除术和腹腔镜手术是十二指肠肿瘤治疗的重要方法, 而且具有微创的特点, 随着早期诊断率的提高、内镜技术以及腹腔镜技术的发展完善, 相信其应用会越来越广泛, 以争取使恶性肿瘤获得早期诊断和治疗, 使得PTD患者获得良好的预后.
十二指肠肿瘤好发于中年人, 多位于十二指肠降部, 病理类型良性肿瘤以腺瘤为多, 恶性肿瘤以腺癌为多. 因十二指肠在解剖和生理上都具有特殊性, 缺乏早期特异性临床表现, 易延误诊断.
沈克平, 主任医师, 上海中医药大学附属龙华医院
腹腔镜胰十二指肠切除术治疗十二指肠肿瘤有很多成功报道, 较常规开腹手术具有创伤小、痛苦轻、恢复快的优点, 是十二指肠肿瘤微创治疗的重要组成部分.
赵金都等对原发性十二指肠腺癌的诊治进行了报道, 认为其早期起病隐匿, 随着影像学技术进步和内镜的广泛应用, 其检出率逐年提高, 能否根治性切除及肿瘤分期是患者预后的最显著因素.
本文较详细地介绍了十二指肠肿瘤诊断方面的新方法以及外科治疗方面的新术式, 也介绍了十二指肠肿瘤姑息治疗的方法.
本文系统综述了十二指肠肿瘤的诊治进展, 具有很好的学术价值.
编辑: 郭鹏 电编:闫晋利
| 1. | Zhan J, Xia ZS, Zhong YQ, Zhang SN, Wang LY, Shu H, Zhu ZH. Clinical analysis of primary small intestinal disease: A report of 309 cases. World J Gastroenterol. 2004;10:2585-2587. [PubMed] |
| 3. | Hatzaras I, Palesty JA, Abir F, Sullivan P, Kozol RA, Dudrick SJ, Longo WE. Small-bowel tumors: epidemiologic and clinical characteristics of 1260 cases from the connecticut tumor registry. Arch Surg. 2007;142:229-235. [PubMed] [DOI] |
| 4. | Lu Y, Fröbom R, Lagergren J. Incidence patterns of small bowel cancer in a population-based study in Sweden: increase in duodenal adenocarcinoma. Cancer Epidemiol. 2012;36:e158-e163. [PubMed] [DOI] |
| 5. | Dabaja BS, Suki D, Pro B, Bonnen M, Ajani J. Adenocarcinoma of the small bowel: presentation, prognostic factors, and outcome of 217 patients. Cancer. 2004;101:518-526. [PubMed] [DOI] |
| 6. | Overman MJ, Hu CY, Kopetz S, Abbruzzese JL, Wolff RA, Chang GJ. A population-based comparison of adenocarcinoma of the large and small intestine: insights into a rare disease. Ann Surg Oncol. 2012;19:1439-1445. [PubMed] [DOI] |
| 7. | Sendt W, Wurst C, Settmacher U, Altendorf-Hofmann A. [Adenocarcinoma of small bowel. An underdiagnosed disease]. Chirurg. 2012;83:374-380. [PubMed] [DOI] |
| 10. | Poultsides GA, Huang LC, Cameron JL, Tuli R, Lan L, Hruban RH, Pawlik TM, Herman JM, Edil BH, Ahuja N. Duodenal adenocarcinoma: clinicopathologic analysis and implications for treatment. Ann Surg Oncol. 2012;19:1928-1935. [PubMed] [DOI] |
| 11. | Aparicio T, Zaanan A, Svrcek M, Laurent-Puig P, Carrere N, Manfredi S, Locher C, Afchain P. Small bowel adenocarcinoma: epidemiology, risk factors, diagnosis and treatment. Dig Liver Dis. 2014;46:97-104. [PubMed] [DOI] |
| 12. | Terada T. Pathologic observations of the duodenum in 615 consecutive duodenal specimens in a single Japanese hospital: II. malignant lesions. Int J Clin Exp Pathol. 2012;5:52-57. [PubMed] |
| 14. | Hu JX, Miao XY, Zhong DW, Dai WD, Liu W, Hu W. Surgical treatment of primary duodenal adenocarcinoma. Hepatogastroenterology. 2006;53:858-862. [PubMed] |
| 15. | 颜 綦先, 王 军, 李 丽, 刘 宇, 邵 小娟, 郭 严, 崔 红莉, 杨 均, 潘 大维, 肖 潇. 胶囊内镜在诊断不明原因消化系出血中的临床应用. 重庆医学. 2011;40:1281-1282. |
| 16. | Conio M, De Ceglie A, Filiberti R, Fisher DA, Siersema PD. Cap-assisted EMR of large, sporadic, nonampullary duodenal polyps. Gastrointest Endosc. 2012;76:1160-1169. [PubMed] [DOI] |
| 17. | Maieron A, Hubner D, Blaha B, Deutsch C, Schickmair T, Ziachehabi A, Kerstan E, Knoflach P, Schoefl R. Multicenter retrospective evaluation of capsule endoscopy in clinical routine. Endoscopy. 2004;36:864-868. [PubMed] [DOI] |
| 18. | Honda W, Ohmiya N, Hirooka Y, Nakamura M, Miyahara R, Ohno E, Kawashima H, Itoh A, Watanabe O, Ando T. Enteroscopic and radiologic diagnoses, treatment, and prognoses of small-bowel tumors. Gastrointest Endosc. 2012;76:344-354. [PubMed] [DOI] |
| 19. | Hangai S, Nakamura F, Yamada A, Watabe H, Ichikawa M, Koike K, Kurokawa M. Usefulness of double-balloon enteroscopy for evaluation of duodenal follicular lymphoma. Ann Hematol. 2012;91:1819-1820. [PubMed] [DOI] |
| 20. | 李 惠民, 朱 望东, 刘 晓明, 李 哲, 徐 朝霞, 龚 雪鹏. 十二指肠肿瘤CT及低张十二指肠造影诊断及价值探讨. 中华实用诊断与治疗杂志. 2008;22:905-907. |
| 21. | Jayaraman MV, Mayo-Smith WW, Movson JS, Dupuy DE, Wallach MT. CT of the duodenum: an overlooked segment gets its due. Radiographics. 2001;21 Spec No:S147-S160. [PubMed] [DOI] |
| 25. | Gress F, Gottlieb K, Sherman S, Lehman G. Endoscopic ultrasonography-guided fine-needle aspiration biopsy of suspected pancreatic cancer. Ann Intern Med. 2001;134:459-464. [PubMed] [DOI] |
| 26. | Azih LC, Broussard BL, Phadnis MA, Heslin MJ, Eloubeidi MA, Varadarajulu S, Arnoletti JP. Endoscopic ultrasound evaluation in the surgical treatment of duodenal and peri-ampullary adenomas. World J Gastroenterol. 2013;19:511-515. [PubMed] [DOI] |
| 27. | Kim HK, Lo SK. Endoscopic approach to the patient with benign or malignant ampullary lesions. Gastrointest Endosc Clin N Am. 2013;23:347-383. [PubMed] [DOI] |
| 30. | Watanabe N, Hayashi S, Kato H, Shimizu M, Kamisaki Y, Noguchi K, Kishida M, Matsunari I, Hisada K, Seto H. FDG-PET imaging in duodenal cancer. Ann Nucl Med. 2004;18:351-353. [PubMed] [DOI] |
| 37. | Seiler CA, Wagner M, Sadowski C, Kulli C, Büchler MW. Randomized prospective trial of pylorus-preserving vs. Classic duodenopancreatectomy (Whipple procedure): initial clinical results. J Gastrointest Surg. 2000;4:443-452. [PubMed] [DOI] |
| 38. | 彭 健, 张 阳德, 李 年丰, 龚 连生, 李 珍发, 汤 伟, 李 坚, 刘 勤, 王 渊景, 张 洋. 腹腔镜胰十二指肠切除术. 中国现代医学杂志. 2008;18:3633-3634. |
| 41. | Stauffer JA, Raimondo M, Woodward TA, Goldberg RF, Bowers SP, Asbun HJ. Laparoscopic partial sleeve duodenectomy (PSD) for nonampullary duodenal neoplasms: avoiding a whipple by separating the duodenum from the pancreatic head. Pancreas. 2013;42:461-466. [PubMed] [DOI] |
| 42. | Corcione F, Pirozzi F, Cuccurullo D, Piccolboni D, Caracino V, Galante F, Cusano D, Sciuto A. Laparoscopic pancreaticoduodenectomy: experience of 22 cases. Surg Endosc. 2013;27:2131-2136. [PubMed] [DOI] |
| 44. | Stauffer JA, Adkisson CD, Riegert-Johnson DL, Goldberg RF, Bowers SP, Asbun HJ. Pancreas-sparing total duodenectomy for ampullary duodenal neoplasms. World J Surg. 2012;36:2461-2472. [PubMed] [DOI] |
| 45. | Tran KT, Smeenk HG, van Eijck CH, Kazemier G, Hop WC, Greve JW, Terpstra OT, Zijlstra JA, Klinkert P, Jeekel H. Pylorus preserving pancreaticoduodenectomy versus standard Whipple procedure: a prospective, randomized, multicenter analysis of 170 patients with pancreatic and periampullary tumors. Ann Surg. 2004;240:738-745. [PubMed] [DOI] |
| 47. | Cavaniglia D, Petrucciani N, Lorenzon L, Caterino S, Cavallini M. Partial duodenectomy with end-to-end anastomosis for duodenal gastrointestinal stromal tumor. Am Surg. 2012;78:E273-E275. [PubMed] |
| 49. | Nikfarjam M, Muralidharan V, McLean C, Christophi C. Local resection of ampullary adenocarcinomas of the duodenum. ANZ J Surg. 2001;71:529-533. [PubMed] [DOI] |
| 50. | Cubas RF, Ballarino EA, Nieto FA, Diaz MD. Local resection of a gastrointestinal stromal tumor of the third portion of the duodenum. Am Surg. 2012;78:E22-E23. [PubMed] |
| 51. | Hoeppner J, Kulemann B, Marjanovic G, Bronsert P, Hopt UT. Limited resection for duodenal gastrointestinal stromal tumors: Surgical management and clinical outcome. World J Gastrointest Surg. 2013;5:16-21. [PubMed] [DOI] |
| 54. | Takahashi T, Ando T, Kabeshima Y, Kawakubo H, Shito M, Sugiura H, Omori T. Borderline cases between benignancy and malignancy of the duodenum diagnosed successfully by endoscopic submucosal dissection. Scand J Gastroenterol. 2009;44:1377-1383. [PubMed] [DOI] |
| 55. | Jung JH, Choi KD, Ahn JY, Lee JH, Jung HY, Choi KS, Lee GH, Song HJ, Kim DH, Kim MY. Endoscopic submucosal dissection for sessile, nonampullary duodenal adenomas. Endoscopy. 2013;45:133-135. [PubMed] [DOI] |
| 56. | Zhong YS, Shi Q, Wu HF, Yao LQ, Zhou PH, Xu MD, Chen SY. Endoscopic resection for the treatment of duodenal Brunner's adenomas. J Laparoendosc Adv Surg Tech A. 2012;22:904-909. [PubMed] [DOI] |
| 57. | Matsumoto S, Miyatani H, Yoshida Y. Endoscopic submucosal dissection for duodenal tumors: a single-center experience. Endoscopy. 2013;45:136-137. [PubMed] |
| 58. | Jaganmohan S, Lynch PM, Raju RP, Ross WA, Lee JE, Raju GS, Bhutani MS, Fleming JB, Lee JH. Endoscopic management of duodenal adenomas in familial adenomatous polyposis--a single-center experience. Dig Dis Sci. 2012;57:732-737. [PubMed] [DOI] |
| 59. | Artifon EL, Frazão MS, Wodak S, Carneiro FO, Takada J, Rabello C, Aparício D, de Moura EG, Sakai P, Otoch JP. Endoscopic ultrasound-guided choledochoduodenostomy and duodenal stenting in patients with unresectable periampullary cancer: one-step procedure by using linear echoendoscope. Scand J Gastroenterol. 2013;48:374-379. [PubMed] [DOI] |
| 60. | Kim KO, Kim TN, Lee HC. Effectiveness of combined biliary and duodenal stenting in patients with malignant biliary and duodenal obstruction. Scand J Gastroenterol. 2012;47:962-967. [PubMed] [DOI] |
| 61. | Kim K, Chie EK, Jang JY, Kim SW, Oh DY, Im SA, Kim TY, Bang YJ, Ha SW. Role of adjuvant chemoradiotherapy for duodenal cancer: a single center experience. Am J Clin Oncol. 2012;35:533-536. [PubMed] [DOI] |
| 62. | Lee SY, Lee JH, Hwang DW, Kim SC, Park KM, Lee YJ. Long-term outcomes in patients with duodenal adenocarcinoma. ANZ J Surg. 2013; May 8. [Epub ahead of print]. [PubMed] |
| 65. | He J, Ahuja N, Makary MA, Cameron JL, Eckhauser FE, Choti MA, Hruban RH, Pawlik TM, Wolfgang CL. 2564 resected periampullary adenocarcinomas at a single institution: trends over three decades. HPB (Oxford). 2014;16:83-90. [PubMed] [DOI] |