修回日期: 2014-06-25
接受日期: 2014-07-05
在线出版日期: 2014-08-28
目的: 探讨胰十二指肠切除术(pancreaticoduodenectomy, PD)的开腹行PD(open pancreaticoduodenectomy, OPD)和微创手术(minimally invasive pancreaticoduodenectomy, MIPD)的疗效的对比.
方法: 计算机检索在2014-03-31前在Medline、EMBASE、Science Direct、Springer link公开发关于PD的开腹和微创手术方法的疗效的文献, 按纳入排除标准由2位研究者独立进行文献筛选、资料提取和方法学质量评价后, 采用RevMan5.2.7软件进行Meta分析.
结果: 共纳入8篇文献进行系统评价, 包含MIPD 204例, OPD 419例. Meta分析结果显示: MIPD和OPD在术后围手术期并发症发生率、胰瘘发生率、术后胃排空障碍、胆瘘、术后出血、再手术、病死率及R0切除方面的差异无统计学意义(P>0.05); 在手术时间、术中出血量及术后住院时间的差异有统计学意义(P<0.05).
结论: MIPD能减少PD术后住院时间和术中出血量, 且围手术期并发症和术后病理诊断与传统的OPD基本无差异, 可以作为胰十二指肠切除术的常规术式, 值得临床的推广, 未来仍需要大样本、多中心、前瞻性随机对照的高质量的临床研究来进一步验证.
核心提示: 本研究发现, 在围手术期并发症发生率、胰瘘发生率、术后胃排空障碍、胆瘘、术后出血、再手术以及病死率方面, 微创手术和传统开腹手术基本无差异. 在术后病理诊断方面, 手术的R0切除率的差异也无统计学意义, 说明微创胰十二指肠切除术(pancreaticoduodenectomy, PD)的安全性和有效性和传统的开腹PD(open pancreaticoduodenectomy)差异不大.
引文著录: 李瑞阳, 黄强, 林先盛, 刘臣海, 杨骥, 胡俊, 汪超. 胰十二指肠切除术的开腹和微创手术方法疗效的比较. 世界华人消化杂志 2014; 22(24): 3690-3698
Revised: June 25, 2014
Accepted: July 5, 2014
Published online: August 28, 2014
AIM: To evaluate the safety and efficacy between minimally invasive pancreaticoduodenectomy and open pancreaticoduodenectomy.
METHODS: Medline, EMBASE, Science Direct and Springer link databases (till March 31, 2014) were searched by computer to collect the articles that compared the efficacy and safety of minimally invasive pancreaticoduodenectomy vs open pancreaticoduodenectomy. The trials were selected according to the inclusive and exclusive criteria, and the quality of the included trials was assessed. The data were extracted and analyzed using RevMan 5.2.7 software.
RESULTS: A total of 8 articles were included in the present meta-analysis. The meta-analysis showed that there were no significant differences in perioperative complications, mortality, pancreatic fistula, delayed gastric empty, postoperative hemorrhage, reoperation, mortality or R0 resection rate between the minimally invasive pancreaticoduodenectomy group and open pancreaticoduodenectomy group (P > 0.05). There were significant differences in operative time, estimated blood loss and length of hospital stays between the two groups (P < 0.05).
CONCLUSION: This meta-analysis indicates that minimally invasive pancreaticoduodenectomy is associated with shorter hospital stay and less estimated blood loss compared with open surgery, although there are no differences in preoperational complications or postoperative pathological diagnosis. Minimally invasive approach can be a reasonable alternative to laparotomy pancreaticoduodenectomy with potential advantages. Nevertheless, future large-volume, well-designed randomized control trials with extensive follow-up are awaited to confirm and update the findings of this analysis.
- Citation: Li RY, Huang Q, Lin XS, Liu CH, Yang J, Hu J, Wang C. Efficacy and safety of minimally invasive pancreaticoduodenectomy vs open pancreaticoduodenectomy: A systematic review and meta-analysis. Shijie Huaren Xiaohua Zazhi 2014; 22(24): 3690-3698
- URL: https://www.wjgnet.com/1009-3079/full/v22/i24/3690.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i24.3690
自从1935年, Whipple等[1]开展世界上第一例胰十二指肠切除术(pancreaticoduodenectomy, PD)后, PD即作为壶腹部周围肿瘤和某些良性疾病的标准术式, 现已经被各级医院广泛应用[2-4]. 目前最常见的术式是开腹行PD(open pancreaticoduodenectomy, OPD), 但术后创伤较大, 且并发症较高[3], 遂出现微创手术, 目前腔镜外科已经广泛地应用外科手术领域, 世界上第1例报道的腹腔镜胰十二指肠切除术(laparoscopic pancreaticoduodenectomy, LPD)在1994年[5], 紧接着2003年出现了机器人胰腺切除术(robotic pancreatectomy)[6]和机器人胰十二指肠切除术(robotic PD)[7]. 微创手术(minimally invasive pancreaticoduodenectomy, MIPD)现在已经成为目前的发展方向. 与传统的开放性手术相比, 微创手术更能降低患者术后的疼痛、恢复更快等. 目前对于传统开放手术和微创手术的选择, 存在着争议性, 并且已有相关病例对照研究比较MIPD和OPD的优缺点, 且病例数较少, 多为单中心研究, 为进一步明确两种手术的可行性和优缺点, 我们应用系统评价的方法评价两种手术的疗效和安全性的差异, 为临床提供循证医学证据.
计算机检索在2014-03-31前在Medline、EMBASE、Science Direct、Springer link公开发关于胰十二指肠切除术的开腹和微创手术方法的疗效的英文临床对照文献. 检索策略: 按照Cochrane协作网手工手册要求制定检索策略: 检索词为: "laparoscopic pancreaticoduodenectomy"、"duodenopancreatectomy"、"minimally invasive pancreaticoduodenectomy"、"robotic pancreaticoduodenectomy", 并对以上检索词采用不同策略检索, 并追查已经纳入文献或者综述文献的参考文献以尽可能全面收集资料.
1.2.1 文献纳入标准: (1)纳入研究应是2014-03-31前公开发表的英文文献; (2)文献中需要包含MIPD(本研究MIPD包括: 腹腔镜辅助胰十二指肠切除术、全腹腔镜下胰十二指肠切除术、机器人辅助胰十二指肠切除术、全机器人胰十二指肠切除术)和OPD组的基本情况和围手术期的相关指标的比较; (3)文献设计类型应是队列研究、病例对照研究或者随机对照研究; (4)前瞻性研究和回顾性研究予以纳入; (5)关于术后并发症的比较时需交代术后并发症的诊断标准.
1.2.2 文献排除标准: (1)无相关对比研究的研究; (2)方法学交代不健全的研究, 资料不全的研究, 重复发表或重复利用数据的研究取其中之一, 其他的不予纳入; (3)文献中未给出相关变量或指标说明或评价手术组和内镜组疗效的区别; (4)试验设计缺乏严格对照的文献、综述文献、个案报道等不予以纳入; (5)文献全文语言非英文书写的不予以纳入.
1.2.3 文献筛选及资料提取: 严格按照Cochrane协作组的系统评价文献筛选规范[8]和Meta分析报告规范PRISMA标准进行文献筛选[9], 由两位研究者独立阅读文献进行筛选, 整个筛选过程采用盲法. 先独立阅读所获文献的题目及摘要, 剔除明显不符合纳入标准的文献, 再对可能符合纳入标准的文献阅读全文, 以确定该文献是否真正符合纳入标准. 对筛选过程中有分歧而难以确定是否纳入的文献通过讨论或由第三个研究者决定其是否纳入. 两位研究人员独立地对符合纳入标准的试验进行资料提取(第一作者、发表年限、人群构成、研究类型等), 再填写资料提取表格, 并交叉核对提取的资料, 缺乏的资料通过于临床试验的通讯作者联系予以补充.
1.2.4 文献质量评估: 因该主题缺乏随机对照文献, 均为病例对照研究和队列研究, 故采用NOS量表(modified Newcastle-Ottawa scale)[10-13], 具体包含病例的选择、组间的可比性和术后并发症的评价. 评分分为0-9分, 其中≥6分视为高质量文献.
统计学处理 本文采用Cochrane协作网提供的RevMan5.2.7软件进行统计学分析. 显著性水平设定为P = 0.05, 用I2评估异质性大小, I2<25%提示有轻度异质性, I2在25%-75%之间提示中度异质性, I2>75%以上则提示明显异质性, 若存在异质性则进行亚组分析或者敏感性分析. 二项分类资料计算相对危险度(relative risk, RR)为合并统计量, 连续变量资料计算加权均数差(weighted mean difference, WMD)为合并统计量. 统计结果用95%可信区间(confidence interval, CI)表示, 以漏斗图(funnel plot model)判断发表偏倚. 纳入研究进行异质性检验, 异质性检验P>0.05时表示各研究间无明显异质性, 此时合并分析采用固定效应模型, 否则采用随机效应模型.
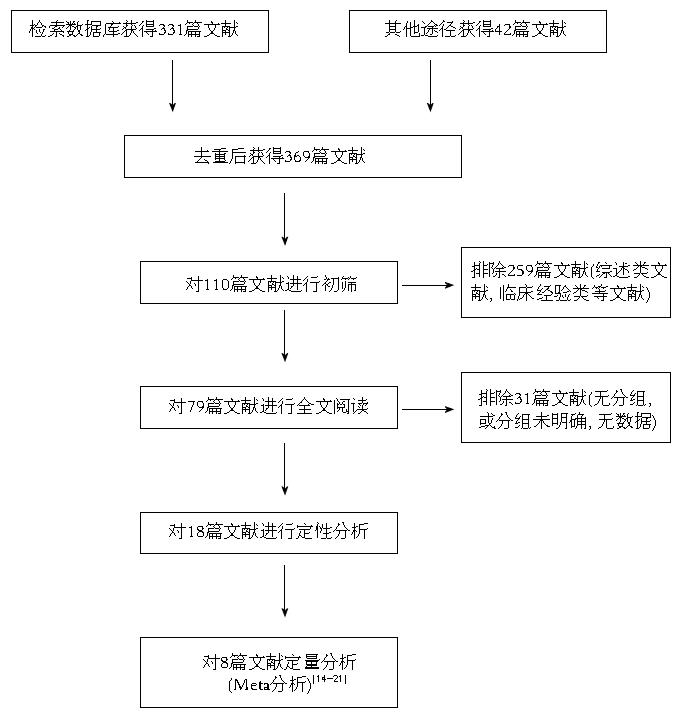
经严格按照纳入排除标准筛选后, 共纳入8篇研究[14-21], 纳入文献的基本情况详如表1. 其中5篇文献为前瞻性临床对照研究[14,16,19-21], 3篇回顾性病例对照研究[15,17,18], 全组中共包含MIPD例数204例, OPD数419例. 各研究中均交代两组之间的基本情况[年龄、性别、体质量指数(body mass index, BMI)指数: 差异无统计学意义, 具有可比性]和术后病理的具体情况. 各研究组间一般因素的基本情况如表2. 总文献筛选流程如图1.
| 纳入文献 | 国家 | 实验设计 | 纳入病例数(n) | |
| 微创组(LP/R) | 开腹(OPD) | |||
| Cho等[14]2009 | 日本 | 前瞻性研究 | LAPD: 15 | OPD: 15 |
| Buchs等[15]2011 | 美国 | 回顾性研究 | RTPD: 44 | OPD: 39 |
| Zhou等[16]2011 | 中国 | 前瞻性研究 | RTPD: 8 | OPD: 8 |
| Zureikat等[17]2011 | 美国 | 回顾性研究 | LTPD: 14 | OPD: 14 |
| Kuroki等[18]2012 | 日本 | 回顾性研究 | LAPD: 20 | OPD: 31 |
| Chalikonda等[19]2012 | 美国 | 前瞻性研究 | RAPD: 30 | OPD: 30 |
| Lai等[20]2012 | 中国香港 | 前瞻性研究 | RAPD: 20 | OPD: 67 |
| Asbun等[21]2012 | 美国 | 前瞻性研究 | LTPD: 53 | OPD: 215 |
| 合计 | 204 | 419 | ||
| 纳入文献 | 性别(男/女) | 年龄(岁) | NOS评分 | ||
| 微创组 | 开腹组 | 微创组 | 开腹组 | ||
| Cho等[14]2009 | 9/6 | 8/7 | 64.0±10.0 | 68.0±9.0 | 5 |
| Buchs等[15]2011 | 22/22 | 14/25 | 63.0±13.5 | 56.0±15.8 | 5 |
| Zhou等[16]2011 | 3/5 | 4/4 | 69.2±15.1 | 68.0±12.1 | 6 |
| Zureikat等[17]2011 | 11/3 | 7/7 | 69.8±10.2 | 67.4±11.0 | 6 |
| Kuroki等[18]2012 | 11/9 | 21/10 | 71.2±8.8 | 73.5±7.3 | 5 |
| Chalikonda等[19]2012 | 16/14 | 16/14 | 62.6±6.75 | 61.1±7.75 | 6 |
| Lai等[20]2012 | 12/8 | 29/38 | 66.4±11.9 | 62.1±12.1 | 6 |
| Asbun等[21]2012 | 29/24 | 95/120 | 62.9±14.14 | 67.3±11.53 | 7 |
严格按照NOS评分标准, 按照标准中的病例的选择、组间的可比性分析和术后并发症的评价方面, 对纳入文献进行综合评价, 具体评分如表2, 由表2可知, 平均分数为5.75分, 其中6分以上文献6篇, 剩余2篇文献评分5分, 主要是一般情况对比中未包含BMI以及ASA评分等. 总体文献的质量较高.
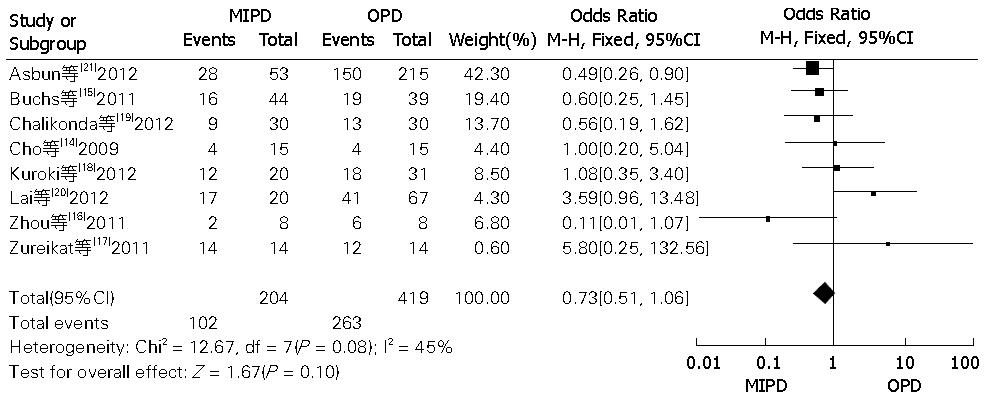
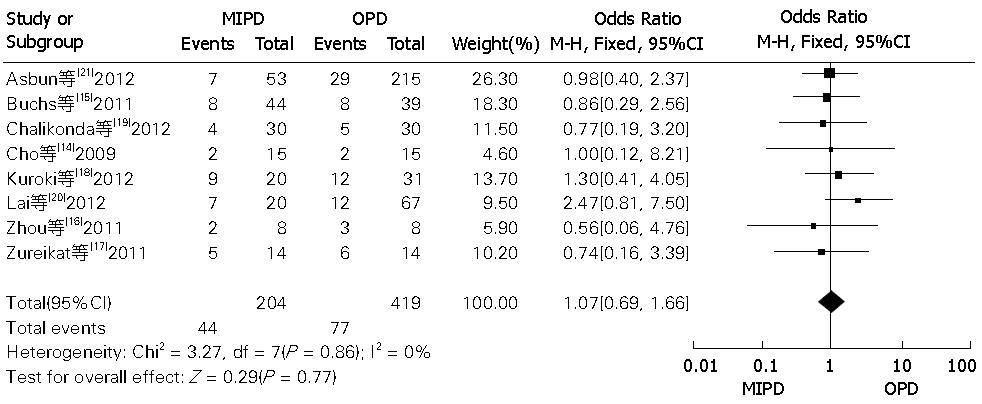
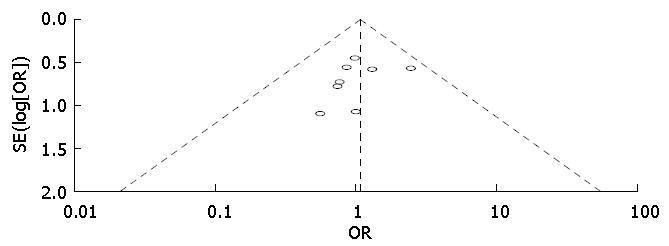
2.3.1 MIPD和OPD围手术期相关并发症的比较: 本组Meta分析中包含围手术期相关并发症(包括围手术期总并发症、术后胰瘘、术后胃排空障碍、术后出血发生率、术后胆瘘、再手术、病死率)的比较, MIPD和OPD术后相关并发症的比较的Meta分析如表3. 其中围手术期并发症发生率的森林图如图2, 术后胰瘘的发生率比较的森林图如图3. 由表3可知: MIPD与OPD比较, 围手术期并发症发生率、胰瘘发生率、术后胃排空障碍、胆瘘、术后出血、再手术以及病死率的差异无统计学意义(P>0.05), 说明MIPD并不能减少围手术期相关并发症的发生率. 其中围手术期总并发症的比较的漏斗图如图4, 从图4可以看出, 漏斗基本对称, 说明纳入文献的偏倚较少, 对结果影响较小.
| 比较项目 | 纳入文献 | MIPD | OPD | 异质性检验 | OR/WMD(95%CI) | ||
| I2(%) | P值 | 95%CI | P值 | ||||
| 围手术期并发症 | 14-21 | 204 | 419 | 45 | 0.08 | 0.73(0.51-1.06) | 0.10 |
| 胰瘘 | 14-21 | 204 | 419 | 0 | 0.86 | 1.07(0.69-1.66) | 0.77 |
| 胃排空障碍 | 14-21 | 204 | 419 | 0 | 0.90 | 0.90(0.49-1.68) | 0.75 |
| 胆瘘 | 15-17, 20, 21 | 139 | 343 | 4 | 0.38 | 0.93(0.35-2.49) | 0.89 |
| 出血 | 14-17, 20, 21 | 164 | 358 | 0 | 0.83 | 1.31(0.62-2.76) | 0.45 |
| 再手术 | 15-17, 19-21 | 169 | 373 | 0 | 0.53 | 0.56(0.26-1.20) | 0.14 |
| 病死率 | 15-17, 19-21 | 169 | 373 | 0 | 0.81 | 0.89(0.38-2.07) | 0.78 |
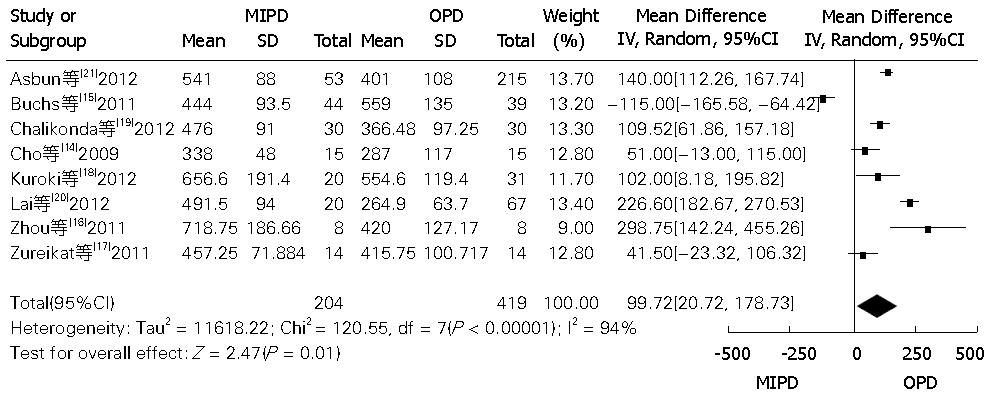
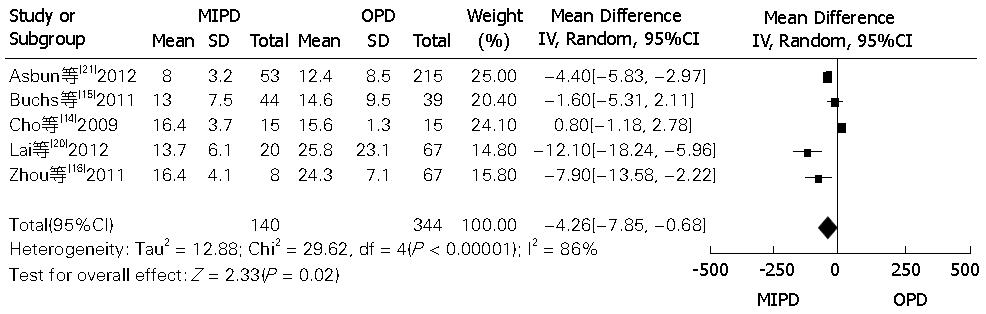
2.3.2 微创手术和开放手术手术时间、术中出血量和术后住院时间的比较: MIPD和OPD手术在术中手术时间、术中出血和术后住院时间的比较的Meta分析如表4. 其中手术时间和术后住院时间的比较的森林图如图5, 图6.
| 比较项目 | 纳入文献 | MIPD | OPD | 异质性检验 | WMD | ||
| I2(%) | P值 | 95%CI | P值 | ||||
| 手术时间 | 14-21 | 204 | 419 | 94 | <0.0001 | 99.72(20.72, 178.73) | 0.01 |
| 术中出血 | 14-16, 18-21 | 190 | 405 | 94 | <0.0001 | -393.75(-714.84, -72.30) | 0.02 |
| 术后住院时间 | 14-16, 20, 21 | 140 | 344 | 86 | <0.0001 | -4.26(-7.85, -0.68) | 0.02 |
由表4可知: MIPD和OPD在术中出血, 手术时间以及术后住院时间的差异有统计学意义(P<0.05). MIPD组在术中出血和术后住院时间较OPD时间短, 差异有统计学意义. 说明微创手术可以显著地缩短手术对于机体的打击和术中出血较少. 而MIDP组手术时间较长(P>0.05).
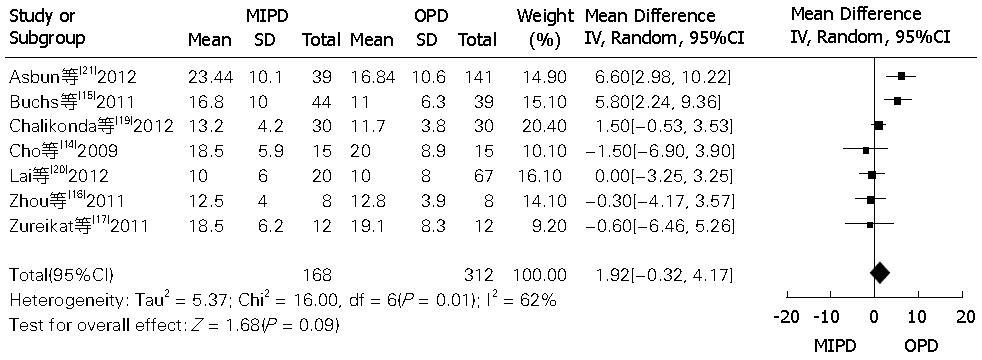
2.3.3 MIPD和OPD术后病理的比较: MIPD和OPD手术在术后标本病理的比较(包括手术的R0切除率和手术标本的淋巴结数目)分析如表5. 其中术后淋巴结数目的森林图如图7. 由表5可知, 术后病例的R0切除率和术后标本淋巴结数目的差异无统计学意义, 即是术后标本切除对于病理学检查无统计学意义. 手术方式对于术后诊断无明显差异.
| 比较项目 | 纳入文献 | MIPD | OPD | 异质性检验 | WMD | ||
| I2(%) | P值 | 95%CI | P值 | ||||
| R0切除率 | 14, 16, 17, 19-21 | 153 | 297 | 0 | 0.51 | 2.29(-0.55, 5.13) | 0.51 |
| 标本淋巴结数目 | 14-17, 19-21 | 168 | 312 | 62 | 0.01 | 1.92(-0.32, 4.17) | 0.09 |
随着近年来, 腔镜技术的进步, 目前微创外科已成为腹部外科的主要的发展方向, 尤其是在胰腺手术方面[22], 目前胰十二指肠切除术是腹腔镜外科手术中难度最大的手术, 目前国内开展的较少, 且可行性和安全性受到争议[23], 目前的微创PD包括: 腹腔镜(辅助)胰十二指肠切除术、机器人(辅助)胰十二指肠切除术. 本文即使用系统评价的方法, 来进一步明确胰十二指肠切除术的微创和传统开腹手术的区别. 系统评价结果显示: MIPD在围手术期并发症发生率、胰瘘发生率、术后胃排空障碍、胆瘘、术后出血、再手术以及病死率方面和OPD比较差异无统计学意义(P>0.05), 且术后标本的病理诊断和R0切除率的差异无统计学意义(P>0.05). 但是MIPD术中出血较传统的OPD少, 差异有统计学意义(P<0.05), 术后住院时间也较传统的OPD手术短(P<0.05). OPD的手术时间较MIPD短(P<0.05).
通过本研究可知, 在围手术期并发症发生率、胰瘘发生率、术后胃排空障碍、胆瘘、术后出血、再手术以及病死率方面, 微创手术和传统开腹手术基本无差异(P>0.05). 在术后病理诊断方面, 手术的R0切除率的差异也无统计学意义, 这说明微创PD的安全性和有效性和传统的开腹PD差异不大. 这也是微创PD得以普及的原因之一, 但是MIPD的主要的缺点是手术时间较长(P<0.05), 这主要是因为腔镜下操作的灵活性明显较开放手术下降, 镜头易被污染, 且一旦出血时止血困难, 腹腔镜下的缝合难度亦较大; 单个镜头视野涵盖结构少, 病灶难以辨别; 而且缺乏触觉, 无法提供更全面的探查信息等[23-26]. 这些缺点可能影响了MIPD的效率, 在使用相关器械时可能会减少手术术中的困难(如出血等), 但是会增加手术的费用[27-30]. 本研究也显示: MIPD手术的术中出血量较少, 术后的住院时间显著减少, 患者的生活质量随之提高. 术后住院时间较短、切口较小、手术出血较少、术后生活质量高等是微创胰十二指肠切除术的优点, 另外加上术后的并发症和病死率等方面与传统的开腹手术差异不大, 微创胰十二指肠切除术值得临床推广.
系统评价作为一种观察性研究[31], 有一定的局限性: (1)对于本研究的主要的局限性是因为缺乏随机对照研究, 所有纳入的研究均为临床病例对照研究, 因此可能无法提供强有力的数据来说明相关结果; (2)另外本文的局限性有于纳入不同国家地区的研究, 因此纳入研究的研究对象的差异不可避免, 存在选择偏倚, 参加对象的人群特征如发病率等不同, 和腹腔镜的技术和操作者的技术经验也不尽相同, 这可能影响了试验的结果; (3)纳入研究的病例数较少, 这也会影响数据的可靠性; (4)由于本文的纳入文献选择仅为英文文献, 可能存在文献选择的偏倚, 影响试验结果; (5)纳入文献未介绍了相关的预后和随访, 这也可能影响 试验结果.
总之, 微创外科手术已经成为目前腹部外科的主要发展方向, 因此基于目前的研究结果, MIPD能减少PD术后住院时间和术中出血量, 且术后并发症和术后病理诊断与传统的OPD基本无差异, 可以作为胰十二指肠切除术的常规术式, 值得临床的推广. 但是未来仍需要大样本、多中心、前瞻性随机对照试验、包含预后的高质量的关于PD的微创和开腹手术的研究.
胰十二指肠切除术(pancreaticoduodenectomy, PD)作为腹部外科最大的手术, 是壶腹部周围肿瘤和某些良性疾病的标准术式, 目前的手术方式主要是开腹手术, 随着科学技术的发展, 腹腔镜和微创手术逐渐成为未来手术的发展方向, 微创手术和开腹手术各有优缺点, 存在争议, 目前尚无相关系统评价对两种手术方式进行比较.
薛东波, 教授, 哈尔滨医科大学附属第一医院
由于目前尚无文献系统性文献来评价微创小切口行胰十二指肠切除术和传统开腹胰十二指肠切除术的优缺点, 因此本文应用循证医学的方法来比较两种不同术式的差异性, 为临床选择提供证据.
目前认为, 开腹胰十二指肠切除术手术安全性较高, 但术后的创伤大、高并发症等特点使之成为腹部外科难度最大的手术之一, 随着科学技术的发展, 微创手术, 如腹腔镜胰十二指肠切除术、机器人辅助胰十二指肠切除术等, 其术后创伤较小, 术后生存质量高等特点, 这是目前外科手术的发展方向.
本文采用系统评价的方法将胰十二指肠切除术的两种手术方法做比较, 为临床的治疗方法的选择提供建议.
本研究提示, 微创小切口胰十二指肠切除术能显著减少术后的住院时间和书中出血量, 术后生存率较高, 且其围手术期并发症和术后病理诊断与传统开腹手术差异不大, 可以作为胰十二指肠切除术的常规手术术式, 值得临床推广.
微创小切口胰十二指肠切除术(minimally Invasive pancreaticoduodenectomy, MIPD): 应用微创切口方式进行胰十二指肠切除术, 目前主要包含全腹腔镜下胰十二指肠切除术、腹腔镜辅助胰十二指肠切除术、全机器人胰十二指肠切除术、机器人辅助胰十二指肠切除术.
本文通过循证医学的方法来探讨胰十二指肠切除术的两种手术方式的比较, 理论依据及临床论证充足, 有统计价值, 有临床应用价值.
编辑: 郭鹏 电编:闫晋利
| 1. | Whipple AO, Parsons WB, Mullins CR. TREATMENT OF CARCINOMA OF THE AMPULLA OF VATER. Ann Surg. 1935;102:763-779. [PubMed] [DOI] |
| 2. | Cameron JL, Pitt HA, Yeo CJ, Lillemoe KD, Kaufman HS, Coleman J. One hundred and forty-five consecutive pancreaticoduodenectomies without mortality. Ann Surg. 1993;217:430-435; discussion 435-438. [PubMed] [DOI] |
| 3. | Winter JM, Cameron JL, Campbell KA, Arnold MA, Chang DC, Coleman J, Hodgin MB, Sauter PK, Hruban RH, Riall TS. 1423 pancreaticoduodenectomies for pancreatic cancer: A single-institution experience. J Gastrointest Surg. 2006;10:1199-1210; discussion 1210-1211. [PubMed] [DOI] |
| 4. | McPhee JT, Hill JS, Whalen GF, Zayaruzny M, Litwin DE, Sullivan ME, Anderson FA, Tseng JF. Perioperative mortality for pancreatectomy: a national perspective. Ann Surg. 2007;246:246-253. [PubMed] [DOI] |
| 5. | Gagner M, Pomp A. Laparoscopic pylorus-preserving pancreatoduodenectomy. Surg Endosc. 1994;8:408-410. [PubMed] [DOI] |
| 6. | Melvin WS, Needleman BJ, Krause KR, Ellison EC. Robotic resection of pancreatic neuroendocrine tumor. J Laparoendosc Adv Surg Tech A. 2003;13:33-36. [PubMed] [DOI] |
| 7. | Giulianotti PC, Coratti A, Angelini M, Sbrana F, Cecconi S, Balestracci T, Caravaglios G. Robotics in general surgery: personal experience in a large community hospital. Arch Surg. 2003;138:777-784. [PubMed] |
| 8. | Higgins JPT, Green S. Cochrane Handbook for Systematic Reviews of Interventions. Version 5.1.0. Oxford. UK: The Cochrane Collaboration 2011; 115-135. |
| 9. | Moher D, Liberati A, Tetzlaff J, Altman DG. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement. Int J Surg. 2010;8:336-341. [PubMed] |
| 11. | Taggart DP, D'Amico R, Altman DG. Effect of arterial revascularisation on survival: a systematic review of studies comparing bilateral and single internal mammary arteries. Lancet. 2001;358:870-875. [PubMed] [DOI] |
| 13. | Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses. Eur J Epidemiol. 2010;25:603-605. [PubMed] [DOI] |
| 14. | Cho A, Yamamoto H, Nagata M, Takiguchi N, Shimada H, Kainuma O, Souda H, Gunji H, Miyazaki A, Ikeda A. Comparison of laparoscopy-assisted and open pylorus-preserving pancreaticoduodenectomy for periampullary disease. Am J Surg. 2009;198:445-449. [PubMed] [DOI] |
| 15. | Buchs NC, Addeo P, Bianco FM, Ayloo S, Benedetti E, Giulianotti PC. Robotic versus open pancreaticoduodenectomy: a comparative study at a single institution. World J Surg. 2011;35:2739-2746. [PubMed] [DOI] |
| 16. | Zhou NX, Chen JZ, Liu Q, Zhang X, Wang Z, Ren S, Chen XF. Outcomes of pancreatoduodenectomy with robotic surgery versus open surgery. Int J Med Robot. 2011;7:131-137. [PubMed] [DOI] |
| 17. | Zureikat AH, Breaux JA, Steel JL, Hughes SJ. Can laparoscopic pancreaticoduodenectomy be safely implemented? J Gastrointest Surg. 2011;15:1151-1157. [PubMed] [DOI] |
| 18. | Kuroki T, Adachi T, Okamoto T, Kanematsu T. A non-randomized comparative study of laparoscopy-assisted pancreaticoduodenectomy and open pancreaticoduodenectomy. Hepatogastroenterology. 2012;59:570-573. [PubMed] |
| 19. | Chalikonda S, Aguilar-Saavedra JR, Walsh RM. Laparoscopic robotic-assisted pancreaticoduodenectomy: a case-matched comparison with open resection. Surg Endosc. 2012;26:2397-2402. [PubMed] [DOI] |
| 20. | Lai EC, Yang GP, Tang CN. Robot-assisted laparoscopic pancreaticoduodenectomy versus open pancreaticoduodenectomy--a comparative study. Int J Surg. 2012;10:475-479. [PubMed] [DOI] |
| 21. | Asbun HJ, Stauffer JA. Laparoscopic vs open pancreaticoduodenectomy: overall outcomes and severity of complications using the Accordion Severity Grading System. J Am Coll Surg. 2012;215:810-819. [PubMed] [DOI] |
| 22. | Briggs CD, Mann CD, Irving GR, Neal CP, Peterson M, Cameron IC, Berry DP. Systematic review of minimally invasive pancreatic resection. J Gastrointest Surg. 2009;13:1129-1137. [PubMed] [DOI] |
| 24. | Corcione F, Pirozzi F, Cuccurullo D, Piccolboni D, Caracino V, Galante F, Cusano D, Sciuto A. Laparoscopic pancreaticoduodenectomy: experience of 22 cases. Surg Endosc. 2013;27:2131-2136. [PubMed] [DOI] |
| 25. | Nguyen KT, Zureikat AH, Chalikonda S, Bartlett DL, Moser AJ, Zeh HJ. Technical aspects of robotic-assisted pancreaticoduodenectomy (RAPD). J Gastrointest Surg. 2011;15:870-875. [PubMed] [DOI] |
| 26. | Mesleh MG, Stauffer JA, Bowers SP, Asbun HJ. Cost analysis of open and laparoscopic pancreaticoduodenectomy: a single institution comparison. Surg Endosc. 2013;27:4518-4523. [PubMed] [DOI] |
| 27. | Winer J, Can MF, Bartlett DL, Zeh HJ, Zureikat AH. The current state of robotic-assisted pancreatic surgery. Nat Rev Gastroenterol Hepatol. 2012;9:468-476. [PubMed] [DOI] |
| 28. | Kang CM, Choi SH, Hwang HK, Lee WJ, Chi HS. Minimally invasive (laparoscopic and robot-assisted) approach for solid pseudopapillary tumor of the distal pancreas: a single-center experience. J Hepatobiliary Pancreat Sci. 2011;18:87-93. [PubMed] [DOI] |
| 29. | Schmidt CM, Turrini O, Parikh P, House MG, Zyromski NJ, Nakeeb A, Howard TJ, Pitt HA, Lillemoe KD. Effect of hospital volume, surgeon experience, and surgeon volume on patient outcomes after pancreaticoduodenectomy: a single-institution experience. Arch Surg. 2010;145:634-640. [PubMed] [DOI] |
| 30. | D'Annibale A, Orsini C, Morpurgo E, Sovernigo G. [Robotic surgery: considerations after 250 procedures]. Chir Ital. 2006;58:5-14. [PubMed] |
| 31. | Longnecker MP. Re: "Point/counterpoint: meta-analysis of observational studies". Am J Epidemiol. 1995;142:779-782. [PubMed] |