修回日期: 2014-05-10
接受日期: 2014-05-19
在线出版日期: 2014-07-28
目的: 观察RhoGTP酶解离抑制蛋白2(RhoGTPase dissociation inhibitor 2, RhoGDI2)、细胞因子诱导的凋亡抑制因子1(cytokine-induced apoptosis inhibitor 1, CIAPIN1)在胃癌患者组织中的表达状况, 并评价其与胃癌临床病理特征的相关性, 分析两者表达相关性.
方法: 采用免疫组织化学技术检测94例胃癌组织中RhoGDI2、CIAPIN1的表达状况, 并分析两者表达相关性.
结果: 胃癌组织中RhoGDI2和CIAPIN1蛋白表达阳性率分别为67.02%、77.66%; RhoGDI2和CIAPIN1在胃癌中的蛋白表达与胃癌分化程度、肿瘤浸润深度、淋巴结转移个数、有无远处转移和TNM分期显著相关; RhoGDI2与CIAPIN1的表达正相关.
结论: 胃癌组织RhoGDI2、CIAPIN1的蛋白表达水平密切相关. CIAPIN1极可能受到Rho-GDI2的调控, 为RhoGDI2在胃癌浸润转移过程中的下游靶点基因, 两者很可能共同参与调节胃癌的侵袭转移过程.
核心提示: RhoGTP酶解离抑制蛋白2(RhoGTPase dissociation inhibitor 2, RhoGDI2)及其疑似下游靶点基因细胞因子诱导的凋亡抑制因子1(cytokine-induced apoptosis inhibitor 1, CIAPIN1)在大多数胃癌组织中的蛋白表达水平均较在胃正常黏膜组织中升高, 且与各项临床病理特征(胃癌分化程度、浸润深度、淋巴结转移、远处转移和TNM分期)密切相关. RhoGDI2与CIAPIN1的表达正相关. 综合以上研究结果, 揭示胃癌组织RhoGDI2和CIAPIN1的表达与肿瘤侵袭转移有关, CIAPIN1极可能是RhoGDI2在肿瘤浸润转移过程中直接的下游调控靶基因.
引文著录: 石干, 廖家智, 何星星, 孙圣斌, 黄曼玲, 杨静, 吴杰. 胃癌中RhoGDI2、CIAPIN1的原位表达及其相关性. 世界华人消化杂志 2014; 22(21): 3106-3112
Revised: May 10, 2014
Accepted: May 19, 2014
Published online: July 28, 2014
AIM: To detect the expression of RhoGTPase dissociation inhibitor 2 (RhoGDI2) and cytokine-induced apoptosis inhibitor 1 (CIAPIN1) in gastric cancer and to analyze their clinical significance.
METHODS: Immunohistochemistry was used to detect the expression of RhoGDI2 and CIAPIN1 in 94 gastric cancer specimens.
RESULTS: The positive rates of RhoGDI2 and CIAPIN1 in gastric cancer were 67.02% and 77.66%, respectively. The expression of RhoGDI2 and CIAPIN1 was related to tumor differentiation, depth of invasion, lymph node metastasis, distant metastasis and TNM stage in gastric cancer. There was a positive correlation between the expression of RhoGDI2 and that of CIAPIN1.
CONCLUSION: The expression of RhoGDI2 is correlated with that of CIAPIN1 in gastric cancer. CIAPIN1 is very likely to be regulated by RhoGDI2, and functions as a downstream target gene of RhoGDI2 in tumor invasion and metastasis. Both of them may be involved in regulating the invasion and metastasis of gastric cancer.
- Citation: Shi G, Liao JZ, He XX, Sun SB, Huang ML, Yang J, Wu J. Expression of RhoGDI2 and CIAPIN1 in gastric carcinoma. Shijie Huaren Xiaohua Zazhi 2014; 22(21): 3106-3112
- URL: https://www.wjgnet.com/1009-3079/full/v22/i21/3106.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v22.i21.3106
在我国, 胃癌死亡人数居恶性肿瘤的首位, 其5年生存率很低. 肿瘤转移是致使胃癌患者死亡的主要原因. 研究胃癌发生及转移相关机制具有重要意义. RhoGTP酶解离抑制蛋白2(RhoGTPase dissociation inhibitor 2, RhoGDI2)是新近发现的一种肿瘤转移抑制基因, 能下调处于活化状态的Rho家族GTP酶的活性. 在各种人类肿瘤的发生发展过程中, RhoGDI2的表达水平各异[1]. RhoGDI2能够促进或抑制肿瘤的侵袭和转移, 不同类型的肿瘤中他的表达水平及功能都不同[2]. 现今国内外有关RhoGDI2在胃癌中的研究报道甚少. 我们先前的研究检测到RhoGDI2在胃癌组织中呈高表达状态[3]. 细胞因子诱导的凋亡抑制因子1(cytokine-induced apoptosis inhibitor 1, CIAPIN1)是一种新近被证实与肿瘤凋亡和多药耐药相关的基因, 最近有报道显示在RhoGDI2过表达的SNU-484胃癌细胞株中通过沉默CIAPIN1基因表达能显著抑制肿瘤的侵袭[4], 初步揭示CIAPIN1与胃癌侵袭也有关联. 我们据此推测CIAPIN1极可能受RhoGDI2的调控, 为RhoGDI2介导的胃癌细胞侵袭过程中的下游靶蛋白之一. 目前国内外尚无联合检测RhoGDI2和CIAPIN1在胃癌组织中蛋白水平的表达状况及两基因相关性的文献报道, 本研究通过免疫组织化学方法, 分别对94例胃癌患者组织中RhoGDI2和CIAPIN1蛋白水平的表达状况进行检测, 初步探讨RhoGDI2与CIAPIN1之间的表达相关性及其与各项临床病理特征之间的关系.
选择2013-01/2014-01于华中科技大学同济医学院附属武汉市中心医院的胃癌住院患者94例, 经消化内镜中心胃镜活检获取. 统计其性别、年龄、肿瘤位置、原发灶直径和组织学分级等资料, 记录其住院病历诊疗资料、后续胃癌手术术中所见、临床分期(肿瘤浸润深度、有无淋巴结转移及远处转移)并进行统计分析. 胃镜检查活检前所有患者均未行放化疗. 本研究经华中科技大学同济医学院伦理委员会批准, 履行告知义务并获患者知情同意. 具体入组病例临床资料分类如表1. 另选取非肿瘤胃组织标本(手术切除新鲜胃癌组织癌旁5 cm组织)24例做对照组, 病理结果示"黏膜呈轻度慢性炎症改变"或"正常胃黏膜表现". 胃癌TNM分期采用AJCC标准(2010). 一抗兔抗人多克隆抗体RhoGDl2(#ab15198)、兔抗人多克隆抗体CIAPIN1(#BC2568)、EliviSionTM plus试剂盒(#40405a)、DAB显色试剂盒(#ARl022)均购自武汉博士德生物技术公司.
| 临床病理特征 | n | CIAPIN1蛋白 | RhoGDI2蛋白 | ||||||
| + | 阳性率(%) | χ2值 | P值 | + | 阳性率(%) | χ2值 | P值 | ||
| 性别 | 0.83 | >0.05 | 1.06 | >0.05 | |||||
| 男 | 57 | 42 | 73.68 | 44 | 77.19 | ||||
| 女 | 37 | 24 | 64.86 | 25 | 67.57 | ||||
| 年龄(岁) | 0.18 | >0.05 | 0.08 | >0.05 | |||||
| <60 | 33 | 23 | 69.70 | 24 | 72.73 | ||||
| ≥60 | 61 | 45 | 73.77 | 46 | 75.41 | ||||
| 肿瘤位置 | 0.34 | >0.05 | 3.67 | >0.05 | |||||
| 贲门胃底 | 21 | 16 | 76.19 | 18 | 85.71 | ||||
| 胃体 | 24 | 17 | 70.83 | 16 | 66.67 | ||||
| 胃角 | 23 | 16 | 69.57 | 17 | 73.91 | ||||
| 胃窦 | 26 | 18 | 69.23 | 16 | 61.53 | ||||
| 原发灶直径(cm) | 0.15 | >0.05 | 3.23 | >0.05 | |||||
| <5 | 52 | 39 | 75.00 | 42 | 80.77 | ||||
| ≥5 | 42 | 30 | 71.43 | 27 | 64.29 | ||||
| 组织学分级 | 5.20 | <0.05 | 11.83 | <0.05 | |||||
| 高-中分化 | 37 | 18 | 48.65 | 19 | 51.35 | ||||
| 低分化 | 57 | 41 | 71.93 | 48 | 84.21 | ||||
| 原发灶分期 | 7.44 | <0.05 | 13.65 | <0.05 | |||||
| T1-2 | 34 | 16 | 47.06 | 16 | 47.06 | ||||
| T3-4 | 60 | 45 | 75.00 | 50 | 83.33 | ||||
| 淋巴结转移 | 3.97 | <0.05 | 5.35 | <0.05 | |||||
| N0 | 7 | 3 | 42.86 | 4 | 57.14 | ||||
| N1+N2+N3 | 87 | 67 | 77.01 | 77 | 88.51 | ||||
| 远处转移 | 7.30 | <0.05 | 8.49 | <0.05 | |||||
| M0 | 23 | 11 | 47.83 | 10 | 43.48 | ||||
| M1 | 71 | 55 | 77.46 | 54 | 76.06 | ||||
| 临床分期 | 6.40 | <0.05 | 7.25 | <0.05 | |||||
| Ⅰ+Ⅱ | 46 | 24 | 52.17 | 28 | 60.87 | ||||
| Ⅲ+Ⅳ | 48 | 37 | 70.83 | 41 | 85.42 | ||||
1.2.1 免疫组织化学染色检测(EliviSionTM plus): 切片脱蜡, 乙醇脱水, 水洗; 3%H2O2去离子水避光孵育15 min, PBS洗涤3次, 每次5 min; 热修复抗原; 擦干边缘水分, 滴加0.3%Triton X-100, 37 ℃温盒孵育后PBS洗3次, 每次5 min; 滴加BSA封闭液, 室温下孵育20 min, 滴加一抗(1:200), 4 ℃过夜; PBS洗3次, 每次5 min; 滴加聚合物增强剂(试剂A), 室温孵育20 min, PBS洗3次, 每次5 min; 滴加酶标羊抗鼠聚合物(试剂B), 室温孵育, PBS洗3次, 每次5 min; 新鲜配制DAB显色, 蒸馏水洗涤; 苏木素复染, 0.1%盐酸分化, PBS返蓝, 自来水冲洗; 梯度乙醇脱水干燥, 二甲苯透明, 中性树胶封片. 将已知的阳性切片作为阳性对照, 以PBS代替一抗作阴性对照. RhoGDI2阳性细胞为棕色或黄色, 阳性颗粒均定位于细胞胞浆或细胞胞核. CIAPIN1阳性细胞为棕色或黄色, 阳性颗粒均定位于细胞胞浆.
1.2.2 免疫组织化学染色结果评定: 所有切片采用盲法, 由两位病理科医生独立阅片, 每个样本均选择3张切片, 采用十字分区法取5个不同视野(×200倍), 至少计数800-1000个细胞. 参照Remmele和Stegner提出的免疫反应积分(IRS)评分法[5], 观察染色强度, 计数免疫组织化学标记准确定位的阳性细胞占显微镜视野内细胞数的比例并计分, 将二者计分的乘积作为最后结果.
统计学处理 采用SPSS18.0软件进行χ2检验, P<0.05为差异有统计学意义.
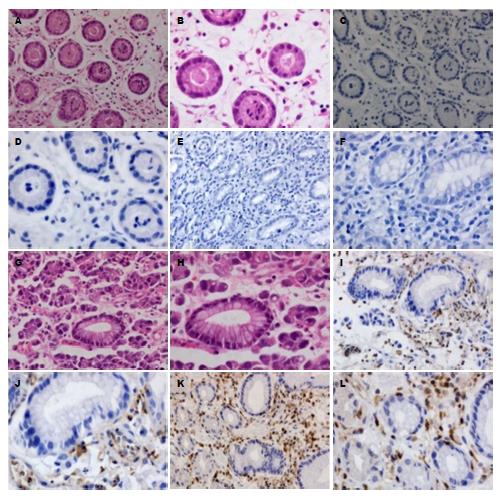
肿瘤细胞为RhoGDI2的阳性表达细胞, 主要位于胞浆或胞核. 其在胃癌组织中表达率为67.02%(63/94), 在非癌胃组织(病理结果示"黏膜呈轻度慢性炎症改变"或"正常胃黏膜表现")中表达率为16.67%(4/24), 差异有统计学意义(χ2 = 19.75, P<0.01); 低分化型胃癌组显著高于高-中分化型胃癌组(χ2 = 11.83, P<0.05); 随浸润深度(分别浸润至黏膜层、黏膜下层、肌层、浆膜层)增加, RhoGDI2的表达率增加(χ2 = 13.65, P<0.05); 淋巴结转移组显著高于无转移组(χ2 = 5.35, P<0.05); 远处转移组显著高于无转移组(χ2 = 8.49, P<0.05); 临床分期Ⅲ+Ⅳ期组明显高于Ⅰ+Ⅱ期组(χ2 = 7.25, P<0.05). RhoGDI2表达与性别、年龄、肿瘤部位、原发灶大小无相关性(P>0.05)(表1, 图1).
肿瘤细胞为CIAPIN1的阳性表达细胞, 主要位于胞浆. CIAPIN1在胃癌组织表达率为77.66%(73/94), 在非癌胃组织(病理结果示"黏膜呈轻度慢性炎症改变"或"正常胃黏膜表现")中表达率为12.50%(3/24), 差异有统计学意义(χ2 = 35.41, P<0.05); 低分化型胃癌组显著高于高-中分化型胃癌组(χ2 = 5.20, P<0.05); 随浸润深度(分别浸润至黏膜层、黏膜下层、肌层、浆膜层)增加, CIAPIN1的表达率增加(χ2 = 7.44, P<0.05); 淋巴结转移组显著高于无转移组(χ2 = 3.97, P<0.05); 远处转移组显著高于无转移组(χ2 = 7.30, P<0.05); 临床分期Ⅲ+Ⅳ期组明显高于Ⅰ+Ⅱ期组(χ2 = 6.40, P<0.05). CIAPIN1表达与性别、年龄、肿瘤部位、原发灶大小无相关性(P>0.05)(表1, 图1).
我国的胃癌死亡人数及发病率居恶性肿瘤的首位, 而胃癌患者致死的主要原因是肿瘤侵袭转移. 胃癌侵袭转移过程中涉及许多特殊基因, 包括促进转移的转移基因和控制转移的转移抑制基因. 有关胃癌侵袭转移的分子机制尚未完全阐明, 寻找及研究胃癌侵袭转移相关基因在胃癌侵袭转移过程中的表达变化与分子机制, 可以加深我们对于胃癌侵袭转移调控机制的理解和认识, 同时也为胃癌侵袭转移的早期诊断和靶向干预提供理论基础. RhoGDI2是一种肿瘤转移抑制基因, 也是一种"非传统意义上"的肿瘤转移抑制基因, 近两年有研究显示: RhoGDI2能够促进或抑制肿瘤的侵袭和转移, 在不同类型的肿瘤中其表达水平和功能不同[6]. 曾有报道RhoGDI2在膀胱癌[7]、肺癌[8]以及霍奇金淋巴瘤中[9]表达下调, 也有研究提示RhoGDI2在卵巢癌[10,11]、白血病[12]和胃癌[13]等组织中表达上调. 国内外关于胃癌中RhoGDI2的相关研究报道甚少. 2009年Cho等[13]通过对小样本量胃癌组织检测后发现, RhoGDI2在正常胃黏膜组织中低表达或不表达, 而在进展期胃癌组织中高表达, 且与淋巴转移明显相关. 我们先前的一项大样本量研究也观测到胃癌组织中RhoGDI2高表达, 其在胃癌细胞的细胞核或细胞浆内均有表达, RhoGDI2能够正向调控胃癌的侵润转移[3].
最近Cho等[4]发现在RhoGDI2过表达的SNU-484胃癌细胞株中, 通过使CIAPIN1基因沉默表达后, 能明显抑制胃癌细胞株的侵润生长, 从侧面推断CIAPIN1蛋白在RhoGDI2介导胃癌细胞侵润生长过程中可能具有特殊意义, 初步揭示CIAPIN1是一种与胃癌侵袭转移相关的重要基因, 可能是与RhoGDI2相关的胃癌侵袭转移过程中重要的下游靶基因之一. 该研究不足之处在于: 未继续深入将RhoGDI2与CIAPIN1在蛋白水平的表达进行进一步分析检测, 证实两者的表达相关性, 从而进一步阐明两者在胃癌侵润转移分子调控机制中的上下游关系. 细胞因子诱导的凋亡抑制因子1又名Anamorsin、V62, 是一种新近被证实与肿瘤凋亡和多药耐药相关的分子. 其基本生物学功能尚不明确, CIAPIN1基因在不同组织器官来源的肿瘤组织及肿瘤细胞株的表达水平不一致. 在肺癌[14]、肾透明细胞癌组织[15]、食管鳞癌组织[16]及结肠癌组织[17], CIAPIN1基因的表达水平较正常组织显著减少或无表达. 曾有报道显示, 通过小干扰RNA(small interfering RNA, siRNA)技术使CIAPIN1高表达的肿瘤细胞株基因表达沉默后, 可抑制肿瘤细胞株的增殖[18]. 也有研究表明, 将CIAPIN1高表达的肝细胞癌(hepatocellular carcinoma, HCC)细胞系BEL7402、SMMC-7721、HepG2、HHCC的CIAPIN1基因敲除, 结果HCC细胞周期受抑于S期, 从而抑制HCC细胞的增殖; 采用siRNA/CIAPIN技术抑制SMMC-7721的肿瘤活性后直接种植于裸鼠HCC能明显抑制肿瘤的生长[19]. 目前鲜见有关于CIAPIN1在胃癌中的报道.
胃癌的侵袭、转移是肿瘤细胞和宿主细胞相互发生作用的连续过程, 也是多因素、多环节参与的结果. 目前已证实在不同类型的肿瘤中RhoGDI2的表达水平不同; 而且, CIAPIN1在不同组织来源的肿瘤组织表达水平各异, 在不同肿瘤的发生发展及增殖凋亡过程中发挥着不同作用. 现今国内外尚无有关于RhoGDI2和CIAPIN1在胃癌组织中蛋白水平的表达及二者间相关性的文献报道, 本实验通过免疫组织化学方法, 分别对94例胃癌组织中RhoGDI2和CIAPIN1的蛋白表达水平进行了检测, 结果发现, RhoGDI2和CIAPIN1蛋白在大多数胃癌组织中的表达水平均较正常黏膜组织中的表达水平高, 且与胃癌的分化程度、浸润深度、淋巴结转移、远处转移和TNM分期有关: 组织分化程度较高、肿瘤浸润较浅、没有淋巴结转移及远处转移、临床分期较早的患者, RhoGDI2和CIAPIN1蛋白表达水平较低; 而组织分化程度较高、肿瘤浸润较深、存在淋巴结转移及远处转移、临床分期较晚的患者, RhoGDI2和CIAPIN1蛋白表达水平较高; RhoGDI2与CIAPIN1表达水平呈正相关. 以上研究结果表明RhoGDI2和CIAPIN1蛋白的表达存在相关性, CIAPIN1极有可能是RhoGDI2在调控胃癌发生发展过程中重要的下游靶基因, CIAPIN1的表达受到RhoGDI2的直接调控, 两者很可能在促进胃癌侵袭转移过程中共同发挥着重要作用.
总之, 胃癌组织中RhoGDI2、CIAPIN1表达水平与肿瘤侵袭转移过程密切相关; CIAPIN1的表达受到RhoGDI2的直接调控, 极可能是RhoGDI2在调控胃癌发生发展过程中重要的下游靶点. CIAPIN1基因的生物学功能尚不明确, 内源性和外源性CIAPIN1基因可能发挥着不同功能, CIAPIN1在胃癌侵袭转移过程中的高表达可能与多因素、多基因相关. 对胃癌RhoGDI2及其上下游调控基因展开进一步研究有助于寻找潜在的抑制肿瘤侵袭转移的干预靶点, 从而给未来肿瘤的靶向治疗带来新的希望.
RhoGTP酶解离抑制蛋白2(RhoGTPase dissociation inhibitor 2, Rho-GDI2)是近年来发现的一种肿瘤转移抑制基因. 在不同类型的肿瘤中, RhoGDI2表达水平不同, 也发挥着促进或抑制肿瘤侵袭和转移的不同功用. 我们之前的研究观测到RhoGDI2在胃癌中蛋白表达水平升高, 而国内外尚无有关联合对RhoGDI2和细胞因子诱导的凋亡抑制因子1(cytokine-induced apoptosis inhibitor 1, CIAPIN1)在胃癌组织中蛋白水平的表达及二者间相关性的研究报道.
张小晋, 主任医师, 北京积水潭医院
通过基因芯片技术对转染Rho-GDI2前后胃癌细胞的差异表达基因展开分析, 进一步研究RhoGDI2调控CIAPIN1的分子机制, 亦可发现RhoGDI2在调节胃癌细胞侵袭转移过程中相关的其他上下游调控基因靶点.
2012年Cho等发现在RhoGDI2过表达的SNU-484胃癌细胞株中通过沉默CIAPIN1基因能显著抑制肿瘤的侵袭, 一定程度上说明CIAPIN1蛋白在RhoGDI2介导胃癌细胞侵袭过程中具有重要意义, 初次揭示CIAPIN1是与胃癌侵袭相关的重要基因, 可能为RhoGDI2介导的胃癌细胞侵袭过程中重要的下游靶蛋白之一. 但该研究未进一步对RhoGDI2与CIAPIN1的表达就组织及蛋白水平展开比较研究.
在此前研究基础上, 通过本实验我们首次对胃癌RhoGDI2、CIAPIN1的蛋白表达水平进行联合检测, 并研究其表达相关性. 结果表明, RhoGDI2、CIAPIN1在大多数胃癌组织中的蛋白表达水平均较在胃正常黏膜组织中升高, 且与胃癌分化程度、浸润深度、淋巴结转移、远处转移和TNM分期密切相关; RhoGDI2、CIAPIN1表达呈正相关.
对RhoGDI2的疑似上下游靶点基因(如: CIAPIN1等)及其在肿瘤发生发展过程中的调控机制进行后续研究, 有望发掘出更多相关基因, 从而通过抑制肿瘤侵袭转移的相关干预靶点, 为未来开发治疗肿瘤药物提供新的策略.
本文为后续研究RhoGDI2的其他上下游基因及其调控机制打下了基础, 也为未来临床肿瘤治疗药物的开发提供了新的思路.
编辑 田滢 电编 都珍珍
| 1. | Smith SC, Theodorescu D. Learning therapeutic lessons from metastasis suppressor proteins. Nat Rev Cancer. 2009;9:253-264. [PubMed] [DOI] |
| 2. | Griner EM, Theodorescu D. The faces and friends of RhoGDI2. Cancer Metastasis Rev. 2012;31:519-528. [PubMed] [DOI] |
| 4. | Cho HJ, Baek KE, Kim IK, Park SM, Choi YL, Nam IK, Park SH, Im MJ, Yoo JM, Ryu KJ. Proteomics-based strategy to delineate the molecular mechanisms of RhoGDI2-induced metastasis and drug resistance in gastric cancer. J Proteome Res. 2012;11:2355-2364. [PubMed] [DOI] |
| 5. | Yamashita H, Nishio M, Toyama T, Sugiura H, Zhang Z, Kobayashi S, Iwase H. Coexistence of HER2 over-expression and p53 protein accumulation is a strong prognostic molecular marker in breast cancer. Breast Cancer Res. 2004;6:R24-R30. [PubMed] [DOI] |
| 6. | Gildea JJ, Seraj MJ, Oxford G, Harding MA, Hampton GM, Moskaluk CA, Frierson HF, Conaway MR, Theodorescu D. RhoGDI2 is an invasion and metastasis suppressor gene in human cancer. Cancer Res. 2002;62:6418-6423. [PubMed] |
| 7. | Theodorescu D, Sapinoso LM, Conaway MR, Oxford G, Hampton GM, Frierson HF. Reduced expression of metastasis suppressor RhoGDI2 is associated with decreased survival for patients with bladder cancer. Clin Cancer Res. 2004;10:3800-3806. [PubMed] [DOI] |
| 8. | Niu H, Li H, Xu C, He P. Expression profile of RhoGDI2 in lung cancers and role of RhoGDI2 in lung cancer metastasis. Oncol Rep. 2010;24:465-471. [PubMed] |
| 9. | Ma L, Xu G, Sotnikova A, Szczepanowski M, Giefing M, Krause K, Krams M, Siebert R, Jin J, Klapper W. Loss of expression of LyGDI (ARHGDIB), a rho GDP-dissociation inhibitor, in Hodgkin lymphoma. Br J Haematol. 2007;139:217-223. [PubMed] [DOI] |
| 10. | Zhou JW, Gan NY, Zhang WJ. [The expression of MKP-1 and p-ERK(1/2) in primary ovarian epithelial tumor tissues]. Fenzi Xibao Shengwu Xuebao. 2009;42:224-230. [PubMed] |
| 11. | Stevens EV, Banet N, Onesto C, Plachco A, Alan JK, Nikolaishvili-Feinberg N, Midkiff BR, Kuan PF, Liu J, Miller CR. RhoGDI2 antagonizes ovarian carcinoma growth, invasion and metastasis. Small GTPases. 2011;2:202-210. [PubMed] [DOI] |
| 12. | Cui JW, Li WH, Wang J, Li AL, Li HY, Wang HX, He K, Li W, Kang LH, Yu M. Proteomics-based identification of human acute leukemia antigens that induce humoral immune response. Mol Cell Proteomics. 2005;4:1718-1724. [PubMed] [DOI] |
| 13. | Cho HJ, Baek KE, Park SM, Kim IK, Choi YL, Cho HJ, Nam IK, Hwang EM, Park JY, Han JY. RhoGDI2 expression is associated with tumor growth and malignant progression of gastric cancer. Clin Cancer Res. 2009;15:2612-2619. [PubMed] [DOI] |
| 14. | Wang Y, Qi HW, Li XH, Chen XX, Liu J. [CIAPIN1 expression in human lung cancer tissues and inhibitory effects of the gene on human pulmonary carcinoma NCI-H446 cells]. Xibao Yu Fenzi Mianyixue Zazhi. 2008;24:434-437. [PubMed] |
| 15. | He L, Wang H, Jin H, Guo C, Xie H, Yan K, Li X, Shen Q, Qiao T, Chen G. CIAPIN1 inhibits the growth and proliferation of clear cell renal cell carcinoma. Cancer Lett. 2009;276:88-94. [PubMed] [DOI] |
| 16. | Zheng X, Zhao Y, Wang X, Li Y, Wang R, Jiang Y, Gong T, Li M, Sun L, Hong L. Decreased expression of CIAPIN1 is correlated with poor prognosis in patients with esophageal squamous cell carcinoma. Dig Dis Sci. 2010;55:3408-3414. [PubMed] [DOI] |
| 17. | Shi H, Zhou Y, Liu H, Chen C, Li S, Li N, Li X, Zhang X, Zhang H, Wang W. Expression of CIAPIN1 in human colorectal cancer and its correlation with prognosis. BMC Cancer. 2010;10:477. [PubMed] [DOI] |
| 18. | Hao Z, Li X, Qiao T, Li S, Lv Y, Fan D. Downregulated expression of CIAPIN1 may contribute to gastric carcinogenesis by accelerating cell proliferation and promoting cell cycle progression. Cancer Biol Ther. 2009;8:1064-1070. [PubMed] [DOI] |
| 19. | Li X, Pan Y, Fan R, Jin H, Han S, Liu J, Wu K, Fan D. Adenovirus-delivered CIAPIN1 small interfering RNA inhibits HCC growth in vitro and in vivo. Carcinogenesis. 2008;29:1587-1593. [PubMed] [DOI] |