修回日期: 2013-09-19
接受日期: 2013-09-30
在线出版日期: 2013-11-08
目的: 评价国产奥沙利铂(Oxaliplatin, L-OHP)联合替加氟(Tegafur, FT-207)与奥沙利铂联合氟脲嘧啶(5-fluorouracil, 5-FU)对结直肠癌术后辅助治疗的近期疗效及不良反应.
方法: 对2008-01/2010-12在湖南省肿瘤医院分别接受FT-207联合L-OHP方案及5-FU、L-OHP方案化疗的51例患者的临床资料进行回顾性分析.
结果: FT-207联合L-OHP方案与5-FU联合L-OHP方案两组中位无病生存期分别为36 mo、29 mo, 两组比较差异有统计学意义. 不良反应主要为轻中度的外周神经毒性、骨髓抑制和恶心呕吐.
结论: 替加氟可以替代氟尿嘧啶用于结直肠癌的术后辅助治疗.
核心提示: 本文通过评价国产奥沙利铂联合替加氟与奥沙利铂联合氟脲嘧啶对结直肠癌术后辅助治疗的近期疗效及不良反应, 试验结果有一定差异, 替加氟与氟尿嘧啶比较, 其在结直肠癌辅助治疗中有优势.
引文著录: 李永亮, 刑珊珊, 罗以, 袁志军, 朱跃红, 吴尉. 替加氟或氟尿嘧啶联合奥沙利铂对结直肠癌术后辅助化疗的疗效比较. 世界华人消化杂志 2013; 21(31): 3460-3463
Revised: September 19, 2013
Accepted: September 30, 2013
Published online: November 8, 2013
AIM: To compare the therapeutic effects and safety of Tegafur or 5-fluorouracil (5-FU) combined with oxaliplatin in adjuvant therapy of colorectal cancer.
METHODS: Clinical data for 51 patients who underwent adjuvant chemotherapy with Tegafur or 5-FU combined with oxaliplatin from January 2008 to December 2010 at Hunan Provincial Tumor Hospital were retrospectively analyzed.
RESULTS: The median disease-free survival was significantly longer in the Tegafur plus oxaliplatin group than in the 5-FU plus oxaliplatin group (36 mo vs 29 mo, P < 0.05). Major toxic reactions were nausea, vomiting, myelosuppression and peripheral neurotoxicity.
CONCLUSION: Tegafur can replace fluorouracil for adjuvant therapy of colorectal cancer.
- Citation: Li YL, Xing SS, Luo Y, Yuan ZJ, Zhu YH, Wu W. Effects of Tegafur or 5-fluorouracil combined with oxaliplatin in adjuvant chemotherapy of colorectal cancer. Shijie Huaren Xiaohua Zazhi 2013; 21(31): 3460-3463
- URL: https://www.wjgnet.com/1009-3079/full/v21/i31/3460.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v21.i31.3460
结直肠癌(colorectal cancer, CRC)是目前最常见的恶性肿瘤之一, 全世界结直肠癌的发病率和死亡率居所有肿瘤的第3位[1]. 我国结直肠癌患者每年新发约15万例, 死亡率超过7/10万, 且病死率仍有逐年上升趋势[2], CRC发病年龄明显前移, 平均58岁, 比欧美等国家提前12-18岁[3,4]. 目前对结直肠癌的治疗以手术为主, 术后对有高危因素的Ⅱ期及Ⅲ期结直肠癌患者行辅助化疗以减少复发率, 延长生存时间[5]. 专家组推介氟脲嘧啶(5-fluorouracil, 5-FU)+亚叶酸钙(calcium folinate, CF)+奥沙利铂(Oxaliplatin, L-OHP)联合的方案作为结直肠癌术后辅助化疗的标准方案. 此方案较为安全可靠, 但在疗效上仍有不尽人意的地方. 积极寻找有效、低毒的新型药物已受到广大研究者的普遍重视. 我们尝试用替加氟(Tegafur, FT-207)代替5-FU进行辅助化疗的研究, 对2008-01/2010-12在湖南省肿瘤医院治疗的51例结直肠癌进行FT-207或5-FU联合L-OHP的化疗方案治疗的疗效及不良反应进行比较观察, 结果报道如下.
2008-01/2010-12湖南省肿瘤医院收治的, 经病理学检查并结合临床、影像学等确诊, 接受根治手术的结直肠癌的患者, 近1 mo内未接受过化疗, Karnofsky评分>70分; 治疗前血常规、肝肾功能、心电图正常, 无化疗禁忌症, 共51例. 分为A、B两组. A组26例: 男19例, 女7例; 年龄20-63岁, 中位年龄51岁; 高分化腺癌3例, 中分化腺癌15例, 低分化腺癌6例, 黏液腺癌2例; Ⅲ期18例, Ⅱ期8例. B组25例: 男19例, 女6例; 年龄31-66岁, 中位年龄47岁; 高分化腺癌2例, 中分化腺癌15例, 低分化腺癌5例, 黏液腺癌3例; Ⅲ期18例, Ⅱ期7例.
1.2.1 治疗: A组: L-OHP(江苏恒瑞医药股份有限公司)85 mg/m2, 2 h静脉滴入, d1; CF 400 mg/m2, 2 h静滴, d1; FT-207(方克, 齐鲁制药有限公司)400 mg/m2静脉推注d1, 续以FT-207 2400/m2微量注射静脉泵静脉滴入46 h, 2 wk重复, 共4周期. B组: L-OHP 85 mg/m2, 2 h静滴, d1; CF 400 mg/m2, 2 h静滴, d1; 5-FU(天津金耀氨基酸有限公司)400 mg/m2静脉推注d1, 续以5-FU 2400 mg/m2, 微量注射静脉泵静脉滴入46 h, 2 wk重复, 共4周期. 化疗过程中常规使用止吐剂盐酸昂丹司琼8 mg, 2次/d, 入小壶; 同时配合护肝治疗. 化疗期间忌食冷饮, 禁用冷水和接触冰冷物体. 所有病例完成≥2个化疗周期后评价疗效, 化疗中、化疗后记录不良反应.
1.2.2 观察指标: 无疾病生存期(disease-free survival, DFS)为治疗开始至疾病复发或由于疾病进展导致患者死亡的时间. 不良反应评价按照WHO抗癌药物不良反应分为0-Ⅳ度. 观察指标: 每次化疗前后复查血常规、肝肾功能、心电图. 完成2周期化疗后全面复查影像学, 对肿瘤病灶进行评价, 观察近期疗效和不良反应.
1.2.3 随访: 经门诊复查或电话对患者进行随访, 随访时间为36-61 mo, 中位随访时间为41 mo, 无失访患者.
统计学处理 采用SPSS13.0软件进行统计分析, 率的比较采用χ2检验, 采用Kaplan-Meier方法进行生存分析, 其差异应用Log-rank检验. P<0.05为差异具有统计学意义.
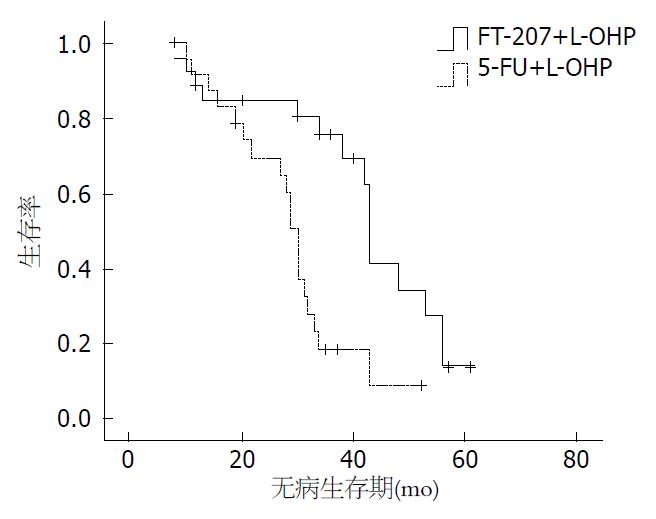
全组病例至2013-03随访结束, A组: 其中11例无病生存, 26例患者DFS 8-61 mo; B组: 其中6例无病生存, 25例患者DFS 8-52 mo. A、B两组中位DFS分别为36 mo和29 mo, 1年DFS分别为92.3%(24/26)和88.0%(22/25); 2年DFS分别为76.9%(20/26)和64%(16/25); 3年DFS分别为53.8%(14/26)和16%(4/25). 两组发生率比较, 差异有统计学意义(P<005, 图1).
全部51例患者均可评价不良反应, 两组患者的主要不良反应为胃肠道反应、周围神经毒性和骨髓抑制, 且多为Ⅰ-Ⅱ度. A组和B组, 白细胞下降以Ⅰ-Ⅱ度为主, 分别为69.2%、92%, Ⅲ、Ⅳ度粒细胞下降的发生率分别为3.8%和8%, 两组比较有统计学意义(P<0.05). Ⅲ、Ⅳ度腹泻的发生率分别为7.7%和12%, 两组皆无Ⅲ、Ⅳ度周围神经毒性病例发生, 差异无统计学意义(P>0.05, 表1). 其他不良反应, 如肝功能损害、恶心呕吐、贫血、血小板减少等, 两组发生率比较, 差异均无统计学意义(P>0.05, 表1).
| 不良反应 | FT-207+L-OHP组 | 5-FU+L-OHP组 | P值 | ||||||||
| 0度 | Ⅰ度 | Ⅱ度 | Ⅲ度 | Ⅳ度 | 0度 | Ⅰ度 | Ⅱ度 | Ⅲ度 | Ⅳ度 | ||
| 白细胞下降 | 8 | 7 | 10 | 1 | 0 | 2 | 8 | 13 | 2 | 0 | <0.05 |
| 贫血 | 19 | 5 | 1 | 1 | 0 | 16 | 6 | 2 | 0 | 1 | >0.05 |
| 血小板减少 | 17 | 4 | 3 | 2 | 0 | 17 | 3 | 4 | 1 | 0 | >0.05 |
| 腹泻 | 21 | 3 | 0 | 2 | 0 | 19 | 2 | 1 | 3 | 0 | >0.05 |
| 恶心呕吐 | 6 | 9 | 9 | 1 | 1 | 6 | 5 | 12 | 2 | 0 | >0.05 |
| 周围神经毒性 | 15 | 6 | 5 | 0 | 0 | 16 | 5 | 4 | 0 | 0 | >0.05 |
| 丙氨酸氨基转移酶升高 | 19 | 5 | 2 | 0 | 0 | 18 | 4 | 3 | 0 | 0 | >0.05 |
结直肠癌是我国常见恶性肿瘤之一, 近年来发病率和死亡率有逐年上升的趋势. 美国NCCN指南将奥沙利铂、亚叶酸钙和氟尿嘧啶持续静脉注射联合方案作为结直肠癌术后辅助化疗推介方案之一[6,7]. 奥沙利铂是第三代铂类药物, 通过产生烷化结合物作用于DNA, 形成链内和链间交联, 从而抑制DNA的合成及抑制[8]. 5-FU是一种嘧啶类抗癌药物, 对消化系肿瘤及其他实体肿瘤有良好的疗效. 体内及体外的临床研究表明, 奥沙利铂与5-FU有明显的协同作用[9], 而CF生化调节可使5-FU增效. 但5-FU半衰期只有10 min左右, 其极易被正常器官和肿瘤组织产生的二氢嘧啶脱氢酶快速降解(达85%以上)而失活[10]. 并且, 5-FU作为细胞周期特异性药物, 有显著的时间依赖性特点, 故需长期持续输注, 使之不断作用于癌细胞的S期, 以增强抑制作用, 但结果往往还是不如人意.
替加氟为氟尿嘧啶的衍生物, 在体内经肝脏活化逐渐转变为氟尿嘧啶, 能干扰和阻断DNA、RNA及蛋白质合成, 从而达到抑制肿瘤的效果. 替加氟主要作用于S期, 是抗嘧啶类的细胞周期特异性药物, 其作用机制、疗效及抗瘤谱与氟尿嘧啶相似, 但作用更持久, 毒性更低-半衰期为5 h, 血药浓度高于5-FU, 药效更为稳定; 化疗指数为5-FU的2倍, 毒性仅为5-FU的1/7-1/4, 在慢性毒性实验中未见严重的骨髓抑制, 对免疫的影响较为轻微[11]. Bajetta等[12]报道替加氟联合奥沙利铂治疗结直肠癌联合用药的有效率为38.9%. Hsiao等[13]报道替加氟联合奥沙利铂治疗转移性结直肠癌的肿瘤控制率接近64%.
从图1可以看出, A、B两组中位无病生存时间分别为36 mo和29 mo, 1年DFS分别为92.3%(24/26)和88.0%(22/25); 2年DFS分别为76.9%(20/26)和64%(16/25); 3年DFS分别为53.8%(14/26)和16%(4/25), 两组发生率比较, 差异有统计学意义.
从表1可以看出, 本文A组与B组方案的主要不良反应中, 白细胞下降以Ⅰ-Ⅱ度为主, 分别为69.2%、92%, 两组比较有统计学意义(P<0.05), 提示替加氟联合奥沙利铂与氟尿嘧啶联合奥沙利铂比较, 前者的白细胞下降程度要轻; 贫血、血小板降低、神经毒性; 消化系反应及肝毒性等方面, 两组比较无统计学意义(P>0.05), 提示两组间相关毒性无明显差别.
总之, 替加氟联合奥沙利铂方案对结直肠癌术后辅助治疗的疗效优于氟尿嘧啶与奥沙利铂联合的方案; 替加氟为主的联合化疗方案与氟尿嘧啶联合奥沙利铂方案不良反应比较, 替加氟组的白细胞下降较氟尿嘧啶组有优势; 其他方面不良反应比较, 两组无明显差别. 故此, 替加氟联合奥沙利铂方案化疗可考虑作为结直肠癌术后辅助治疗一线方案. 甚至我们认为, 替加氟可以替代氟尿嘧啶用于结直肠癌的术后辅助治疗.
当然, 因本研究为回顾性研究, 入选病例数相对较少, 可能存在某些偏差. 如本研究中氟尿嘧啶组的3年DFS仅16%, 低于MOSAIC试验[14]及NSABP C-07研究[15]报道结果, 考虑可能与化疗周期不足及入组病例较少造成抽样误差有关. 替加氟用于结直肠癌的术后辅助治疗, 其远期疗效及不良反应, 尚需要进一步的随机大样本前瞻性研究验证.
FOLFOX方案被推介为结直肠癌术后辅助治疗的标准方案, 有一定疗效, 但进一步提高疗效, 仍是目前研究的热点.
汤静, 主管药师, 上海交通大学附属第一人民医院药学部; 彭宗根, 研究员, 中国医学科学院医药生物技术研究所病毒室
目前结直肠癌术后辅助化疗的标准方案的疗效有限, 探索高效、低毒的新型疗法及化疗组合仍需研究.
国际多中心的MOSAIC试验, 报道了氟尿嘧啶、亚叶酸钙联合奥沙利铂在结直肠癌辅助化疗的积极疗效, NSABP C-07研究起到很好的验证效果.
本文通过评价国产奥沙利铂(L-OHP)联合替加氟(FT-207)与奥沙利铂联合氟脲嘧啶(5-FU)对结直肠癌术后辅助治疗的近期疗效及不良反应, 以分析疗法的优势, 实验结果显示两组疗效和不良反应有一定的差异, 结果对目前临床有一定的治疗指导作用.
编辑: 郭鹏 电编:鲁亚静
| 1. | Parkin DM, Bray F, Ferlay J, Pisani P. Global cancer statistics, 2002. CA Cancer J Clin. 2005;55:74-108. [PubMed] [DOI] |
| 5. | Grávalos C, García-Escobar I, García-Alfonso P, Cassinello J, Malón D, Carrato A. Adjuvant chemotherapy for stages II, III and IV of colon cancer. Clin Transl Oncol. 2009;11:526-533. [PubMed] [DOI] |
| 6. | Engstrom PF, Arnoletti JP, Benson AB, Chen YJ, Choti MA, Cooper HS, Covey A, Dilawari RA, Early DS, Enzinger PC. NCCN Clinical Practice Guidelines in Oncology: colon cancer. J Natl Compr Canc Netw. 2009;7:778-831. [PubMed] |
| 7. | Engstrom PF, Arnoletti JP, Benson AB, Chen YJ, Choti MA, Cooper HS, Covey A, Dilawari RA, Early DS, Enzinger PC. NCCN Clinical Practice Guidelines in Oncology: rectal cancer. J Natl Compr Canc Netw. 2009;7:838-881. [PubMed] |
| 10. | Malet-Martino M, Martino R. Clinical studies of three oral prodrugs of 5-fluorouracil (capecitabine, UFT, S-1): a review. Oncologist. 2002;7:288-323. [PubMed] [DOI] |
| 12. | Bajetta E, Di Bartolomeo M, Buzzoni R, Mariani L, Zilembo N, Ferrario E, Lo Vullo S, Aitini E, Isa L, Barone C. Uracil/ftorafur/leucovorin combined with irinotecan (TEGAFIRI) or oxaliplatin (TEGAFOX) as first-line treatment for metastatic colorectal cancer patients: results of randomised phase II study. Br J Cancer. 2007;96:439-444. [PubMed] [DOI] |
| 13. | Hsiao SC, Lin JF, Chuang MT, Lee YA, Wu DL. Retrospectively comparative evaluation of the first- and second-line chemotherapy with campto and oxaliplatin combined with oral tegafur/uracil (UFT)/leucovorin (LV) in patients with metastatic colorectal cancer. Int Surg. 2009;94:298-303. [PubMed] |
| 14. | André T, Boni C, Mounedji-Boudiaf L, Navarro M, Tabernero J, Hickish T, Topham C, Zaninelli M, Clingan P, Bridgewater J. Oxaliplatin, fluorouracil, and leucovorin as adjuvant treatment for colon cancer. N Engl J Med. 2004;350:2343-2351. [PubMed] [DOI] |
| 15. | Kuebler JP, Wieand HS, O'Connell MJ, Smith RE, Colangelo LH, Yothers G, Petrelli NJ, Findlay MP, Seay TE, Atkins JN. Oxaliplatin combined with weekly bolus fluorouracil and leucovorin as surgical adjuvant chemotherapy for stage II and III colon cancer: results from NSABP C-07. J Clin Oncol. 2007;25:2198-2204. [PubMed] [DOI] |