修回日期: 2012-12-05
接受日期: 2012-12-20
在线出版日期: 2012-12-28
目的: 总结临床隐匿性胃癌的氟脱氧葡萄糖(fluorodeoxyglucose, FDG) PET/CT影像表现特点.
方法: 回顾分析26例临床隐匿性胃癌的临床及PET/CT影像资料. 男18例, 女8例, 年龄41-83岁, 平均年龄60.8岁, 皆以转移瘤症状为首发症状, 经胃镜活检证实24例, 经开腹手术证实2例. 以目测法分别分析FDG PET和CT影像, 依据其异常表现的强度分为强阳性、弱阳性和阴性; 再综合PET和CT表现, 根据诊断的难易程度分为3型: 易诊型、疑诊型和难诊型.
结果: PET表现为强阳性者57.7%(15/26), 弱阳性者23.1%(6/26), 阴性者19.2%(5/26). 同机CT表现强阳性者76.9%(20/26), 弱阳性者11.5%(3/26), 阴性者11.5%(3/26). 易诊型为53.8%(14/26), 疑诊型为34.6%(9/26), 难诊型为11.5%(3/26).
结论: 临床隐匿性胃癌大约88.4%的患者可通过FDG PET/CT检查发现或提示胃癌.
引文著录: 王欣, 于丽娟, 陆佩欧, 田墨涵, 李迎辞, 王洪. 临床隐匿性胃癌的FDG PET/CT征象. 世界华人消化杂志 2012; 20(36): 3695-3700
Revised: December 5, 2012
Accepted: December 20, 2012
Published online: December 28, 2012
AIM: To investigate the use of fluorodeoxyglucose (FDG) positron emission tomography ( PET)/CT imaging in diagnosis of clinically occult gastric cancer.
METHODS: The imaging data for 26 patients with clinically occult gastric cancer who underwent FDG PET/CT imaging were reviewed retrospectively. They were hospitalized for metastatic tumors and therefore underwent FDG PET/CT for detecting carcinoma of unknown primary origin. They were finally diagnosed with gastric cancer by endoscopy (n = 24) or laparoscopy (n = 2). Based on imaging manifestations, the patients were divided into three groups: easily diagnosed, suspected, and hardly diagnosed.
RESULTS: PET imaging showed 57.7% (15/26) of intensively positive cases, 23.1% (6/26) of positive cases, and 19.2% (5/26) of negative cases. CT imaging showed 76.9% (20/26) of intensively positive cases, 11.5% (3/26) of positive cases, and 11.5% (3/26) of negative cases. The percentages of easily diagnosed, suspected, and hardly diagnosed patients were 53.8% (14/26), 34.6% (9/26) and 11.5% (3/26), respectively.
CONCLUSION: FDG PET/CT imaging can help diagnose clinically occult gastric cancer in about 88.4% of patients.
- Citation: Wang X, Yu LJ, Lu PO, Tian MH, Li YC, Wang H. FDG PET/CT diagnosis of clinically occult gastric cancer. Shijie Huaren Xiaohua Zazhi 2012; 20(36): 3695-3700
- URL: https://www.wjgnet.com/1009-3079/full/v20/i36/3695.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i36.3695
以转移灶为首发症状的胃癌, 被称为临床隐匿性胃癌, 在胃癌中约占4%的比重; 这些患者往往缺乏与胃部相关的临床症状和体征, 使原发病变的寻找变得复杂; 帮助这些患者尽快确定原发病变的部位, 有利于尽快开始正确的治疗, 减轻患者的痛苦[1,2]. 一体化的PET/CT氟脱氧葡萄糖显像, 在探查缺少临床症状的偶发瘤、常规检查隐匿的恶性肿瘤及转移灶方面, 有很大的优势[3-5]. 但作者未见有关临床隐匿性胃癌的氟脱氧葡萄糖(fluorodeoxyglucose, FDG)PET/CT 显像的报道.
我们回顾分析了2007-2012在哈尔滨医科大学附属第三医院PET-CT中心, 以查找原发灶为目的, 最终证明为胃癌的患者的FDG PET/CT检查资料, 总结这部分疾病的PET/CT影像特点, 意在总结经验, 以期提高对这类胃癌的FDG PET/CT表现的认识.
回顾分析2007-2012在哈尔滨医科大学附属第三医院PET-CT中心, 以查找原发灶为目的行FDG PET/CT检查, 最终证明为胃癌的患者 的临床及FDG PET/CT的影像资料. 共26例, 男18例, 女8例, 年龄41-83岁, 平均年龄60.8岁; 皆以转移瘤症状为首发症状, 其中锁骨上淋巴结转移瘤3例、腹膜后淋巴结肿大6例、腹股沟淋巴结转移瘤1例、骨转移瘤4例、肝转移瘤8例、因腹水和或腹腔肿物疑卵巢癌行PET/CT检查4例. 经胃镜活检证实24例, 经开腹手术证实2例.
1.2.1 PET/CT检查方法: 检查前禁食6 h以上, 静脉注射FDG 0.8-0.12 mCi/kg, 平静休息50-70 min后行PET/CT扫描, 扫描前口服500 mL纯净水, 以使胃腔膨胀. 第一次扫描结束后1 h行第二次扫描(延迟扫描), 扫描前再次饮水500 mL. PET/CT扫描仪为Discovery ST(GE corporation), PET采集2D模式, 2.5 min/床位, 迭代法重建; CT螺旋扫描120 kV, 120-200 mA, 0.75螺距, 3.75 mm层厚重建. 以CT数据为PET作衰减校正. 系统根据扫描前血糖水平、注射剂量及身高、体质量自动计算标准化摄取值(standard uptake value, SUV). FDG经mini-TRACE(GE Corporation)和FN自动化合成系统生产, 放化纯度>98 %.
1.2.2 胃癌FDG PET/CT影像表现分析方法: 由2位有5年以上CT及PET/CT工作经验医生共同在影像工作站观察PET/CT影像, 以二者的一致意见为准. PET判断胃癌以目测为主, 当胃区出现明显高于肝脏的局灶或弥漫异常放射性浓聚时, 且延迟显像放射性浓聚持续存在, 为PET强阳性(++); 当胃部出现较小的放射性浓聚灶, 或异常放射性浓聚不易与生理性摄取区分时, 为PET弱阳性(+); 当胃区呈现均匀的本底样放射性摄取时, 为PET阴性(-). 在同机CT图像上, 当胃壁呈现明显局限性或弥漫性不规则增厚, 胃壁厚度>1.0 cm, 为CT强阳性(++); 当在适度充盈胃壁呈现范围较小的局限增厚, 或胃壁弥漫轻度增厚、僵硬, 或胃壁局限密度略增高, 如有上述异常, 判断为CT弱阳性(+); 如CT无明确异常表现, 为CT阴性(-). 根据诊断的难易程度分为易诊型、疑诊型和难诊型. 当PET和CT影像均为强阳性表现时为易诊型, 即PET+CT = ++++; 当PET+CT = ++/+++为疑诊型; 当PET+CT = -/+时为难诊型.
26例临床隐匿性胃癌的临床及FDG PET/CT表现资料见表1. PET表现为强阳性者57.7%(15/26), FDG摄取SUVmax介于6.2-13.0; 弱阳性者23.1%(6/26), FDG摄取SUVmax介于3.5-6.4; 阴性者19.2%(5/26). 同机CT表现强阳性者76.9%(20/26), 弱阳性者11.5%(3/26), 阴性者11.5%(3/26).
| 编号 | 性别 | 年龄 | 首发转移部位 | 胃癌发生部位 | FDG PET表现 | 同机CT表现 | 组织学诊断 |
| 1 | 女 | 65 | 淋巴结 | 胃窦 | ++ | ++ | 腺癌 |
| 2 | 男 | 43 | 淋巴结 | 胃体和窦 | ++ | ++ | 低分化腺癌 |
| 3 | 男 | 71 | 淋巴结 | 胃体和窦 | ++ | ++ | 腺癌 |
| 4 | 男 | 84 | 肝 | 胃底贲门 | ++ | ++ | 腺癌 |
| 5 | 男 | 41 | 肝 | 胃体 | ++ | ++ | 腺癌 |
| 6 | 男 | 62 | 肝 | 胃体 | ++ | ++ | 腺癌 |
| 7 | 男 | 81 | 肝 | 胃体 | ++ | ++ | 腺癌 |
| 8 | 男 | 56 | 肝 | 胃窦 | ++ | ++ | 腺癌 |
| 9 | 男 | 63 | 肺肝 | 胃体和窦 | ++ | ++ | 腺癌 |
| 10 | 女 | 63 | 肺 | 胃底贲门 | ++ | ++ | 腺癌 |
| 11 | 男 | 61 | 骨 | 胃体 | ++ | ++ | 低分化腺癌 |
| 12 | 男 | 60 | 淋巴结 | 胃体 | ++ | ++ | 腺癌 |
| 13 | 男 | 60 | 淋巴结 | 胃底贲门 | ++ | ++ | 腺癌 |
| 14 | 男 | 57 | 淋巴结 | 胃窦 | ++ | ++ | 腺癌 |
| 15 | 女 | 72 | 骨转移 | 胃窦 | ++ | + | 腺癌 |
| 16 | 男 | 42 | 骨 | 胃底和体 | + | ++ | 低分化腺癌 |
| 17 | 女 | 62 | 淋巴结 | 胃底和体 | + | ++ | 腺癌 |
| 18 | 女 | 48 | 骨 | 胃体 | - | ++ | 低分化腺癌 |
| 19 | 女 | 59 | 腹水 | 胃体 | - | ++ | 印戒细胞癌 |
| 20 | 女 | 73 | 腹水 | 胃体 | - | ++ | 黏液腺癌 |
| 21 | 女 | 47 | 卵巢 | 胃体 | - | ++ | 印戒细胞癌 |
| 22 | 男 | 62 | 肝 | 胃窦 | + | + | 腺癌 |
| 23 | 男 | 63 | 肝 | 胃体 | + | + | 腺癌 |
| 24 | 男 | 69 | 淋巴结 | 胃底贲门 | + | - | 低分化腺癌 |
| 25 | 男 | 73 | 肝 | 贲门 | + | - | 低分化鳞癌 |
| 26 | 男 | 44 | 腹水 | 胃窦 | - | - | 低分化腺癌 |
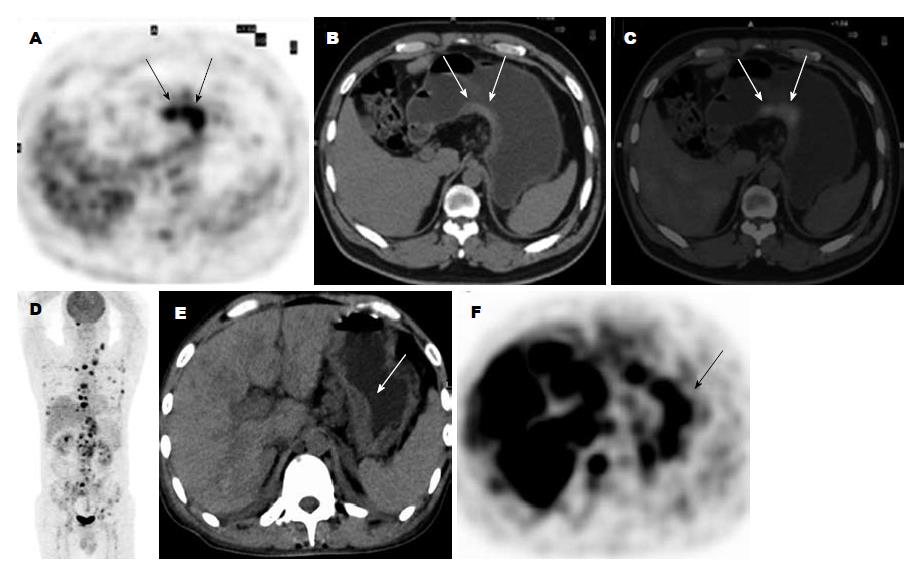
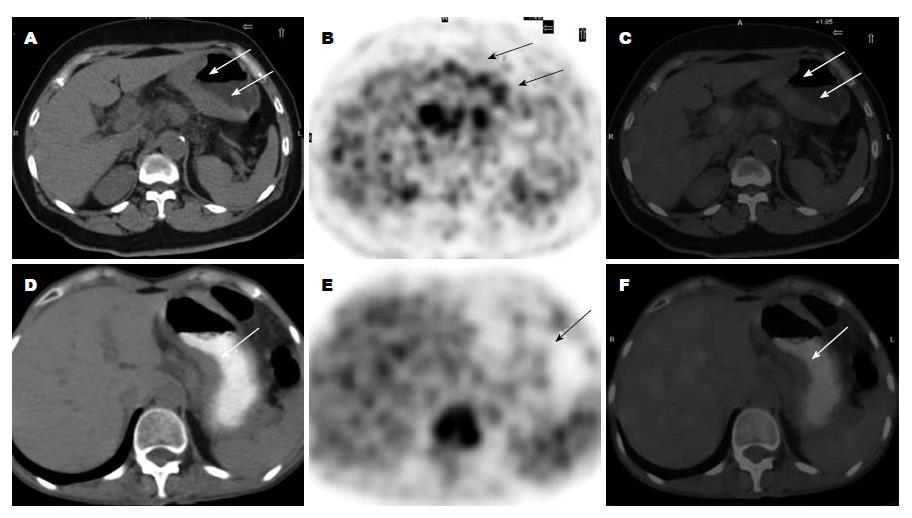
PET呈现明显异常放射性浓聚, 同机CT呈现明显异常胃壁增厚的双重强阳性者, 即易诊型为53.8%(14/26, 图1). 疑诊型为34.6%(9/26), 其中4例PET表现FDG摄取高于肝脏, 但无法与良性或生理性摄取区分, 但CT呈现明显胃壁增厚, 提示胃癌可能(图2A-C); 另外4例PET表现阴性而CT呈现明显强阳性(图2D-F); 1例PET表现强阳性, 而CT上局部胃壁增厚与良性的黏膜皱襞粗大不易区分.
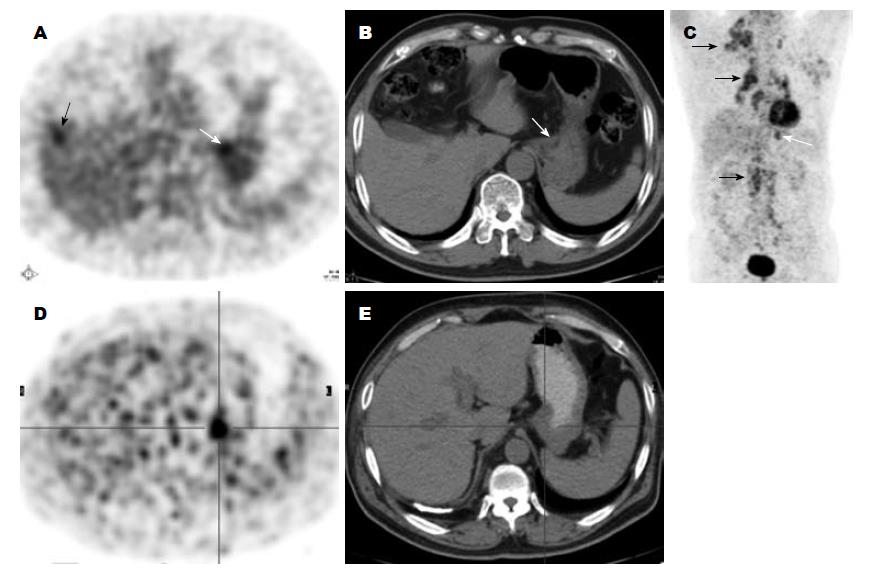
难诊型为11.5%(3/26); 其中PET和CT均为阴性者1例(3.8%), 为胃窦低分化腺癌; 另外2例PET呈现弱阳性, 都是贲门癌(图3), PET上可见贲门区小灶放射性浓聚, 而CT无异常表现, 呈阴性, 内镜活检证实1例为贲门低分化腺癌, 另1例为低分化鳞癌, 最小病灶为直径1.5 cm的扁平状溃疡灶.
以转移灶症状为首发症状的癌症, 往往原发病表现不明显, 而患者心理压力大, 心情急切, 一些年老体弱的患者难以承受过多的侵入式检查; 一体化的FDG PET/CT检查, 具有代谢显像和解剖影像的双重能力, 无疑为这样的患者提供了一种安全、便捷的诊断手段. 国内外陆续发表的有关报道显示: FDG PET/CT在不明来源转移瘤的原发病灶的查找上优于常规检查手段, 骨转移瘤, 淋巴结转移瘤, 脑转移瘤的原发灶的检出率在58%-88%左右[6-10].
胃癌的FDG 显像的应用存在一些限制, 主要有两方面: 一方面胃本身为消化道的空腔脏器, 存在平滑肌蠕动、黏膜新陈代谢形成的FDG生理性摄取[11-13], 而胃黏膜的炎性病变, 如幽门螺旋杆菌感染所致浅表和糜烂性胃炎, 也会导致胃壁呈现弥漫的非特异性放射性浓聚[14], 这就给正常和异常的区分, 以及良性和恶性的区分带来困难; 另一方面, 研究显示, 胃癌的FDG摄取与葡萄糖转运蛋白(glucose transporter 1, Glut-1)的表达关系密切[15,16], 不同组织学类型的胃癌的Glut-1阳性表达率不同[17], 印戒细胞癌、黏液腺癌、非聚集生长类型的低分化腺癌以及一部分早期胃癌, 由于缺少Glut1的过度表达, 而无明显FDG摄取, 造成PET影像的假阴性[16,18]; 而低分化癌的FDG阳性率较低, 提示FDG的摄取程度与恶性度不相关[19,20]. 早期胃癌的FDG PET的阳性率较低, 文献报道0%-44%[21-23], 因而不建议用于胃癌的筛查; 进展期胃癌的FDG PET阳性率34%-94%[24-26]; 近些年来, 随着一体化PET/CT的临床应用, 与PET同机的CT解剖图像辅助作用,使进展期胃癌的诊断率进一步得以提高[27,28].
临床隐匿性胃癌属于已经发生远处转移的晚期胃癌, 本组病例显示大约88.5%的患者可通过FDG PET/CT检查发现或提示胃癌. 其中半数以上病例在FDG PET/CT影像上同时呈现明显的放射性浓聚和CT形态异常, 诊断很容易确立; 另外还有大约23.1%(6/26)的患者虽然在FDG- PET影像上不明确, 但CT呈现明显的异常, 拟补了FDG影像的不足, 提示胃部的恶性肿瘤的存在可能, 进一步通过针对胃部的活检也能很快明确诊断. 对于胃癌, 同样存在"小病灶, 大转移"现象, 这种现象对PET和CT都构成挑战; 本组病例中有3例表现出这种现象, 其中1例为胃体大弯的溃疡型胃癌, CT可见突向胃腔的"火山口样"腔内龛影, PET相应部位见局限放射性浓聚灶; 另外2例为贲门癌, 最小的癌灶在内镜下为直径1.5cm的扁平溃疡状病灶. 贲门部由于存在FDG的生理性摄取[14], 局限的小的放射性摄取灶易被误认为生理性摄取而漏诊, 小癌灶在CT图像上也可呈现阴性表现, 尤其是未使用低张药物和扩张胃腔的处理方法时, 因此贲门部的小癌大转移, 对PET/CT的诊断是个挑战, 需要额外加以注意.
本组病例中PET和CT都为阴性的纯阴性病例只有一例, 是胃窦的浸润生长的腺癌, 但在实际工作中该病例并没有被漏诊, 因为该患者自带的增强CT显示出胃壁的局限异常强化, 这提示我们FDG PET/CT与增强CT的结合会使其诊断能力进一步提升. 应用FDG PET/CT探查临床隐匿性胃癌时, 检查方法以及CT技术的应用很重要; 良好的胃部CT影像是诊断的重要组成部分, 所以检查前要充分的禁食, 可饮水或造影剂或牛奶以适度的充盈胃腔[29,30], 应用恰当的CT扫描剂量以便形成清晰的解剖图像. 通常认为胃癌的远处转移常见于肝脏、淋巴结及腹腔的种植转移, 骨转移相对较少; 本组病例中4例皆以骨转移瘤为首发症状, 并且3例是低分化腺癌, 大体类型是弥漫型, 其中2例患者年龄在40-50岁之间, 提示骨转移可与非肠型胃癌关系密切.
总之, 临床隐匿性胃癌大约88.5%的患者可通过FDG PET/CT检查发现或提示胃癌; 其中CT的加入使诊断的灵敏度大幅提升. 难诊型主要为易于误诊和漏诊的 "小病灶大转移"表现的胃癌, 需要特别注意的是贲门癌, 易于误诊为生理性摄取而漏诊.
正电子发射计算机断层成像/X线计算机断层成像(PET/CT), 将PET的功能成像和CT解剖成像整合为一体化成像仪, 他的全身成像模式, 代谢与形态双重影像能力, 为中晚期肿瘤患者提供了一种安全、便捷的诊断手段. 18F-脱氧葡萄糖(FDG) PET/CT在不明来源转移瘤的原发病灶的查找上优于常规检查手段.
肖恩华, 教授, 中南大学湘雅二医院放射教研室
国内外报道显示: FDG PET/CT在不明来源转移瘤的原发病灶的查找上优于常规检查手段, 骨转移瘤, 淋巴结转移瘤, 脑转移瘤的原发灶的检出率在58%-88%左右.
本组病例显示临床隐匿性胃癌大约88.5%的患者可通过FDG PET/CT检查发现或提示胃癌. 其中半数以上病例在FDG PET/CT影像上同时呈现明显异常, 诊断很容易确立; 另外还有大约23.1%(6/26)的患者, PET和CT影像可互相补充, 提示胃部的恶性肿瘤存在的可能, 进一步通过针对胃部的活检也能很快明确诊断. 假阴性主要为"小病灶, 大转移" 的胃癌, 需要特别注意贲门癌, 易于误诊为生理性摄取而漏诊.
PET/CT扫描前应嘱患者充分饮水, 使胃壁舒张, 有助于减少胃壁的生理性摄取和CT的诊断.
临床隐匿性胃癌: 以转移瘤症状为首发症状的胃癌, 在胃癌中约占4%.
以转移灶症状为首发症状的临床隐匿的癌症, 临床上寻找原发病有时很困难, 本研究显示临床隐匿性胃癌大约88.4%的患者可通过FDG PET/CT检查发现或提示胃癌, 对临床诊断有一定参考作用.
编辑: 翟欢欢 电编:鲁亚静
| 3. | Choi JY, Lee KS, Kwon OJ, Shim YM, Baek CH, Park K, Lee KH, Kim BT. Improved detection of second primary cancer using integrated [18F] fluorodeoxyglucose positron emission tomography and computed tomography for initial tumor staging. J Clin Oncol. 2005;23:7654-7659. [PubMed] [DOI] |
| 4. | Choi JY, Lee KS, Kim HJ, Shim YM, Kwon OJ, Park K, Baek CH, Chung JH, Lee KH, Kim BT. Focal thyroid lesions incidentally identified by integrated 18F-FDG PET/CT: clinical significance and improved characterization. J Nucl Med. 2006;47:609-615. [PubMed] |
| 5. | Israel O, Yefremov N, Bar-Shalom R, Kagana O, Frenkel A, Keidar Z, Fischer D. PET/CT detection of unexpected gastrointestinal foci of 18F-FDG uptake: incidence, localization patterns, and clinical significance. J Nucl Med. 2005;46:758-762. [PubMed] |
| 6. | Wong WL, Sonoda LI, Gharpurhy A, Gollub F, Wellsted D, Goodchild K, Lemon C, Farrell R, Saunders M. 18F-fluorodeoxyglucose positron emission tomography/computed tomography in the assessment of occult primary head and neck cancers--an audit and review of published studies. Clin Oncol (R Coll Radiol). 2012;24:190-195. [PubMed] [DOI] |
| 7. | Roh JL, Kim JS, Lee JH, Cho KJ, Choi SH, Nam SY, Kim SY. Utility of combined (18)F-fluorodeoxyglucose-positron emission tomography and computed tomography in patients with cervical metastases from unknown primary tumors. Oral Oncol. 2009;45:218-224. [PubMed] [DOI] |
| 8. | 梁 颖, 吴 宁, 李 蒙, 郑 容, 刘 瑛, 张 雯杰, 李 静, 赵 平. 18F-FDG PET/CT在查找骨转移瘤原发灶中的价值. 中国医学影像技术. 2009;25:2275-2277. |
| 11. | Shammas A, Lim R, Charron M. Pediatric FDG PET/CT: physiologic uptake, normal variants, and benign conditions. Radiographics. 2009;29:1467-1486. [PubMed] [DOI] |
| 12. | Kamimura K, Fujita S, Nishii R, Wakamatsu H, Nagamachi S, Yano T, Ogita M, Umemura Y, Fujimoto T, Nakajo M. An analysis of the physiological FDG uptake in the stomach with the water gastric distention method. Eur J Nucl Med Mol Imaging. 2007;34:1815-1818. [PubMed] [DOI] |
| 13. | Koga H, Sasaki M, Kuwabara Y, Hiraka K, Nakagawa M, Abe K, Kaneko K, Hayashi K, Honda H. An analysis of the physiological FDG uptake pattern in the stomach. Ann Nucl Med. 2003;17:733-738. [PubMed] [DOI] |
| 14. | Takahashi H, Ukawa K, Ohkawa N, Kato K, Hayashi Y, Yoshimoto K, Ishiyama A, Ueki N, Kuraoka K, Tsuchida T. Significance of (18)F-2-deoxy-2-fluoro-glucose accumulation in the stomach on positron emission tomography. Ann Nucl Med. 2009;23:391-397. [PubMed] [DOI] |
| 15. | Alakus H, Batur M, Schmidt M, Drebber U, Baldus SE, Vallböhmer D, Prenzel KL, Metzger R, Bollschweiler E, Hölscher AH. Variable 18F-fluorodeoxyglucose uptake in gastric cancer is associated with different levels of GLUT-1 expression. Nucl Med Commun. 2010;31:532-538. [PubMed] |
| 16. | Yamada A, Oguchi K, Fukushima M, Imai Y, Kadoya M. Evaluation of 2-deoxy-2-[18F]fluoro-D-glucose positron emission tomography in gastric carcinoma: relation to histological subtypes, depth of tumor invasion, and glucose transporter-1 expression. Ann Nucl Med. 2006;20:597-604. [PubMed] [DOI] |
| 17. | Kawamura T, Kusakabe T, Sugino T, Watanabe K, Fukuda T, Nashimoto A, Honma K, Suzuki T. Expression of glucose transporter-1 in human gastric carcinoma: association with tumor aggressiveness, metastasis, and patient survival. Cancer. 2001;92:634-641. [DOI] |
| 18. | Stahl A, Ott K, Weber WA, Becker K, Link T, Siewert JR, Schwaiger M, Fink U. FDG PET imaging of locally advanced gastric carcinomas: correlation with endoscopic and histopathological findings. Eur J Nucl Med Mol Imaging. 2003;30:288-295. [PubMed] [DOI] |
| 19. | Esteves FP, Schuster DM, Halkar RK. Gastrointestinal tract malignancies and positron emission tomography: an overview. Semin Nucl Med. 2006;36:169-181. [PubMed] [DOI] |
| 20. | Rosenbaum SJ, Stergar H, Antoch G, Veit P, Bockisch A, Kühl H. Staging and follow-up of gastrointestinal tumors with PET/CT. Abdom Imaging. 2006;31:25-35. [PubMed] [DOI] |
| 21. | Sohn YJ, Jang JS, Choi SR, Kwon HC, Jung GJ, Kim MC, Jeong JS. Early detection of recurrence after endoscopic treatment for early gastric cancer. Scand J Gastroenterol. 2009;44:1109-1114. [PubMed] [DOI] |
| 22. | Terauchi T, Murano T, Daisaki H, Kanou D, Shoda H, Kakinuma R, Hamashima C, Moriyama N, Kakizoe T. Evaluation of whole-body cancer screening using 18F-2-deoxy-2-fluoro-D-glucose positron emission tomography: a preliminary report. Ann Nucl Med. 2008;22:379-385. [PubMed] [DOI] |
| 23. | Tsujimoto H, Sugasawa H, Ono S, Ichikura T, Yamamoto J, Hase K. Has the accuracy of preoperative diagnosis improved in cases of early-stage gastric cancer? World J Surg. 2010;34:1840-1846. [PubMed] [DOI] |
| 24. | Chen J, Cheong JH, Yun MJ, Kim J, Lim JS, Hyung WJ, Noh SH. Improvement in preoperative staging of gastric adenocarcinoma with positron emission tomography. Cancer. 2005;103:2383-2390. [PubMed] [DOI] |
| 25. | Kwee RM, Kwee TC. Imaging in assessing lymph node status in gastric cancer. Gastric Cancer. 2009;12:6-22. [PubMed] [DOI] |
| 26. | Mukai K, Ishida Y, Okajima K, Isozaki H, Morimoto T, Nishiyama S. Usefulness of preoperative FDG PET for detection of gastric cancer. Gastric Cancer. 2006;9:192-196. [PubMed] [DOI] |
| 28. | 胡 晓燕, 吴 湖炳, 王 全师, 周 文兰, 李 洪生, 王 丽娟. 18F-FDG PET/CT显像对胃癌术前分期的临床价值. 中国临床医学影像杂志. 2010;21:852-855. |
| 29. | Tian J, Chen L, Wei B, Shao M, Ding Y, Yin D, Yao S. The value of vesicant 18F-fluorodeoxyglucose positron emission tomography (18F-FDG PET) in gastric malignancies. Nucl Med Commun. 2004;25:825-831. [PubMed] [DOI] |
| 30. | Zhu Z, Li F, Mao Y, Cheng W, Cheng X, Dang Y. Improving evaluation of primary gastric malignancies by distending the stomach with milk immediately before 18F-FDG PET scanning. J Nucl Med Technol. 2008;36:25-29. [PubMed] [DOI] |