修回日期: 2012-08-24
接受日期: 2012-10-16
在线出版日期: 2012-10-28
目的: 对比评估内镜下套扎或硬化剂治疗与内镜治疗联合普萘洛尔对预防食管静脉曲张破裂再出血的疗效.
方法: 将69例肝硬化患者随机分为2组, 即单纯内镜治疗组(套扎或硬化剂治疗)40例和联合治疗组(套扎或硬化剂治疗后服用普萘洛尔)29例. 随访1年以上并评估治疗后再出血情况、死亡率及再出血相关死亡率, 并根据日本门脉高压协会诊断标准评估两种治疗方法对内镜下食管曲张静脉外观特征的影响.
结果: 治疗前后2组患者肝功能、血常规、电解质无显著差异. 单纯内镜治疗后食管曲张静脉的直径显著减小(治疗前 vs 治疗后, 10.92±2.91 vs 8.45±2.26, P<0.05), 联合治疗组曲张静脉直径虽减小但不具有统计学意义(治疗前vs 治疗后, 10.14±2.46 vs 8.95±2.21, P>0.05). 治疗后联合治疗组曲张静脉近端距门齿距离明显下移(治疗前 vs 治疗后, 22.79±2.83 vs 24.85±3.96, P<0.05), 且曲张静脉表面红色征较治疗前明显减少(治疗前 vs 治疗后, 100% vs 76.19%, P<0.05). 与单纯内镜治疗组相比, 联合治疗组胃底静脉曲张(治疗前 vs 治疗后, 10.34% vs 28.10%, P<0.05)及门脉高压性胃病的发生率均高于治疗前(治疗前 vs 治疗后, 10.34% vs 42.86%, P<0.05). 2组曲张静脉形态均主要由串珠状转变为蚯蚓状, 且均具有统计学意义(P<0.05). 2组间再出血率(单纯内镜治疗组 vs 联合治疗组, 50.00% vs 51.71%, P>0.05)无统计学差异, 但联合治疗组患者死亡率显著低于单纯内镜治疗组(联合治疗组 vs 单纯内镜治疗组, 7.41% vs 27.50%, P<0.05), 且2组患者主要的死因为上消化道再出血.
结论: 内镜治疗后联合普萘洛尔预防食管静脉曲张破裂再出血在一定程度上可以降低患者死亡风险、减少内镜下曲张静脉高危再出血因素.
引文著录: 王进广, 孔德润. 内镜干预及联合普萘洛尔预防食管静脉曲张破裂再出血的疗效. 世界华人消化杂志 2012; 20(30): 2944-2950
Revised: August 24, 2012
Accepted: October 16, 2012
Published online: October 28, 2012
AIM: To compar e the efficacy of endoscopic variceal ligation (EVL) or endoscopic injection sclerotherapy (EIS) alone versus EVL or EIS plus propranolol in the prophylaxis of esophageal variceal rebleeding.
METHODS: Sixty-nine cirrhotic patients were divided randomly into endoscopic intervention group (EIG, n = 40; EVL or EIS) and combination intervention group (CIG, n = 29; EVL or EIS plus propranolol). The mortality, mortality due to rebleeding, and rate of rebleeding were compared between the two groups. All patients were followed for more than one year. In addition, changes in endoscopic characteristics of esophageal varices were evaluated according to the criterion of the Japan Society for Portal Hypertension.
RESULTS: There were no significantly differences in liver function, routine blood parameters, and serum electrolytes between the two groups. After intervention, the diameter of varices decreased significantly in the EIG group (10.92 ± 2.91 vs 8.45 ± 2.26, P < 0.05), but showed no significance in the CIG group (10.14 ± 2.46 vs 8.95 ± 2.21, P > 0.05). The distance from the proximal end of varices to the fore-tooth (22.79 ± 2.83 vs 24.85 ± 3.96, P < 0.05) and the rate of recurrence of red signs in varices (100% vs 76.19%, P < 0.05) decreased significantly after intervention in the CIG group. The morbidity of gastric varices and portal hypertensive gastropathy were both higher after intervention in the CIG group (10.34% vs 28.10%, P < 0.05; 10.34% vs 42.86%, P < 0.05). The appearance of varices in both groups changed from rosary-like to earthworm-like pattern. The rate of rebleeding between two groups displayed no significant difference (50.00% vs 51.71%, P > 0.05). However, the mortality in the CIG group was significantly lower than that in the EIG group (27.50% vs 7.41%, P < 0.05), and the main cause of death in both groups was upper gastrointestinal bleeding.
CONCLUSION: Endoscopic intervention combined with propranolol can decrease the risk of death and reduce endoscopic re-bleeding in the prevention of esophageal variceal re-bleeding.
- Citation: Wang JG, Kong DR. Efficacy of endoscopic intervention alone versus endoscopic intervention plus propranolol in the prophylaxis of esophageal variceal rebleeding. Shijie Huaren Xiaohua Zazhi 2012; 20(30): 2944-2950
- URL: https://www.wjgnet.com/1009-3079/full/v20/i30/2944.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i30.2944
食管静脉曲张是肝硬化失代偿期的严重并发症, 常导致患者因上消化道出血而致病情加重或死亡. 目前, 国内外针对食管静脉曲张破裂出血的预防和治疗有多种临床干预措施, 均具有一定的疗效[1-3]. 与其他干预措施相比, 内镜下套扎或硬化剂治疗具有创伤小、恢复快、费用低、患者易接受等优点, 已在临床广泛开展. 目前国内外研究表明, 内镜下治疗可以有效地预防出血, 降低患者因出血而导致的死亡率[4]. 此外, 临床上开展通过药物预防出血也收到一定的成效, 特别是对非选择性β-肾上腺素受体阻滞剂普萘洛尔的研究和临床应用较普遍, 且多与内镜治疗联合预防食管曲张静脉破裂出血[5]. 国内外众多研究者已经开展了多项研究以评估普萘洛尔预防出血时患者血流动力学的变化, 但很少涉及到内镜或药物治疗后食管曲张静脉内镜下直观表现的变化情况[6,7]. 本研究旨在评估内镜及联合药物治疗后对曲张静脉的影响, 同时比较两种治疗方式用于预防再出血疗效的长期随访情况.
选取2005-2012年在我院消化内科住院且经临床资料、影像学或肝穿刺活检明确诊断肝硬化的患者69例, 其中男50例, 女19例, 最小年龄19岁, 最大82岁, 平均年龄50岁. 肝硬化病因为: 乙肝后肝硬化49例, 隐源性肝硬化7例, 酒精性肝硬化5例, 原发性胆汁性肝硬化3例, 特发性门脉高压2例, 血吸虫性肝硬化2例, 布加综合征1例. 所有患者既往均有消化道出血史, 活动性出血停止1 wk后接受内镜治疗或药物治疗. 其中套扎治疗36例, 硬化剂治疗33例. 将患者随机分为单纯内镜治疗组(40例)与联合治疗组(29例). 本研究排除有服用普萘洛尔禁忌的患者, 排除标准如下: 哮喘病史或有支气管痉挛病史者; 静息基础心率低于55次/min或静息基础血压低于90/60 mmHg; 伴有Ⅲ度或ⅡB房室传导阻滞; 严重或急性心衰的患者; 肝功能Child-Pugh C级的患者; 伴有肝性脑病或门静脉血栓; 年龄<18岁或>85岁. 本研究同时排除不愿合作者或服药后不耐受者.
1.2.1 内镜处置及评估项目: 患者入院后经内科保守治疗, 待活动性出血停止1 wk后行内镜下套扎或硬化剂治疗. 同时根据日本门脉高压研究协会食管静脉曲张内镜所见记录标准[8]评估内镜下曲张静脉的外观表现, 包括食管曲张静脉起始端距门齿距离、曲张静脉数量、曲张静脉直径及外观形态, 有无红色征、血栓头、血泡、血管间交通支, 同时评估曲张静脉严重程度. 患者于每次治疗2 mo后再次进行内镜治疗, 或于再发出血后行内镜治疗, 并同时记录上述曲张静脉特征. 服用普萘洛尔的患者在再次出血时同时行内镜检查或治疗, 记录内镜下曲张静脉表现. 出院后继续服用普萘洛尔, 起始量为10 mg, tid, 并根据患者的血压、心率变异情况调整用量, 直至心率降至55次/min, 或降至基础心率的75%以下, 或患者最大耐受量, 同时患者血压不得低于90/60 mmHg, 否则予以排除. 本实验中患者服用普萘洛尔最小量为40 mg, 最大为80 mg, 最长服药时间36 mo, 最短12.5 mo, 平均15.5 mo.
1.2.2 内镜评估: 采用日本Olympus公司GIF-XQ260电子胃镜评估患者食管曲张静脉特征. 所有患者在接受首次套扎或硬化剂治疗时记录食管曲张静脉直径、曲张静脉近端距门齿距离、曲张静脉数量、形态及严重程度, 同时评估有无红色征、血栓头、血泡、静脉间交通支. 患者在接受最后一次内镜治疗或检查时再次记录上述曲张静脉特征. 内镜下曲张静脉特征的评估由固定人员操作.
1.2.3 随访: 患者经内科治疗好转后出院, 长期随访患者服药情况及再发出血率、死亡情况. 重点记录患者服药后血压、心率变异情况、再发出血率、死亡率以及再出血相关死亡率. 同时定期通知患者复查肝功能、血常规、止凝血及电解质, 并记录检查结果. 本研究中最长随访时间为95.5 mo, 最短为12.5 mo, 平均21.5 mo, 直至患者行脾切除、分流/断流术、肝移植的临床干预, 或直至患者死亡.
统计学处理 采用SPSS13.0软件包处理实验数据. 计量资料采用mean±SD表示, 计数资料采用率表示. 计量资料的组内差异性比较采用方差齐性检验(F检验)及独立样本资料的t检验方法分析. 计数资料间率的比较采用四格表Fisher确切概率法检验. 采用Cox回归模型及Log-Rank检验法分析两组间的出血差异性, 两组间组间死亡率的比较用Fisher确切概率法分析. 两组出血峰值分布采用中位数M及四分位数间距Q表示. 检验水准P = 0.05.
比较患者经治疗后肝功能、血常规、电解质及凝血状况, 具体结果见表1.
| 单纯内镜治疗组 | 联合治疗组 | |||
| 治疗前 | 治疗后 | 治疗前 | 治疗后 | |
| 白蛋白(g/L) | 30.16±5.66 | 30.84±5.95 | 33.13±8.09 | 34.84±6.78 |
| 胆红素(μmol/L) | 20.64±9.94 | 21.60±13.07 | 23.92±17.54 | 19.07±11.13 |
| ALT(U/L) | 37.38±24.22 | 26.50±13.25 | 43.54±37.25 | 27.41±15.11 |
| AST(U/L) | 44.16±19.74 | 33.00±10.59 | 45.64±33.70 | 34.18±12.13 |
| PT(s) | 17.21±5.30 | 17.12±2.37 | 16.09±2.64 | 15.62±2.41 |
| PT延长时间(s) | 1.95±3.70 | 1.92±1.56 | 1.21±2.15 | 0.99±1.22 |
| 肝功能评分(n) | 7.67±2.03 | 7.78±2.33 | 7.35±1.44 | 6.22±1.52 |
| 血红蛋白(g/L) | 73.68±22.15 | 89.20±31.33 | 82.14±24.33 | 85.79±30.81 |
| 白细胞(×109/L) | 4.38±2.13 | 4.30±3.04 | 5.03±3.90 | 4.70±3.13 |
| 血小板(×109/L) | 121.32±113.24 | 82.20±61.03 | 93.57±60.70 | 131.21±91.93 |
| 血钠(mmol/L) | 136.86±6.79 | 141.07±2.60 | 136.91±8.36 | 128.71±36.50 |
| 血氯(mmol/L) | 102.75±7.52 | 105.78±1.65 | 104.75±3.21 | 106.21±3.17 |
| 腹水量(cm) | 4.39±2.90 | 1.79±2.99 | 2.83±3.37 | 0.92±1.62 |
每位研究对象在最初都接受内镜治疗, 同时至少再接受一次内镜检查或治疗以评估患者曲张静脉内镜下的变化. 结果如表2所示.
| 单纯内镜治疗组 | 联合治疗组 | |||
| 治疗前 | 治疗后 | 治疗前 | 治疗后 | |
| 曲张静脉位置(cm) | 23.69±3.53 | 24.55±4.06 | 22.79±2.83 | 24.85±3.96 |
| 曲张静脉数量 | 3.79±0.61 | 3.91±0.29 | 3.46±0.79 | 3.70±0.73 |
| 曲张静脉直径(mm) | 10.92±2.91 | 8.45±2.26 | 10.14±2.46 | 8.95±2.21 |
| 曲张静脉形态(n, 串珠状/蚯蚓状/ 蔓状/结节状/扁平状/其他)(%) | 87.18/5.12/2.56/ 2.56/2.56/0 | 27.27/59.10/0/ 0/13.63/0 | 93.10/6.90/0/ 0/0/0 | 38.10/42.85/4.76/ 4.76/9.52/0 |
| 红色征(%) | 94.87 | 81.82 | 100 | 76.19 |
| 静脉间交通支(%) | 12.82 | 0 | 0 | 4.76 |
| 血泡(%) | 10.26 | 4.35 | 6.90 | 9.52 |
| 血栓头(%) | 2.56 | 4.55 | 10.34 | 4.76 |
| 曲张静脉严重程度(轻/中/重)(%) | 0/2.56/97.44 | 0/13.64/86.36 | 0/0/100 | 0/14.29/85.71 |
| 血管破口(%) | 5.13 | 13.64 | 10.34 | 4.76 |
| 胃底静脉曲张(%) | 20.08 | 13.64 | 10.34a | 38.10a |
| 门脉高压性胃病(%) | 7.69 | 13.64 | 10.34a | 42.86a |
| 心率(次/min) | - | - | 76.70±4.89 | 64.00±6.62 |
| 平均内镜治疗次数 | 1.68±0.80 | 1.90±0.90 | ||
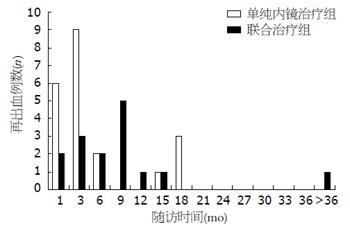
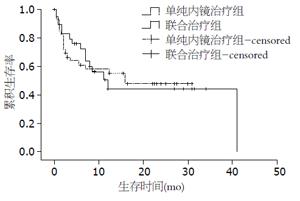
2.3.1 再出血情况: 根据随访时限将随访记录划分为14个时间段, 分别为首次内镜治疗后1、3、6、6、12、15、18、21、24、27、30、33、36 mo及36 mo以上, 以统计分析患者再出血、死亡情况. 单纯内镜治疗组患者再出血例数为20例, 共计34人次, 平均0.85次/人±1.17次/人; 而联合治疗组患者再出血例数为15例, 共计31人次, 平均为1.07次/人±1.25次/人. 2组间再出血情况无统计学意义(P>0.05). 本研究中2组患者再出血随时间分布情况及2组间再出血率差异见图1, 2.
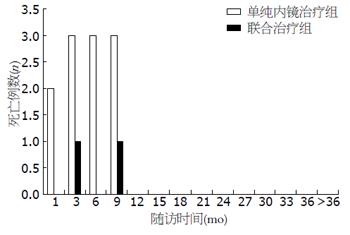
2.3.2 两组患者死亡率情况比较: 随访过程的终点为患者采取外科手术、TIPS、肝移植或死亡. 本研究中所有患者在接受其他预防出血措施干预前均有消化道出血史, 且无患者因不能耐受服药而排除出研究组. 本研究中共有13例患者发生死亡, 其中单独内镜治疗组死亡11例, 死亡率为27.5%(11/40); 联合治疗组死亡2例, 死亡率为6.9%(2/29), 2组间死亡率比较具有统计学意义(P<0.05). 与单纯内镜治疗相比, 经过内镜联合普萘洛尔治疗后患者死亡率明显降低(图3).
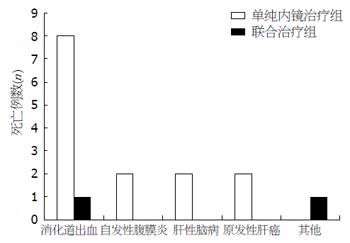
2.3.3 两组患者死因分布情况: 2组患者在接受不同的处理后死亡相关因素分布情况见图4. 图中对导致患者死亡的因素进行拆分归类, 如将死因"消化道出血伴SBP"拆分为"消化道出血"和"SBP"分别统计, 依次类推.
普萘洛尔用于预防食管静脉曲张破裂出血已有多年, 且临床对比观察发现其预防食管曲张静脉破裂导致消化道出血疗效确切. 本研究采用随机对照法评估内镜治疗后服用普萘洛尔预防曲张静脉再出血的疗效.
本研究中共有患者69例, 所有患者均接受内镜套扎或硬化剂治疗, 将内镜治疗后患者随机分为单纯内镜治疗组和内镜治疗后服用普萘洛尔的联合治疗组. 从表1中可以看出, 经过干预后的长期随访发现, 虽然2种治疗方法对患者肝功能、血常规、电解质的生化指标均无显著影响, 但联合治疗组患者在接受治疗后反映肝功能的生化指标, 如血清白蛋白水平(治疗前 vs 治疗后, 33.13±8.09 vs 34.84±6.78, P>0.05)较治疗前有所增加, 总血清胆红素水平(治疗前 vs 治疗后, 23.92±17.54 vs 19.07±11.13, P>0.05)、PT(治疗前 vs 治疗后, 16.09±2.64 vs 15.62±2.41, P>0.05)、PT延长时间(治疗前 vs 治疗后, 1.21±2.15 vs 0.99±1.22, P>0.05)、腹水量(治疗前 vs 治疗后, 2.83±3.37 vs 0.92±1.62, P>0.05)均较治疗前有所降低, 总体肝功能Child-Pugh评分(治疗前 vs 治疗后, 7.35±1.44 vs 6.22±1.52, P>0.05)较前减小, 而单纯内镜治疗组上述指标变化不明显. 这在一定程度上也反映了普萘洛尔预防食管曲张静脉破裂出血的效应与肝功能状态改善的相关性. 有研究表明[9,10], 肝功能状态是食管曲张静脉破裂出血的危险因素, 特别是血清白蛋白水平与腹水的存在情况, 但普萘洛尔预防曲张静脉出血的效应与肝功能改善之间的具体机制尚不明确. 我们同时观察到, 联合治疗组患者血小板计数较治疗前升高(治疗前 vs 治疗后, 93.57±60.70 vs 131.21±91.92, P>0.05), 这提示, 联合普萘洛尔治疗可能在一定程度上改善脾功能亢进、减少血小板的消耗从而降低再出血风险. 这与既往许多研究报道的结果相一致[11,12]. 另外, 服用普萘洛尔治疗后, 内镜下所见患者食管曲张静脉近端距门齿距离(治疗前 vs 治疗后, 22.79±2.83 vs 24.85±3.96, P<0.05)明显下移, 且红色征(治疗前 vs 治疗后, 100% vs 76.19%, P<0.05)显著减少, 这在一定程度上提示门脉压力的降低及再出血风险的减小, 而单纯内镜治疗组患者中曲张静脉近端距门齿的距离虽下移、红色征发生率减少, 但均不具有统计学意义. 研究发现, 联合治疗组患者胃底静脉曲张(治疗前 vs 治疗后, 10.34% vs 38.10%, P<0.05)及门脉高压性胃病(治疗前 vs 治疗后, 10.34% vs 42.86%, P<0.05)的发生率较治疗前显著地升高. 与单纯内镜治疗组(治疗前 vs 治疗后, 10.92±2.91 vs 8.45±2.26, P<0.05)相比, 联合治疗组患者食管曲张静脉直径没有明显改善(治疗前 vs 治疗后, 10.14±2.46 vs 8.95±2.21, P>0.05). 这种差异性可能与内镜治疗的方式及次数有关. 本研究中, 联合治疗组患者平均内镜治疗次数多于单纯内镜治疗组(单纯内镜治疗组 vs 联合治疗组, 1.68±0.80 vs 1.90±0.90, P>0.05), 可能由此引起的侧支循环开放的效应超过加用普萘洛尔后降低门脉压的效应, 从而导致联合治疗组门脉高压性胃病及胃底静脉曲张的发生率较治疗前升高的差异, 但这并不能代表两组患者药物疗效的差异. 有研究表明[13], 内镜下食管曲张静脉套扎及硬化剂治疗对食管曲张静脉侧支循环的再次形成及门脉高压性胃病的发病率有明显影响, 且两种治疗方式之间存在差异. 食管曲张静脉内镜下套扎或硬化剂治疗后门静脉压力的变化与治疗次数及治疗前有无其他的侧支循环开放有关[14,15], 行内镜下食管曲张静脉套扎或硬化剂治疗后, 治疗次数越多、脐静脉或胃底静脉侧支未形成或侧支较少可能会加重门脉血流动力学紊乱, 增加胃底静脉等侧支循环负荷. 正常情况下, 胃左静脉为向肝型血流, 但门脉高压发生后胃左静脉成为食管曲张静脉的主要血供来源. 在此情况下, 该静脉通路血流方向可以转变为离肝型从而促进食管曲张静脉的形成. Pereira等[16]研究发现, 经过内镜下套扎或硬化剂治疗后, 门脉高压状态下的胃左静脉离肝型血流可以转变为向肝型或双向型, 从而减少曲张静脉内血流量并降低食管静脉压, 但同时可能会由于食管曲张静脉分流受阻增加门静脉压力并促进其他侧支循环开放. 另外, 采用两种不同方法治疗后, 食管串珠状曲张静脉数均明显减少, 且主要转变为蚯蚓状, 两组患者均具有统计学意义(P<0.05). 这说明, 经过单纯内镜治疗或加服普萘洛尔治疗后, 2组患者再出血风险均明显降低. 此外, 两组患者经不同的治疗后曲张静脉严重程度均有好转, 但不具有统计学意义(P>0.05). 且单纯内镜治疗组食管曲张静脉红色征[治疗前 vs 治疗后, 94.87%(37/39) vs 81.82%(18/22), P>0.05]的表现没有得到显著的改善. 另需注意的是, 虽然两组在血栓头、血管破口、曲张静脉数量上的变化均无统计学意义(P>0.05), 但单纯内镜治疗组患者在经过治疗后, 上述内镜下曲张静脉特征的发生率较治疗前有所升高. 以上资料均表明, 在本研究中, 单纯内镜治疗组的疗效稍逊于联合治疗治疗组, 且前者再出血风险较后者高.
本研究发现, 在单纯内镜治疗组随访期间共20例患者发生消化道再出血, 共计34人次, 其中最少再出血次数为1次, 最多4次, 大多数再出血发生在初次内镜治疗后9 mo内, 以最初的3 mo内最高, 达9例; 且从图1中可以看出, 治疗后15-18 mo患者再出血率再次升高. 混合组患者共发生消化道再出血15例, 共计31人次, 最少出血1次, 最多3次, 出血集中发生在3-12 mo, 以9-12 mo最高. 再出血率在2组间均无统计学意义[单纯内镜治疗组 vs 联合治疗组, 20/40(50%) vs 15/29(51.72%), P>0.05]. 这说明, 从治疗后再出血情况看, 加服普萘洛尔并不能够显著的降低再出血率, 但可以延迟患者首次再出血峰值时间[单纯内镜治疗组: M = 2.00; Q(0.25, 12.75); 联合治疗组: M = 3.50; Q(1.50-6.25)]. 这种再出血率的差异与目前关于内镜联合普萘洛尔预防出血的研究结果相似. 有研究表明[17], 单纯套扎治疗及套扎后加用普萘洛尔均能够有效地预防高危静脉首次出血、降低曲张静脉再发率, 但并不能降低套扎患者首次出血及死亡风险. 这种差异性可能与本研究中所有患者既往均有出血史相关. De等[18]通过研究表明, 普萘洛尔预防出血的疗效与既往出血史及患者的年龄呈负相关. 同时, 也有研究发现[9], 内镜下套扎治疗后联合普萘洛尔与单硝酸异山梨酯治疗并不能降低患者的再出血风险, 再出血风险因素可能与肝功能(腹水、低蛋白血症)以及肝静脉压力梯度相关, 且Avgerinos等[10]研究发现, 与单纯服用普萘洛尔相比, 硬化剂治疗后加用普萘洛尔的患者再出血率、相关性胃病的发生率以及肝硬化相关并发症的发生率均升高, 独立的相关危险因素为血清白蛋白水平. 本研究中纳入的肝硬化患者全部为失代偿期肝硬化, 治疗前后腹水没有得到明显的改善, 且均存在低蛋白血症. 另外, 所有患者首次胃镜检查发现食管静脉曲张均为重度, 红色征明显, 出血风险极高. 既往研究表明[13,14], 食管曲张静脉套扎后门静脉压力的变化与治疗次数及有无其他的侧支循环开放有关. 虽然内镜下治疗可以破坏存在高危出血风险的曲张静脉, 但反复的内镜下套扎或硬化剂治疗及其他侧支循环的开放可能会促使门脉高压继续发展, 新生血管会再次形成并导致再出血[19]; 而联合治疗组患者在内镜治疗后加服普萘洛尔可以在一定程度上减少门静脉血流量, 相对而言从门脉高压发生发展的机制中延缓了食管静脉曲张的形成、延迟再出血的发生, 但并不能阻止门脉高压的发展.
由于联合治疗组患者死亡率较低, 无法进行Cox回归模型分析, 我们采用χ2检验分析2组间死亡率的差异. 通过对比2组患者的死亡率我们可以发现, 单纯内镜治疗组患者死亡率明显高于联合治疗组患者, 且两组患者间死亡率[单纯内镜治疗组 vs 联合治疗组, 11/40(27.5%) vs 2/29(6.90%), P<0.05]具有统计学意义. 在随访期间, 前者有11例发生死亡, 而后者仅2例死亡. 单纯内镜治疗组患者死亡主要发生在最初6 mo内, 且该组患者发生的死亡时间主要与我们观察到的消化道再出血的特征相一致. 这提示单纯内镜治疗后早期再出血应引起我们的高度重视. 而联合治疗组患者死亡总体风险较小. 本研究中, 联合治疗组患者共发生2例死亡, 其中1例发生在9-12 mo, 也与消化道再出血发生的高危时期相一致. 另一例死亡原因为心肌梗死, 与消化道出血无关. 通过两组对比我们猜测, 普萘洛尔不仅可以通过直接降低门脉压力降低患者死亡率及再出血相关的死亡率, 且可能还通过其他机制改善患者的一般状况及肝功能, 如降低肠道细菌移位和肠黏膜通透性、降低内毒素血症及自发性腹膜炎(SBP)的发生率[20-22], 这从死因分析中可以看出, 单纯内镜治疗组有2例发生SBP, 而联合治疗组无病例发生. 且有研究表明[22,23], 上述病理生理状态可能与患者的出血风险及死亡率相关.
因此, 我们需要高度重视患者在接受内镜治疗后早期的再出血、死亡情况及再出血相关的死亡. 对于单纯内镜治疗早期的患者, 仍需要采取内镜强化治疗或药物干预预防再出血, 这可以在很大程度上降低患者再出血率及再出血相关的死亡率, 但同时需注意, 反复多次内镜下治疗可能会促使其他侧支循环的开放, 特别是胃底静脉曲张的形成.
食管静脉曲张破裂出血是肝硬化门脉高压的一个严重并发症. 内镜下套扎或硬化剂治疗是预防出血的重要措施, 可以达到短期内快捷止血的效果. 普萘洛尔用于止血效果确切, 但药效发挥缓慢, 二者结合应用预防出血可能会达到更佳的效果.
黄晓东, 主任医师, 武汉市中心医院消化内科
Sarin等研究发现, 单纯套扎和套扎后服用普萘洛尔预防首次出血效果相似, 且后者曲张静脉再发率降低. 但Kumar等发现, 套扎治疗后服用普萘洛尔并不能降低患者的再出血率, 再出血相关的危险因素为腹水、低白蛋白和较高的肝静脉压力梯度.
本文采用前瞻性随机对照研究方法, 对内镜下套扎或硬化剂治疗以及内镜治疗后服用普萘洛尔后食管曲张静脉外观特征的改变及疗效进行了对比分析.
本文表明, 内镜治疗后服用普萘洛尔可以显著改善食管曲张静脉高危出血因素, 同时降低患者死亡率及再出血相关死亡率, 但仍需多样本的严格对照研究.
本文的科学性、创新性和可读性均能较好地反映我国胃肠病学和肝病学临床研究的先进水平.
编辑: 田滢 电编:闫晋利
| 1. | Chen YI, Ghali P. Prevention and management of gastroesophageal varices in cirrhosis. Int J Hepatol. 2012;2012:750150. [PubMed] [DOI] |
| 2. | Sarin SK, Gupta N, Jha SK, Agrawal A, Mishra SR, Sharma BC, Kumar A. Equal efficacy of endoscopic variceal ligation and propranolol in preventing variceal bleeding in patients with noncirrhotic portal hypertension. Gastroenterology. 2010;139:1238-1245. [PubMed] [DOI] |
| 4. | Hsu YC, Chung CS, Wang HP. Application of endoscopy in improving survival of cirrhotic patients with acute variceal hemorrhage. Int J Hepatol. 2011;2011:893973. [DOI] |
| 5. | Drastich P, Lata J, Petrtyl J, Bruha R, Prochazka V, Vanasek T, Zdenek P, Skibova J, Hucl T, Spicak J. Endoscopic variceal band ligation compared with propranolol for prophylaxis of first variceal bleeding. Ann Hepatol. 2011;10:142-149. [PubMed] |
| 6. | Rivet C, Robles-Medranda C, Dumortier J, Le Gall C, Ponchon T, Lachaux A. Endoscopic treatment of gastroesophageal varices in young infants with cyanoacrylate glue: a pilot study. Gastrointest Endosc. 2009;69:1034-1038. [PubMed] [DOI] |
| 7. | Jutabha R, Jensen DM, Martin P, Savides T, Han SH, Gornbein J. Randomized study comparing banding and propranolol to prevent initial variceal hemorrhage in cirrhotics with high-risk esophageal varices. Gastroenterology. 2005;128:870-881. [DOI] |
| 8. | Tajiri T, Yoshida H, Obara K, Onji M, Kage M, Kitano S, Kokudo N, Kokubu S, Sakaida I, Sata M. General rules for recording endoscopic findings of esophagogastric varices (2nd edition). Dig Endosc. 2010;22:1-9. [PubMed] [DOI] |
| 9. | Kumar A, Jha SK, Sharma P, Dubey S, Tyagi P, Sharma BC, Sarin SK. Addition of propranolol and isosorbide mononitrate to endoscopic variceal ligation does not reduce variceal rebleeding incidence. Gastroenterology. 2009;137:892-901, 901. e1. |
| 10. | Avgerinos A, Armonis A, Manolakopoulos S, Rekoumis G, Argirakis G, Viazis N, Vlachogiannakos J, Adamopoulos A, Kanaghinis T, Raptis SA. Endoscopic sclerotherapy plus propranolol versus propranolol alone in the primary prevention of bleeding in high risk cirrhotic patients with esophageal varices: a prospective multicenter randomized trial. Gastrointest Endosc. 2000;51:652-658. [DOI] |
| 11. | Sakai K, Iwao T, Oho K, Toyonaga A, Sata M. Propranolol ameliorates thrombocytopenia in patients with cirrhosis. J Gastroenterol. 2002;37:112-118. [DOI] |
| 13. | Sarin SK, Govil A, Jain AK, Guptan RC, Issar SK, Jain M, Murthy NS. Prospective randomized trial of endoscopic sclerotherapy versus variceal band ligation for esophageal varices: influence on gastropathy, gastric varices and variceal recurrence. J Hepatol. 1997;26:826-832. [DOI] |
| 14. | Lo GH, Liang HL, Lai KH, Chang CF, Hwu JH, Chen SM, Lin CK, Chiang HT. The impact of endoscopic variceal ligation on the pressure of the portal venous system. J Hepatol. 1996;24:74-80. [DOI] |
| 15. | Kanke K, Ishida M, Yajima N, Saito M, Suzuki Y, Masuyama H, Hiraishi H, Terano A. [Gastric mucosal congestion following endoscopic variceal ligation--analysis using reflectance spectrophotometry]. Nihon Shokakibyo Gakkai Zasshi. 1996;93:701-706. [PubMed] |
| 16. | Pereira SP, Wilkinson ML. Prospective randomized trial of endoscopic sclerotherapy versus variceal band ligation for esophageal varices: influence on gastropathy, gastric varices and variceal recurrence. Gastrointest Endosc. 1997;46:384-385. [DOI] |
| 17. | Sarin SK, Wadhawan M, Agarwal SR, Tyagi P, Sharma BC. Endoscopic variceal ligation plus propranolol versus endoscopic variceal ligation alone in primary prophylaxis of variceal bleeding. Am J Gastroenterol. 2005;100:797-804. [PubMed] [DOI] |
| 18. | De BK, Sen S, Biswas PK, Sengupta D, Biswas J, Santra A, Hazra B, Maity AK. Propranolol in primary and secondary prophylaxis of variceal bleeding among cirrhotics in India: a hemodynamic evaluation. Am J Gastroenterol. 2000;95:2023-2028. [PubMed] [DOI] |
| 20. | Senzolo M, Cholongitas E, Burra P, Leandro G, Thalheimer U, Patch D, Burroughs AK. beta-Blockers protect against spontaneous bacterial peritonitis in cirrhotic patients: a meta-analysis. Liver Int. 2009;29:1189-1193. [PubMed] [DOI] |
| 21. | Turnes J, Garcia-Pagan JC, Abraldes JG, Hernandez-Guerra M, Dell'Era A, Bosch J. Pharmacological reduction of portal pressure and long-term risk of first variceal bleeding in patients with cirrhosis. Am J Gastroenterol. 2006;101:506-512. [PubMed] [DOI] |
| 22. | Senzolo M, Fries W, Buda A, Pizzuti D, Nadal E, Sturniolo GC, Burroughs AK, D'Incà R. Oral propranolol decreases intestinal permeability in patients with cirrhosis: another protective mechanism against bleeding? Am J Gastroenterol. 2009;104:3115-3116. [PubMed] [DOI] |