修回日期: 2012-03-20
接受日期: 2012-04-19
在线出版日期: 2012-05-18
目的: 探讨线阵超声内镜对直肠子宫内膜异位症(rectal endometriosis, RE)的诊断价值.
方法: 对20例子宫内膜异位症患者于外科手术前行线阵超声内镜检查直肠, 超声扫描频率为7.5 MHz, 根据直肠壁内有无边界不规则的低回声结节或团块判断直肠是否受累, 并将超声内镜检查结果与手术中所见及术后病理进行比较.
结果: 20例患者中有12例经线阵超声内镜检查发现直肠壁内有异位子宫内膜病灶, 其余8例患者的直肠壁正常. 超声内镜诊断为RE的12例患者术中均见盆腔异位子宫内膜病灶与肠壁粘连紧密, 手术切除的直肠病灶送检均见子宫内膜组织. 超声内镜下未见直肠受累的8例患者盆腔子宫内膜异位病灶与肠壁无粘连或轻度粘连, 易分离, 分离缘组织送检未见子宫内膜组织. 线阵超声内镜检查结果与手术中所见及术后病理完全一致.
结论: 线阵超声内镜检查是诊断RE的可靠方法, 可对子宫内膜异位症患者是否伴有直肠受累做出准确的术前评估.
引文著录: 李银鹏, 王娜, 张琳, 朱惠明, 王立生, 师瑞月. 线阵超声内镜对直肠子宫内膜异位症的诊断价值. 世界华人消化杂志 2012; 20(14): 1252-1255
Revised: March 20, 2012
Accepted: April 19, 2012
Published online: May 18, 2012
AIM: To assess the value of linear endoscopic ultrasonography (EUS) in the diagnosis of rectal endometriosis (RE).
METHODS: Twenty patients with endometriosis were referred for linear EUS prior to the surgical intervention to evaluate the rectal involvement. RE was diagnosed by the presence of a hypoechoic nodule or mass with irregular margins in the rectal wall. Linear EUS findings were compared with the results of surgical exploration and histopathologic examination.
RESULTS: Linear EUS allowed to detect endometriotic lesions in the rectal wall in 12 cases, and the rectal wall was considered normal in 8 cases. In RE cases diagnosed by linear EUS, surgical exploration showed that pelvic ectopic endometrial lesions adhered closely to the rectal wall, and the histopathologic results confirmed infiltration of the rectal wall by endometriotic lesions. For the 8 patients with no linear EUS evidence of rectal infiltration, there was mild adhesion or no adhesion between pelvic ectopic endometrial lesions and the rectal wall, and histopathologic examination showed that the rectum was not involved by endometriotic lesions. The findings of linear EUS were coincident with those of surgical exploration and histopathologic examination.
CONCLUSION: Linear EUS is a reliable method for diagnosis of rectal endometriosis and can be used for accurate pre-surgical assessment of the rectal involvement in patients with endometriosis.
- Citation: Li YP, Wang N, Zhang L, Zhu HM, Wang LS, Shi RY. Value of linear endoscopic ultrasonography in the diagnosis of rectal endometriosis. Shijie Huaren Xiaohua Zazhi 2012; 20(14): 1252-1255
- URL: https://www.wjgnet.com/1009-3079/full/v20/i14/1252.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v20.i14.1252
子宫内膜异位症是指有功能的子宫内膜组织位于子宫腔以外的部位所引起的疾病. 若异位的子宫内膜浸润至腹膜后且深度超过5 mm即为深度浸润型子宫内膜异位症(deep infiltrating endometriosis, DIE). DIE常导致不孕和/与浸润深度相关的难治性盆腔疼痛[1], 其中约13%的病例伴有直肠受累[2], 即发生直肠子宫内膜异位症(rectal endometriosis, RE). RE虽是良性病, 但表现出恶性病变的生长特征. 异位病灶可随每次月经周期不断增大并向周围浸润生长, 对药物治疗反应差, 多需手术治疗[3,4], 但术前肠镜、钡剂灌肠造影、电子计算机X射线断层扫描技术(computed tomography, CT)或核磁共振成像(magnetic resonance imaging, MRI)检查常难以准确判断直肠是否受累[4]. 超声内镜是一种高频腔内超声, 因可对直肠壁进行清晰的分层次观察而常用于直肠占位性病变的诊断. 我院于2010年起采用线阵超声内镜对接受手术治疗的子宫内膜异位症患者进行术前直肠检查, 以了解是否伴有直肠受累, 并将超声内镜检查结果与手术中所见及术后病理进行比较, 以评判线阵超声内镜在RE中的诊断价值.
2010-10/2011-11在我院妇科诊断为子宫内膜异位症并接受手术治疗的20例患者, 术前均接受直肠线阵超声内镜检查以了解有无直肠受累. 患者均为已婚女性, 年龄25-43岁, 平均33.6岁±4.9岁, 其中16例主诉痛经, 1例主诉不孕, 3例痛经伴肛门坠胀感. 经肠镜检查5例患者见直肠内有广基隆起, 其中2例隆起表面黏膜光滑, 另3例表面粗糙不平, 其余患者肠镜检查直肠均无异常.
按肠镜检查法行肠道准备. 患者左侧卧位, 采用PENTAX EG3630U电子线阵扫描超声内镜检查, 探头频率5-7.5 MHz, 配HITACHI EUB 525超声诊断仪. 检查时进镜至直肠乙状结肠交界处. 先于内镜下仔细观察直肠壁有无溃疡或隆起病灶, 然后将探头朝向直肠前壁, 抽尽直肠腔内气体后, 再向直肠内注入脱汽水, 选用7.5 MHz频率自上而下并稍向左右旋转探头对直肠进行超声扫描. 超声下异位的子宫内膜累及直肠的判定方法参照文献[5], 若超声下观察到直肠壁内出现边界不规则的低回声结节或团块即判断为RE.
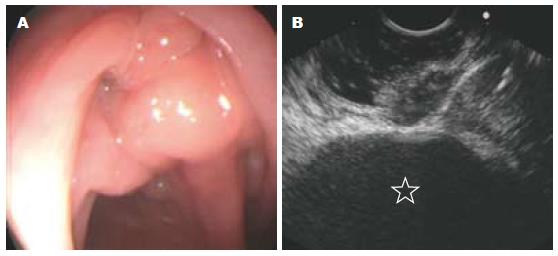
20例子宫内膜异位症患者中, 12例经超声扫描发现直肠壁中出现低回声结节或团块影, 边界不规则, 主体部分位于固有肌层, 可侵及黏膜下层或突破浆膜层, 黏膜层均未见受累(图1), 超声内镜诊断为RE. 其余8例超声扫描直肠壁均正常. 20例患者中5例内镜下见直肠广基隆起, 其中4例经超声内镜检查发现隆起为直肠壁内低回声病灶所致, 诊断为RE, 另1例超声扫描直肠壁层次结构完整清晰, 各层均未见增厚, 肠镜所见隆起为盆腔病变外压所致.
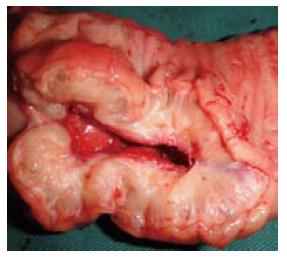
20例患者中, 超声内镜诊断为RE的12例患者术中均见盆腔异位子宫内膜病灶与肠壁粘连紧密, 不能分离, 其中2例行直肠盘状切除, 10例行直肠节段切除, 直肠病灶剖开后呈灰白改变(图2), 病灶送检均见子宫内膜组织. 超声内镜下未见直肠受累的8例患者术中发现盆腔子宫内膜异位病灶与肠壁无粘连或轻度粘连, 粘连易分离, 分离缘组织送检未见子宫内膜组织.
RE是DIE的严重形式. DIE主要发生在盆腔的后半部分, 可能与直肠子宫凹是盆腔内最低部位可关. 逆流的经血在重力作用下易积聚在直肠子宫凹, 经血内的子宫内膜向周边浸润生长, 因此, 盆腔DIE易伴发RE, 且异位子宫内膜病灶多位于直肠的前壁及侧壁. RE的治疗包括药物治疗和手术治疗2种方式. 药物治疗可缓解症状, 并可使病灶缩小, 但效果通常较短暂, 且肠壁内的纤维病灶停药后可重新激活. 手术彻底清除异位的子宫内膜病灶可避免复发并提高患者的生活质量[3,6,7], 因此, 目前治疗RE仍主张手术切除为主. DIE伴有直肠受累时, 手术通常需要妇科医生与胃肠外科医生的共同参与, 而术前准确判断直肠是否受累有利于手术方案的确定和手术人员的安排.
子宫内膜异位症是否伴有直肠受累术前诊断比较困难. 当异位的子宫内膜累及直肠黏膜时可出现经期便血症状, 但临床上黏膜受累的病例很少见[8], 更多见的是异位病灶于直肠的固有肌层及黏膜下层, 肠道症状多不明显. 本组12例确诊RE中仅3例表现出肠道症状, 其余主要以痛经为主诉, 提示有肠道症状的RE只是冰山一角. 此外, 虽然RE的肠道症状与月经周期相关, 但部分肠易激综合征患者的症状也受月经期的影响[9,10], 因此, 单从症状与月经周期的关系难以诊断RE. 肠镜检查仅对直肠黏膜受累型RE有意义, 当黏膜未受累时, 肠镜检查直肠黏膜大多光滑, 有时虽可见直肠前壁或侧壁隆起性包块, 但难以判断隆起是肠壁本身受累还是外压所致. 本组12例RE, 肠镜发现直肠隆起5例, 其中1例最后证实系外压所致, 表明肠镜对RE的诊断价值有限. 钡剂造影和CT对判断直肠壁是否受累也不够准确[4]. MRI对肠道子宫内膜异位症的诊断准确率也只有74.6%左右[11]. 超声内镜是内镜与超声的完美结合, 进入直肠后, 可在内镜直视下观察直肠管壁的情况, 同时能对直肠壁进行超声扫描. 直肠壁在超声内镜下通常可分为5层, 由内到外依次呈现高回声-低回声-高回声-低回声-高回声, 分别对应于黏膜层-黏膜肌层-黏膜下层-固有肌层-浆膜层, 当其中某一层次出现局灶性增厚或出现累及多层次的病灶, 超声下均可清晰分辨, 并可根据病灶回声的高低不同及内部回声是否均匀对病变做出初步判断.
超声内镜在直肠疾病方面既往主要用于直肠黏膜下肿瘤的诊断和直肠癌分期, 近年来有人[5,12]运用环扫型超声内镜对子宫内膜异位症患者行直肠检查以判断直肠是否受累, 结果显示环扫型超声内镜对判断子宫内膜异位症是否伴有直肠受累的敏感性和特异性均约90%. 本研究采用线阵超声内镜对20例子宫内膜异位症患者术前行直肠检查, 结果在12例(60%)患者直肠壁中发现低回声占位, 该低回声主要位于固有肌层, 可侵及黏膜下层及浆膜层. 其余8例直肠壁层次清晰, 未见肠壁出现增厚性改变和异常回声. 随后的术中所见及术后病理均证实线阵超声内镜所见的12例直肠壁内低回声占位为异位的子宫内膜组织, 表明线阵超声内镜可对子宫内膜异位症患者直肠是否受累进行准确的术前判断. 环扫型超声内镜对直肠扫描时, 每一扫描平面均为直肠的横断面, 因此, 可对直肠壁行环周检查, 行直肠扫描时将超声探头从直肠乙状结肠交界处向肛侧拉动即可, 不易遗漏病灶. 线阵超声镜检查则是对直肠行纵断面扫描, 要观察直肠全周时, 必须旋转镜身. 但异位的子宫内膜侵及直肠时, 病灶多位于直肠前壁和侧壁, 甚至累及直肠全周, 通常不单独累及后壁, 因此, 采用线阵超声扫描时, 只需将探头朝向直肠前壁并稍左右旋转即可. 本组研究结果也表明, 线阵超声镜诊断RE并不存在病灶遗漏问题, 是判断子宫内膜异位症是否累及直肠的有效手段.
值得注意的是, 由于直肠异位子宫内膜病灶在超声上可表现为跨越肠壁多个层次的低回声占位, 呈现出恶性病变的特征, 需与直肠其他低回声病变相区别. 直肠的平滑肌瘤或间质瘤虽在超声下也表现为低回声病变, 但此二者均局限于管壁的固有肌层或黏膜肌层内, 轮廓光滑, 边界清晰, 与RE较易区分. 诊断RE最重要的是与直肠癌相鉴别. 直肠癌为起源于直肠黏膜的恶性肿瘤, 其生长方式为由黏膜层向浆膜层方向浸润生长, 当RE累及黏膜层时两者在超声表现上不易鉴别, 但内镜下活检可明确诊断. 此外, 异位的直肠子宫内膜病灶存在恶变的可能[13-15], 但由于子宫内膜异位伴有直肠受累时多主张手术治疗, 因此, 术后病理有助于鉴别, 对于拒绝手术治疗者, 有必要行超声内镜引导下细针穿刺活检或追踪观察.
总之, 尽管线阵超声内镜的主要功能是用于超声引导下的细针穿刺活检和治疗, 但仍不失其基本的诊断价值. 对于DIE患者而言, 线阵超声内镜检查是诊断RE的可靠方法, 对术前判断子宫内膜异位症患者是否伴有直肠受累有重要作用.
直肠子宫内膜异位症(RE)常需手术治疗, 但术前诊断困难, 部分患者术前可能被漏诊或误诊. 而国内对于直肠子宫内膜异位症诊断研究的相关资料较少.
徐辉雄, 教授, 主任医师, 同济大学附属第十人民医院暨上海市第十人民医院超声科
肠镜检查、CT或钡剂灌肠检查对RE的诊断价值有限, 国外有研究用环扫型超声内镜对深度浸润型子宫内膜异位症(DIE)患者的直肠进行检查以了解肠道受累情况.
本研究以线阵超声内镜为工具, 通过线阵超声内镜检查评判子宫内膜异位症患者是否伴有直肠受累, 证实线阵超声内镜检查是诊断RE的一种无创伤且可靠的.
文章阐述了线阵超声内镜技术在直肠子宫内膜异位症中的应用, 为临床医生诊断RE提供了新的手段.
编辑: 张姗姗 电编:闫晋利
| 1. | Koninckx PR, Meuleman C, Demeyere S, Lesaffre E, Cornillie FJ. Suggestive evidence that pelvic endometriosis is a progressive disease, whereas deeply infiltrating endometriosis is associated with pelvic pain. Fertil Steril. 1991;55:759-765. [PubMed] |
| 2. | Chapron C, Fauconnier A, Dubuisson JB, Barakat H, Vieira M, Bréart G. Deep infiltrating endometriosis: relation between severity of dysmenorrhoea and extent of disease. Hum Reprod. 2003;18:760-766. [PubMed] [DOI] |
| 3. | Dousset B, Leconte M, Borghese B, Millischer AE, Roseau G, Arkwright S, Chapron C. Complete surgery for low rectal endometriosis: long-term results of a 100-case prospective study. Ann Surg. 2010;251:887-895. [PubMed] [DOI] |
| 4. | Houtmeyers P, Ceelen W, Gillardin JM, Dhondt M, Pattyn P. Surgery for gastrointestinal endometriosis: indications and results. Acta Chir Belg. 2006;106:413-416. [PubMed] |
| 5. | Bazot M, Malzy P, Cortez A, Roseau G, Amouyal P, Daraï E. Accuracy of transvaginal sonography and rectal endoscopic sonography in the diagnosis of deep infiltrating endometriosis. Ultrasound Obstet Gynecol. 2007;30:994-1001. [PubMed] [DOI] |
| 6. | Dubernard G, Piketty M, Rouzier R, Houry S, Bazot M, Darai E. Quality of life after laparoscopic colorectal resection for endometriosis. Hum Reprod. 2006;21:1243-1247. [PubMed] [DOI] |
| 7. | Minelli L, Fanfani F, Fagotti A, Ruffo G, Ceccaroni M, Mereu L, Landi S, Pomini P, Scambia G. Laparoscopic colorectal resection for bowel endometriosis: feasibility, complications, and clinical outcome. Arch Surg. 2009;144:234-239; discussion 239. [PubMed] [DOI] |
| 8. | Remorgida V, Ferrero S, Fulcheri E, Ragni N, Martin DC. Bowel endometriosis: presentation, diagnosis, and treatment. Obstet Gynecol Surv. 2007;62:461-470. [PubMed] [DOI] |
| 9. | Adeyemo MA, Spiegel BM, Chang L. Meta-analysis: do irritable bowel syndrome symptoms vary between men and women? Aliment Pharmacol Ther. 2010;32:738-755. [PubMed] [DOI] |
| 10. | Jane ZY, Chang CC, Lin HK, Liu YC, Chen WL. The association between the exacerbation of irritable bowel syndrome and menstrual symptoms in young Taiwanese women. Gastroenterol Nurs. 2011;34:277-286. [PubMed] [DOI] |
| 11. | Faccioli N, Foti G, Manfredi R, Mainardi P, Spoto E, Ruffo G, Minelli L, Mucelli RP. Evaluation of colonic involvement in endometriosis: double-contrast barium enema vs. magnetic resonance imaging. Abdom Imaging. 2010;35:414-421. [PubMed] [DOI] |
| 12. | Ribeiro HS, Ribeiro PA, Rossini L, Rodrigues FC, Donadio N, Aoki T. Double-contrast barium enema and transrectal endoscopic ultrasonography in the diagnosis of intestinal deeply infiltrating endometriosis. J Minim Invasive Gynecol. 2008;15:315-320. [PubMed] [DOI] |
| 13. | Kobayashi S, Sasaki M, Goto T, Asakage N, Sekine M, Suzuki T, Tsukada K, Yamasaki S, Ukawa S. Endometrioid adenocarcinoma arising from endometriosis of the rectosigmoid. Dig Endosc. 2010;22:59-63. [PubMed] [DOI] |
| 14. | Micha JP, Mendivil AA, Epstein HD, Laflamme LA, Goldstein BH. Endometrioid adenocarcinoma arising from endometriosis: a case report. J Reprod Med. 2011;56:507-510. [PubMed] |
| 15. | Peiretti M, Zakashansky K, Melis GB, Mais V. Unusual case of adenocarcinoma arising in endometriosis mimicking colorectal cancer in a young woman with a Müllerian anomaly. Fertil Steril. 2008;90:199.e13-e15. [PubMed] |