修回日期: 2011-05-23
接受日期: 2011-06-10
在线出版日期: 2011-06-18
目的: 研究抑制JNK信号通路对结肠癌HT-29细胞增殖和细胞凋亡的影响.
方法: 将人结肠癌细胞株HT-29分为正常对照组和JNK抑制剂组(用SP600125预处理细胞24 h), 用四甲基偶氮唑盐比色法(MTT法)检测细胞增殖水平, 用脱氧核酸末端转移酶介导的缺口末端标记法(TUNEL法)观察细胞凋亡情况.
结果: 使用SP600125处理后的HT-29细胞, Western blot法检测p-JNK表达水平. 与正常对照组比较p-JNK表达明显降低(0.246±0.044 vs 1.092±0.060, P<0.01). 与正常对照组比较, JNK抑制剂组细胞增殖水平明显下降(0.287±0.008 vs 0.479±0.012, P<0.01), 细胞凋亡指数明显升高(13.000±1.080 vs 1.000±0.147, P<0.01).
结论: 抑制JNK信号通路的激活, 可以显著降低人结肠癌细胞HT-29的增殖水平, 并能诱导其细胞凋亡.
引文著录: 张志永, 张谢夫. 抑制JNK信号通路对结肠癌HT-29细胞增殖和凋亡的影响. 世界华人消化杂志 2011; 19(17): 1830-1833
Revised: May 23, 2011
Accepted: June 10, 2011
Published online: June 18, 2011
AIM: To investigate the role of the c-Jun N-terminal kinase (JNK) signaling pathway in the proliferation and apoptosis of human colon carcinoma HT-29 cells.
METHODS: HT-29 cells were divided into two groups: normal control group and JNK inhibitor group (pretreated with SP600125 for 24 h). MTT assay was used to detect cell proliferation, and TUNEL assay was used to detect apoptosis.
RESULTS: The proliferation of HT-29 cells of the JNK inhibitor group was lower than that of the normal control group (0.287 ± 0.008 vs 0.479 ± 0.012, P < 0.01). The apoptosis index of HT-29 cells of the JNK inhibitor group was higher than that of the normal control group (13.000 ± 1.080 vs 1.000 ± 0.147, P < 0.01).
CONCLUSION: Inhibition of the JNK signaling pathway significantly inhibited cell proliferation but promoted apoptosis in human colon carcinoma cell line HT-29.
- Citation: Zhang ZY, Zhang XF. Inhibition of the JNK signaling pathway suppresses cell proliferation but promotes apoptosis in human colon carcinoma cell line HT-29. Shijie Huaren Xiaohua Zazhi 2011; 19(17): 1830-1833
- URL: https://www.wjgnet.com/1009-3079/full/v19/i17/1830.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v19.i17.1830
结肠癌是一种常见的恶性肿瘤. 近几年由于人们饮食习惯和饮食结构的改变以及人口老龄化, 我国结直肠癌的发病率和病死率均保持上升趋势. 其中, 结肠癌的发病率上升尤为显著, 大多数患者发现时已属于中晚期[1]. 常规的治疗手段如手术、化疗、放疗疗效并不理想. 因此, 进一步阐明结肠癌的发病机制, 寻找有效的干预靶点已经成为国内广大研究者关注的焦点. 本研究初步研究了c-Jun氨基末端酶(c-Jun N-terminal kinase, JNK)信号转导通路对结肠癌发病的影响.
人结肠癌细胞株HT-29来自中山大学医学院. 胎牛血清、RPMI 1640购自美国Gibco公司. JNK抑制剂SP600125购自上海碧云天公司. TUNEL细胞凋亡原位检测试剂盒及细胞全蛋白提取试剂盒购自南京凯基生物公司. p-JNK抗体购自北京博奥森公司. 辣根过氧化酶标记山羊抗兔IgG购自北京中杉金桥公司. HRP标记β-actin购自武汉博士德公司.
1.2.1 细胞培养及分组: 将HT-29细胞冻存管从液氮罐中取出, 迅速置于37 ℃水浴中, 轻轻摇晃令其尽快融化; 使用无菌吸管吸出细胞悬液, 转移至无菌离心管中, 滴加10 mL培养基, 1 000 r/min离心5 min; 将上清倒去后, 加入培养基作适当稀释, 制成单细胞悬液, 再转入无菌培养瓶中37 ℃培养箱中培养. 细胞培养2-3 d后, 更换1次培养液, 待细胞长满至80%左右时, 使用胰蛋白酶消化, 使细胞至漂浮状态, 终止消化后1:2分瓶传代. 将HT-29细胞分为正常对照组、JNK抑制剂组. JNK抑制剂组处理前1 d将对数生长期细胞用胰蛋白酶消化后, 接种于6孔板, 保证每孔有5×105个细胞; 用DMSO将JNK抑制剂SP600125稀释后加入到细胞培养基中, 轻轻晃动使其均匀分布, 使其总浓度60 μmol/L, 培养24 h后收集细胞, 用于细胞增殖以及细胞凋亡检测.
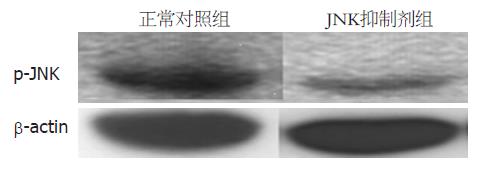
1.2.2 Western blot检测p-JNK蛋白的表达: HT-29细胞用PBS清洗2遍; 抽提细胞总蛋白并定量. 取50 μg蛋白样品到10% SDS-PAGE胶上样, 电压90 V, 恒压电泳120 min; 跑好的胶在转膜液中浸泡20 min; 从下至上分别放入滤纸、胶、PVDF膜、滤纸, 夹子夹好放入倒好转膜液的转膜槽中, 电压90 V, 恒压电泳120 min. 将膜取出, 加入5%脱脂奶粉的PBS室温封闭1 h. 分别加入一抗p-JNK(1:200), β-actin(1:1 000)到5%脱脂牛奶中, 在室温下振荡孵化1.5 h, 然后洗膜4次: 1×PBS 15 min 1次; 5 min 3次; 分别加入二抗(1:3 000)到5%脱脂牛奶中, 在室温孵化1 h, 洗膜4次: 1×PBS 15 min 1次; 5 min 3次;以1:40比例混合显色基质B液和A液, 均匀滴加膜上, 静置2 min, 用保鲜膜将膜包好, 轻轻挤出多余显色基质, 放入暗盒, 曝光4 min后, 蛋白表达情况使用凝胶成像分析系统进行检测. 获得的图像用软件ImageTool 3.0测灰度值, 并与内参相比得其相对值, 取4次重复实验结果的均值进行比较.
1.2.3 MTT法检测细胞增殖: HT-29细胞计数后, 以2×104的密度接种到96孔细胞培养板中; 细胞预处理后培养24 h, 显微镜下观察贴壁生长良好后每孔加入100 μL的MTT试剂, 继续培养4 h; 除去培养液, 每孔加入150 μL的无血清的DMSO, 振荡10 min充分融解结晶物; 选择570 nm波长, 在酶标仪上检测各孔吸光度值(A值). 每孔A值减去空白孔A值为测试孔A值. 活细胞数与A值成正比. 每组设4个复孔, 取其平均值.
1.2.4 TUNEL法检测细胞凋亡: 蒸馏水浸洗细胞爬片数次. 细胞爬片于PBS洗5 min×3次. 在细胞爬片上滴加TdT酶反应液, 37 ℃孵育1 h. 细胞爬片于PBS洗5 min×3次. 在细胞爬片上滴加streptavidin-HRP工作液, 37 ℃孵育30 min. 细胞爬片于PBS洗5 min×3次. DAB显色, 水洗终止反应. 苏木素复染1 min, 自来水冲洗5 min. 脱水、晾干、中性树胶封片, 结果观察. 结果分析方法: 选择10个典型视野, 高倍镜下计数至少1 000个肿瘤细胞, 凋亡指数(apoptosis index, AI) = TUNEL阳性肿瘤细胞数/肿瘤细胞数×100%. 每组设4个复孔, 取其平均值.
统计学处理 采用SPSS13.0统计学软件进行数据处理, 统计方法采用两独立样本t检验, 数据以mean±SD表示.
正常对照组、JNK抑制剂组HT29细胞中p-JNK的相对表达强度分别是1.092±0.060、0.246±0.044, 两组间差异具有统计学意义(P<0.01, 图1). 此结果表明, JNK抑制剂处理后, p-JNK蛋白的表达被抑制.
JNK抑制剂组HT-29细胞的增殖明显弱于正常对照组(0.287±0.008 vs 0.479±0.012, P<0.01), 这提示抑制JNK信号通路后, 能阻止结肠癌HT29细胞的增殖.
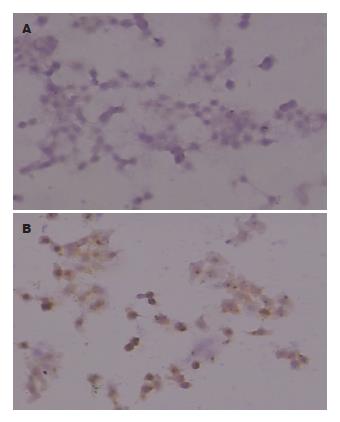
TUNEL阳性细胞显示以下特点: 细胞呈圆形、皱缩、核固缩、整个细胞着色深、细胞核内有较强的TUNEL阳性染色, 部分细胞质内也呈现少量阳性染色(图2). JNK抑制剂组的细胞凋亡指数比正常对照组升高(13.000±1.080 vs 1.000±0.147, P<0.01). 这说明抑制JNK信号通路后能促进结肠癌HT29细胞的凋亡.
JNK是1993年被Hibi等[2]发现的促分裂原活化蛋白激酶, 是促分裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)家族的主要成员之一, JNK信号途径可以调控细胞生长、癌基因转化、细胞分化和细胞凋亡等多种病理生理过程[3,4]. 近年来研究表明, JNK与多种疾病发生机制有关, 从而使JNK在临床上可作为一个潜在的分子治疗靶[5].
目前许多实验都观察到在肿瘤组织中JNK活性增高, JNK与肿瘤发生密切相关[6,7]. Uhlirova等[8]通过致癌物Ras/Raf诱导果蝇肿瘤形成, 发现Raf与JNK起协同作用, 诱导细胞异常增生. Nateri等[9]剔除小鼠c-Jun基因或者改变JNK磷酸化位点时, 能使小鼠肠道肿瘤变小, 肿瘤细胞减少, 并且延长小鼠的寿命. 但She等[10]的研究却发现, 在剔除了JNK基因的小鼠对TPA诱导的皮肤癌有显著敏感性, 并且肿瘤数目多、直径大, 表明JNK在皮肤癌的发生重是一个重要的抑制物. 这些研究结果提示JNK信号通路在肿瘤的发生重的作用可能相当复杂和多样化.
JNK信号通路与结肠和结肠癌的相关性也开受到关注. 最近的研究发现结肠癌细胞JNK磷酸化可激活其下游成员使结肠癌基质金属蛋白酶的分泌增加, 导致结肠癌细胞的运动和侵袭力增加, 最终促进癌细胞的转移[11]. 王若明等[12]通过免疫组织化学方法研究72例结直肠癌和40例正常大肠组织中JNK和MRP1蛋白表达及其关系. 结果表明, JNK蛋白在结直肠癌组织中的阳性表达率为47.22%, 明显高于在正常结肠组织中的表达(7.5%), JNK蛋白阳性表达还与肿瘤分化、淋巴结转移、远处转移及Dukes分期显著相关. 以上研究已经说明JNK信号通路的激活可能在促进结肠癌的发生发展中发挥了重要作用. 王晓艳等[13]研究指出抑瘤基因NGX6在结肠癌中主要通过抑制JNK通路的活性而发挥其抑瘤作用, 这提示阻断JNK信号通路对结肠癌具有一定的抑制作用. 本研究采用JNK信号通路的特异性抑制剂SP600125预处理人结肠癌HT-29细胞后, 肿瘤细胞的增殖明显得到抑制, 结果证实了抑制JNK信号通路的激活可以抑制结肠癌的增殖.
细胞凋亡是一个多基因参与、复杂的生理和病理过程, 研究肿瘤细胞的凋亡一直是肿瘤研究领域的重点和热点, 细胞凋亡与结直肠癌的发生发展有重要关系[14]. 目前, 通过诱导肿瘤细胞凋亡来治疗肿瘤备受人们关注. 郑江华等[15]探讨了JNK信号通路在δ氨基酮戊酸-光动力疗法诱导SW480细胞凋亡中的作用, 发现激活JNK信号通路可以抑制该疗法诱导SW480细胞凋亡. 本研究发现, JNK抑制剂组的人结肠癌HT-29细胞凋亡指数比正常对照组显著增强, 说明抑制JNK信号通路后能促进肿瘤细胞凋亡, 与郑江华等的报道结果一致. 提示我们JNK通路可能成为治疗结肠癌的新靶点, 抑制JNK通路的激活可以促进肿瘤细胞的凋亡从而发挥抗肿瘤效应. 干预JNK信号通路可以成为防治结肠癌的又一种策略.
JNK是在哺乳动物细胞内广泛存在的一种丝氨/苏氨酸蛋白激酶, 属于促分裂原活化蛋白激酶(MAPK)家族. 近年的研究表明JNK信号途径可以调控细胞生长、细胞分化、细胞凋亡、癌基因转化等多个重要的生物学过程, 与多种疾病相关.
房林, 副教授, 同济大学附属上海市第十人民医院普外科
近年来对JNK信号通路的研究主要集中在其激活后对多种生理过程的调节作用方面. 已经证明JNK信号功能的失调与神经退行性疾病、慢性炎症、出生缺陷、癌症等多种疾病的发生直接相关. JNK信号通路的调控方式, 以及其和其他信号通路的相互作用是当前本领域的研究热点.
She等研究表明JNK基因对TPA诱导的皮肤癌有明显的抑制作用, 而Nateri等的实验却表明JNK磷酸化位点发生突变的小鼠小肠肿瘤变小, 寿命延长.
本研究首次在人结肠癌HT-29细胞中研究了抑制JNK信号通路后其增殖和凋亡变化情况, 间接提示了在结肠癌组织中JNK过度表达可能起到了促进细胞增殖, 抑制细胞凋亡的作用.
本研究证实JNK信号通路对结肠癌的发生发展起重要作用, JNK信号通路可能是结肠癌治疗的潜在靶点之一.
本文结构合理, 条理清晰, 讨论得当, 具有较好的实用价值.
编辑: 李薇 电编:何基才
| 2. | Hibi M, Lin A, Smeal T, Minden A, Karin M. Identification of an oncoprotein- and UV-responsive protein kinase that binds and potentiates the c-Jun activation domain. Genes Dev. 1993;7:2135-2148. [PubMed] [DOI] |
| 3. | Johnson GL, Nakamura K. The c-jun kinase/stress-activated pathway: regulation, function and role in human disease. Biochim Biophys Acta. 2007;1773:1341-1348. [PubMed] |
| 4. | Lin MT, Beal MF. Mitochondrial dysfunction and oxidative stress in neurodegenerative diseases. Nature. 2006;443:787-795. [PubMed] [DOI] |
| 5. | Mori Y, Gotoh Y. [Role of the JNK signaling pathway]. Tanpakushitsu Kakusan Koso. 2008;53:1252-1257. [PubMed] |
| 6. | Wagner EF, Nebreda AR. Signal integration by JNK and p38 MAPK pathways in cancer development. Nat Rev Cancer. 2009;9:537-549. [PubMed] [DOI] |
| 8. | Uhlirova M, Jasper H, Bohmann D. Non-cell-autonomous induction of tissue overgrowth by JNK/Ras cooperation in a Drosophila tumor model. Proc Natl Acad Sci U S A. 2005;102:13123-13128. [PubMed] [DOI] |
| 9. | Nateri AS, Spencer-Dene B, Behrens A. Interaction of phosphorylated c-Jun with TCF4 regulates intestinal cancer development. Nature. 2005;437:281-285. [PubMed] [DOI] |
| 10. | She QB, Chen N, Bode AM, Flavell RA, Dong Z. Deficiency of c-Jun-NH(2)-terminal kinase-1 in mice enhances skin tumor development by 12-O-tetradecanoylphorbol-13-acetate. Cancer Res. 2002;62:1343-1348. [PubMed] |
| 13. | 王 晓艳, 沈 守荣, 刘 芬, 彭 娅, 李 桂源, 范 松青. 结肠癌中NGX6抑制EGFR/K-ras/JNK/c-Jun/cyclin D1信号通路的研究. 生物化学与生物物理进展. 2008;35:570-576. |