修回日期: 2011-03-08
接受日期: 2011-03-16
在线出版日期: 2011-04-08
目的: 研究外科超声吸引器(CUSA)系统在解剖性肝切除术中的断肝技术参数设置, 寻找最佳的断肝参数设置, 以提高CUSA在肝切除中临床效率.
方法: 优化CUSA技术参数设置, 将31例采用CUSA实施Glisson蒂横断式解剖性肝切除的肝实质占位患者分为两组: 优化参数设置组(n = 21)和厂家推荐参数设置组(n = 10). 对比分析两组手术时间、术中出血量、术中输血量, 术后腹腔引流量和肝功能康复情况.
结果: 两组患者均于术后4 wk内康复出院. 优化参数组和推荐参数组恶性肿瘤根治率分别为85.7%和90%, 组间无显著差异. 优化参数设置组手术时间短、出血量、输血量均优于推荐参数设置组(3.8 h±0.8 h vs 6.2 h±1.9 h; 1 150 mL±460 mL vs 2 900 mL±510 mL; 530 mL±300 mL vs 1 760 mL±1 700 mL, 均P<0.05), 优化设置组术后肝酶学康复优于推荐参数组, 而两组术后24 h引流量无显著差异.
结论: 优化CUSA参数设置可增加对肝组织的保护、减少术中出血和缩短手术时间, 从而显著提高断肝效果.
引文著录: 唐继红, 付必莽, 唐波, 李晗宇, 朱洪, 李铁汉, 刘锋, 张捷. 优化外科超声吸引器参数设置对解剖性肝切除的作用. 世界华人消化杂志 2011; 19(10): 1040-1044
Revised: March 8, 2011
Accepted: March 16, 2011
Published online: April 8, 2011
AIM: To evaluate the clinical effects of anatomic hepatectomy with Cavitron ultrasonic surgical aspirator (CUSA) using optimized parameter settings.
METHODS: Thirty-one patients with space-occupying lesions of the liver who underwent hepatectomy with CUSA were divided into two groups: patients using recommended parameters for CUSA (control group, n = 10) and those using optimized parameters (optimization group, n = 21). Total blood loss, blood transfusion, operative time, and recovery of liver function after operation were compared between the two groups.
RESULTS: All the patients recovered in 4 weeks after operation. Radical treatment was achieved in 90% of patients using recommended parameters and in 87.5% of those using optimized ones, with no significant different between the two groups. Total blood loss, blood transfusion, operative time, and recovery of liver function after operation were better in the optimization group than in the control group (3.8 h ± 0.8 h vs 6.2 h ± 1.9 h; 1 150 mL ± 460 mL vs 2 900 mL ± 510 mL; 530 mL ± 300 mL vs 1 760 mL ± 1 700 mL, all P < 0.05). The mean amount of abdominal drainage in 24 h after operation was not remarkably different between the two groups.
CONCLUSION: Using optimized parameters for CUSA can improve the clinical effects and efficiency of anatomic hepatectomy for patients with space-occupying lesions of the liver.
- Citation: Tang JH, Fu BM, Tang B, Li HY, Zhu H, Li TH, Liu F, Zhang J. Clinical effects of anatomic hepatectomy with Cavitron ultrasonic surgical aspirator using optimized parameter settings. Shijie Huaren Xiaohua Zazhi 2011; 19(10): 1040-1044
- URL: https://www.wjgnet.com/1009-3079/full/v19/i10/1040.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v19.i10.1040
肝部分切除是治疗肝脏占位性疾病的主要手段, 随着肝移植时代的到来现, 肝脏外科也进入到精准解剖学性肝切除时代. ExcelTM型外科超声吸引器(cavitron ultrasonic surgical aspirator, CUSA)的应用是最具代表性的新兴技术, 该设备精细而准确的解剖学高选择性切肝技术推动了肝切部分除技术的进步[1,2]. 因此, 熟练掌握该设备的使用技巧可以明显提高肝切除的效果. 我们在切肝过程中发现, 调整和优化CUSA系统参数设置可提高组织选择性、减少术中失血等, 从而获得较厂家推荐的参数设置更为理想的切肝效果. 本文以临床实践为基础, 总结出CUSA的优化参数设置, 并于2008-12/2010-10以厂家推荐的参数设置为对照进行临床对照研究, 证实了优化CUSA ExcelTM系统参数设置可有效地减少肝切除断肝过程中的出血和肝损伤, 提高解剖性肝切除的临床效果. 现报道如下.
总病例31例, 均为2008-12/2010-10住院患者, 其中男17例, 女14例, 年龄28-61(48.2±8.7)岁. 原发性肝细胞癌(hepatocellular carcinoma, HCC)21例, 胆管细胞癌1例, 肝脏局灶结节性增生2例, 肝血管瘤7例. 术前肝功能Child A级28例, B级3例. 手术方式: 行右半肝1例, 左半肝1例, SⅢ 1例, SⅣ2例, SⅤ3例, SⅥ 2例, SⅦ3例, SⅧ3例, SⅡⅢ2例, SⅥⅦ3例, SⅤⅥ2例, SⅤⅧ4例, SⅤⅧⅥ+射频1例, SⅢⅥⅦ1例, SⅢⅥ+射频1例, SⅤⅥ1例.
1.2.1 手术操作: 2组患者均由同一术者完成, 使用美国Valleylab公司生产的CUSA ExcelTM-8 System超声外科吸引器, 手柄频率23 kHz、带Valleylab Force FX双极电刀手控附件. 取上腹"J"形或上腹"人"字形切口充分暴露肝脏. 术中B超探查明确确认肝占位部位、大小、数目及与血管关系, 并标记切除线. 常规顺逆结合切除胆囊, 显露第一肝门. 以Takasaki等[3]的肝三段解剖理论基础, 术前用参照文献[4]行肝内血管三维重建, 采用Glisson鞘横断解剖性肝切除, 阻断Glisson鞘并确认拟切除肝段或叶的缺血线, 结扎并切断支配需切除肝叶的Glisson鞘; 如果需切除肝段, 则先以CUSA解剖第一肝门部肝实质, 暴露需要切除的肝段Glisson鞘, 结扎之并确认缺血线. 然后交替阻断需保留侧肝脏Glisson鞘, 控制CVP在3-5 cmH2O, 用CUSA沿切标记线离断肝实质, >2 mm管道予以结扎, 余下管道用连发钛夹处理, 切除病变肝段.
1.2.2 分组和观察指标: 根据就诊顺序分为Ⅰ组(n = 10)和Ⅱ组(n = 21): Ⅰ组采用CUSA厂家推荐的参数设置参数断肝, Ⅱ采用课题组优化设置参数断肝. 2组间资料具有可比性. 2组间相关参数具有可比性. 对比分析2组手术时间、术中出血量、术中输血量、术后腹腔引流量和肝功能康复情况. 肝脏质地分为软(正常肝脏或轻度肝硬化伴中度脂肪肝, 肝脏形态大小正常)、中(中度肝硬化, 表明明显结节感, 质地变硬, 肝脏形态大小正常或轻度缩小)、硬(肝脏因硬化显著缩小, 表明结节明显且大小不一, 质地坚硬)3种.
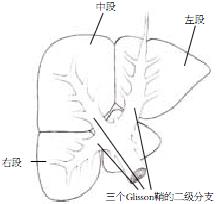
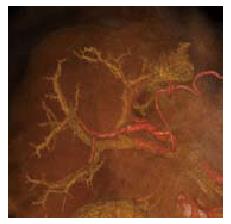
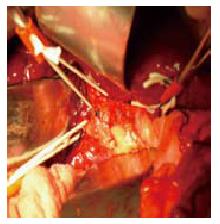
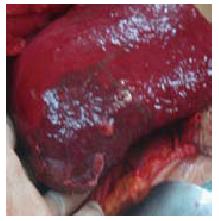
术前Philips 256层iCT重建后肝脏门脉及动脉结构清晰, 结合文献报道的肝三段理论和Gllison鞘横断解剖性肝切除为指导, 顺利行解剖性肝切除(图1-5).
通过调整振幅和变动组织选择性, 可以提高血管损伤和减少岀血, 增加断肝速度(表1).
| 破碎要求 | 肝脏 硬度 | 手柄频率(KHz) | 组织选择性 | 吸引(%) | 冲洗(mL/min) | 振幅(%) | |||||
| Ⅰ组 | Ⅱ组 | Ⅰ组 | Ⅱ组 | Ⅰ组 | Ⅱ组 | Ⅰ组 | Ⅱ组 | Ⅰ组 | Ⅱ组 | ||
| 精细 | 软 | 23 | 23 | ++++ | +++ | 50 | 50 | 3-5 | 3-5 | 60-80 | 20-40 |
| 普通 | 中 | 23 | 23 | +++; ++ | +++; ++ | 70 | 60 | 5-6 | 5-6 | 80-100 | 30-50 |
| 快速 | 硬 | 23 | 23 | +; Std | +; Std | 100 | 60 | 8-10 | 5-6 | 100 | 30-50 |
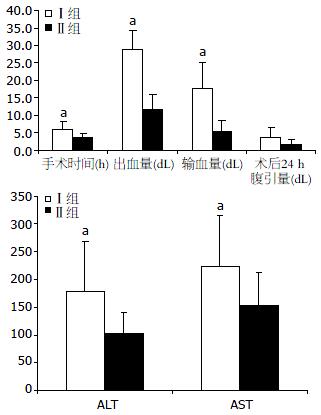
Ⅰ组手术时间、出血量、输血量和术后24 h引流量分别为(6.2±1.9) h、(2 900±510) mL和(1 760±1 700) mL, Ⅱ组为(3.8±0.8) h、(1 150±460) mL和(530±300) mL, 组间比较均具有显著性(P<0.05); 但术后引流量Ⅰ组为(370±290) mL, Ⅱ组为(170±110) mL, 组间比较无显著差异(P>0.05). Ⅱ组术后肝酶学康复优于Ⅰ组(图6).
两组均未出现严重并发症, 术后4 wk内康复出院. 两组间复发率等指标无显著差异(P<0.05): Ⅰ组恶性肿瘤根治率为90%(1/10), 未达根治1例为门脉左主干癌栓形成, 目前随访4 mo生存良好, 根治者随访3-18 mo, 复发率20%(2/10), 其余患者生存良好. Ⅱ组恶性肿瘤根治率85.7%(3/18), 未达根治者1例为肿瘤浸润门脉右主干1例(残留肿瘤组织直径约1.5 cm)、SⅤⅧⅥ+射频1例和SⅢⅥ+射频1例. 根治性切除18例中, 随访18 mo, 生存率100%、复发率4.5%(1/22), 死亡率9.5%(2/21), 2例死亡均为非根治病例.
CUSA利用超声波对人体组织的热效应、机械效应和空化作用等原理, 将要切除的组织粉碎, 再经冲洗液与切除组织碎屑混合乳化, 经超声探头上的吸引装置吸除[5,6]. CUSA具有超声振荡切割、冲洗乳化与吸引3种功能, 能选择性地保留肝实质内的血管等结构, 减少或避免血管、胆管的损伤. 具有出血少、术野洁净、对血管和周围组织损伤保护性好、手术操作安全可靠、术后反应轻等特点, 使切割更精确, 对周围组织损伤较小[1,7,8]. CUSA与传统切肝技术相比, 在控制失血、肝组织保护、复杂部位肝解剖等方面有明显的优势[9,10]. 特别是恰当的设备参数设置配合操作者的技术, 可以最大限度地显露肝实质内管道结构并予以保护、避免损伤肝内血管, 从而显著提高手术效果和肿瘤切除率, 保护肝功能损害和减少术后并发症[2,7,11].
CUSA最佳功能的发挥与其术中使用技术参数密切相关, 恰当的参数设置保证最大限度的保护对健康肝脏和血管的损害[12]. 但是目前尚未见到对CUSA用于切肝参数优化的文献报道. 能够参考的资料仅是来源于厂家推荐的参考设置参数, 但我们在使用过程中发现对于不同的质地的肝组织, 厂家推荐的参数设置并非最佳设置. 手柄的振幅和组织选择性是影响肝组织游离的主要因素[5,13]. 因此我们主要针对调整手柄振幅和组织选择性来提高切肝的速度和对血管的保护作用. 本研究显示, 与厂家推荐参数比较, 我们的优化方案调整了振幅、组织选择性和吸引等环节, 使得各参数间配合更佳默契. 调低振幅在减慢超声震荡效率的情况下可增加对组织的保护, 配合适当的冲洗水流量和吸引, 可更好地暴露管道组织, 有利于减少目标管道组织表明的水分和积血, 得以提高电凝止血效率. 调低振幅看似降低了断肝效率, 但由于出血的减少和电凝止血效果的改善, 总体断肝时间得以减少. 研究结果证实, Ⅱ组手术时间、出血量、输血量和术后24 h引流量等指标均显著优于Ⅰ组. 究其原因在于CUSA的优化参数设置可以提高组织选择性和对细小血管的保护, 同时最大限度地减少对健康肝组织的损伤, 从而有效地减少了出血、提高了断肝效率、节省了手术时间. 而厂家推荐的参数设置虽然可以快速断肝, 但是由于组织选择性未达到最佳水平, 以至于术中用于止血的时间过长, 从而造成出血量增加和延长手术时间. 但是如果术中止血彻底, 两组参数设置都是安全的, 因此术后引流量并无显著差异. 优化参数设置组术后ALT和AST的康复指标明显好于推荐参数设置组也佐证了上述推测.
结合本研究结果, 我们初步总结出以下经验: (1)术前通过MRI、iCT等影像检查, 充分了解每个患者肝脏病变、相关管道解剖特征, 术前作出可行的手术方案, 并在术中通过术中超声定位进一步明确解剖结构, 是手术成败的重要环节; (2)针对不同病理状态的肝实质, 调整设备操控指标, 实时优化CUSA参数设置, 在结合良好的目标肝段入肝血流阻断, 并严格按照肝段或叶的解剖标志并结合阻断后缺血线在无Glisson系统分布的平面断肝; (3)CUSA沿管道走向纵向适当频度移动CUSA刀头, 对肝实质作用较长时间充分粉碎肝实质组织, 断面显露管道结构时, 应首先距目标管道0.5-1.0 cm由浅入深解剖管道周围组织, 完全暴露管道组织后再行钛夹或者结扎离断. <1.0 mm结构可以电凝离断, 2.0-3.0 mm结构连发钛夹钳闭即可, 3.0 mm以上宜细线结扎. 电凝止血时务必和吸引功能最佳配合、保证充分的吸引, 因为电凝只有在充分暴露血管并且无积血时才能给血管最大的能量传递以便凝固止血. 我们做法为术者持CUSA显露断面管道, 第一助手电凝、钛夹钳夹或结扎管道, 第二助手以精细剪刀离断目标管道, 第三助手负责暴露并辅助保持创面干洁, 有序的配合有助于准确操作、减少失误、缩短手术时间.
总之, CUSA系统使断肝技术进入精肝切除时代, 但需要与准确的肝脏断面解剖径路、有效的离断肝段阻断和协调的操作配合相结合, 才能使其价值得到充分体现.
肝部分切除是治疗肝脏占位性疾病的主要手段, 随着肝移植时代的到来现, 肝脏外科也进入到精准解剖学性肝切除时代. ExcelTM型外科超声吸引器(CUSA)的应用是最具代表性的新兴技术, 该设备精细而准确的解剖学高选择性切肝技术推动了肝切部分除技术的进步.
于聪慧, 教授, 中国人民解放军北京军区总医院肝胆外科
目前尚未见到对CUSA用于切肝参数优化的文献报道. 能够参考的资料仅是来源于厂家推荐的参考设置参数, 但本课题组在使用过程中发现对于不同的质地的肝组织, 厂家推荐的参数设置并非最佳设置. 手柄的振幅和组织选择性是影响肝组织游离的主要因素. 因此本课题组主要针对调整手柄振幅和组织选择性来提高切肝的速度和对血管的保护作用.
优化CUSA参数设置可增加对肝组织的保护、减少术中出血和缩短手术时间, 从而显著提高断肝效果.
本文可读性较好, 为临床医师提供一定的经验和总结.
编辑: 曹丽鸥 电编:何基才
| 1. | 陈 心葵, 杨 军. 超声外科手术吸引器及临床应用概况. 国外医学•生物医学工程分册. 1997;20:17-20. |
| 2. | 孔 连宝, 王 学浩, 张 峰, 李 相成, 蒋 维维. 超声刀技术在肝肿瘤切除术及活体肝移植术中的应用. 南京医科大学学报(自然科学版). 2008;28; 1155-1157. |
| 3. | Takasaki K. Glissonean pedicle transection method for hepatic resection: a new concept of liver segmentation. J Hepatobiliary Pancreat Surg. 1998;5:286-291. [PubMed] [DOI] |
| 4. | 付 必莽, 张 捷, 孙 勇, 唐 继红, 顾 亚律, 唐 波, 胡 明道, 杨 达宽, 何 晓顺, 黄 洁夫. 256层智能CT精准肝切除模型的建立及临床应用. 肝胆外科杂志. 2010;18:202-205. |
| 6. | Mark A. Neurohr, Newport, KY, inventor. Ultrasonic surgical instruments. United States patent US20080234710A1. 2008;Sep 25. |
| 7. | Takatsuki M, Eguchi S, Yamanouchi K, Tokai H, Hidaka M, Soyama A, Miyazaki K, Hamasaki K, Tajima Y, Kanematsu T. Two-surgeon technique using saline-linked electric cautery and ultrasonic surgical aspirator in living donor hepatectomy: its safety and efficacy. Am J Surg. 2009;197:e25-e27. [PubMed] [DOI] |
| 8. | Gurusamy KS, Pamecha V, Sharma D, Davidson BR. Techniques for liver parenchymal transection in liver resection. Cochrane Database Syst Rev. 2009;CD006880. [PubMed] |
| 9. | Fasulo F, Giori A, Fissi S, Bozzetti F, Doci R, Gennari L. Cavitron Ultrasonic Surgical Aspirator (CUSA) in liver resection. Int Surg. 1992;77:64-66. [PubMed] |
| 10. | Nagano Y, Matsuo K, Kunisaki C, Ike H, Imada T, Tanaka K, Togo S, Shimada H. Practical usefulness of ultrasonic surgical aspirator with argon beam coagulation for hepatic parenchymal transection. World J Surg. 2005;29:899-902. [PubMed] [DOI] |
| 11. | Xu JS, Guo H. Study on a micro-knife and its vibration signal acquisition system. Piezoelectricity, Acoustic Waves, and Device Applications (SPAWDA) and. 2009;131. |
| 12. | Cimino WW. Ultrasonic surgery: power quantification and efficiency optimization. Aesthet Surg J. 2001;21:233-241. [PubMed] [DOI] |