修回日期: 2010-01-05
接受日期: 2010-01-11
在线出版日期: 2010-02-28
目的: 探讨戊己丸不同配比方对大鼠体外肝微粒体CYP1A2酶活性的影响, 从"中药配伍-代谢"关系探讨中药配伍机制.
方法: 按L9(34)正交表, 戊己丸的配比设计为9个受试复方, 以非那西丁为探针药, HPLC检测戊己丸对大鼠体外肝微粒体CYP1A2酶活性的影响.
结果: 黄连、吴茱萸、白芍提取物及戊己丸方1-9抑制CYP1A2的生药IC50分别为: 28.07、989.69、6633.28、57.92、104.38、321.28、32.17、80.09、71.47、76.76、40.41、29.45 mg/L; 黄连及戊己丸可以显著抑制CYP1A2酶活性, 不同配比戊己丸抑制CYP1A2酶活性作用不同, 有统计学差异; 随着黄连、吴茱萸两药在戊己丸方中剂量水平的增高, 戊己丸组方抑制CYP1A2酶活性的能力增强, 随着白芍在戊己丸方中剂量水平的增高可以减弱该组方抑制CYPA2酶活性的能力, 且戊己丸组方中吴茱萸和白芍配比不同可以影响方中黄连抑制CYP1A2酶活性的程度.
结论: 戊己丸配比不同, 对CYP1A2酶活性的抑制作用不同, 这种差异可能是不同配比戊己丸药效学、药动学差异的原因所在.
引文著录: 翁小刚, 李玉洁, 杨庆, 梁日欣, 王怡薇, 刘晓霓, 韩晓, 张甘霖, 隋峰, 朱晓新. 戊己丸不同配比方对大鼠体外CYP1A2酶活性的影响. 世界华人消化杂志 2010; 18(6): 586-591
Revised: January 5, 2010
Accepted: January 11, 2010
Published online: February 28, 2010
AIM: To investigate the effects of Wuji Pill with different compatibility on the enzymatic activity of cytochrome P450 1A2 (CYP1A2) in rat liver microsomes in vitro.
METHODS: Using phenacetin as a substrate probe, the effects of Wuji Pill with different compatibility (No.1-9) on the enzymatic activity of CYP1A2 were detected by high-performance liquid chromatography (HPLC).
RESULTS: The half maximal inhibitory concentrations (IC50) of Rhizoma Coptidis, Fructus Evodiae Rutaecarpae, Radix Paeoniae Alba and Wuji Pill (No.1-9) on the enzymatic activity of CYP1A2 were 28.07, 989.69, 6633.28, 57.92, 104.38, 321.28, 32.17, 80.09, 71.47, 76.76, 40.41 and 29.45 mg/L, respectively. Rhizoma Coptidis and Wuji Pill (No.1-9) could significantly suppress the enzymatic activity of CYP1A2. The suppressive effects of Rhizoma Coptidis in Wuji Pill on the activity of CYP1A2 depend on the proportion of Fructus Evodiae Rutaecarpae and Radix Paeoniae Alba in Wuji Pill. With the increase in the proportion of Rhizoma Coptidis and Fructus Evodiae Rutaecarpae in Wuji Pill, the suppressive effects of Wuji Pill on the activity of CYP1A2 were strengthened. With the increase in the proportion of Radix Paeoniae Alba in Wuji Pill, the suppressive effects of Wuji Pill on the activity of CYP1A2 was weakened.
CONCLUSION: Wuji Pill with different compatibility shows different suppressive effects on the enzymatic activity of CYP1A2. This may explain why Wuji Pill with different compatibility has different pharmacodynamic and pharmacokinetic characteristics.
- Citation: Weng XG, Li YJ, Yang Q, Liang RX, Wang YW, Liu XN, Han X, Zhang GL, Sui F, Zhu XX. Effects of Wuji Pill with different compatibility on the activity of cytochrome P450 1A2 in rat liver microsomes in vitro. Shijie Huaren Xiaohua Zazhi 2010; 18(6): 586-591
- URL: https://www.wjgnet.com/1009-3079/full/v18/i6/586.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v18.i6.586
戊已丸可疏泻肝之郁火、调和脾胃, 是临床治疗肠易激综合征(irritable bowel syndrome, IBS)常用有效方剂, 最早见于宋代刘昉《幼幼新书》卷二十六, 由黄连、吴茱萸、白芍各五两组成, 《医方考》将方中药物用量改为黄连十两、吴茱萸二两、白芍二两, 黄连、吴茱萸、白芍用药比例由1:1:1改为5:1:1, 而《中国药典》(2005年版)收载本方的比例为: 黄连300 g, 吴茱萸(制)50 g, 白芍(炒)300 g. 宫海民等[1]比较了戊已丸中黄连、吴茱萸、白芍1:1:1和5:1:1两种配比的药效, 其中1:1:1配伍组长于镇痛, 而5:1:1配伍组长于抗炎, 提示戊已丸配比不同, 所产生的药效也不尽相同. 本课题组前期药理研究也表明, 戊己丸不同配比方有不同的药效特点[2].
复方用药是中医治病的主要形式, 也是辨证论治理论精髓具体表现. 中药成分复杂, 作用形式多样, 中药化学成分(原型药或代谢物)是其作用的物质基础, 因此, 中药复方的配伍变化体现不同疗效与其化学成分代谢特征存在关联. 本课题组从"中药配伍-代谢"关系探讨复方配伍机制, 以戊己丸为范例, 研究戊己丸配伍(比)与机体主要肝药酶-CYP450之间的相互影响, 本文报道戊己丸不同配比方对大鼠体外CYP1A2酶活性的影响, CYP1A2主要在肝脏表达, 人类CYP1A2的含量约占肝脏CYP450总量的13%, 参与咖啡因(90%以上的咖啡因清除由该酶介导)、非那西丁、醋氨酚等20多种药物的代谢, 并且在十几种前致癌物的激活或灭活中发挥重要作用[3,4].
本实验以方剂对CYP1A2酶活性的影响为主效应, 以IC50作为量化观察指标, 研究戊己丸配伍的数、量、相互比例与方剂主效应的关系, 为探讨中药复方配伍机制提供新的研究思路.
Wistar大鼠, ♂, 体质量200 g±20 g, 北京维通利华实验动物技术有限公司提供, 许可证编号: SCXK(京)2007-0001, SPF级; HPLC色谱仪(美国Waters 2695自动进样液相仪, Waters 2489-UV检测器, Empower数据处理系统), Kromasil-C18色谱柱(250 mm×4.6 mm, 5 μm), 美国Avanti J-30I超高速离心机; 美国Sorvall super T21高速离心机; 日本MDF-U 50V超低温冰箱(-80 ℃); 连续加样器; 国产BHW-2电热恒温水浴箱; 分析天平; 匀浆器. 非那西丁、对乙酰氨基酚、6-磷酸葡萄糖、β-萘黄酮均购自Sigma公司; 氧化型辅酶Ⅱ(北京纵横洋洲公司), 苯巴比妥钠注射液(天津金耀氨基酸有限公司), BCA试剂盒(北京赛驰生物科技有限公司), 精密pH试纸, 色谱纯乙腈(Tedia, 美国), 甲醇(色谱纯, 天津四友试剂公司), 高纯水, 氯化镁(分析纯), 氯化钾(分析纯), 氢氧化钾(分析纯), 磷酸. 黄连、制吴茱萸、炒白芍饮片均购自北京卫仁饮片厂; 黄连醇提物、制吴茱萸醇提物、炒白芍混合提取物(醇提加水提)由中日友好医院剂型室按优选工艺分别进行提取.
1.2.1 戊己丸受试复方配比设计: 按照L9(34)正交表, 采用以下9个不同配比戊己丸, 其中方4为药典收录方. 方1-9中黄连、制吴茱萸、炒白芍的比例分别为: 3:1:3; 3:2:6; 3:6:12; 6:1:6; 6:2:12; 6:6:3; 12:1:12; 12:2:3; 12:6:6.
1.2.2 实验分组与药物配制: 实验分为12组: 戊己丸不同配比方1-9; 黄连、制吴茱萸、炒白芍各单味药提取物; 各组药物均采用500 mL/L甲醇溶液作为溶剂, 取相应量的黄连醇提物、制吴茱萸醇提物与炒白芍提取物混合, 按各自组方成分比例配制.
1.2.3 大鼠肝微粒体制备: 参照文献[5]方法, 大鼠经苯巴比妥钠与β-萘黄酮诱导CYP450酶生成增加后, 用高速离心法制备肝微粒体, -80 ℃保存备用. 以小牛血清白蛋白为标准品, 采用BCA试剂盒法测定微粒体蛋白含量, 蛋白浓度为1.2 g/L.
1.2.4 肝微粒体混合酶系组成: 为测定药物对CYP450同工酶的IC50值, 每一受试药设7个浓度及溶剂对照, 8个受试条件, 每1条件做平行3个孵育管, 1个受试药每次需做24个孵育管, 每次配制12 mL微粒体混合酶系溶液, 其组成为: 1.2.3项下肝微粒体悬液1.2 mL, 0.4 mol/L MgCl2溶液120 μL, 1.65 mol/L KCl2溶液120 μL, 6-磷酸葡萄糖15 mg, 氧化型辅酶Ⅱ20 mg, 纯净水4.56 mL, 0.2 mol/L磷酸盐缓冲液(pH7.4)6 mL, 震荡混匀; 混合酶系配制在冰浴上进行, 临用时现配.
1.2.5 CYP1A2酶代谢活性检测: 每1孵育管加入5 μL受试药溶液之后, 吸取120 μL浓度为100 μmol/L的CYP1A2特征底物-非那西丁溶液, 加入1.2.4项下的12 mL肝微粒体混合酶系溶液中, 混匀, 均匀加入24个孵育管内, 每1孵育管添加0.5 mL, 混匀. 以上操作在冰浴上进行, 之后将孵育管置37 ℃水浴中孵育3 h后, 加入0.5 mL冰冷甲醇终止反应, 转入1.5 mL离心管, 4 ℃冰箱放置3 h沉淀蛋白后, 18 000 r/min离心20 min, 取上清液20 μL, HPLC进样测定非那西丁代谢产物-对乙酰氨基酚浓度, 对乙酰氨基酚的生成量与CYP1A2酶活性呈正相关[6].
1.2.6 HPLC检测方法学建立: (1)HPLC条件: Kromasil-C18色谱柱(250 mm×4.6 mm, 5 μm); 流动相A: 5%乙腈、15%甲醇、80%水; 流动相B: 10%乙腈、60%甲醇、30%水; 梯度洗脱程序: 0 min(100% A), 8 min(80% A, 20% B), 12 min(60% A, 40% B), 20 min(100% A); 运行时间: 40 min; 流速: 1 mL/min; 柱温: 30 ℃; 检测波长: 245 nm; 进样量: 20 μL; (2)对照品储备液配制: 精密称取非那西丁、对乙酰氨基酚一定量, 配制10 mL的0.5 g/L非那西丁和10 mL的0.31 g/L对乙酰氨基酚储备液; (3)标准曲线测定: 取一定量对乙酰氨基酚储备液, 以50%肝微粒体混合酶系溶液: 50%甲醇的混合溶液(与孵育体系最终溶液成分一致)稀释, 配制0.375、0.185、0.09、0.04、0.02、0.01 mg/L浓度对照品溶液, 每1梯度浓度溶液进样20 μL测定, 重复进样2次, 取平均值, 以组分的峰面积(A)为纵坐标, 组分浓度(c, mg/L)为横坐标, 进行线性回归; (4)方法回收率: 取适量对乙酰氨基酚对照品储备液, 以50%肝微粒体混合酶系溶液: 50%甲醇的混合溶液分别配制高、中、低3个浓度的对乙酰氨基酚混合溶液, 3个浓度溶液分别进样20 μL, 按上述HPLC条件测定相应成分含量, 以含量测定值比实际值计算方法回收率; (5)最低检测限: 根据S/N(信噪比)≥3计算.
1.2.7 戊己丸不同配比方对大鼠CYP1A2酶活性的影响: 本实验12个戊己丸提取物组方终浓度(特指CYP1A2酶代谢活性实验受试药的最高浓度, 由终浓度依次往下对半稀释6个浓度, 作为IC50测定所需梯度浓度), 详见表1. 每1受试药的每1受试浓度(共8个受试浓度, 包括溶剂对照)做3个平行孵育管, 平行实验2次, 按1.2.5项下步骤检测受试药对CYP1A2酶活性的影响. pH值对CYP450酶活性影响较大[7], pH6-8为CYP450酶生理pH值范围, 实验均需调定孵育管内pH值至7.0左右.
| 分组 | 黄连 | 制吴茱萸 | 炒白芍 | 总浓度 |
| 黄连 | 672.24 | - | - | 672.24 |
| 提取物 | ||||
| 制吴茱萸 | - | 4 259.32 | - | 4 259.32 |
| 提取物 | ||||
| 炒白芍 | - | - | 35 870 | 35 870 |
| 提取物 | ||||
| 方1 | 168 | 56 | 168 | 392 |
| 方2 | 168 | 112 | 336 | 616 |
| 方3 | 168 | 336 | 672 | 1 176 |
| 方4 | 336 | 56 | 336 | 728 |
| 方5 | 336 | 112 | 672 | 1 120 |
| 方6 | 336 | 336 | 168 | 840 |
| 方7 | 672 | 56 | 672 | 1 400 |
| 方8 | 672 | 112 | 168 | 952 |
| 方9 | 672 | 336 | 336 | 1 344 |
统计学处理 计算加与不加受试药物的情况下, 非那西丁经CYP1A2代谢产生对乙酰氨基酚的量, 按照以下公式计算不同浓度受试药对CYP1A2酶活性的抑制率: 抑制率(%) = (不加受试药对乙酰氨基酚生成量-加受试药对乙酰氨基酚生成量)/不加受试药对乙酰氨基酚生成量×100%; 然后采用改良Bliss法计算IC50值[8]. 若某受试药IC50>50 μmol/L, 说明药物抑制能力弱; 若IC50<50 μmol/L, 说明该药物抑制能力强. 数据以mean±SD表示, 采用SPSS11.5统计软件进行t检验, 单因素方差分析、多因素方差分析及正交t值法计算.
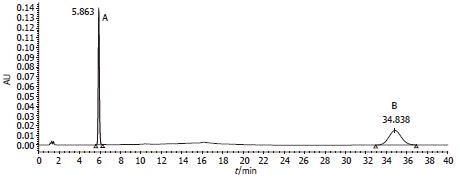
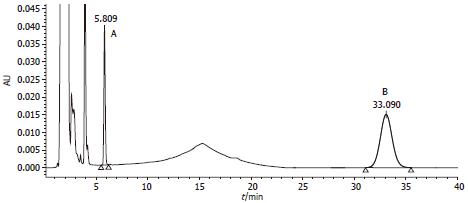
对乙酰氨基酚回归方程: A = 3397.3c-2342.2, (n = 6, r = 0.9997), 表明对乙酰氨基酚在0.01-0.375 mg/L浓度范围内具有良好的线性关系; 对乙酰氨基酚平均回收率为99.58%, 最低检测浓度为0.01 mg/L. 相应图谱见图1, 图2.
戊己丸不同配比方对CYP1A2的抑制影响存在较大差异(表2).
| 分组 | 孵育实验终浓度[μg(生药)/mL] | 终浓度下对乙酰氨基酚生成抑制率(%) |
| 黄连提取物 | 672.24 | 97.91±0.32 |
| 制吴茱萸提取物 | 4 259.32 | 87.19±0.85 |
| 炒白芍提取物 | 35 870 | 80.53±3.18 |
| 方1 | 392 | 82.68±3.68 |
| 方2 | 616 | 90.04±2.42 |
| 方3 | 1 176 | 89.09±3.85 |
| 方4 | 728 | 96.83±0.95 |
| 方5 | 1 120 | 96.25±0.47 |
| 方6 | 840 | 96.79±0.29 |
| 方7 | 1 400 | 97.39±0.42 |
| 方8 | 952 | 95.05±1.24 |
| 方9 | 1 344 | 98.58±0.34 |
戊己丸组方中3味药单用均能对CYP1A2酶活性产生抑制作用, 黄连IC50值非常低, 对CYP1A2的抑制作用显著, 是戊己丸方中抑制CYP1A2酶活性的主要物质, 制吴茱萸IC50值较高, 对CYP1A2酶活性抑制不明显, 炒白芍IC50值很高, 对CYP1A2酶活性抑制较弱; 不同配比情况下复方中的吴茱萸和炒白芍拆方IC50值均较单味药IC50值极显著降低. 方2、6、8中黄连拆方IC50值与黄连单味药中IC50值比较无显著差异, 方1、4、5、9中黄连拆方IC50值比黄连单味药中IC50值显著降低, 方3、7中黄连拆方IC50值比黄连单味药中IC50值显著升高(表3).
| 分组 | 受试药拆方[μg (生药)/mL] | 提取物组方IC50[μg(生药)/mL] | ||
| 黄连提取物 | 制吴茱萸提取物 | 炒白芍提取物 | ||
| 黄连提取物 | 28.07±1.398 | - | - | 28.07±1.398 |
| 制吴茱萸提取物 | - | 989.69±110.953 | - | 989.69±110.953 |
| 炒白芍提取物 | - | - | 6 633.28±336.094 | 6 633.28±336.094 |
| 方1 | 24.82±1.850a | 8.27±0.617f | 24.82±1.851h | 57.92±4.319 |
| 方2 | 28.47±2.107 | 18.98±1.405f | 56.94±4.214h | 104.38±7.725 |
| 方3 | 45.90±2.784d | 91.79±5.568f | 183.59±11.136h | 321.28±19.488 |
| 方4 | 14.85±1.173d | 2.47±0.195f | 14.85±1.173h | 32.17±2.541 |
| 方5 | 24.03±1.396a | 8.01±0.465f | 48.06±2.791h | 80.09±4.652 |
| 方6 | 28.59±3.062 | 28.59±3.062f | 14.29±1.531h | 71.47±7.656 |
| 方7 | 36.84±2.988b | 3.07±0.249f | 36.84±2.988h | 76.76±6.224 |
| 方8 | 28.53±6.143 | 4.75±1.024f | 7.13±1.536h | 40.41±8.702 |
| 方9 | 14.72±2.499d | 7.36±1.249f | 7.36±1.249h | 29.45±4.997 |
(1)单因素方差分析: 方1-9的组间两两比较均有显著差异; (2)多因素方差分析: 方1-9中, 黄连, 制吴茱萸, 炒白芍均有3个剂量水平, 随着黄连和制吴茱萸的剂量水平增加, 可以造成组方对CYP1A2酶活性抑制作用的加强, 而随着炒白芍剂量水平的增加, 可以造成组方对CYP1A2酶活性抑制作用的减弱; (3)正交t值法计算: 见表4, 在戊己丸的3种因素(3味药)3水平(3味药在9个复方组合中均有小、中、大3个剂量水平配伍)正交设计实验中, 除炒白芍小、中剂量水平差别不会导致戊己丸组方对CYP1A2酶活性产生有统计学差异的影响外, 其余两药各剂量水平间比较及炒白芍中、大剂量水平间和小、大剂量水平间比较均能显著改变相应戊己丸组方对CYP1A2酶活性的影响.
| 统计项 | 黄连 | 制吴茱萸 | 炒白芍 | t值 |
| M1 | 483.58 | 166.85 | 169.80 | t(0.05, 45) = 2.0145 |
| M2 | 183.73 | 224.88 | 166.00 | t(0.01, 45) = 2.6910 |
| M3 | 146.62 | 422.2 | 478.13 | t(0.001, 45) = 3.5235 |
| D1-2 | 299.85 | -58.03 | 3.80 | |
| D2-3 | 37.11 | -197.32 | -312.13 | |
| D1-3 | 336.96 | -255.35 | -308.33 | |
| t1-2 | 28.0769 | 5.4337 | 0.3558 | |
| t2-3 | 3.4748 | 18.4763 | 29.2267 | |
| t1-3 | 31.5517 | 23.9101 | 28.8709 | |
| P1-2 | [t = 28.0769>3.5235]d | [t = 5.4337>3.5235]d | t = 0.3558<2.0145 | |
| P2-3 | [t = 3.4748>2.6910]b | [t = 18.4763>3.5235]d | [t = 29.2267>3.5235]d | |
| P1-3 | [t = 31.5517>3.5235]d | [t = 23.9101>3.5235]d | [t = 28.8709>3.5235]d |
戊己丸方含黄连、吴茱萸、白芍, 黄连属苦寒清热药, 入心、胃经可泻心火、清胃热, 吴茱萸属温阳散寒药, 归肝、脾、胃、肾经, 可温中止呕, 助阳止泻, 芍药性味苦、平, 入肝、脾经, "白芍药益脾", 长于养血敛阴, 柔肝止痛[9]; 由此可见, 戊己丸疏泻肝火、调和脾胃之功, 能治腹痛泻痢、呕吐吞酸等症, 乃方中3味药集结所长, 协同制衡而表现出的整体药效, 又因3味药性味、归经及功效各有不同侧重, 故从戊己丸方解亦能推测戊己丸不同配伍配比可造成其药效特点之差异, 但其配伍机制尚需进行现代科学研究方可揭去复方用药奥秘之面纱.
中药复方应用是中医辨证论治的精髓, 只有探明中药复方配伍机制才有能更好地利用中医药这一民族瑰宝为人民的健康卫生服务. 目前中药配伍研究虽已取得一定成就, 但尚不能完全阐明复方配伍机制. 配伍研究实验设计可采用析因设计、正交设计、均匀设计等, 中药复方一般药味较多, 如何分析主药, 找出最佳组合及最优剂量, 从而达到精简处方的目的, 值得重视和研究. 孙卫民和孙瑞元根据中药方剂研究特点, 按正交设计原理及F值与t值的特定关系, 提出了正交t值法[10], 本法能较合理解释复方配伍各因素、水平间的相互作用.
我们以戊己丸为范例, 采用黄连, 制吴茱萸, 炒白芍作为戊己丸组方用药, 前期进行了一系列配伍相关研究, 可以证明不同配比戊己丸药效上有不同侧重, 不同配比戊己丸血药动力学参数各有不同, 以及胃肠吸收、代谢也有明显差异, 并且从Caco-2细胞, P-糖蛋白等层次初步分析了造成以上差异的机制[11,12], 课题组希望通过对戊己丸配伍的范例研究, 建立一种有效的中药复方配伍研究方法, 即从配伍药效, 配伍中药吸收、分布、代谢、排泄等环节, 整体、细胞、亚细胞等水平研究中药配伍, 综合分析、阐述中药配伍机制.
中药复方是由配伍中药一定的数(中药味数)、量(剂量水平)、比(各组成药味的数、量比例)构建起来的在主效应上有别于单味药的新个体(方剂), 方剂主效应的观察指标可以是药效、代谢或毒性方面的, 配伍药物数、量、比变化可以导致方剂整体效应发生量变甚至质变. 本实验进行戊己丸不同配比方对大鼠CYP1A2酶活性的影响研究, 以戊己丸对CYP1A2酶活性的影响作为方剂主效应, 探讨戊己丸配伍数、量、比变化与方剂主效应差异的相关性, 从"药物配伍-代谢"关系阐述中药配伍机制. 实验表明, 戊己丸可以显著抑制体外大鼠肝微粒体CYP1A2酶活性, 黄连是抑制CYP1A2酶活性的主要物质, 吴茱萸和白芍虽抑制CYP1A2酶活性作用较弱, 但不同配比情况下复方中的吴茱萸和白芍拆方IC50值均较单味药IC50值极显著降低, 这主要是因为各复方中加入了对CYP1A2酶活性抑制极显著的黄连造成的, 吴茱萸、白芍两药在方中配比不同还可造成黄连抑制CYP1A2酶活性能力的改变, 并且按L9(34)正交设计的戊己丸方1-9在抑制CYP1A2酶活性作用上, 组间比较均有显著差异, 复方中黄连本身的不同比例和引入对CYP1A2酶活性影响不显著的不同配比吴茱萸和白芍后, 对CYP1A2酶活性造成了相互制衡或者相互促进的作用.
戊己丸方1-9中, 黄连、吴茱萸、白芍均有3个剂量水平, 随着黄连和吴茱萸的剂量水平增加, 可以造成组方对CYP1A2酶活性抑制作用的加强, 而随着白芍剂量水平的增加, 可以造成组方对CYP1A2酶活性抑制作用的减弱; 黄连、吴茱萸、白芍各自的3个剂量水平, 除白芍小、中剂量水平差别不会导致戊己丸组方对CYP1A2酶活性产生统计学差异的影响外, 其余2药各剂量水平间比较及白芍中、大剂量水平间和小、大剂量水平间比较均能显著改变相应戊己丸组方对CYP1A2酶活性的影响.
总之, 本实验揭示戊己丸配伍数、量、比不同与方剂主效应差异存在密切相关, 那么, 不同配比戊己丸在药效上的差异, 是否与不同配比戊己丸进入机体后对肝微粒体CYP1A2造成了不同的抑制作用, 从而导致戊己丸本身在机体内被代谢的差异(药物被代谢差异可造成机体内药效物质的差异)有关? 以及戊己丸对肝微粒体其他CYP450同工酶是否有类似作用? 体外实验结果是否可被体内实验印证? 这有待进一步实验研究及分析阐述, 作者将另行撰文报道.
药物代谢性相互作用[13,14]是导致患者发生不良反应乃至严重不良反应或死亡的重要原因, 戊己丸及黄连均是现代临床常用中药(复方), 从本实验结果看, 临床使用戊己丸及黄连, 尤其存在多药共用的情况下, 务必要注意防范可能因戊己丸或黄连抑制CYP1A2酶活性而出现的不良药物代谢性相互作用.
CYP1A2是参与药物代谢的CYP450酶中的重要同工酶之一, 代谢是中药(复方)起作用的重要环节, 戊己丸是临床治疗肠易激综合征(IBS)常用有效方剂, 不同配比戊己丸历代医家均有应用, 从"中药配伍-代谢"关系研究戊己丸配伍作用规律对于指导临床用药, 揭示中药复方用药奥秘具有现实意义.
李康, 副教授, 广东药学院药科学院药物分析教研室
目前主要从亚细胞、细胞及整体水平研究药物对CYP450酶的影响作用, 如从肝微粒体、肝原代细胞培养或体内实验研究CYP450酶活性或基因、蛋白表达等. 中药与CYP450酶之间的关系研究难点在于中药(复方)成分多样, 对CYP450酶影响作用复杂, CYP450酶对不同中药成分代谢情况也同样复杂, 亟待研究的问题是如何采用有效研究模式及严密的数理统计分析, 从中药与代谢酶之间纷繁复杂的相互影响关系中探索两者之间的作用规律.
杜贵森报道其在临床运用戊己丸时, 扩大该方剂运用范围, 凡遇情志内伤、肝胃不和所致的多种疾病, 每选用戊己丸作基础方、加味施治于临床, 取得满意的疗效. 王丹等认为中药对CYP450的作用, 受多种内外因素的影响, 中药不同来源, 各种炮制加工、制剂等工艺过程均会对CYP450产生不同影响作用, 如何排除各种非实验因素的影响, 并合理进行实验设计, 是当前中药对CYP450活性作用研究中的难点.
本文以方剂对CYP1A2酶活性的影响为主效应, 以IC50作为量化观察指标, 研究戊己丸配伍的数、量、相互比例与方剂主效应的关系, 为探讨中药复方配伍机制提供新的研究思路.
药物代谢性相互作用是导致患者发生不良反应乃至严重不良反应或死亡的重要原因, 戊己丸及黄连均是现代临床常用中药(复方), 从本实验结果看, 临床使用戊己丸及黄连, 尤其存在多药共用的情况下, 务必要注意防范可能因戊己丸或黄连抑制CYP1A2酶活性而出现的不良药物代谢性相互作用.
本研究在中医药研究思路中有很大的创新性和探索性, 实验方法尚可, 结果具有一定借鉴意义.
编辑: 李瑞敏 电编:何基才
| 6. | Kokwaro GO, Glazier AP, Ward SA, Breckenridge AM, Edwards G. Effect of malaria infection and endotoxin-induced fever on phenacetin O-deethylation by rat liver microsomes. Biochem Pharmacol. 1993;45:1235-1241. [PubMed] [DOI] |
| 11. | 鲍 天冬. 戊已丸提取物不同配伍的药物动力学实验研究. 北京: 中国中医科学院 2007; 1-175. |
| 12. | 董 宇. 戊己丸不同配伍的肠吸收特征及与P-gp相互作用研究. 北京: 中国中医科学院 2008; 1-124. |