修回日期: 2010-06-09
接受日期: 2010-06-22
在线出版日期: 2010-08-18
目的: 观察复方氯胺酮口服液(CKOS)对大鼠胃排空、肠转运速度、胃动素水平的影响, 进一步评价其临床应用的安全性.
方法: 选Wister大鼠125只, 随机分成5组, 每组25只, 每组又分成5个时点, 每个时点5只. 对照组(C组): 蒸馏水1 mL灌胃; 调味剂组: 调味剂溶液(含清甜素、巧克力香精、除苦剂)1 mL灌胃; 咪达唑仑组(MID组): 咪达唑仑溶液1 mL灌胃, 剂量为10 mg/kg; 氯胺酮组(KET组): 氯胺酮溶液1 mL灌胃, 剂量为100 mg/kg; CKOS组: CKOS溶液(含氯胺酮剂量为100 mg/kg、咪达唑仑剂量为10 mg/kg加调味剂等)1 mL灌胃. 立刻用0.2%酚红1 mL灌胃. 分别于0、30、60、120、360 min 5个时点断头取血2 mL, 检测血浆胃动素. 将30 min时点对应的大鼠取出胃肠, 观察色素在小肠移行速度, 用分光光度计检测胃内色素残留率.
结果: C组30、60 min胃动素水平分别为219.6 ng/L±13.05 ng/L、235.4 ng/L±22.43 ng/L较0点水平178.3 ng/L±15.32 ng/L有显著的升高(均P<0.01), T组30、60min胃动素较0点也有明显升高(均P<0.01), 且与C组对应时点相比, 也有显著差异(均P<0.01), 表明调味剂能促进胃动素的分泌. KET组、MID组、CKOS组30、60 min胃动素水平都低于C组对应时点(均P<0.05或0.01). T组30 min胃残留率为30.29%±7.42%比C组30 min残留率(46.07%±6.01%)显著减少(P<0.01), T组小肠推进比显著大于C组(P<0.01). KET组、MID组和CKOS组的30 min胃残留率显著大于C组(P<0.05或0.01). KET组小肠推进比显著小于C组(P<0.01).
结论: CKOS口服减慢大鼠胃液体排空速度; CKOS对胃动素分泌有一定的抑制作用.
引文著录: 韩盛, 张锦, 汤隽. 复方氯胺酮口服液对胃肠动力的影响. 世界华人消化杂志 2010; 18(23): 2405-2409
Revised: June 9, 2010
Accepted: June 22, 2010
Published online: August 18, 2010
AIM: To investigate the effects of Compound Ketamine Oral Solution (CKOS) on gastric emptying rate, intestinal transit rate, and plasma motilin levels in rats and to evaluate the safety of application of CKOS to clinical practice.
METHODS: One hundred and twenty-five Wistar rats were randomly divided into five groups (25 rats each): control group (intragastrically given 1 mL distilled water), sauce group (intragastrically given 1 mL sauce solution), midazolam (MID) group (intragastrically given 1 mL MID solution, 10 mg/kg), ketamine (KET) group (intragastrically given 1 mL KET solution, 100 mg/kg), and CKOS group (intragastrically given 1 mL CKOS). These groups were further divided into five subgroups (five rats each) for testing at different time points. After gastric administration, each rat was intragastrically given 1 mL of 0.2% phenolphthalein. Blood samples were taken at 0, 30, 60, 120 and 360 min to measure plasma motilin levels. The stomach and small intestine of the rats in the 30-min subgroup were removed to measure the rates of gastric emptying and intestinal transit, respectively.
RESULTS: In the control group, the motilin levels at 30 and 60 min were significantly higher than that at baseline (219.6 ng/L ± 13.05 ng/L and 235.4 ng/L ± 22.43 ng/L vs 178.3 ng/L ± 15.32 ng/L, both P < 0.01). In the sauce group, the motilin levels at 30 and 60 min were significantly higher than that at baseline and those at corresponding time points in the control group (all P < 0.01). The motilin levels at 30 and 60 min in the KET, MID and CKOS groups were lower than those in the control group at corresponding time points (all P < 0.01 or 0.05). There were no differences in the motilin levels among the KET, MID and CKOS groups. The rates of gastric emptying and intestinal transit were significantly higher in the sauce group than in the control group (both P < 0.01). The rates of gastric emptying at 30 min in the KET, MID and CKOS groups were significantly lower than that in the control group (all P < 0.01 or 0.05). The rate of intestinal transit in the KET group was lower than that in the control group (P < 0.01).
CONCLUSION: CKOS can slow down gastric emptying in rats. KET and MID can inhibit excretion of motilin.
- Citation: Han S, Zhang J, Tang J. Effects of Compound Ketamine Oral Solution on gastrointestinal motility in rats. Shijie Huaren Xiaohua Zazhi 2010; 18(23): 2405-2409
- URL: https://www.wjgnet.com/1009-3079/full/v18/i23/2405.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v18.i23.2405
目前临床常用的麻醉前给药方法是经直肠、经鼻、肌注途径给药, 不仅小儿不易接受, 且造成术前恐惧, 影响术后小儿的身心健康. 口服给药是一个比较方便易行、小儿较易接受的用药途径[1,2]. 复方氯胺酮口服液(Compound Ketamine Oral Solution, CKOS)是我们与药科大学合作共同研制的麻醉前口服用药剂型. 在前期临床应用中发现其镇静效果满意率可达到90%以上[3]. 虽尚未发现反流误吸的病例, 但该药是否增加反流误吸的危险还不清楚. 任何降低食管下端括约肌张力, 减慢胃排空和肠转运动速度, 增加胃酸分泌的因素都会增加反流误吸的危险. 研究表明胃动素(motilin, MTL)可以增强胃动力[4]. CKOS对MTL的影响还不清楚. 本研究通过动物实验观察CKOS对大鼠胃排空、肠转运速度、MTL水平的影响, 探讨其对胃肠动力的影响.
Wister大鼠125只, ♂, 体质量200 g±25 g, 中国医院大学实验动物中提供, 实验前大鼠禁食12 h, 禁水2 h. 酚红、NaOH(沈阳化学制剂公司购置)、复方氯胺酮口服液(沈阳药科大学配制)、752型分光光度计(上海光谱仪器有限公司生产)、MTL放免试剂盒(解放军总医院东亚放免研究所)、氯胺酮(华北制药, 批号: 20040217)、咪达唑仑(徐州恩华药业公司, 批号: B1153).
1.2.1 分组: Wister大鼠125只, 随机分成5组, 每组25只, 每组又分成5个时点, 每个时点5只(各组各时点大鼠体质量无统计学差异). C(Control, 对照)组: 蒸馏水1 mL灌胃; T组(调味剂组): 调味剂溶液1 mL灌胃, 含清甜素, 巧克力香精, 除苦剂; MID(Midazolam, 咪达唑仑)组: MID溶液1 mL灌胃, 剂量为10 mg/kg; KET(Ketamine, 氯胺酮)组: KET溶液1 mL灌胃, 剂量为100 mg/kg; CKOS组: CKOS溶液(含KET剂量为100 mg/kg、MID剂量为10 mg/kg加调味剂等)1 mL灌胃.
1.2.2 步骤: 每只1 mL溶液灌胃后, 立刻用0.2%酚红1 mL灌胃. 分别于0、30、60、120、360 min 5个时点断头取血2 mL, 置于含30 μL 10% EDTA和30 μL抑肽酶塑料管中混匀, 3 500 r/min, 4 ℃离心15 min, 取血浆-20 ℃保存. 迅速将30 min时点对应的大鼠开腹取全胃肠, 自幽门括约肌处取胃, 沿大弯侧剪开, 将胃内色素残留物充分洗于5 mL 0.1% NaOH中, 3 500 r/min离心15 min, 取上清滤液, 以752型分光光度计, 波长560 nm测吸光度. 另测定1 mL 0.2%酚红加1 mL蒸馏水和5 mL 0.1% NaOH的吸光度为基础光密度. 按公式(样品吸光度/基础吸光度×100%)计算胃液体残留率, 同时量取幽门括约肌至色素最前端及至盲肠的距离, 以二者之比作为小肠推进比. 血浆MTL测定采用放免法, 参照试剂盒说明进行.
统计学处理 应用SPSS10.0版本统计分析软件, 所得参数以mean±SD表示, 以方差分析进行统计学处理.
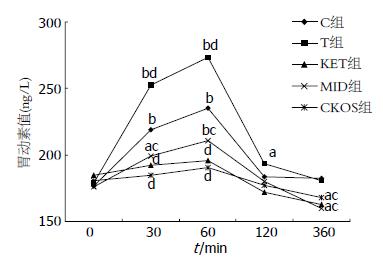
各组大鼠0 min MTL无统计学差异(P>0.05). C组和T组灌胃后MTL水平上升, 60 min后达到最高. C组30 min、60 min MTL较0 min有显著的升高(P<0.01), T组30、60 min MTL较0 min也有明显升高(P<0.01), 且与C组相同时点相比, 也有显著差异(P<0.01), 表明调味剂能促进MTL的分泌. KET组、CKOS组30、60 min MTL水平与0 min相比无统计学差异(P>0.05), MID组30、60 min MTL水平高于0 min(P<0.05或<0.01), KET组、MID组、CKOS组30、60 min MTL水平都低于C组相同时点(P<0.01或<0.05), 并显著低于T组相同时点(P<0.01), KET组、MID组、CKOS组3组之间无统计学差异(P>0.05). 360 min KET组和MID组的MTL水平低于组内0 min, 也低于C组(P<0.05, 表1, 图1).
| 分组 | 0 min | 30 min | 60 min | 120 min | 360 min |
| C组 | 178.3±15.32 | 219.6±13.05b | 235.4±22.43b | 183.8±22.87 | 182.2±8.58 |
| T组 | 179.2±17.48 | 252.6±21.45bd | 273.6±18.35bd | 193.4±23.25a | 180.6±16.01 |
| KET组 | 184.8±18.27 | 192.2±14.20d | 195.8±17.63d | 171.8±12.83 | 162.8±20.25ac |
| MID组 | 175.8±14.67 | 199.4±11.17ac | 211.0±17.51bc | 180.0±11.73 | 159.8±10.96ac |
| CKOS组 | 180.8±9.63 | 185.0±10.42d | 190.4±12.10d | 177.0±11.47 | 168.0±13.45 |
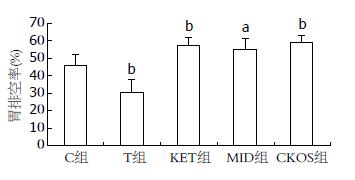
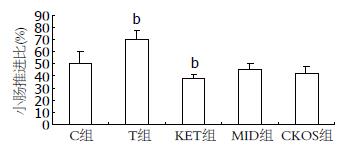
T组30 min胃残留率比C组显著减少(P<0.01), T组小肠推进比显著大于C组(P<0.01). KET组、MID组和CKOS组的30 min胃残留率显著大于C组(P<0.01或<0.05). KET组小肠推进比显著小于C组(P<0.01), MID组和CKOS组小肠推进比也小于C组, 但没有统计学差异(P>0.05. 表2, 图2, 3).
小儿术前哭闹不合作一直是临床尚未解决的一大难题. 在前期研究中通过动物实验和临床研究已经证实了CKOS口服用药起效快、镇静效果确切, 患儿及其家属易于接受[3], 并通过动物实验证明对大鼠重要脏器有保护作用[5,6], 对胃黏膜无明显刺激性[7]. CKOS使小儿术前合作程度增加、哭闹大大减少, 但其术后恶心、呕吐, 反流、窒息发生率如何尚不清楚, 本研究目的是为了进一步证实该剂型对胃肠动力的影响. 本研究发现KET组的30 min胃残留率、小肠推进比与C组相比, 有明显的统计学差异, 表明KET都能够减慢大鼠胃对液体的排空和小肠推进速度. MID组和CKOS组的30 min胃残留率与C组相比, 也有明显的统计学差异, 表明MID和CKOS都能够减慢大鼠胃液体的排空速度.
为了使小儿更容易接受CKOS, 我们在口服液中加了赋形剂, 调味剂由清甜素、巧克力香精、除苦剂和蒸馏水组成, 其热卡密度和渗透压大于蒸馏水. 研究结果证实调味剂组的排空速度和小肠推进速度要快于对照组. CKOS的成分由KET、MID和调味剂构成. KET 、MID都能够减慢大鼠胃液体的排空速度, CKOS组与KET和MID组相比没有统计学差异, 表明CKOS对胃肠动力的抑制没有随联合用药而进一步加强, 这可能是KET和MID与调味剂综合作用的结果. Inada等[8]给小鼠静脉注入催眠剂量的MID和生理盐水后, 用含有荧光物质的液体灌胃, 30 min后观察胃排空和肠转运情况, 发现MID能够以剂量相关的方式抑制胃排空和肠转运速度. 本研究的结果显示MID能够抑制胃排空, 这与Inada的研究结果一致. MID组的小肠推进比为45.31%±4.93%, 与C组的小肠推进比(50.36%±9.25%)相比没有统计学差异(P = 0.059). 这一点与Inada的研究结果不一致, 可能与用药剂量不同有关.
本研究结果显示KET口服能够减慢胃液体排空和肠转运速度. 胃排空受年龄、容量、热卡密度和渗透压等因素影响. 300 mL盐水的排空速度要大于150 mL盐水的排空速度. Grant等[9]研究了止痛剂量的KET对成人胃动力的影响, 比较KET 0.5 mg/kg肌注与生理盐水肌注后对乙酰胺基酚的吸收情况, 发现两者没有差异. 吸入麻醉药对胃肠动力有抑制作用. Freye等[10]比较KET和MID联合静脉输入剂量分别为5 mg/(kg•h)、0.5 mg/(kg•h)与吸入1.5%的安氟醚对胃肠动力的影响, 发现两者没有统计学差异. 在前期研究中, 我们发现CKOS中的KET能够抑制大鼠的脑星形细胞和胃的兴奋性受体N-甲基D-门冬氨酸受体1(N-methyl-D-aspartate receptor 1, NMDAR1)的表达, 而MID能够加强抑制性受体γ-氨基丁酸A受体(gamma-aminobutyric acid A receptor, GABAAR)的表达[11,12]. KET 5 mg/(kg•h)和MID 0.5 mg/(kg•h)静脉输入对胃动力抑制作用可能是分别通过抑制胃平滑肌上的NMDAR1和能够兴奋胃腺体中的GABAAR来实现的.
MTL是启动胃肠收缩活动的兴奋性脑肠肽, 是增加胃肠动力的重要激素, MTL不足导致胃肠平滑肌松弛、胃张力及蠕动减弱、胃排空时间延长、胃液潴留增加[13]. 本研究结果显示KET组、MID组、CKOS组在30 min和60 min的MTL水平都低于C组和T组, 由此可以推断KET、MID、CKOS对灌胃后MTL分泌增加反应的抑制, 是他们减慢胃排空和肠转运速度的原因之一.
麻醉用药异丙酚具有显著的镇吐作用. 有文章报道异丙酚降低血浆MTL水平, 异丙酚的镇吐作用可能与降低血浆MTL水平有关[14]. CKOS组的MTL水平没有大幅度上升, 不会导致因MTL水平过高而引起的恶心和呕吐. 在许多临床研究中, 经常采用KET和MID单独或联合混以较大容量的甜饮料术前口服. 本研究表明KET、MID单独或联合口服会减慢胃液体排空和肠转运速度, 如术前口服液体量较大, 会增加胃储留, 增加反流误吸的危险. CKOS口服减慢大鼠胃液体排空速度. 但在临床应用时, 30 kg以下的小儿口服容量小于7.5 mL, 由于容量较小, 降低了反流误吸的危险. CKOS临床应用是安全可行的.
目前小儿麻醉前用药一直没有成熟的剂型, 而且口服用药溶液量较大. 复方氯胺酮口服液具有用药容量少, 口味易被患儿接受, 镇静效果满意等特点. 在临床应用上也有较高的安全性.
李勇, 副教授, 上海中医药大学附属市中医医院消化科
许多研究表明: 小儿麻醉前用药采用口服的方式较易被患儿及其家属接受, 也能达到理想的镇静效果. 但其是否增加反流误吸的危险目前还不清楚. 这个问题限制了这种方式在临床上的广泛应用. 术前口服药对胃肠动力的影响需要进行深入研究.
Takefumi等给小鼠静脉注入催眠剂量的MID和生理盐水后, 发现MID能够以剂量相关的方式抑制胃排空和肠转运速度.
本研究观察了口服CKOS对大鼠胃肠动力的影响. 发现KET、MID单独或联合口服会减慢胃液体排空和肠转运速度.
本研究思路较清晰, 实验设计尚合理, 统计学处理方法恰当, 具有一定的临床现实意义.
编辑: 曹丽鸥 电编:何基才
| 1. | 苏 岚. 小儿口服麻醉前用药. 国外医学·麻醉学与复苏分册. 2001;22:207-208. |
| 4. | Tack J. Georges Brohee Prize 1994. Motilin and the enteric nervous system in the control of interdigestive and postprandial gastric motility. Acta Gastroenterol Belg. 1995;58:21-30. [PubMed] |
| 8. | Inada T, Asai T, Yamada M, Shingu K. Propofol and midazolam inhibit gastric emptying and gastrointestinal transit in mice. Anesth Analg. 2004;99:1102-1106, table of contents. [PubMed] [DOI] |
| 9. | Grant IS, Nimmo WS, Clements JA. Lack of effect of ketamine analgesia on gastric emptying in man. Br J Anaesth. 1981;53:1321-1323. [PubMed] [DOI] |
| 10. | Freye E, Sundermann S, Wilder-Smith OH. No inhibition of gastro-intestinal propulsion after propofol- or propofol/ketamine-N2O/O2 anaesthesia. A comparison of gastro-caecal transit after isoflurane anaesthesia. Acta Anaesthesiol Scand. 1998;42:664-669. [PubMed] [DOI] |