修回日期: 2010-04-06
接受日期: 2010-04-13
在线出版日期: 2010-05-08
目的: 分析国产奥曲肽(依普比善)及进口奥曲肽(善宁)治疗Ⅱ级以上肿瘤治疗相关性急性腹泻的疗效及药物经济学.
方法: 138例放疗及化疗相关性Ⅱ-Ⅲ级腹泻患者列入本观察研究, 66例接受善宁治疗、72例接受依普比善, 首剂均为100 µg, 皮下注射, tid, 连续治疗3 d后判断疗效.
结果: 善宁组腹泻完全缓解率为75.8%, 依普比善组为79.2%, 没有显著性差异. 依普比善治疗Ⅲ级腹泻第2天及第3天用量剂量高于善宁组. 善宁组治疗方案的成本效果分析值为1148.7, 依普比善组为507.3.
结论: 依普比善与善宁处理肿瘤治疗相关性腹泻方面疗效相当, 但依普比善更符合药物经济学原则. 处理重度腹泻时提高依普比善剂量是合理选择, 且提高依普比善剂量并没有显著不良反应发生.
引文著录: 邱红, 熊慧华, 胡广原, 汪锐, 唐曦. 国产、进口奥曲肽处理肿瘤治疗相关性腹泻138例. 世界华人消化杂志 2010; 18(13): 1400-1403
Revised: April 6, 2010
Accepted: April 13, 2010
Published online: May 8, 2010
AIM: To compare the efficacy of domestic and imported octreotide (Sandostatin) in the treatment of acute diarrhea associated with anti-tumor therapy.
METHODS: One hundred and thirty-eight patients with grade II or III diarrhea were enrolled into the study, of which 66 received Sandostatin treatment, and 72 were given domestic octreotide (100 µg, tid). Therapeutic efficacy was evaluated after a 3-day treatment.
RESULTS: No significant difference was noted in the complete remission rate of diarrhea between patients treated with Sandostatin and domestic octreotide (75.8% vs 79.2%, P > 0.05). The doses of domestic octreotide used on days 2 and 3 were significantly higher than those of Sandostatin (both P < 0.05). The cost-effectiveness value for Sandostatin was significantly higher than that for domestic octreotide (1148.7 vs 507.3, P < 0.05).
CONCLUSION: Domestic octreotide has equivalent efficacy and superior cost-effectiveness to Sandostatin in treating acute diarrhea associated with anti-tumor therapy. Increasing the dose of domestic octreotide is a reasonable choice in the management of grade III diarrhea.
- Citation: Qiu H, Xiong HH, Hu GY, Wang R, Tang X. Domestic versus imported octreotide in the treatment of acute diarrhea associated with anti-tumor therapy: an analysis of 138 cases. Shijie Huaren Xiaohua Zazhi 2010; 18(13): 1400-1403
- URL: https://www.wjgnet.com/1009-3079/full/v18/i13/1400.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v18.i13.1400
生长抑素对应的靶腺体包括脑组织、垂体、胰岛细胞、胃肠组织等, 他作用于胃肠道组织时可抑制胃肠道的内外分泌功能、降低肠蠕动、增加离子及营养物质吸收、促进脉管收缩等功能[1], 最近研究认为生长抑素还可抑制细胞增殖, 具有抗肿瘤作用[2]. 奥曲肽与生长抑素受体2、6亚型高度亲和, 生理效应与生长抑素类似, 具有缓解腹泻、控制疼痛等作用. 与伊利替康联合5-FU及甲酰四氢叶酸(简称IFL)化疗方案相关的两项晚期结肠癌临床试验(N9741及C89803)报道了较高的急性腹泻相关死亡率, 癌症治疗相关性腹泻得到越来越多的临床重视[3]. 国外有多项研究表明: 在治疗及预防化疗相关性腹泻方面, 奥曲肽疗效明显优于洛哌丁胺及安慰剂[4-6], 目前国际姑息治疗委员会已将奥曲肽列为腹泻症状处理的基本用药. 国产醋酸奥曲肽(依普比善)在治疗食管胃底静脉曲张出血方面具有满意疗效[7], 我们在临床使用中发现依普比善治疗盆腔放疗相关性腹泻的疗效明显优于洛哌丁胺, 不良反应低. 为比较依普比善与进口奥曲肽(善宁)在治疗肿瘤相关性腹泻方面的差异, 本研究进行如下治疗观察, 现报道如下.
根据美国NCI腹泻程度分级及肿瘤治疗相关性腹泻处理指南, 138例具有生长抑素治疗指征的Ⅱ及Ⅲ级腹泻患者纳入本观察项目, 根据指南其中Ⅱ级腹泻患者合并下列症状之一, 如肠绞痛、Ⅱ级以上恶心呕吐、发热、白细胞下降、ECOG评分小于2. 出于伦理学考虑, Ⅳ级腹泻患者未纳入研究. 所有患者诊断均有病理学依据.
1.2.1 治疗: 发生抗肿瘤治疗相关性腹泻、且初诊医生判断无需进行静脉补液治疗的患者随机分入善宁治疗组及依普比善治疗组. 66例患者接受善宁治疗, 72例患者接受依普比善治疗. 善宁及依普比善给药初始剂量为100 µg, 皮下注射, 每隔8 h 1次. 给药第1天后观察腹泻如果保持不变或加剧, 增加药物剂量为200 µg, 皮下注射, 每隔8 h 1次; 增加剂量给药24 h后, 症状没有改善或加剧, 则增加药物剂量300 µg, 皮下注射, 每隔8 h 1次. 所有患者根据相关检查给予对应症状处理措施及饮食指导, 治疗期间密切观察患者体征及症状. 如果患者腹泻发生在抗肿瘤治疗期间, 经高年资医师判断该患者是否需要停止抗肿瘤治疗以及是否需要输液治疗.
1.2.2 有效性判断: 每隔24 h对患者进行一次腹泻症状评估. 治疗3 d后, 如恢复平常大便次数或大便增加次数为1-2次/d, 认为腹泻完全缓解. 如果未达以上标准, 认为治疗失败. 记录两组患者抗肿瘤治疗停止天数以及需要输液治疗情况.
1.2.3 药效经济学分析: 成本-效果分析是应用成本与效果的比值表示每获得一份效果所需要的净成本. 记录两组生长抑素用量及费用成本, 采用成本-效果分析方法来表示药物治疗成本效果分析.
统计学处理 用mean±SD表示定量数据, 采用SPSS13.0软件的两独立样本t检验进行均值比较分析; 分类数据用SPSS13.0进行χ2检验分析. 显著性差异水平为P<0.05.
两组年龄、性别、诊断、抗肿瘤治疗方式、KPS评分、腹泻程度方面没有显著性差异, 具有可比性(表1).
| 分组 | 善宁组 | 依普比善组 | P值 |
| 年龄(岁) | 48.3±9.3 | 47.9±7.5 | 0.764 |
| 性别n(%) | |||
| 男 | 37(56.1) | 35(48.6) | 0.399 |
| 女 | 29(43.9) | 37(51.4) | |
| 病理诊断n(%) | |||
| 膀胱癌 | 1(1.5) | 0(0.0) | 0.744 |
| 原发灶不明转移癌 | 1(1.5) | 0(0.0) | |
| 肺癌 | 10(15.2) | 10(13.9) | |
| 宫颈癌 | 9(13.6) | 11(15.3) | |
| 结肠癌 | 7(10.6) | 10(13.9) | |
| 淋巴瘤 | 2(3.0) | 3(4.2) | |
| 前列腺癌 | 3(4.5) | 4(5.5) | |
| 食管癌 | 4(6.1) | 4(5.5) | |
| 胃癌 | 14(21.2) | 8(11.1) | |
| 直肠癌 | 11(16.7) | 15(20.8) | |
| 子宫内膜癌 | 4(6.1) | 6(8.3) | |
| 恶性黑色素瘤 | 0(0.0) | 1(1.4) | |
| KPS评分 | 79.2±5.3 | 79.8±4.9 | 0.479 |
| 抗肿瘤治疗方式n(%) | |||
| 放疗 | 11(16.7) | 19(26.4) | 0.363 |
| 同步放化疗 | 11(16.7) | 12(16.7) | |
| 化疗 | 44(66.6) | 41(56.9) | |
| 腹泻程度分级n(%) | |||
| Ⅱ级 | 35(53.0) | 27(37.5) | 0.087 |
| Ⅲ级 | 31(47.0) | 45(62.5) |
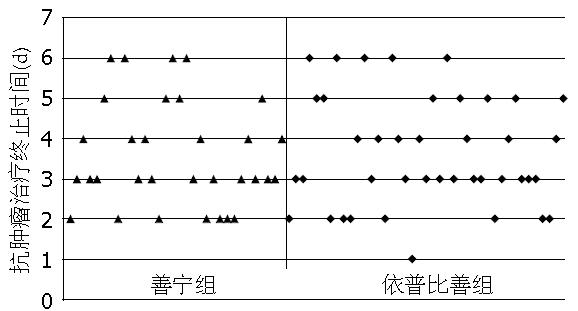
两组在腹泻缓解率及是否需要输液治疗方面没有显著性差异, 疗效相当(表2). 善宁组共有37例患者的腹泻症状发生在抗肿瘤治疗进行中, 其中有32例(86.5%)患者因腹泻中止治疗, 依普比善组对应别为51例及41例(80.4%), 两组因腹泻抗肿瘤治疗中止情况没有差异(P = 0.453). 图1散点图分析显示两组抗肿瘤治疗中止持续时间无差异(P = 0.276).
| 分组 | 善宁组 | 依普比善组 | P值 | |
| 腹泻缓解率n(%) | ||||
| II级 | 是 | 28(80.0) | 24(91.9) | 0.552 |
| 否 | 7(20.0) | 3(11.1) | ||
| III级 | 是 | 22(71.0) | 33(73.3) | 0.821 |
| 否 | 9(29.0) | 12(26.7) | ||
| 总有效率 | 50(75.8) | 57(79.2) | 0.632 | |
| 需要输液治疗n(%) | ||||
| 是 | 42(63.6) | 49(68.1) | 0.584 | |
| 否 | 24(36.4) | 23(31.9) |
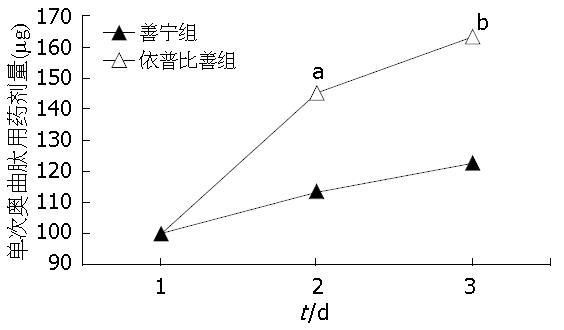
Ⅱ级腹泻两组所有日均单次用量均为100 µg, 单次花费善宁组为135.0元, 依普比善组为49.6元. Ⅲ级腹泻治疗后缓解患者两组日均单次用药剂量见图2, 依普比善用量在第2及第3天均高于善宁组, 统计学有显著性差异. 善宁组治疗方案的成本效果分析值为1148.7, 而依普比善组为507.3, 提示国产醋酸奥曲肽治疗更符合药效经济学.
善宁组头晕1例, 注射部位疼痛2例; 依普比善组头晕3例, 注射部位疼痛4例, 注射后腹部不适感为3例. 所有不良反应均为轻度, 未影响患者治疗.
肠隐窝未分化细胞增殖池不断补充脱落的肠表面上皮细胞, 该细胞对化疗及放射线尤为敏感, 肠上皮再生受损及毛细血管渗出可影响黏膜屏障功能, 肠吸收功能下降, 导致水样腹泻. 伊立替康活性代谢产物SN38直接作用于肠黏膜上皮细胞的拓扑异构酶-Ⅰ, 引起DNA双链断裂, 细胞死亡, 导致肠结构和功能的改变. 腹泻是伊立替康等化疗药物常见不良反应, 化疗相关性腹泻发生率可高达82%, 其中1/3可为Ⅲ、Ⅳ级重度腹泻[8]. 盆腔放疗中以腹绞痛及腹泻为特征的急性放疗性肠炎发生率为50%左右, 前列腺癌调强放射治疗腹泻的发生率仍可达36.7%, 同步放化疗时放疗相关性腹泻的发生率更高, 有报道可达80%以上[9]. 长期腹泻除导致电解质紊乱等并发症外, 还常迫使化疗药物减量、放射治疗中断, 影响抗肿瘤治疗效果.
癌症治疗相关性腹泻的治疗方法包括补液、预防性使用抗生素、止泻等, 其中洛哌丁胺是急性腹泻治疗标准用药, 但有效率并不高. 奥曲肽具有抑制肠蠕动、减少肠分泌作用, 已经被国际姑息治疗协会列为姑息治疗基本药物, 关于长效奥曲肽治疗的一些临床试验也在进行中. 国外研究表明善宁治疗化疗相关性腹泻有效率可达85%以上[4-6], 刘东屏等报道善宁治疗肠道菌群失调致腹泻的3及7 d有效率分别为37.5%和78.1%[10], 邱冬等采用善宁治疗常规治疗无效的化疗难治性腹泻的3 d有效率为84.7%[11]. 在本研究中, 善宁及国产醋酸奥曲肽(依普比善)治疗化疗放疗相关性腹泻的总有效率分别为75.8%及79.2%, 两组没有显著性差异, 两组患者需要输液支持对症治疗的比例也没有明显差异, 抗肿瘤治疗中止持续时间类似, 显示依普比善与善宁疗效相当. 需要指出的是善宁组及依普比善组腹泻治疗的3 d有效率均略低于部分国内及国外报道的85%以上, 其原因可能是由于参与此研究的部分患者止泻治疗期间仍然持续进行抗肿瘤治疗, 某种程度上影响了奥曲肽的3 d治疗效果评价.
虽然善宁与依普比善疗效相当, 但根据腹泻程度的分层分析仍然可以看到两组在用药剂量调整方面的部分差异. 两组在Ⅱ级腹泻的用药方面, 日均单次100 µg的用量均可以达到满意控制效果. Ⅲ级腹泻的处理虽然疗效相当, 但是依普比善组第2及第3天的调整剂量高于善宁组, 具有显著性差异. 根据此结果我们认为, 采用依普比善处理较重腹泻时, 为了获得更迅速的腹泻控制率, 初期即提高依普比善剂量似乎是较合理选择, 而且在本研究中我们没有观察到提高依普比善剂量后有严重不良反应发生.
成本和效果是药物经济学研究的两大要素, 药物经济学分析类型有成本-效果分析、成本-效用分析、成本-效益分析等. 成本-效果分析是应用成本与效果的比值以表示每获得一份效果所需要的净成本, 在医学方面有广泛应用, 是目前医院药物经济学研究中最常用的方法. 成本-效果分析常用计算成本-效果比和计算增量成本-效果比两种方法. 根据本次调查原始资料进行的成本-效果分析法显示, 以腹泻缓解作为疗效指标时, 获得同等治疗疗效的前提下, 依普比善组费用较低, 其成本效果分析值仅为善宁组的50%左右. 因此从降低医疗费用角度考虑, 依普比善比善宁具有优势.
皮下注射奥曲肽的不良反应包括头痛(6%)、头晕(5%)、恶性呕吐(5%-10%)以及注射部位疼痛(7.7%)[12]等. 善宁组及依普米善组患者, 出现了头晕、注射部位疼痛、腹部不适等症状, 但这些不良反应发生率相对较低, 且都为轻度, 不影响患者治疗, 提示皮下注射两种治疗方案的安全性较好.
总之, 依普比善在处理肿瘤治疗相关性急性腹泻方面疗效与善宁相当, 更符合药物经济学原则, 可推荐用于化放疗相关急性腹泻的处理. 与肿瘤治疗相关性腹泻治疗指南推荐的善宁基本用量相比, 使用依普比善在处理Ⅲ级以上腹泻时, 提高药物剂量可能更为合理.
在晚期结肠癌化疗的两项临床试验中, 化疗及放疗相关性腹泻是常见治疗不良反应, 常常导致患者抗肿瘤治疗中断, 严重时会危及患者生命. 控制和处理肿瘤治疗相关性腹泻具有重要意义, 而在有关晚期结肠癌化疗的两项临床试验中观察到较为严重的与IFL方案相关的腹泻反应使得临床对此更为重视.
梅林, 教授, 北京大学医学部生理学与病理生理学系神经调节和消化内分泌研究室.
目前常用的腹泻治疗方法在处理肿瘤治疗相关性腹泻中有效率并不理想, 而生长抑素在腹泻方面的治疗应用逐步得到关注和研究, 尤其是在重度腹泻、恶性肠梗阻方面显示了其治疗优势. 摸索生长抑素在国人中的最佳用药剂量仍然需要较多研究和探索.
国外关于生长抑素在处理肿瘤治疗相关性腹泻的前瞻性随机临床试验证实了该药对比洛哌丁胺及安慰剂的优势, 目前生长抑素治疗已经被列为国际姑息治疗腹泻治疗的基本用药. 在化疗相关性腹泻处理指南中也指出生长抑素是中重度腹泻的标准用药.
本研究在国内首次比较了国产奥曲肽与进口奥曲肽处理肿瘤治疗相关性腹泻的疗效, 并能够指出国产奥曲肽在重度腹泻治疗上的不足之处.
国产醋酸奥曲肽(依普比善)在处理肿瘤治疗相关性急性腹泻更符合药物经济学原则, 可推荐用于化放疗相关急性腹泻的处理.
成本-效果分析: 药物经济学常用的一个考核指标, 通过应用成本与效果的比值表示每获得一份效果所需要的净成本, 在医学方面有广泛应用, 常用计算成本-效果比和计算增量成本-效果比两种方法.
本文选题尚可, 有较好的临床参考价值.
编辑: 李军亮 电编: 吴鹏朕
| 1. | Reichlin S. Somatostatin and its receptor. Introduction. Ciba Found Symp. 1995;190:1-6. [PubMed] |
| 2. | Prommer EE. Established and potential therapeutic applications of octreotide in palliative care. Support Care Cancer. 2008;16:1117-1123. [PubMed] [DOI] |
| 3. | Ashley AC, Sargent DJ, Alberts SR, Grothey A, Campbell ME, Morton RF, Fuchs CS, Ramanathan RK, Williamson SK, Findlay BP. Updated efficacy and toxicity analysis of irinotecan and oxaliplatin (IROX) : intergroup trial N9741 in first-line treatment of metastatic colorectal cancer. Cancer. 2007;110:670-677. [PubMed] [DOI] |
| 4. | Cascinu S, Fedeli A, Fedeli SL, Catalano G. Octreotide versus loperamide in the treatment of fluorouracil-induced diarrhea: a randomized trial. J Clin Oncol. 1993;11:148-151. [PubMed] |
| 5. | Barbounis V, Koumakis G, Vassilomanolakis M, Demiri M, Efremidis AP. Control of irinotecan-induced diarrhea by octreotide after loperamide failure. Support Care Cancer. 2001;9:258-260. [PubMed] [DOI] |
| 6. | Cascinu S, Fedeli A, Fedeli SL, Catalano G. Control of chemotherapy-induced diarrhea with octreotide. A randomized trial with placebo in patients receiving cisplatin. Oncology. 1994;51:70-73. [PubMed] [DOI] |
| 8. | Maroun JA, Anthony LB, Blais N, Burkes R, Dowden SD, Dranitsaris G, Samson B, Shah A, Thirlwell MP, Vincent MD. Prevention and management of chemotherapy-induced diarrhea in patients with colorectal cancer: a consensus statement by the Canadian Working Group on Chemotherapy-Induced Diarrhea. Curr Oncol. 2007;14:13-20. [PubMed] [DOI] |
| 9. | Sanguineti G, Endres EJ, Parker BC, Bicquart C, Little M, Chen G, Berilgen J. Acute toxicity of whole-pelvis IMRT in 87 patients with localized prostate cancer. Acta Oncol. 2008;47:301-310. [PubMed] [DOI] |
| 12. | Petersenn S. Efficacy and limits of somatostatin analogs. J Endocrinol Invest. 2005;28:53-57. [PubMed] |