修回日期: 2009-11-19
接受日期: 2009-11-23
在线出版日期: 2009-12-08
目的: 探讨彩色超声在胃肠道间质瘤(GIST)诊断中的应用价值.
方法: 回顾性分析经病理证实的45例GIST的超声声像图特征, 将超声与手术病理结果进行对比分析.
结果: 超声测量肿瘤的最大径线数值病理测量方法差异无统计学意义(t = 1.328, P>0.05). 肿瘤的形态及内部回声与其危险性高低有关: 危险性低、形态规则、内部回声均; 危险性高, 形态不规则, 内呈现混杂回声. 彩色血流分布与肿瘤危险性高低无明显相关. 超声在胃GIST的诊断准确率高于肠道GIST.
结论: 彩色超声检查在GIST诊断中具有实用价值, 结合其他检查可提高GIST诊断准确性.
引文著录: 杨力, 段洪涛, 宋奕宁, 王功伟, 李建国. 彩色超声在胃肠道间质瘤诊断中的应用. 世界华人消化杂志 2009; 17(34): 3568-3571
Revised: November 19, 2009
Accepted: November 23, 2009
Published online: December 8, 2009
AIM: To analyze the value of color Doppler sonography in the diagnosis of gastrointestinal stromal tumor (GIST).
METHODS: The color Doppler sonographic images obtained in 45 patients with pathologically confirmed GIST were analyzed retrospectively. The sonographic findings were compared with pathological results.
RESULTS: There was no statistical difference in diagnostic accuracy of tumor size assessment between color Doppler sonography and pathological examination (t = 1.328, P > 0.05). Tumor size, internal echo and morphology were critical factors for differentiation of low- and high-risk GIST. Color Doppler sonography has a higher accuracy in the diagnosis of GIST in the stomach than in the intestinal tract.
CONCLUSION: Color Doppler sonography is an effective method for diagnosis of GIST. Color Doppler sonography in combination with other examinations may improve diagnostic accuracy in patients with GIST.
- Citation: Yang L, Duan HT, Song YN, Wang GW, Li JG. Clinical value of color Doppler sonography in the diagnosis of gastrointestinal stromal tumor. Shijie Huaren Xiaohua Zazhi 2009; 17(34): 3568-3571
- URL: https://www.wjgnet.com/1009-3079/full/v17/i34/3568.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i34.3568
胃肠道间质瘤(gastrointestinal stromal tumor, GIST)是最常见的胃肠道间叶源性肿瘤, 以往多归入平滑肌瘤范畴, 近年来的研究已证实, 他是一类具有自身形态学特征、特定的免疫表型的肿瘤. GIST早期无任何症状, 随着肿瘤的不断生长, 临床上出现多种非特异性症状. 超声检查作为腹部疾病的最常规检查手段之一, 在GIST的诊断中有其优势. 本文回顾性分析我院经手术病理证实的45例GIST的超声检查资料, 以探讨超声在GIST诊断中的价值.
选择2006-02/2009-04在我院行超声检查, 住院手术确诊为GIST的患者45例, 其中男22例, 女23例, 年龄36-83(平均54.5±24.5)岁. 患者临床症状: 腹部不适、腹胀痛19例; 胃肠道出血(呕血、便血、黑便、大便潜血试验阳性)16例; 腹部包块3例; 食管癌根治手术中发现2例, 体检时发现5例.
使用GE logiq9、Aloka 4000、Alokaα10型彩色超声诊断仪, 腹部探头频率3.5-5.0 MHz. 患者空腹, 平卧位, 常规探查腹、盆腔实质性脏器及周围大血管, 同时扫查胃肠走行区, 发现肿块, 记录肿块部位、大小、形态、回声类型、有无液化坏死区, 以及肿块的活动度. 启动彩色多普勒, 观察肿块的血流特点及肿块与周围血管结构的关系. 若怀疑来源胃部, 嘱患者饮水500-600 mL, 并变换体位对胃部进行多切面观察. 用计算机影像工作站和仪器内置存储设备记录图像. 病理危险性分级标准参照文献[1], 本文将极低度危险性病例列入低度危险性病理诊断中.
统计学处理 采用SPSS12.0统计软件将超声检查结果与手术病理结果对比分析.
肿瘤危险性分级: 高度危险性15例, 中度危险性13例, 低度危险性17例. 单发44例, 多发1例(图1). 肿瘤发生部位: 胃部25例(55.55%), 十二指肠5例, 空回肠9例, 结肠3例, 腹腔1例, 食管下段2例.
2.2.1 肿瘤的大小: 超声测量肿瘤最小2.5 cm×2.2 cm×2.0 cm, 最大37 cm×19 cm×7 cm. 45例患者中, 30例病理有完整的标本大小记录. 将超声测量肿瘤的最大径线数值与病理测量的最大径线数值进行配对样本的t检验, 2种测量方法差异无统计学意义(t = 1.328, P>0.05).
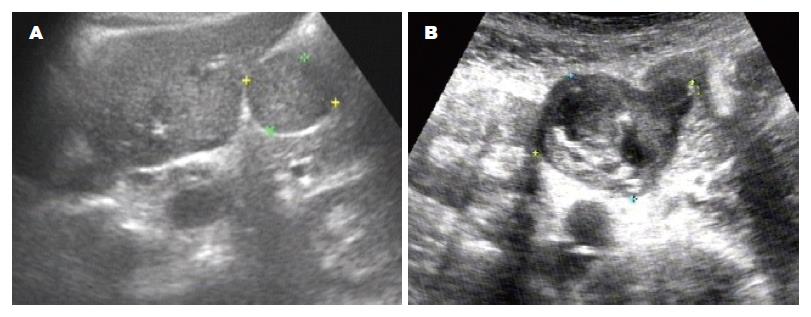
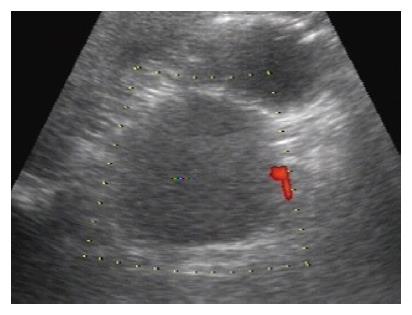
2.2.2 形态与内部回声: 肿瘤的形态及内部回声与肿物的大小有关, 即与其危险性高低相关: 肿瘤较小, 即直径为2.0-5.0 cm, 病理为低至中度危险性, 形态规则, 圆形或椭圆形, 均匀的等低回声(图2A); 肿瘤的直径大于5 cm以上时, 病理为高危险性, 形态不规则, 部分呈分叶状, 内部呈现不均匀的混杂回声, 可呈囊实性, 内有液性无回声区(图2B). 应用彩色多普勒超声检查, 肿瘤内部及边缘见少量点条状血流信号(图3), 可取到低速动静脉血流频谱. 彩色血流分布与肿瘤危险性高低未见明显相关.
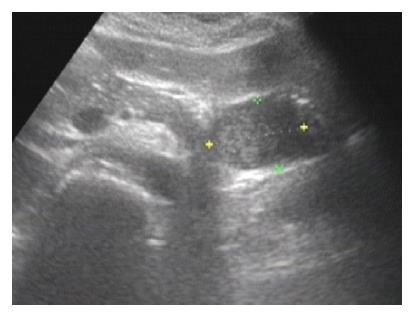
2.2.3 肿瘤来源: 25例胃部GIST, 超声提示21例(84%), 4例超声误判断为胰尾部肿瘤1例(图4), 左肝肿瘤2例, 腹腔淋巴结1例. 5例十二指肠GIST, 超声提示2例(40%), 余3例超声提示十二指肠占位. 9例空、回肠病例中, 5例(55.55%)超声诊断为小肠GIST, 4例提示腹、盆腔占位; 3例结肠病例, 1例提示GIST, 1例提示结肠占位未定性, 1例提示腹膜后占位. 1例腹腔间质瘤为腹腔多发肿物, 为小肠GIST复发, 超声正确提示.
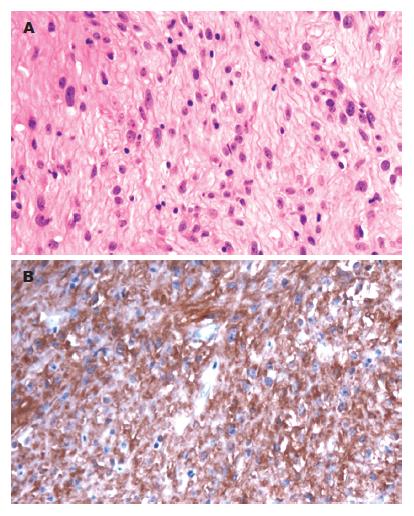
GIST被定义为组织学上由梭形、上皮样、偶或多形性细胞排列成束状或弥漫状图像, 免疫表型上表达c-kit基因蛋白产物KIT(CD117), 由突变的c-kit或血小板源性生长因子受体(platelet-derived growth factor, PDGFR) α基因驱动的间叶源性肿瘤, 可以发生在从食管到直肠整个消化系, 在胃部最多见[1-2]. GIST生物学行为不稳定, 从良性到恶性往往缺乏明确的分界, 因此目前较一致的病理分级是根据肿瘤的大小和核分裂象分为: 极低度危险性, 低度危险性, 中度危险性, 高度危险性[3-4].
随着超声诊断仪的不断改进, 超声技术的提高, 超声除了在腹部实质性脏器的诊断中有其不可替代的作用外, 在胃肠道疾病诊断中也起到越来越重要的作用. 本组45例中除2例食管下段GIST是在食管癌手术中发现, 超声无法观察外, 其中43例确诊病例超声均有阳性发现. 通过对超声测量的肿瘤最大径线数值与病理有完整的的标本大小记录的30例进行统计检验发现, 两种方法差异无统计学意义. 证明超声测量GIST的大小是可信的, 即通过超声测量的肿瘤大小来推断其危险性同样是可信的. 已知肿瘤大小与其危险性高低高度相关, 肿瘤的大小不同, 其在超声图像中的形态及内部回声亦有不同: 偏良性肿瘤, 形态规则, 内部回声均匀; 偏恶性肿瘤, 其形态不规则, 内部显示混杂回声及液性无回声. 这些特征与一般的良恶性肿瘤的超声鉴别特点也相一致[5]. 但在彩色多普勒超声中, 彩色血流分布与肿瘤危险性高低未见明显相关, 这与既往相关报道一致[6].
本组结果显示, 超声对胃部GIST定位准确度为84%, 明显高于十二指肠及小肠病例, 主要因为胃的解剖位置相对固定, 通过饮水可使胃腔充盈, 清晰的显示胃壁的各层结构及肿块与胃壁的关系, 肿瘤发生于黏膜下、肌层或浆膜下, 可向腔内、腔外或腔内外生长[7]. 在胃部误诊为来源肝左叶肿瘤的病例肿瘤较大, 为胃小弯侧浆膜层外生性肿物, 饮水后检查仍然无法与肝左叶分界. 4例超声提示为腹盆腔占位的小肠GIST中, 2例也因为肿瘤巨大, 与周围脏器关系不明而无法判定其来源. 1例结肠占位的诊断中, 在结肠走形区域见肿物回声, 周围肠管轻度扩张, 超声诊断为结肠癌可能性大, 实为黏膜下GIST向腔内生长引起轻度肠梗阻. 1例因患者体胖, 腹部胀气明显, 反复加压及变换体位后, 肿瘤位置显示不佳, 误诊为腹膜后占位. 目前, 胃肠道疾病的重要检查手段是胃镜, 肠镜及消化系造影. 由于GIST长于胃肠道间质, 其生长方式有腔内生长, 腔内/外生长, 腔外生长. 胃镜肠镜多局限于消化系壁内形态及黏膜的显示[8], 而超声对于胃肠道外生性肿瘤有很高的显示率[9-10], 但对于胃肠道向腔内生长的病例, 尤其是在肠道, 较大病例, 超声定性困难, 这也是超声的局限性.
2例典型病例. 病例1: 50岁男性患者间断性便血6 mo, 胃镜、肠镜检查都未发现有明显异常, 便血时断时续, 一度中止检查, 最后行超声检查发现右中下腹部5.2 cm×3.4 cm×3.0 cm低回声肿物, 略呈分叶状, 提示肠管外生性肿物, 考虑小肠GIST, 进一步行腹部CT也证实. 最后手术病理诊断为中度危险性回肠GIST. 消化系出血是GIST的症状之一, 胃肠道内为碱性环境, 当出血量不大时, 出血有时可自行停止, 便血间断出现, 影响了进一步的检查和治疗. 病例2: 35岁男性, 无任何不适, 在超声体检时发现, 左中下腹部见圆形低回声肿物, 大小2.5 cm×2.2 cm×2.0 cm, 内部未见明显血流信号, 与肠管活动性一致, 未见肠管扩张, 超声提示小肠外生性肿瘤, 考虑GIST, 后经手术病理证实为低度危险性空肠GIST. GIST早期无任何症状, 据统计约12%是由于其他原因就诊时偶然检查发现的[11].
总之, 超声在GIST诊断中有其优势, 但肿瘤较大时往往不能全面性观察其相对解剖位置, 同时超声检查结果易受肠道气体和腹部脂肪干扰, 也与操作者经验和手法直接相关. 因此, 超声诊断GIST还应积极联合应用其他检查方法, 以提高诊断正确率.
GIST是近年研究的热点, 在病理及治疗上取得了很大进步. 但由于其临床症状缺乏特异性, 早期诊断是GIST临床工作中的难点.
周国雄, 主任医师, 南通大学附属医院消化内科
本文总结了GIST的超声表现, 有助于超声医师认识此病, 使更多的GIST能得到早期诊断与早期治疗.
本文提示, 彩色超声结合其他检查科提高GIST诊断准确性, 对于超声应用于GIST的诊断有良好的推动作用.
本文探讨了彩色超声在GIST诊断中的应用价值, 为GIST的临床诊断提供借鉴及指导, 具有一定的临床应用价值.
编辑: 李军亮 电编: 何基才
| 2. | Tornillo L, Terracciano LM. An update on molecular genetics of gastrointestinal stromal tumours. J Clin Pathol. 2006;59:557-563. [PubMed] [DOI] |
| 3. | Rutkowski P, Symonides M, Zdzienicki M, Siedlecki JA. Developments in targeted therapy of advanced gastrointestinal stromal tumors. Recent Pat Anticancer Drug Discov. 2008;3:88-99. [PubMed] [DOI] |
| 4. | Nakajima T, Miwa S, Ando T, Fujinami H, Kajiura S, Hosokawa A, Takano Y, Sugiyama T. Interstitial cells of Cajal do not harbor c-kit or PDGFRA gene mutations in patients with sporadic gastrointestinal stromal tumors. J Gastroenterol. 2009;44:426-431. [PubMed] [DOI] |
| 7. | 顾 国利, 王 石林, 任 力, 魏 学明, 李 德昌, 周 晓武, 黄 蓉蓉. 胃肠道间质瘤的临床病理分析和免疫组化特点. 世界华人消化杂志. 2006;14:2241-2246. [DOI] |
| 8. | Tateishi U, Hasegawa T, Satake M, Moriyama N. Gastrointestinal stromal tumor. Correlation of computed tomography findings with tumor grade and mortality. J Comput Assist Tomogr. 2003;27:792-798. [PubMed] [DOI] |
| 9. | Burkill GJ, Badran M, Al-Muderis O, Meirion Thomas J, Judson IR, Fisher C, Moskovic EC. Malignant gastrointestinal stromal tumor: distribution, imaging features, and pattern of metastatic spread. Radiology. 2003;226:527-532. [PubMed] [DOI] |
| 10. | Dietrich C, Hartung E, Ignee A. The use of contrast-enhanced ultrasound in patients with GIST metastases that are negative in CT and PET. Ultraschall Med. 2008;29 Suppl 5:276-277. [PubMed] [DOI] |
| 11. | Miettinen M, Sobin LH, Lasota J. Gastrointestinal stromal tumors of the stomach: a clinicopathologic, immunohistochemical, and molecular genetic study of 1765 cases with long-term follow-up. Am J Surg Pathol. 2005;29:52-68. [PubMed] [DOI] |