修回日期: 2009-11-17
接受日期: 2009-11-23
在线出版日期: 2009-12-08
目的: 评价乌司他丁预防内镜逆行胰胆管造影(ERCP)术后胰腺炎的有效性.
方法: 通过使用由Cochrane协作网推荐的方法, 对在世界范围内搜索出的4篇关于乌司他丁在预防ERCP术后胰腺炎(PEP)的随机对照试验进行Meta分析.
结果: 分别对2篇乌司他丁和安慰剂比较的随机对照试验共446例, 以及2篇乌司他丁与加贝酯比较的随机对照试验共207例患者进行了分析, 这些试验均存在统计同质性. 在乌司他丁与安慰剂、加贝酯对照的试验以及小剂量乌司他丁和加贝酯对照的试验中, 乌司他丁组PEP的OR值分别为: 0.35(95%CI: 0.14-0.88)、1.57(95%CI: 0.39-6.24)及1.69(95%CI: 0.39- 7.32).
结论: 据目前的最佳证据, 乌司他丁可以防止PEP, 他与加贝酯有相近的疗效.
引文著录: 郭强, 胡伟明. 乌司他丁预防内镜逆行胰胆管造影术后胰腺炎的系统评价. 世界华人消化杂志 2009; 17(34): 3561-3567
Revised: November 17, 2009
Accepted: November 23, 2009
Published online: December 8, 2009
AIM: To evaluate the efficacy of ulinastatin in the prophylaxis of post-endoscopic retrograde cholangiopancreatography (ERCP) pancreatitis.
METHODS: A method recommended by the Cochrane Collaboration was used to perform a meta-analysis of randomized controlled trials (RCTs) of ulinastatin in the prevention of post-ERCP pancreatitis (PEP). A total of four RCTs were included.
RESULTS: Two RCTs that focus on the comparison of ulinastatin and placebo for 446 patients undergoing ERCP and two RCTs that focus on the comparison of ulinastatin and gabexate for 207 patients were included. Analysis of these RCTs revealed the presence of statistical homogeneity among them. In ulinastatin versus placebo trials, the odds ratio associated with treatment with ulinastatin for PEP was 0.35 (95%CI: 0.14-0.88). In ulinastatin versus gabexate trials, the odds ratio associated with treatment with ulinastatin for PEP was 1.57 (95%CI: 0.39-6.24). A comparison of low-dose ulinastatin and gabexate was also performed, and the odds ratio associated with treatment with ulinastatin for PEP was 1.69 (95%CI: 0.39-7.32).
CONCLUSION: Current best evidence demonstrates that ulinastatin can prevent post-ERCP pancreatitis, and ulinastatin has very similar efficacy to gabexate in the prevention of post-ERCP pancreatitis.
- Citation: Guo Q, Hu WM. Prophylactic use of ulinastatin against post-endoscopic retrograde cholangiopancreatography pancreatitis: a systematic review. Shijie Huaren Xiaohua Zazhi 2009; 17(34): 3561-3567
- URL: https://www.wjgnet.com/1009-3079/full/v17/i34/3561.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i34.3561
自1974年首次应用于临床, 内镜逆行胰胆管造影术(endoscopic retrograde cholangio-pancreatography, ERCP)已发展成一种诊断和治疗多种胆道和胰腺疾病的重要手段. 随着ERCP在临床上的广泛引应用, 其并发症越来越受到临床医生的关注, 其中最常见的是胰腺炎[1], 在已报道的大样本的前瞻性研究中, 其发生率为1.4%-7.2%[1-4]. 因此如何有效地预防ERCP术后胰腺炎(post-ERCP pancreatitis, PEP)已成为研究的热点, 然而目前大量的随机对照试验并未统一地证实何种方法或药物能有效地预防PEP. 在很多系统评价中, 糖皮质激素, 别嘌醇, 奥曲肽等已被证实对预防PEP无效[5-7]. 生长抑素及加贝酯的有效性在各试验中有出入[8-9]. 因此能有效地应用于PEP预防, 不良反应少且经济的药物是目前需要证实的.
乌司他丁是从人尿中提取的一种蛋白酶抑制剂, 在动物实验模型中已证实能通过抑制胰酶活性治疗胰腺炎. 乌司他丁在日本和中国被广泛应用于胰腺炎的治疗, 且较早的被用于PEP的预防[10-11], 然而其是否有效仍有争议, 目前仍无系统评价对其有效性进行评估. 因此我们希望通过Meta分析的方法来提供乌司他丁对于PEP预防效果的有效信息.
以"ERCP-related pancreatitis"、"post-ERCP pancreatitis"、"post-endoscopic retrograde cholangiopancreatography pancreatitis"、"Endoscopic retrograde cholangiopancreatography"、"pancreatitis"、"ercp"、"ulinastatin"为检索词, 检索MEDLINE(1950/2009-09), EMBase(1966-2009), PubMed(1966-2009), The Cochrane Library(2009年第2期); 并以检索词"乌司他丁、胰腺炎、内镜逆行胰胆管造影、ERCP等"检索CBMdisc (1978/2009-09), CNKI(1979/2009-09)数据库, 初检出的文献51篇, 其中英文49篇, 中文2篇.
1.2.1 材料纳入与排除标准: (1)研究设计: 纳入随机对照试验(RCT), 语种为英文和中文; (2)研究对象: 患者年龄>18岁且接受ERCP检查或治疗; (3)干预措施: 试验组予乌司他丁治疗, 对照组予安慰剂或加贝酯治疗; (4)结局指标: 主要结局指标: 高淀粉酶血症发生率, 急性胰腺炎发生率. 次要结局指标: 重症急性胰腺炎发生率, PEP死亡率.
1.2.2 文献筛选与质量评价: 文献筛选由两名评价员独立操作, 首先阅读文章题目, 在排除明显不符合纳入标准的试验后, 如内容相关再阅读文章摘要, 若为随机对照试验, 则阅读全文, 以确定是否真正符合纳入标准, 然后进行交叉核对, 如意见不统一则通过讨论或第三者裁定解决分歧. 纳入研究的方法学质量采用Cochrane Reviewer's Handbook质量评价标准进行. 两位研究者根据以上的评价标准对每1篇符合纳入标准的文献进行方法学的质量评价.
1.2.3 资料提取: 按照预先设计好的资料提取表, 由两名评价者独立提取和录入资料, 如有分歧则通过讨论或由第三者判定解决. 提取的主要资料内容包括: 文章题目、作者、研究对象、研究方法、干预措施、结局测量与评价、是否采用分配隐藏、有无退出、结局推导等.
统计学处理 采用Cochrane协作网提供的RevMan 4.2软件进行Meta分析. 因纳入文献的结果测量指标均为计数资料, 故采用优势比(OR)及其95%CI. 各研究间的异质性检验采用χ2检验, P>0.10, 可认为多个同类研究具有同质性, 采用固定效应模型分析结果; P<0.10, 则认为多个研究结果有异质性, 则寻找异质性原因, 并采用亚组分析和敏感性分析进行处理; 若未找到异质性原因, 则采用随机效应模型进行Meta分析, 反之, 采用固定效应模型分析. 如研究间异质性太大, 无法进行Meta分析时, 则进行描述性分析.
阅读文章题目和摘要后, 因题目或摘要明显不符合要求和非随机对照试验而排除文章36篇, 其中英文35篇, 中文1篇. 排除相同的文章或同一研究不同阶段文章, 保留5篇, 其中英文4篇, 中文1篇. 在阅读全文后, 按照纳入标准, 排除不符合纳入标准的文章1篇. 最终纳入4个RCT, 其中3篇英文, 1篇中文.
在纳入的4个RCT中, 有2个对照组为安慰剂, 另2个对照组为加贝酯. 安慰剂为对照组的RCT中共有446例患者参与试验(Tsujino et al[12]研究406例; 宋爱琳 et al[13]研究40例), Tsujino et al共有4个研究中心, 均在日本. 宋爱琳 et al为单中心研究, 在中国. 加贝酯为对照组的RCT中共有207例患者参与试验(Fujishiro et al[14]研究139例; Ueki et al[15]研究68例), Fujishiro et al共有3个研究中心, 均在日本, Ueki et al为单中心研究, 在日本. 详细结果见表1和表2.
| 项目分类 | Tsujino et al[12] | 宋爱琳 et al[13] |
| 研究类型 | RCT | RCT |
| 随机方法 | 信封随机分配 | 随机, 但未提及方法 |
| 研究对象 | 患者年龄大于18岁且接受ERCP检查 | 患者年龄大于18岁且接受ERCP检查 |
| 干预措施 | 乌司他丁组(15×104 U溶于100 mL | 乌司他丁组(20×104 U溶于250 mL |
| 生理盐水中, 于ERCP术前10 min | 生理盐水中, 于ERCP术前1 h | |
| 开始静滴) vs 安慰剂组(100 mL生理盐水) | 开始静滴) vs 安慰剂组(250 mL生理盐水) | |
| 观察指标 | 胰腺炎和高淀粉酶血症的发生率为主要 | 胰腺炎和高淀粉酶血症的发生率为 |
| 观察指标. 重症急性胰腺炎发生率, ERCP | 观察指标 | |
| 术后胰腺炎死亡率等为次要观察指标 | ||
| 分配隐藏 | 是 | 不清楚 |
| 盲法 | 双盲 | 不清楚 |
| 随访 | 描述充分 | 不清楚 |
| 退出 | 描述充分 | 不清楚 |
| 意向性分析 | 描述充分 | 描述充分 |
| 基线比较 | 男女性别比113/91 vs 131/71, 平均 | 男女性别比9/11 vs 8/12, 平均年龄 |
| 年龄65岁 vs 65岁, 体质量指数 | 48岁 vs 47岁; 疾病分布无明显差异 | |
| 22 vs 22, 疾病分布无明显差异 | ||
| 质量评级 | A级 | B级 |
| 项目分类 | Fujishiro et al[14] | Ueki et al[15] |
| 研究类型 | RCT | RCT |
| 随机方法 | 电脑随机分配 | 电脑随机分配 |
| 研究对象 | 患者年龄大于18岁且接受ERCP检查 | 接受ERCP检查的患者 |
| 干预措施 | 大剂量乌司他丁组(45×104 U溶于 | 乌司他丁组(15×104 U溶于2500 |
| 300 mL盐水中, 每100 mL分别于 | mL糖盐水中, 于术前60-90 min开 | |
| 术前1 h, 术中, 术后11 h快速静滴, | 始静滴, 持续至术后22 h) vs 加贝 | |
| 其他时间1500 mL液体持续静滴) | 酯组(600 mg溶于2500 mL糖盐 | |
| vs 小剂量乌司他丁组(15×104 U | 水中, 于术前60-90 min开始静滴, | |
| 溶于300 mL盐水中, 每100 mL分 | 持续至术后22 h) | |
| 别于术前1 h, 术中, 术后11 h快速滴入, | ||
| 其他时间1500 mL液体持续静滴) vs | ||
| 加贝酯组(900 mg溶于1500 mL液体中, | ||
| 持续静滴) | ||
| 观察指标 | 胰腺炎和高淀粉酶血症的发生率为 | 胰腺炎和高淀粉酶血症的发生率为 |
| 主要观察指标. 重症急性胰腺炎 | 主要观察指标, 腹痛, 重症急性胰腺炎 | |
| 发生率, ERCP术后胰腺炎死亡率等 | 发生率, 高脂肪酶血症等为次要观察指标. | |
| 为次要观察指标 | ||
| 分配隐藏 | 是 | 是 |
| 盲法 | 不清楚 | 不清楚 |
| 随访 | 描述充分 | 描述充分 |
| 退出 | 描述充分 | 描述充分 |
| 意向性分析 | 描述充分 | 描述充分 |
| 基线比较 | 男女性别比27/19 vs 22/24 vs 26/21, | 男女性别比25/9 vs 22/12, 平均年龄66 vs |
| 平均年龄63.9±14.8 vs 65.3±13.3 | 61岁, 体质量指数23 vs 22, 疾病分布 | |
| vs 65.4±12.1岁, 疾病分布无明显差异 | 无明显差异 | |
| 质量评级 | B级 | B级 |
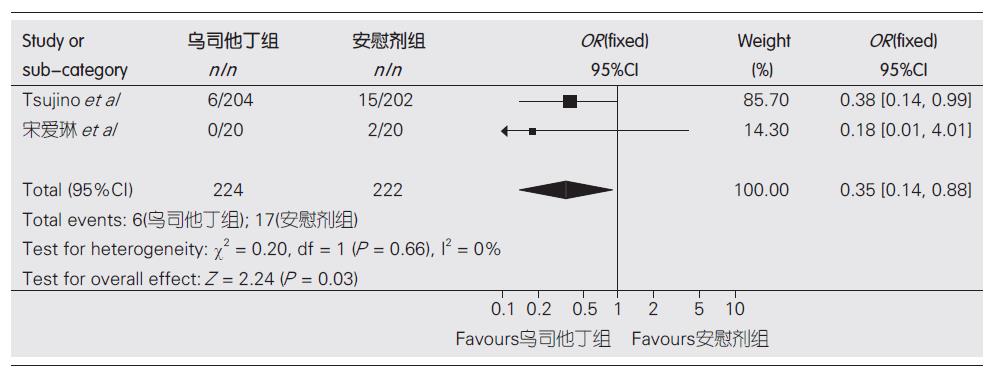
2.3.1 乌司他丁对比安慰剂的胰腺炎发生率: 2个RCT, 共包括446例患者, 均比较了胰腺炎发生率, 且将此指标作为最主要的观察指标. 异质性检验显示2个研究不存在显著的异质性(P = 0.66, I2 = 0%), 故采用固定效应模型进行Meta分析. 结果表明乌司他丁对于PEP的预防有效(OR = 0.35, 95%CI: 0.14-0.88, 图1).
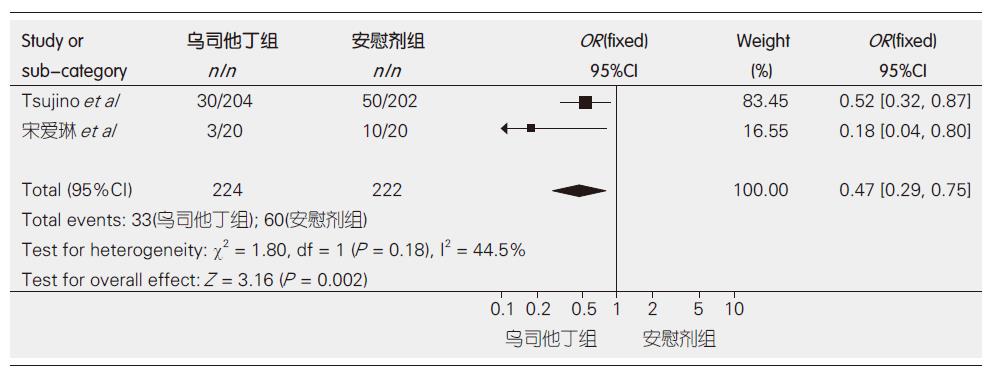
2.3.2 乌司他丁对比安慰剂的高淀粉酶血症发生率: 2个RCT均比较了高淀粉酶血症发生率, 异质性检验显示2个研究不存在显著的异质性(P = 0.18, I2 = 44.5%), 故采用固定效应模型进行Meta分析. 结果表明乌司他丁对于减少ERCP术后高淀粉酶血症的发生有效(OR = 0.47, 95%CI: 0.29-0.75, 图2).
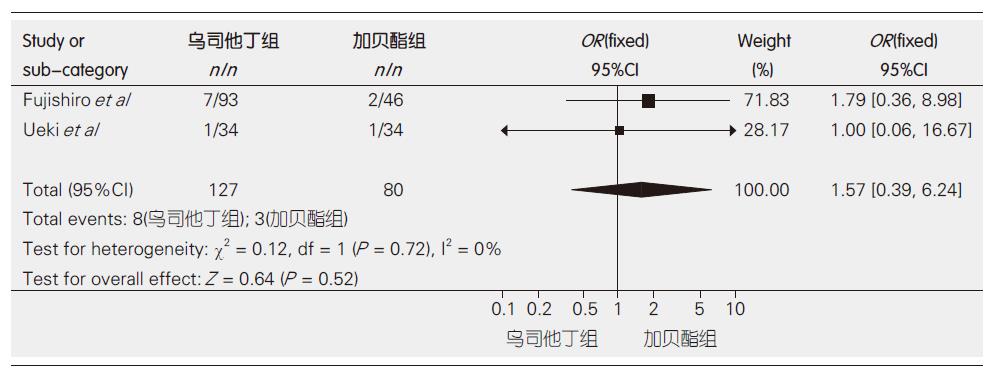
2.3.3 乌司他丁对比加贝酯的胰腺炎发生率: 2个RCT, 共包括207例患者, 均比较了胰腺炎发生率, 且将此指标作为最主要的观察指标. 异质性检验显示2个研究不存在显著的异质性(P = 0.72, I2 = 0%), 故采用固定效应模型进行Meta分析. 结果表明乌司他丁对比加贝酯对于PEP的预防效果无明显差异(OR = 1.57, 95%CI: 0.39-6.24, 图3).
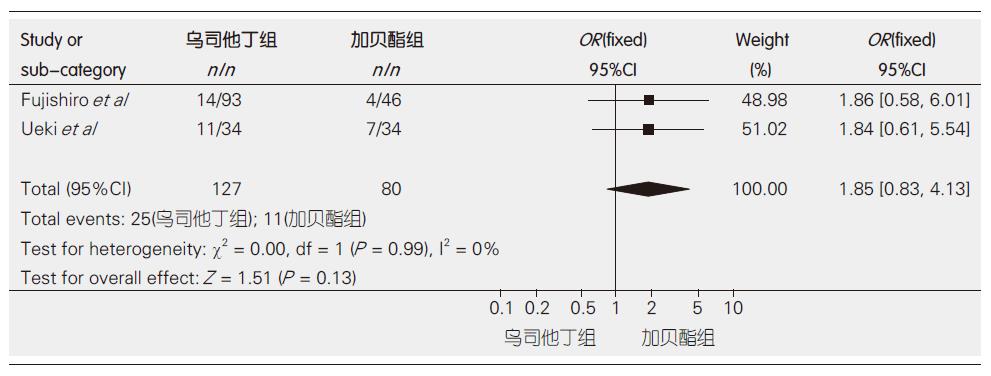
2.3.4 乌司他丁对比加贝酯的高淀粉酶血症发生率: 2个RCT均比较了高淀粉酶血症发生率. 异质性检验显示2个研究不存在显著的异质性(P = 0.99, I2 = 0%), 故采用固定效应模型进行Meta分析. 结果表明乌司他丁对比加贝酯对于减少ERCP术后高淀粉酶血症的发生无明显差异(OR = 1.85, 95%CI: 0.83-4.13, 图4).
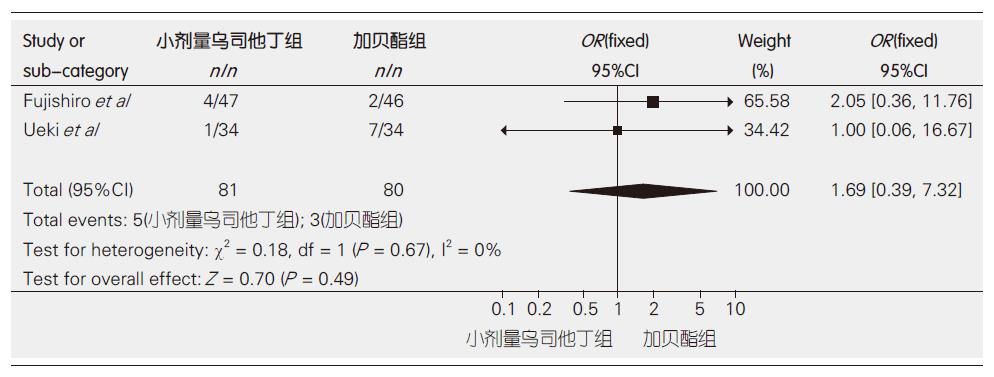
2.3.5 低剂量乌司他丁对比加贝酯的胰腺炎发生率: 2个RCT, 共包括161例患者. 异质性检验显示2个研究不存在显著的异质性(P = 0.67, I2 = 0%), 故采用固定效应模型进行Meta分析. 结果表明低剂量乌司他丁对比加贝酯对于PEP的预防效果无明显差异(OR = 1.69, 95%CI: 0.39-7.32, 图5).
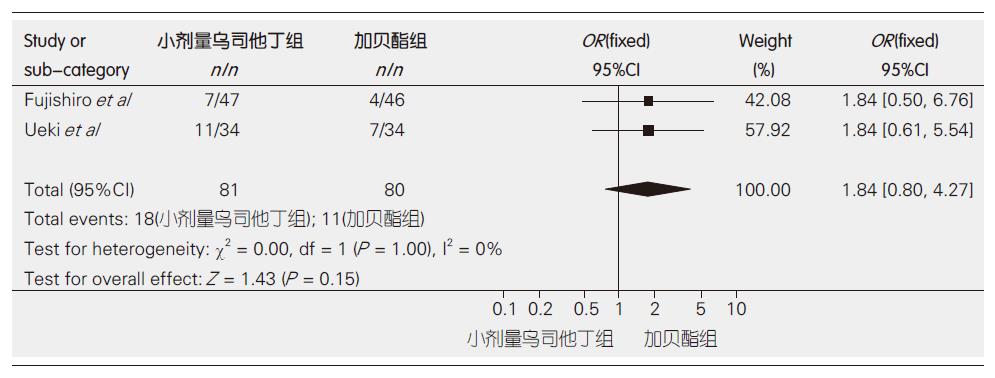
2.3.6 低剂量乌司他丁对比加贝酯的高淀粉酶血症发生率: 2个RCT异质性检验显示2个研究不存在显著的异质性(P = 1.00, I2 = 0%), 故采用固定效应模型进行Meta分析. 结果表明低剂量乌司他丁对比加贝酯对于减少ERCP术后高淀粉酶血症的发生无明显差异(OR = 1.84, 95%CI: 0.80-4.27, 图6).
2.3.7 重症急性胰腺炎发生率、PEP死亡率: 4篇RCT重症急性胰腺炎发生率, PEP死亡率均为0.
改用随机效应模型对数据进行分析, 均未见Meta分析结果逆转. 说明本研究结论具有一定的可靠性.
由于本研究收录的仅仅是发表的文献, 可能存在发表偏倚. 因此, 我们引用了失效安全数对合并相对危险度有显著性差异的指标进行检验. 乌司他丁对比安慰剂的胰腺炎发生率的失安全系数为17; 乌司他丁对比加贝酯的胰腺炎发生率的失安全系数为13, 高于纳入的文献数, 因此本研究的结论具有一定的可靠性.
本系统评价纳入的研究质量较齐. 所有研究按明确的纳入和排除标准, 均为随机、对照研究方法. 对失访者均有描述, 但有些未提及具体的随机方法, 分组隐藏未有描述. 有些文章未提及评价者是否应用盲法. 通过计算失安全系数进行偏倚分析, 本研究的结论具有一定可靠性.
目前, 胰腺炎仍然是ERCP术后最常见也是最有可能致命的并发症. PEP的病理基础仍不清楚, 但有研究表明低龄, 女性, 既往有胰腺炎病史, 接受EST治疗患者是PEP发病的高危人群[2]. 胰酶的激活, 氧自由基活化引起的毛细血管损伤及全身炎症反应综合征, 被认为在胰腺炎的病理过程中起到重要作用. 这也是胰酶活性抑制剂, 胰酶分泌抑制剂, 氧自由基抑制剂, 抗炎因子等用于胰腺炎治疗的药物的药理基础. 在一些已发表的RCT试验中, 胰酶活性抑制剂加贝酯和乌司他丁被证明对于预防PEP有一定效果, 胰酶分泌抑制剂生长抑素也有效, 但其昂贵的费用限制了其在临床上的应用. 另一种胰酶分泌抑制剂奥曲肽在1项系统评价中被证实没有效果. 其他如别嘌醇, 糖皮质激素等在一系列系统评价中也被证实没有效果.
在本研究中, 我们收集了4篇发表在国内及国际期刊上的RCT试验. 并分别对乌司他丁与安慰剂, 乌司他丁与加贝酯, 低剂量乌司他丁与加贝酯就胰腺炎、高淀粉酶血症的发生率进行对比. 试图通过Meta分析的方法来评价乌司他丁的疗效及乌司他丁对比加贝酯的疗效. 由于纳入的2篇对比乌司他丁与加贝酯的RCT还进行了小剂量乌司他丁与加贝酯的对比, 我们还对比评价了小剂量乌司他丁的疗效. 结果表明: 乌司他丁对于PEP的预防, 减少高淀粉酶的发生有效(OR = 0.35, 95%CI: 0.14-0.88; OR = 0.47, 95%CI: 0.29-0.75). 乌司他丁对比加贝酯对于减少PEP及高淀粉酶血症的发生无明显差异(OR = 1.57, 95%CI: 0.39-6.24; OR = 1.85, 95%CI: 0.83-4.13). 小剂量乌司他丁对比加贝酯对于减少PEP及高淀粉酶血症的发生无明显差异(OR = 1.69, 95%CI: 0.39-7.32; OR = 1.84, 95%CI: 0.80-4.27).
乌司他丁与加贝酯相比, 后者还具有松弛Oddi括约肌的功能[16], 其对Oddi括约肌的保护是其优于乌司他丁的一个方面. 然而乌司他丁具有抑酶作用强大、费用较低以及半衰期较长等特点[17]. 在安全性方面, 以往进行的加贝酯试验的1220例患者中, 没有1例发生由于加贝酯引起的严重不良反应[18-20]. 而在Tsujino et al的研究涉及的204例患者中, 没有1例发生由于乌司他丁引起的严重不良反应. 此外, 在Fujishiro et al与Ueki et al的RCT中, 还评估了IL-6等炎症因子的浓度, 结果显示IL-6、IL-8、血清中性粒细胞弹性蛋白酶及C-反应蛋白在乌司他丁组和加贝酯组中无明显差异.
由于乌司他丁使用范围的局限性和医学伦理的限制, 并没有很多的大样本量随机对照试验来进行评估, 且目前的试验质量参差不齐, 可能对本研究的结论有一定的影响. 目前需要多中心, 大样本量, 高质量的随机对照试验来证实乌司他丁预防PEP的有效性. 此外, 由于大部分PEP都属于轻型胰腺炎, 且随着PEP高危因素的研究, 越来越多的人认为常规使用药物预防没有太大必要, 因此专门针对高危人群的随机对照试验需要开展.
目前的研究表明, 乌司他丁对于PEP的预防有效, 且效果与加贝酯无明显差异.
随着ERCP在临床上的广泛引应用, 其并发症越来越受到临床医生的关注, 其中最常见的是胰腺炎. 如何有效地预防PEP已成为研究的热点, 然而目前大量的随机对照试验并未统一地证实何种方法或药物能有效地预防PEP的发生.
季国忠, 教授, 南京医科大学第二附属医院消化科
乌司他丁, 糖皮质激素, 别嘌醇, 奥曲肽, 生长抑素及加贝酯等都被用于预防PEP. 但后三者在一系列系统评价后已被证实对PEP无效, 而乌司他丁是否有效仍有争议, 目前仍无系统评价对其有效性进行评估.
本文通过对在世界范围内搜索出的4篇关于乌司他丁在预防PEP的随机对照试验进行Meta分析. 分别对乌司他丁与安慰剂, 乌司他丁与加贝酯, 低剂量乌司他丁与加贝酯就胰腺炎、高淀粉酶血症的发生率进行了对比. 通过Meta分析的方法评价了乌司他丁的疗效及乌司他丁对比加贝酯的疗效, 为乌司他丁应用于PEP的临床治疗提供了一定参考.
本文提示, 乌司他丁对于PEP的预防有效, 且效果与加贝酯无明显差异. 为乌司他丁对PEP的预防效果提供了有效信息.
本研究对国内外有关应用乌司他丁预防PEP的临床研究结果进行Meta分析, 系统评价了乌司他丁预防PEP的有效性, 为临床应用乌司他丁预防PEP提供了有价值的信息和相应的理论依据.
编辑: 李瑞敏 电编: 何基才
| 1. | Masci E, Toti G, Mariani A, Curioni S, Lomazzi A, Dinelli M, Minoli G, Crosta C, Comin U, Fertitta A. Complications of diagnostic and therapeutic ERCP: a prospective multicenter study. Am J Gastroenterol. 2001;96:417-423. [PubMed] [DOI] |
| 2. | Tsujino T, Isayama H, Komatsu Y, Ito Y, Tada M, Minagawa N, Nakata R, Kawabe T, Omata M. Risk factors for pancreatitis in patients with common bile duct stones managed by endoscopic papillary balloon dilation. Am J Gastroenterol. 2005;100:38-42. [PubMed] [DOI] |
| 3. | Loperfido S, Angelini G, Benedetti G, Chilovi F, Costan F, De Berardinis F, De Bernardin M, Ederle A, Fina P, Fratton A. Major early complications from diagnostic and therapeutic ERCP: a prospective multicenter study. Gastrointest Endosc. 1998;48:1-10. [PubMed] [DOI] |
| 4. | Cheng CL, Sherman S, Watkins JL, Barnett J, Freeman M, Geenen J, Ryan M, Parker H, Frakes JT, Fogel EL. Risk factors for post-ERCP pancreatitis: a prospective multicenter study. Am J Gastroenterol. 2006;101:139-147. [PubMed] [DOI] |
| 5. | Zheng M, Chen Y, Bai J, Xin Y, Pan X, Zhao L. Meta-analysis of prophylactic allopurinol use in post-endoscopic retrograde cholangiopancreatography pancreatitis. Pancreas. 2008;37:247-253. [PubMed] [DOI] |
| 6. | Bai Y, Gao J, Zou DW, Li ZS. Prophylactic octreotide administration does not prevent post-endoscopic retrograde cholangiopancreatography pancreatitis: a meta-analysis of randomized controlled trials. Pancreas. 2008;37:241-246. [PubMed] [DOI] |
| 7. | Bai Y, Gao J, Shi X, Zou D, Li Z. Prophylactic corticosteroids do not prevent post-ERCP pancreatitis: a meta-analysis of randomized controlled trials. Pancreatology. 2008;8:504-509. [PubMed] [DOI] |
| 8. | Arvanitidis D, Anagnostopoulos GK, Giannopoulos D, Pantes A, Agaritsi R, Margantinis G, Tsiakos S, Sakorafas G, Kostopoulos P. Can somatostatin prevent post-ERCP pancreatitis? Results of a randomized controlled trial. J Gastroenterol Hepatol. 2004;19:278-282. [PubMed] [DOI] |
| 9. | Andriulli A, Solmi L, Loperfido S, Leo P, Festa V, Belmonte A, Spirito F, Silla M, Forte G, Terruzzi V. Prophylaxis of ERCP-related pancreatitis: a randomized, controlled trial of somatostatin and gabexate mesylate. Clin Gastroenterol Hepatol. 2004;2:713-718. [PubMed] [DOI] |
| 10. | Jönsson-Berling BM, Ohlsson K. Distribution and elimination of intravenously injected urinary trypsin inhibitor. Scand J Clin Lab Invest. 1991;51:549-557. [PubMed] [DOI] |
| 11. | Ohnishi H, Kosuzume H, Ashida Y, Kato K, Honjo I. Effects of urinary trypsin inhibitor on pancreatic enzymes and experimental acute pancreatitis. Dig Dis Sci. 1984;29:26-32. [PubMed] [DOI] |
| 12. | Tsujino T, Komatsu Y, Isayama H, Hirano K, Sasahira N, Yamamoto N, Toda N, Ito Y, Nakai Y, Tada M. Ulinastatin for pancreatitis after endoscopic retrograde cholangiopancreatography: a randomized, controlled trial. Clin Gastroenterol Hepatol. 2005;3:376-383. [PubMed] [DOI] |
| 13. | 宋 爱琳, 尹 兰宁, 寇 治民. 乌司他丁对内镜逆行胰胆管造影术后高淀粉酶血症及急性胰腺炎的预防作用. 兰州大学学报(医学版). 2005;31:24-25, 40. |
| 14. | Fujishiro H, Adachi K, Imaoka T, Hashimoto T, Kohge N, Moriyama N, Suetsugu H, Kawashima K, Komazawa Y, Ishimura N. Ulinastatin shows preventive effect on post-endoscopic retrograde cholangiopancreatography pancreatitis in a multicenter prospective randomized study. J Gastroenterol Hepatol. 2006;21:1065-1069. [PubMed] [DOI] |
| 15. | Ueki T, Otani K, Kawamoto K, Shimizu A, Fujimura N, Sakaguchi S, Matsui T. Comparison between ulinastatin and gabexate mesylate for the prevention of post-endoscopic retrograde cholangiopancreatography pancreatitis: a prospective, randomized trial. J Gastroenterol. 2007;42:161-167. [PubMed] [DOI] |
| 16. | Kong J, Wu SD, Zhang XB, Li ZS, Shi G, Wang W, Chen JZ. Choledochoscope manometry about different drugs on the Sphincter of Oddi. World J Gastroenterol. 2008;14:5907-5912. [PubMed] [DOI] |
| 17. | Sugiura Y, Nakajima K, Kawase H, Tsubota K, Fujibayashi T, Goto Y. Evaluation of a large dose intravenous administration of urinastatin. Jpn J Acute Med. 1988;12:1153-1156. |
| 18. | Cavallini G, Tittobello A, Frulloni L, Masci E, Mariana A, Di Francesco V. Gabexate for the prevention of pancreatic damage related to endoscopic retrograde cholangiopancreatography. Gabexate in digestive endoscopy--Italian Group. N Engl J Med. 1996;335:919-923. [PubMed] [DOI] |
| 19. | Andriulli A, Clemente R, Solmi L, Terruzzi V, Suriani R, Sigillito A, Leandro G, Leo P, De Maio G, Perri F. Gabexate or somatostatin administration before ERCP in patients at high risk for post-ERCP pancreatitis: a multicenter, placebo-controlled, randomized clinical trial. Gastrointest Endosc. 2002;56:488-495. [PubMed] [DOI] |
| 20. | Masci E, Cavallini G, Mariani A, Frulloni L, Testoni PA, Curioni S, Tittobello A, Uomo G, Costamagna G, Zambelli S. Comparison of two dosing regimens of gabexate in the prophylaxis of post-ERCP pancreatitis. Am J Gastroenterol. 2003;98:2182-2186. [PubMed] [DOI] |