修回日期: 2009-06-18
接受日期: 2009-06-23
在线出版日期: 2009-07-18
目的: 探讨肝切除术后早期应用生长抑素对门静脉血流动力学的影响及可能机制.
方法: 将32只健康家兔随机分为: A组(正常对照组)、B组(生理盐水治疗组)和C组(生长抑素治疗组). 对A组建立门静脉置管动物模型; B组和C组均建立50%肝切除及门静脉置管动物模型, 并于术中及术后早期分别滴注生理盐水和生长抑素. 定期(0.5、1、2 h)检测上述3组动物模型门静脉压力差值, 用超声多普勒检测动物模型门静脉血流方向、血管内径、截面积、平均血流速率及血流量, 同时检测动物模型肝功能变化.
结果: 动物模型在肝切除术后门静脉压力升高, 与A组相比, B组门静脉压力升高幅度明显高于C组(0.5 h: 436.001±169.654 Pa vs 258.012±167.497 Pa, P<0.05; 1 h: 394.324±163.182 Pa vs 224.767±164.653 Pa, P<0.05; 2 h: 193.092±154.356 Pa vs 351.861±183.579 Pa, P<0.05). 术中及术后早期检测A、B、C 3组动物门静脉血管内径和截面积无明显差异, 但C组门静脉平均血流速率及血流量显著低于A组和B组(均P<0.001). 肝切除术后2 h, B组与C组间ALT、AST差异无显著意义.
结论: 肝部分切除术后, 早期应用生长抑素可降低门静脉压力的升高幅度, 这种作用可能与生长抑素降低了门静脉血流速率和血流量相关.
引文著录: 叶华, 何波, 王捷. 肝切除术后早期应用生长抑素对门静脉血流动力学的影响. 世界华人消化杂志 2009; 17(20): 2026-2030
Revised: June 18, 2009
Accepted: June 23, 2009
Published online: July 18, 2009
AIM: To investigate the effects of somatostatin on portal vein hemodynamics in the early stage after hepatectomy and explore the mechanism under such effects.
METHODS: Thirty-two rabbits were randomly divided into three groups: group A (n = 6, control group), group B (n = 13, normal saline treatment group) and group C (n = 13, somatostatin treatment group). Rabbits in all three groups underwent portal vein catheterization, while only those in Groups B and C underwent 50% partial hepatectomy. An intraoperative and postoperative intravenous infusion of normal saline and somatostatin was given. Before and after the treatment (0.5, 1, 2 h), the pressure, flow direction, diameter, hemokinetic velocity, average flow rate and blood flow of the portal vein were detected and compared.
RESULTS: After hepatectomy, the portal pressure increased. The increase in the portal pressure in group B was significantly higher than that in group C (0.5 h: 436.001 ± 169.654 Pa vs 258.012 ± 167.497 Pa, P < 0.05; 1 h: 394.324 ± 163.182 Pa vs 224.767 ± 164.653 Pa, P < 0.05; 2 h: 193.092 ± 154.356 Pa vs 351.861 ± 183.579 Pa, P < 0.05). There were no significant differences in portal diameter and hemokinetic velocity among all the three groups before and after treatment (P > 0.05). However, the average flow rate and blood flow of the portal vein in group C were significant lower than those in groups A and B (both P < 0.05). Two hours after hepatectomy, no significant differences in the expression of ALT and AST were noted between groups A and B.
CONCLUSION: Application of somatostatin in the early stage of hepatectomy may reduce elevated portal pressure, which may be associated with somatostatin-induced decrease in flow rate and blood flow of the portal vein.
- Citation: Ye H, He B, Wang J. Effects of somatostatin on portal vein hemodynamics in the early stage after hepatectomy. Shijie Huaren Xiaohua Zazhi 2009; 17(20): 2026-2030
- URL: https://www.wjgnet.com/1009-3079/full/v17/i20/2026.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i20.2026
目前, 生长抑素(somatostatin, SST)及其类似物已被广泛应用于肝硬化门脉高压食管胃底静脉曲张破裂出血的治疗, 而肝切除术后早期应用SST及其类似物对门静脉血流动力学影响的报道较少. 本研究探讨了兔肝脏大部分切除术后, 早期应用SST类似物思他宁对门静脉血流动力学的影响及其相关机制. 旨在为临床肝切除术后应用SST及其类似物降低门静脉压力(portal vein pressure, PVP), 从而减少手术并发症的发生提供实验依据.
健康家兔32只, 由中山大学医学院实验动物中心提供, 雌雄不限, 月龄10 mo左右, 体质量2.4-3.0 kg, 在无特殊病原菌条件下(SPF)分笼饲养; SST类似物思他宁由瑞士雪兰诺公司提供, 每支3000 µg; 超声多普勒(型号Esaote Technos Dll6)由ESAOTE公司生产.
1.2.1 分组及处理: 健康家兔32只随机分为3组. A组: 正常对照组6只, 氯胺酮肌肉注射麻醉, 消毒后上腹肋缘下切口进腹, 经肠系膜上静脉终末分支插管, 导入门静脉主干, 备测PVP; B组: 生理盐水治疗组13只, 按照A组方法常规麻醉开腹后, 建立门静脉置管+50%肝切除术动物模型. 从阻断肝十二指肠韧带肝缺血开始, 至切肝后2 h内, 经耳缘静脉持续滴入生理盐水100 mL(50 mL/h). C组: SST治疗组13只, 采用与B组相同的方法建立门静脉置管+50%肝切除术动物模型. 从阻断肝十二指肠韧带肝缺血开始, 至切肝后2 h内, 经耳缘静脉持续滴入生理盐水100 mL+思他宁(滴速50 mL/h, 思他宁剂量为84 µg/kg). 上述3组动物在实验指标检测完毕后缝合切口.
1.2.2 PVP测定: A组剖腹后建立门静脉置管模型, 测量0、0.5、1、2 h的PVP; B组、C组剖腹后建立门静脉置管+肝切除术动物模型, 分别测量阻断肝门前、切肝后0.5、1、2 h的PVP.
1.2.3 超声多普勒检测: A组剖腹后建立门静脉置管模型, 测量0、0.5、1、2 h的门静脉平均血流速率、血管内径、截面积、门静脉血流量和血流方向; B组、C组剖腹后建立门静脉置管+肝切除术动物模型, 分别测量阻断肝门前、切肝后0.5、1、2 h的门静脉平均血流速率、血管内径、截面积、门静脉血流量和血流方向.
1.2.4 肝功能检测: B组、C组剖腹后建立门静脉置管+肝切除术动物模型, 分别于阻断肝门前, 切肝后2 h采血检测谷丙转氨酶(ALT)、谷草转氨酶(AST), 了解其动态变化.
统计学处理 所有实验数据以mean±SD表示, 不同组间实验数据差异比较采用t检验和重复测量方差分析, 统计软件采用SPSS11.0 for Windows, P<0.05表示差异有显著性意义.
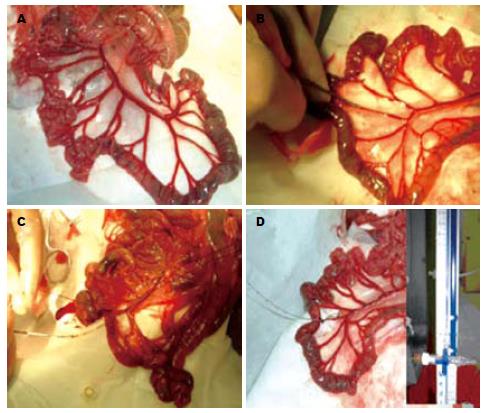
A组与B、C组PVP差值分别比较差异均有显著意义(P<0.05), 表明肝切除术后其PVP明显升高. B组与C组比较, 两者差异有显著意义(P<0.05), 表明SST(思他宁)可明显降低肝切除术后升高的PVP. 同时, C组内不同时间点之间即肝切除术后0.5、1、2 h与术前的PVP差值, 差异无显著意义(F = 2.482, P = 0.102), 表明SST(思他宁)的降压作用是持续而稳定的(图1, 表1).
A、B、C组动物肝切除术前及术后0.5、1、2 h均观察到向肝血流, 未见离肝血流.
各组术后0.5、1、2 h的门静脉血管内径及门静脉截面积数值与术前比较, 三组间均无显著性差异(P>0.05). 各组术后0.5、1、2 h的门静脉平均血流速率数值与术前比较, A组与B组见无差异(P = 0.895), A组及B组与C组均有显著统计学差异(均P<0.001), 显示使用SST后门静脉平均血流速率明显降低. 各组术后0.5、1、2 h的门静脉血流量数值与术前比较的差值, A组与B组和C组间无统计学差异, B组与C组有统计学差异(P = 0.035), 表明SST治疗组较生理盐水治疗组其门静脉血流量明显降低(表2).
| A组(n = 6) | B组(n = 13) | C组(n = 13) | |
| 门静脉血管内径(mm) | |||
| 0.5 h | -0.900±1.594 | 0.623±0.803 | 0.077±0.894 |
| 1 h | 0.100±0.415 | 0.369±1.259 | 0.069±0.988 |
| 2 h | 0.067±0.476 | 0.139±1.161 | -0.339±0.737 |
| 门静脉截面积(mm2) | |||
| 0.5 h | 0.170±1.626 | 2.953±4.995 | 0.781±2.573 |
| 1 h | 0.449±1.841 | 2.946±6.006 | 0.520±2.739 |
| 2 h | 0.653±1.577 | 1.424±4.395 | -1.183±1.069 |
| 门静脉平均血流速率(m/s) | |||
| 0.5 h | -0.013±0.025 | -0.003±0.026 | -0.090±0.037 |
| 1 h | -0.015±0.031 | -0.014±0.030 | -0.112±0.032 |
| 2 h | -0.000±0.020 | -0.006±0.031 | -0.112±0.047 |
| 门静脉血流量(mL/min) | |||
| 0.5 h | -4.823±2.363 | -4.000±22.931 | -18.692±29.310 |
| 1 h | -4.833±3.764 | -7.769±30.362 | -33.308±54.879 |
| 2 h | -5.167±1.941 | -13.308±29.293 | -47.385±26.544 |
B组肝切除术后2 h与术前ALT、AST的差值分别为710.15±403.81 U/L、301.46±239.16 U/L; C组肝切除术后2 h与术前ALT、AST的差值分别为513.77±373.44 U/L、171.85±199.04 U/L. 两组差异无显著意义(P = 0.210, P = 0.147). 表明SST(思他宁)并不引起AST或ALT的升高(表3).
目前, 肝切除术仍是治疗肝脏良恶性肿瘤最常用和最有效的治疗方法. 近年来, 随着外科技术和围手术期处理经验的不断提高和完善, 肝切除术后肝功能衰竭的发生率明显减少, 而术中或术后出血、胆瘘、难治性腹水、肝功能不全等并发症的发生率呈相对升高的趋势. 相关资料显示[1-2], 上述并发症的发生与术后PVP升高的幅度呈正相关. 尽管SST降低门静脉压力的作用已得到广泛认可, 然而直到目前其血液动力学效应仍未完全揭示[3-6], 这在一定程度上限制了SST在临床治疗中的优化用药. 在此, 本研究证明了肝切除术后早期应用SST可以降低PVP升高的幅度, 并在此基础上对SST降低肝切除术后PVP的血流动力学机制进行了初步探讨.
PVP的检测方法有多种, 但由于干扰间接测压法的因素较多, 如检测部位、门静脉直径大小等, 影响数据的准确性和可比性, 而且结果的判断带有一定主观性. 本研究采用术中经肠系膜上静脉的分支插管, 导入门静脉主干, 直接测量PVP. 并间歇输入小剂量肝素以起抗凝作用, 确保导管顺畅, 减少操作因素而产生的误差. 因此这一检测方法更能直接地、动态地反映肝切除术后PVP的变化. 我们的研究发现: 肝切除术后PVP明显升高, 并且是持续、稳定地增高(术后0.2、1、2 h PVP的变化无显著差异). 其机制可能为[7-8]: (1)由于门静脉血流最终汇入肝静脉出肝, 肝切除术后肝静脉的数量减少, 疏导门静脉血流的能力减弱, 造成门静脉淤血、PVP明显升高. (2)阻断肝门和部分肝切除均可引起肝实质的损害, 残留肝脏发生脂肪浸润和组织水肿, 间接导致PVP升高.
我们使用彩色多普勒超声检测了肝切除术前后门静脉直径、血管截面积、平均血流速率、血流量和血流方向变化以及SST对其的影响. 本研究显示, SST治疗组和生理盐水治疗组的门静脉血流方向均为向肝性血流, 未见离肝血流. 使用SST后门静脉直径、血管截面积, 与生理盐水治疗组相比差异无显著意义, 即SST不能够直接收缩门静脉. 而门静脉平均血流速率、血流量锐减, 与生理盐水治疗组相比差异有显著意义. 我们推断SST降低PVP的作用可能是通过降低门静脉血流速率, 从而使门静脉血流量减少. 但SST降低门静脉血流量的详细机制尚不完全清楚, 我们也仅作了初步的探讨, SST对肝切除术后全肝血液动力学的影响及其作用机制还有待进一步研究.
由于麻醉、手术创伤、阻断肝门引起的肝缺血和再灌注损伤, 肝切除术后都会出现肝功能异常, 如谷草转氨酶、谷丙转氨酶、总胆红素的升高. 肝切除术后PVP的升高, 实际上是机体代偿功能的一种表现, 有利于术后肝功能的恢复和肝细胞的再生[9-12]. 思他宁的作用是降低PVP和减少内脏血流量, 用药后是否会加重肝功能损害, 这是需要慎重考虑的问题. 而之前关于大鼠动物实验的结果提示, 肝切除术后早期使用SST可使残肝肝质量增加减慢, 肝细胞的再生受到抑制[13-15]. 因此, 在肝切除术后早期应用SST减少肝断面渗血、胆瘘、术后出血等并发症时, 是否应注意其抑制肝再生的不良反应, 防止诱发肝功能衰竭. 我们初步观察了SST对肝切除术后肝功能的影响, 结果显示, 肝切除术后2 h谷草转氨酶、谷丙转氨酶均显著升高, 但SST治疗组和生理盐水治疗组两组之间升高的程度无明显差异, 表明SST并非如预想般加重肝功能损害.
生长抑素(SST)及其类似物已被广泛应用于肝硬化门脉高压食管胃底静脉曲张破裂出血的治疗, 而肝切除术后早期应用SST及其类似物对门静脉血流动力学影响的报道较少, 本研究探讨兔肝脏大部分切除术后, 早期应用SST类似物思他宁对门静脉血流动力学的影响及其相关机制.
李胜, 研究员, 山东省肿瘤防治研究院肝胆外科
尽管生长抑素降低门静脉压力的作用已得到广泛认可, 然而目前其血液动力学效应仍未完全揭示.
本研究证明肝切除术后早期应用生长抑素可以降低门静脉压力升高的幅度, 并在此基础上对生长抑素降低肝切除术后门静脉压力的血流动力学机制进行了初步探讨.
肝切除术后门静脉压力的升高, 是机体代偿功能的一种表现, 有利于术后肝功能的恢复和肝细胞的再生. 而在肝切除术后早期使用生长抑素可使残肝肝重增加减慢, 肝细胞的再生受到抑制.
本研究选题新颖, 方法有一定特色, 有一定的学术价值.
编辑: 李军亮 电编:何基才
| 4. | Sakamoto M, Ueno T, Nakamura T, Sakata R, Hasimoto O, Torimura T, Sata M. Improvement of portal hypertension and hepatic blood flow in cirrhotic rats by oestrogen. Eur J Clin Invest. 2005;35:220-225. [PubMed] [DOI] |
| 5. | Trebicka J, Hennenberg M, Laleman W, Shelest N, Biecker E, Schepke M, Nevens F, Sauerbruch T, Heller J. Atorvastatin lowers portal pressure in cirrhotic rats by inhibition of RhoA/Rho-kinase and activation of endothelial nitric oxide synthase. Hepatology. 2007;46:242-253. [PubMed] [DOI] |
| 6. | Yang YP, Ma XM, Wang CP, Han J, Lu YY, Xiang Y, Su SH, Feng YY. Effect of increased hepatic platelet activating factor and its receptor portal hypertension in CCl4-induced liver cirrhosis. World J Gastroenterol. 2006;12:709-715. [PubMed] |
| 7. | Patella S, Phillips DJ, Tchongue J, de Kretser DM, Sievert W. Follistatin attenuates early liver fibrosis: effects on hepatic stellate cell activation and hepatocyte apoptosis. Am J Physiol Gastrointest Liver Physiol. 2006;290:G137-G144. [PubMed] [DOI] |
| 8. | Vanheule E, Geerts AM, Reynaert H, Van Vlierberghe H, Geerts A, De Vos M, Colle I. Influence of somatostatin and octreotide on liver microcirculation in an experimental mouse model of cirrhosis studied by intravital fluorescence microscopy. Liver Int. 2008;28:107-116. [PubMed] |
| 9. | Jung Y, Oh SH, Zheng D, Shupe TD, Witek RP, Petersen BE. A potential role of somatostatin and its receptor SSTR4 in the migration of hepatic oval cells. Lab Invest. 2006;86:477-489. [PubMed] [DOI] |
| 10. | Deli A, Kreidl E, Santifaller S, Trotter B, Seir K, Berger W, Schulte-Hermann R, Rodgarkia-Dara C, Grusch M. Activins and activin antagonists in hepatocellular carcinoma. World J Gastroenterol. 2008;14:1699-1709. [PubMed] [DOI] |
| 11. | Xu H, Shi BM, Lu XF, Liang F, Jin X, Wu TH, Xu J. Vascular endothelial growth factor attenuates hepatic sinusoidal capillarization in thioacetamide-induced cirrhotic rats. World J Gastroenterol. 2008;14:2349-2357. [PubMed] [DOI] |
| 12. | Laviña B, Gracia-Sancho J, Rodríguez-Vilarrupla A, Chu Y, Heistad DD, Bosch J, García-Pagán JC. Superoxide dismutase gene transfer reduces portal pressure in CCl4 cirrhotic rats with portal hypertension. Gut. 2009;58:118-125. [PubMed] [DOI] |
| 13. | Reynaert H, Vaeyens F, Qin H, Hellemans K, Chatterjee N, Winand D, Quartier E, Schuit F, Urbain D, Kumar U. Somatostatin suppresses endothelin-1-induced rat hepatic stellate cell contraction via somatostatin receptor subtype 1. Gastroenterology. 2001;121:915-930. [PubMed] [DOI] |
| 14. | Song SH, Leng XS, Li T, Qin ZZ, Peng JR, Zhao L, Wei YH, Yu X. Expression of subtypes of somatostatin receptors in hepatic stellate cells. World J Gastroenterol. 2004;10:1663-1665. [PubMed] |
| 15. | Vorobioff JD, Ferretti SE, Zangroniz P, Gamen M, Picabea E, Bessone FO, Reggiardo V, Diez AR, Tanno M, Cuesta C. Octreotide enhances portal pressure reduction induced by propranolol in cirrhosis: a randomized, controlled trial. Am J Gastroenterol. 2007;102:2206-2213. [PubMed] [DOI] |