修回日期: 2009-05-24
接受日期: 2009-05-25
在线出版日期: 2009-06-28
目的: 探讨应用超声造影技术评价高强度聚焦超声(HIFU)治疗原发性肝细胞癌(HCC)的有效性.
方法: HIFU治疗HCC患者32例, 分别采取部分覆盖肿瘤治疗23例及完全覆盖肿瘤治疗9例, 于治疗前和治疗后1-4 d行超声造影检查, 通过对比观察HIFU治疗前后肿瘤内血流灌注变化来判断肿瘤是否凝固性坏死.
结果: HIFU治疗前超声造影显示肿瘤内血流灌注丰富; HIFU治疗后, 超声造影显示治疗区无血流灌注, 提示治疗区域发生凝固性坏死. 以最终诊断为金标准, 超声造影对肿瘤灭活诊断的准确性高于常规彩超(90.6% vs 46.9%, P<0.05).
结论: 超声造影能准确判断HIFU对肿瘤消融范围及程度, 为HCC患者HIFU治疗后的早期疗效评价提供依据.
引文著录: 林玲, 桂永忠, 梁郑, 陈健, 卢强, 闽敏. 超声造影对高强度聚焦超声治疗肝细胞癌的疗效评价. 世界华人消化杂志 2009; 17(18): 1879-1882
Revised: May 24, 2009
Accepted: May 25, 2009
Published online: June 28, 2009
AIM: To evaluate the role of contrast-enhanced ultrasonography in assessing the short-term therapeutic response of hepatocellular carcinoma with high intensity focused ultrasound (HIFU).
METHODS: Thirty two patients with hepatocellular carcinoma (HCC) received HIFU treatments including 23 part-covered treatments and 9 full-covered treatments. Contrast-enhanced ultrasound (CEUS) imaging was performed to monitor the response of tumor vessels to HIFU ablation before the treatment and 1-4 d after the treatment separately. Simultaneously, all patients underwent routine US for comparison.
RESULTS: Compared with tumor images in the patients before HIFU which showed multiple blood flow signals, clinical images showed an abrupt interruption, followed by the cessation of blood flow within the tumor vessels after HIFU treatment, demonstrating that homogeneous coagulative necrosis occurred in the treatment area. According to the final diagnosis as gold standard, the accuracy of CEUS for HIFU was much better than the conventional ultrasonography (90.6% vs 46.9%, P < 0.05).
CONCLUSION: CEUS can accurately differentiate tumor necrosis and evaluate therapeutic efficacy of HIFU.
- Citation: Lin L, Gui YZ, Liang Z, Chen J, Lu Q, Min M. Contrast-enhanced ultrasound in assessment of the therapeutic efficacy of high intensity focused ultrasound in treating hepatocellular carcinoma. Shijie Huaren Xiaohua Zazhi 2009; 17(18): 1879-1882
- URL: https://www.wjgnet.com/1009-3079/full/v17/i18/1879.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i18.1879
肝细胞癌(hepatocellular carcinoma, HCC)是我国发病率极高的恶性肿瘤之一, 手术是其传统的治疗方法, 但对于中晚期肝癌, 往往手术困难[1]. 随着科学技术的进步, 近年来以微创、介入为发展方向的治疗HCC的新方法不断出现, 其中高强度聚焦超声(high intensity focused ultrasound, HIFU)是近几年飞速发展起来的非侵入性局部肿瘤灭活消融新技术, 其原理是通过超声波汇聚于靶区引起组织瞬间升温而发生凝固性坏死[2-3], 对其疗效观察的方法有常规彩超、增强CT和MRI、DSA血管造影等. 常规彩超因血流敏感性低而使用受限, 超声造影(contrast-enhanced ultrasound, CEUS)则大大提高了病灶内微血管检测的敏感度, 在肝脏肿瘤微创治疗疗效评价中的应用受到肯定[4]. 我们利用CEUS对HCC行HIFU治疗后的近期疗效进行观察, 发现其可以准确的评价HIFU治疗效果, 现将结果报道如下.
2007-04/2008-05我院经HIFU治疗的HCC患者32例, 男30例, 女2例, 年龄36-75(平均年龄55)岁. 肿瘤病灶32个, 直径3.5-12.5 cm. 肿瘤TNM分期: Ⅰ期1例, Ⅱ期8例, Ⅲa期17例, Ⅲb期6例. 全部病例均为住院患者, 治疗前诊断均经相关检查及病理证实.
采用Phlilips IU 22超声诊断仪, C5-2宽频凸阵探头, 匹配实时造影成像技术. 造影剂采用意大利Bracco公司生产的SonoVue, 造影微泡为磷脂微囊六氟化硫, 微泡平均直径2.5 μm. 使用方法为经肘静脉快速注入造影剂, 实时观察造影全过程并行图像存储. 肿瘤HIFU治疗前后1-4 d, 分别行常规超声和超声造影检查, 观察病灶数目、大小、回声、彩色多普勒血流(color doppler flow image, CDFI)及超声造影剂灌注情况等, 评价疗效.
HIFU治疗后以治疗覆盖区CEUS各期均无增强作为灭活的依据, 超声造影以局部有动脉期增强、门脉期及延迟期造影剂逐渐消退, 增强表现同治疗前为肿瘤残存; CDFI诊断肿瘤灭活或残存的依据分别为治疗覆盖区无或有多普勒血流信号. 肿瘤灭活或残存的最终诊断依据两种以上影像学(超声、CT、MRI)、肿瘤标志物水平、穿刺活检、临床随访综合判断.
HIFU治疗使用重庆海扶(HIFU)技术有限公司生产的JC型聚焦超声肿瘤治疗系统. 主要治疗参数为: (1)治疗频率0.8 MHz; (2)焦域平均直径1.3 mm; (3)焦距135 mm; (4)焦域声强5328-16285 W/cm2. HIFU治疗将32例HCC患者分成2组, 第1组: 23例, 患者肿瘤较大, TNM分期: Ⅲa期及Ⅲb期, 采取部分覆盖肿瘤进行治疗; 第2组: 9例, 孤立性肿瘤, TNM分期: Ⅰ期及Ⅱ期, 采取完全覆盖肿瘤进行治疗. HIFU治疗时, 通过超声探头实时监控定位, 确定病灶治疗范围, 进行靶区的三维立体扫描治疗, 并根据每个层面治疗前后靶区回声变化、由计算机图像处理系统判断HIFU治疗效果, 以治疗后靶区回声增强为治疗有效, 并从回声变化反馈调节治疗声功率.
统计学处理 采用SPSS11.0统计软件, 计量资料做配对t检验, 计数资料做组间χ2检验, 以P<0.05为差异有显著性意义.
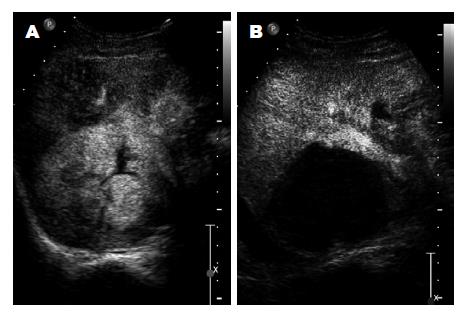
患者肝脏肿瘤超声造影病灶表现为"快进快出"的特点, 即在动脉期肝实质尚未增强时肿瘤病灶已开始增强, 与肝动脉同时增强, 部分患者病灶增强甚至早于肝内动脉; 病灶在动脉期呈高增强; 门脉期及延迟期病灶内造影剂逐渐消退, 消退较周围肝实质快, 病灶表现为低增强(图1A).
HIFU是一种通过热消融对实体肿瘤的局部治疗手段, 利用超声波具穿透性和可聚焦性等物理特征, 将体外低能量超声波聚焦于体内深部肿瘤病灶, 焦点区产生的瞬态高温效应和空化效应致使肿瘤组织发生凝固性坏死, 同时破坏肿瘤滋养血管, 使肿瘤血供障碍产生继发性损伤[5-7]. HIFU治疗成功的关键在于肿瘤是否发生凝固性坏死. 因此, 采用适当的影像学方法及时判断肿瘤的坏死状况至关重要.
近年来, 随着新型超声造影剂及造影成像技术的发展, 超声造影在肝肿瘤诊断和介入治疗疗效评价中应用较多, 表明新一代超声造影剂能够对肿瘤微血管灌注进行实时显像[8], 对肿瘤灭活诊断的敏感性和准确性与增强CT高度一致[9-10]. 但目前对HIFU治疗肝细胞癌的疗效评价报道甚少, 本文旨在探讨超声造影在HIFU治疗原发性肝癌疗效评价中的应用价值.
本研究运用新一代超声造影剂SonoVue对32例HCC患者HIFU治疗疗效进行观察, 并与常规彩超进行比较. 治疗前均通过超声造影检查, 肿瘤血供丰富, 造影剂灌注呈"快进快出", 符合HCC表现. HIFU治疗后, 由于肿瘤组织发生凝固性坏死, 肿瘤血管破坏, 超声造影治疗区域各期均无强化, 提示血供消失, 肿瘤组织已发生凝固性坏死[11]. 对判断肿瘤是否完全灭活提供较为可靠的依据. 本研究中, 与最终诊断相比, 超声造影对肿瘤灭活诊断敏感性为90.5%, 特异性为90.9%, 准确性为90.6%; 常规彩超对肿瘤灭活诊断的敏感性为42.9%, 特异性为54.5%, 准确性为46.9%. 超声造影在肿瘤灭活诊断的准确性明显优于常规彩超, 二者差异有统计学意义(P<0.05). 因此, 超声造影可以作为HIFU治疗后短期影像学随访手段, 而常规彩超由于血流探测敏感性低不能作为随访手段. 我们的这一临床研究结论与同类研究结果相近似[4,12].
本研究中32例患者, 根据治疗方案的不同分为2组, 第1组23例为中晚期患者, 肿瘤病灶较大, 平均直径8.5±2.5 cm, TNM分期: Ⅲa期及Ⅲb期, HIFU治疗为姑息性治疗, 选用部分性覆盖肿瘤进行治疗, 其目的让治疗区域的肿瘤组织凝固性坏死, 达到肿瘤体积缩小, 减缓症状, 为进一步治疗创造机会. HIFU治疗后超声造影提示6例治疗覆盖区有残存. 第2组9例, 为孤立性肿瘤, TNM分期: Ⅰ期及Ⅱ期, 采取完全覆盖肿瘤进行治疗. HIFU治疗后, 超声造影提示5例治疗覆盖区有残存. 针对超声造影增强部位即残存部位, 均再次进行HIFU治疗, 最终使治疗覆盖区完全灭活, 超声造影各期均无增强, 达到了治疗目的. 同时也说明HIFU治疗肝癌病灶局部效果明确, HIFU治疗可造成病灶的凝固性坏死, 其范围和程度取决于病灶为完全或部分性覆盖. HIFU是在体外操作, 可准确、完整地对体内肿瘤进行原位无创切除, 32例肝癌患者HIFU治疗后, 通过临床随访, 患者肝区疼痛缓解、肝癌病灶体积减小、肿瘤标记物下降, 无1例出现重要脏器功能明显异常和严重并发症.
超声造影使得超声诊断水平获得质的飞跃, 为HIFU在肝癌治疗后的疗效评价提供了一种新型有效的方法. 本研究中32例患者共行超声造影43次, 无过敏反应及其他不适发生. 对于CT造影剂过敏者和短期内需多次做造影检查确定疗效者, 超声造影更显其优越性.
目前的研究[13-15]认为, 超声造影可以用于局部治疗后疗效评价及指导穿刺活检及补充治疗, 但仅可作为治疗后短期的疗效评价, 长期疗效评价需进一步研究. 且目前超声造影对0.5 cm以下的肝癌或肝癌卫星灶可能难以显示. 因此, 超声造影对于肝癌HIFU治疗效果的评价仍需进一步的经验积累和长期随访.
高强度聚焦超声(HIFU)是近年才开始应用于临床的微创治疗实体肿瘤的新技术, HIFU治疗原发性肝癌的疗效已被大量临床应用所证实, 但关于治疗后效果的评价的新方法报道尚少. 超声造影(CEUS)是现代超声领域研究的热点之一,他可以敏感地显示肝肿瘤的供血以及微血管灌注情况, 能够为肝脏肿瘤的微创治疗疗效评价提供较为准确的信息.
孙明军, 教授, 中国医科大学附属第一医院内镜中心; 季国忠, 教授, 南京医科大学第二附属医院消化科
超声造影(CEUS)是现代超声领域研究的热点之一,尤其是肝脏肿瘤的研究十分活跃, 但对于微创治疗疗效评估中的应用, 目前的研究仅限于治疗后短期的评估, 长期疗效评价仍有待进一步研究.
超声造影(CEUS)技术的应用为肝脏肿瘤HIFU治疗的疗效评估提供了一种新思路和手段.
本研究主要探讨了超声造影技术在HIFU治疗原发性肝癌的疗效评价中的应用价值, 提出超声造影为一种新型有效的原发性肝癌HIFU 治疗后疗效评估方法, 有一定的新意和临床指导价值.
编辑: 李军亮 电编: 何基才
| 2. | Wu F, Wang ZB, Chen WZ, Zou JZ, Bai J, Zhu H, Li KQ, Jin CB, Xie FL, Su HB. Advanced hepatocellular carcinoma: treatment with high-intensity focused ultrasound ablation combined with transcatheter arterial embolization. Radiology. 2005;235:659-667. [PubMed] [DOI] |
| 3. | Wang XJ, Yuan SL, Lu YR, Zhang J, Liu BT, Zeng WF, He YM, Fu YR. Growth inhibition of high-intensity focused ultrasound on hepatic cancer in vivo. World J Gastroenterol. 2005;11:4317-4320. [PubMed] |
| 6. | Li CX, Xu GL, Jiang ZY, Li JJ, Luo GY, Shan HB, Zhang R, Li Y. Analysis of clinical effect of high-intensity focused ultrasound on liver cancer. World J Gastroenterol. 2004;10:2201-2204. [PubMed] |
| 7. | Wu F, Wang ZB, Chen WZ, Zhu H, Bai J, Zou JZ, Li KQ, Jin CB, Xie FL, Su HB. Extracorporeal high intensity focused ultrasound ablation in the treatment of patients with large hepatocellular carcinoma. Ann Surg Oncol. 2004;11:1061-1069. [PubMed] [DOI] |
| 9. | Maruyama H, Yoshikawa M, Yokosuka O. Current role of ultrasound for the management of hepatocellular carcinoma. World J Gastroenterol. 2008;14:1710-1719. [PubMed] [DOI] |
| 10. | 胡 建群, 叶 新华, 范 伯强, 林 红军, 汪 惠宁, 彭 小静, 苗 毅, 郭 峰, 范 钦和, 俞 同福. 超声造影在肝脏恶性肿瘤射频或微波治疗后近期疗效应用评价. 南京医科大学学报(自然科学版). 2007;27:1290-1293. |
| 14. | Lencioni R, Della Pina C, Crocetti L, Bozzi E, Cioni D. Clinical management of focal liver lesions: the key role of real-time contrast-enhanced US. Eur Radiol. 2007;17 Suppl 6:F73-F79. [PubMed] [DOI] |
| 15. | Maruyama K, Yoshikawa M, Yokosuka O. Contrast-enhanced ultrasonography: a recent application for the diagnosis and treatment of hepatocellular carcinoma. JNMA J Nepal Med Assoc. 2008;47:156-166. [PubMed] |