修回日期: 2009-04-17
接受日期: 2009-04-17
在线出版日期: 2009-05-08
目的: 评价INNO-LiPA HBV DR v2对乙型肝炎病毒(hepatitis B virus, HBV)耐药检测的准确性.
方法: 选取237例慢性HBV感染者经过拉米夫定和(或)阿德福韦酯的抗病毒治疗, 取外周血, 采用INNO-LiPA和聚合酶基因耐药测序分析法测定HBV耐药性.
结果: INNO-LiPA HBV DR v2耐药分析法与聚合酶基因序列分析法测定的耐药检测结果比较, 标本符合率为179/235(76.1%), 氨基酸密码子符合率为1293/1410(91.7%). 与直接测序法有着很高的一致性. 尤其检测混合型耐药灵敏度较直接测序要高.
结论: INNO-LiPA法是一种较灵敏的快速检测HBV耐药型的试验方法.
引文著录: 田敬华, 赵辉, 丛旭, 闫杰, 杜绍财, 魏来. INNO-LiPA HBV DR v2检测乙型肝炎病毒耐药变异的评价. 世界华人消化杂志 2009; 17(13): 1366-1369
Revised: April 17, 2009
Accepted: April 17, 2009
Published online: May 8, 2009
AIM: To assess the accuracy of INNO-LiPA HBV DR v2 for detecting hepatitis B virus (HBV) drug resistance.
METHODS: Sera from 237 chronic hepatitis B patients undergoing lamivudine or adefovir treatment were detected using INNO-LiPA and direct sequencing of the reverse transcriptase region of the HBV Polymerase gene.
RESULTS: Sequencing results were observed for 179/235 samples (76.1%) and 1293/1410 amino acid positions (91.7%). It showed high concordance with directing antiviral drug-resistance mutations, particularly for the sensitive detection of mixed drug-resistance mutations.
CONCLUSION: The INNO-LiPA HBV DR v2 appears to be useful for the rapid antiviral drug-resistance mutations assay of HBV.
- Citation: Tian JH, Zhao H, Cong X, Yan J, Du SC, Wei L. Evaluation of INNO-LiPA in detection of HBV drug resistance mutation. Shijie Huaren Xiaohua Zazhi 2009; 17(13): 1366-1369
- URL: https://www.wjgnet.com/1009-3079/full/v17/i13/1366.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i13.1366
慢性乙型肝炎患者抗病毒治疗过程中发生病毒耐药变异是限制核苷(酸)类似药物治疗的一个主要障碍[1]. 随着治疗时间的延长,拉米夫定(lamivudine, LAM)、阿德福韦酯(adefovir dipivoxil, ADV)等这些抗病毒药物治疗的患者体内可出现变异株, 从而发生病毒学突破, 导致治疗失败[2]. 一些病毒发生的耐药变异已被证实可以引起对几种药物的交叉耐药, 这就限制了对患者的进一步长期有效地治疗[9]. 因此在治疗中早期检测出这些变异, 对选择药物、指导远期治疗非常必要. 基因型耐药的检测对预防和证实发生表型耐药并采取新的治疗措施格外重要[3].
最常见的检测乙型肝炎抗病毒药物耐药变异的方法有直接测序、聚合酶链反应-限制性片段长度多态性分析技术(restriction fragment length polymorphism analysis, PCR-RFLP)和反向杂交线性探针技术(reverse hybridization line probe, LiPA)等. PCR扩增后的直接测序被认为是检测对新药物治疗耐药检测的首选方法. 然而, 只有当变异株超过HBV准种池(quasispecies pool)的20%以上直接测序才能检测到[4]. PCR-RFLP和LiPA方法要更加灵敏, 可以检测到病毒准种池中5%的变异株[5,10]. 但这些方法同样存在缺点. PCR-RFLP只能检测单位点变异, 对仅用于少数耐药变异位点监测不失为一种简便方法, 但随着多种核苷(酸)类似物的相继问世和HBV耐药变异位点的不断出现, 该方法将难以胜任[8]. LiPA检测技术的缺点是对新出现的变异都要设计新的试剂条带, 迫使该技术要定期进行更新. 另外由于核苷酸序列上基因型的不同, 为了检测一个氨基酸置换通常需要许多个探针来检测[10]. 本研究比较直接基因测序法与INNO-LiPA 技术对HBV耐药变异检测的能力.
2006年在我院临床治疗及随访的慢性乙型肝炎患者237例, 其中男146例, 女91例, 年龄23-65岁, 全部符合2000年修订的《病毒性肝炎防治方案》诊断标准[6]. 其中159例患者接受LAM 100 mg/d治疗1年以上, 平均疗程1年半, 并符合临床耐药诊断标准: 血清HBV DNA转阴后又出现HBV DNA反跳至1×108 copy/L以上; 排除LAM治疗过程中患者依从性差而引起的HBV DNA反跳; 排除其他原因引起的丙氨酸转氨酶(ALT)升高. 另78位患者接受LAM和(或)ADV治疗, 治疗过程中发生病毒学突破. INNO-LiPA HBV DR v2试剂盒(比利时Innogenetics公司), 限制性内切酶EcoRⅠ(购自NEB); T4 DNA Ligase、pEASY-T1Cloning vector、E. coli JM109感受态细胞购自北京全式金生物技术有限公司. DNA核酸提取、纯化试剂购自Geneaid公司. Qiagen的HotStar Taq DNA聚合酶.
1.2.1 DNA的提取: 用Geneaid的Viral Nucleic Acid Extraction KitⅡ试剂自100 µL血清提取HBV DNA.
1.2.2 HBV DNA直接测序检测: 提取的HBV DNA进行巢式PCR扩增. 5 µL DNA模板加到PCR反应体系10×缓冲液, 0.4 µL 10 mmol/L dNTP, 引物各10 pmol, 1 U的Taq酶(Invitrogen)共30 µL. 根据HBV聚合酶区序列设计引物. PCR上游引物: SPR1A, 5'-GTTCAGGAACAGTAAGCCC-3'; 下游引物: SPR1B, 5'-GAAAGGCCTTGTAAGTTGGCG-3'[3]; PCR产物长1049 bp. 二轮PCR引物BSA, 5'-AGGACCCCTGCTCGTGTTAC-3'; WS4, 5'-ACATACTTTCCAATCAATAG-3', PCR产物长730 bp(引物由北京三博远志生物技术有限责任公司合成). 扩增条件: 94℃ 30 s, 55℃ 30 s, (第2轮为50℃ 30 s), 72℃ 45 s, 35个循环, 最后72℃延伸7 min. 扩增产物用20 g/L琼脂糖凝胶电泳检测后直接送测序或进行纯化, 克隆.
1.2.3 INNO-LiPA HBV DR v2的测定: 严格按照INNO-LiPA HBV DR v2试剂盒说明书操作. 上游引物 nt 255 to 278(5'-CGTGGTGGACTTCTCTCAATTTTC-3'); 下游引物HBV nt 1121 to 1099(5'-AGAAAGGCCTTGTAAGTTGGCGA-3'); Qiagen HotStar Taq DNA聚合酶(5000 kU/L); Qiagen 10×PCR缓冲液(Tris-HCl, KCl, (NH4)2SO4), 15 mmol/L MgCl2, pH8.7); dNTP(25 mmol/L). 扩增条件: 94℃ 30 s, 55℃ 30 s, 72℃ 40 s, 50个循环, 最后72℃延伸7 min. PCR扩增可得到生物素化的HBV DNA聚合酶区产物. 扩增产物长867 bp. 扩增产物用20 g/L琼脂糖凝胶电泳检测. 可测到的HBV DNA用Auto-LiPA全自动反应仪进行变性、杂交、冲洗、显色. 结果可以在条带上相应的寡核苷酸探针位置显现出颜色.
1.2.4 目的基因的克隆及筛选: PCR扩增产物用20 g/L琼脂糖凝胶电泳检测, 并用UNIQ-10柱式PCR产物回收试剂盒回收DNA片段, 参考试剂盒说明书进行. 经PCR纯化试剂盒纯化后的PCR产物与pEASY-T1 Cloning vector连接并转化E. coli JM109感受态细胞, 蓝白筛选阳性克隆, 重组质粒用EcoRⅠ、Hind Ⅲ双酶切, 后用10 g/L琼脂糖凝胶电泳鉴定. 菌液送测序.
1.2.5 HBV基因序列的测定及分析: PCR产物及克隆菌液送北京三博远志生物技术有限责任公司应用Sanger双脱氧核糖核酸链末端终止法进行测序. 测序结果应用BioEdit 7.0软件进行分析.
1.2.6 INNO-LiPA与测序结果比对: 如果测序与INNO-LiPA结果均为野生株或均为变异株或均为混合株, 可以认为两者检测结果相符. 若一个实验显示变异株而另一实验结果为野生株, 则认为两实验结果不符. 结果不符的标本进行克隆测序予以确认. 每份标本挑取5个克隆.
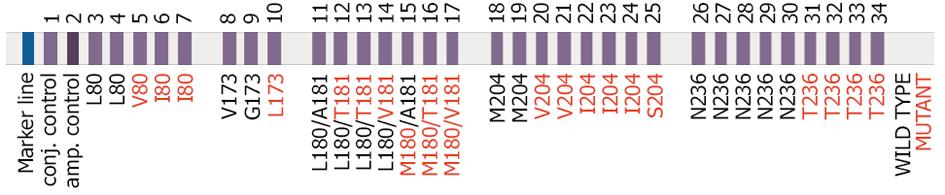
LiPA试剂条上含有34个反应线, 其中2个质控线和32个HBV 探针线, 能够同时检测出: 乙型肝炎病毒聚合酶基因第80位、173位、180位、181位、204位和236密码子的野生型及耐药型突变, 见图1. 结果判读相对简单, 但也存在部分试剂条上部分位置的显色模糊不清楚或显色缺失会给判读带来一些障碍.
本研究共对237份标本同时进行了LiPA与测序的PCR扩增检测. LiPA扩增中有2份标本扩增质控线(amp. control)未出, 提示扩增失败. 结果LiPA与测序结果的标本完全符合率为76.1%(179/235). 共有38个标本(16.2%)LiPA检测为混合株, 而测序仅显示或为变异株或为野生株(表1).
| LiPA | 测序 | ||
| WT(129) | WT+mutant(21) | Mutant(85) | |
| WT(99) | 90 | 2 | 7 |
| WT+mutant(53) | 34 | 15 | 4 |
| Mutant(83) | 5 | 4 | 74 |
在氨基酸密码子的比较中, 密码子完全符合率为91.7%(1293/1410). 考察的6个氨基酸密码子位置中80、173、180、181、236位置两方法符合率分别为95.7%、97.4%、88.9%、94.5%、99.1%, 大部分(5/6)结果符合率都在88%以上, 而204位氨基酸密码子符合率差别较大, 这是由于在rt204位置有V和I两种变异, 可发生的变异模式包括: rtM204V , rtM204I, rtM204V+I. LIPA检测中在rt204位置上有10个标本显示为rtM204V变异, 23个标本显示为rtM204I变异, 相同标本测序显示为野生株; LiPA有27个标本显示为野生株,其中有21个测序为rtM204I变异, 有6个标本为rtM204V变异; 有9个标本显示为rtM204V+I(表2).
| 密码子 | LiPA检测 | 测序检测 | ||
| Mutant | WT | 密码子符合率(%) | ||
| rt80 | Mutant | 36 | 0 | 95.7 |
| WT | 10 | 189 | ||
| rt173 | Mutant | 4 | 6 | 97.4 |
| WT | 0 | 225 | ||
| rt180 | Mutant | 79 | 17 | 88.9 |
| WT | 9 | 130 | ||
| rt181 | Mutant | 1 | 2 | 94.5 |
| WT | 11 | 221 | ||
| rt204 | Mutant | 95 | 33 | 74.5 |
| WT | 27 | 80 | ||
| rt236 | Mutant | 4 | 1 | 99.1 |
| WT | 1 | 229 |
二者比较结果不符标本应用克隆测序验证, 结果34个LiPA测为变异而测序显示为野生株的标本克隆测序所得序列提示有变异.
近年来抗HBV药物中, 核苷类似物的发展很快,已上市的核苷类药物有LAM、ADV、恩替卡韦(entecavir, ETV)及替比夫定(telbivudine, LdT). 但核苷类药物存在各种耐药及交叉耐药, 停药后复发率高[7]. 及早发现体内HBV发生的耐药变异对相应调整用药策略, 联合、序贯治疗或进行个性化治疗都有很好的指导意义, 并可对进一步的治疗进行监测预防. 选择一种好的检测手段来快速、便捷、准确地检测HBV耐药变异非常关键.
PCR产物直接测序一次可准确测序HBV逆转录酶A-E区, 全长549 bp. 可通过一次实验, 检测全部已知和可能的耐药变异位点. 但该方法的灵敏度较差, 只有当变异株所占比例超过HBV准种池20%时才能被检测到[8]. 而且只显示优势菌株的特征, 不能检测出含量较低的变异株. INNO-LiPA方法在国外已获准应用于临床检测[1]. 该法灵敏度高, 可检测出样品中占HBV准种池5%-10%的变异株, 还具有提供信息量大、自动化程度高等优点[8].
本研究通过对比, 验证了LiPA与测序比较有很好地符合率(91.7%), 尤其对混合型耐药有很好的检出. 这对监测患者体内HBV准种池中各型毒株, 及早更换用药方案, 预防耐药意义很大.
实验中应用克隆测序来验证LiPA与测序, 限于克隆数目, 不能完全反映HBV准种的真实情况, 给验证带来困难. 在后续工作中要增加克隆数量做到尽可能反映HBV病毒池各类型准种的真实比例, 另应留取序列标本结合临床指标来跟踪随访验证结果. 实验应用Auto-LiPA全自动反应仪对标本进行全自动地变性、杂交、冲洗、显色, 大大提高了操作的标准化程度. 后期结果目测判读, 个别氨基酸密码子位置条带显现模糊, 可能会存在人为判断误差. 若应用扫描仪器进行结果自动判读, 相信会使INNO-LiPA的操作更加完善.
INNO-LiPA的缺点是: (1)LiPA只能检测目前现存已知的变异. 对新的抗病毒治疗药物发生的新奇变异就需要设计出新的探针, 因此这项技术需要时常地更新. (2)探针区域的多态性可能会使结果表现为不确定. (3)因缺乏对应的探针, 该技术不能提示标本出现新的变异[10].
总之, 与测序方法相比较, INNO-LiPA由于其技术上的简便快速准确, 加上使用Auto-LiPA全自动反应仪的操作标准化, 使他更适合于大通量的科研或临床耐药检测.
持续慢性乙型肝炎是引起终末期肝病和肝细胞癌的一个主要原因. 核苷(酸)类似物已经被证实可以有效控制疾病并可以防止肝细胞癌发生. 然而发生抗病毒耐药是限制核苷(酸)类似物长期应用的一个主要因素. 在治疗中早期检测到这些耐药变异, 对选择药物、指导远期治疗非常必要. 比较, 选择一种好的检测手段来快速、便捷、准确地检测出HBV耐药变异非常关键.
范小玲, 教授, 北京地坛医院综合科; 党双锁, 教授, 西安交通大学医学院第二附属医院感染科.
INNO-LiPA方法在国外已获准应用于临床检测HBV耐药变异, 于国内目前仅限于科研使用, 且从未有实验数据报道.
Degertekin et al最新报道INNO-LiPA 试剂最新版本INNO-LiPA HBV DR v3可检测包括LAM、ADV、ETV与LdT所有常见耐药位点. 涵盖了HBV聚合酶基因逆转录酶区共11个密码子位置(80、173、180、181、184、194、202、204、233、236、250).
本研究以中国北方人群乙型肝炎患者为研究对象, 应用INNO-LiPA技术与传统的直接测序法进行了比对. 对INNO-LiPA技术有了本土的评价.
INNO-LiPA法是一种较灵敏的快速检测HBV耐药型的试验方法.
本文的科学性、实用性和可读性较强, 能较好地反映目前我国检测乙肝病毒检测的水平, 具有较高的临床应用价值.
编辑: 李军亮 电编:吴鹏朕
| 1. | Degertekin B, Hussain M, Tan J, Oberhelman K, Lok AS. Sensitivity and accuracy of an updated line probe assay (HBV DR v.3) in detecting mutations associated with hepatitis B antiviral resistance. J Hepatol. 2009;50:42-48. [PubMed] [DOI] |
| 2. | Ghany M, Liang TJ. Drug targets and molecular mechanisms of drug resistance in chronic hepatitis B. Gastroenterology. 2007;132:1574-1585. [PubMed] [DOI] |
| 3. | Osiowy C, Villeneuve JP, Heathcote EJ, Giles E, Borlang J. Detection of rtN236T and rtA181V/T mutations associated with resistance to adefovir dipivoxil in samples from patients with chronic hepatitis B virus infection by the INNO-LiPA HBV DR line probe assay (version 2). J Clin Microbiol. 2006;44:1994-1997. [PubMed] [DOI] |
| 4. | Lok AS, Zoulim F, Locarnini S, Bartholomeusz A, Ghany MG, Pawlotsky JM, Liaw YF, Mizokami M, Kuiken C. Antiviral drug-resistant HBV: standardization of nomenclature and assays and recommendations for management. Hepatology. 2007;46:254-265. [PubMed] [DOI] |
| 5. | Allen MI, Gauthier J, DesLauriers M, Bourne EJ, Carrick KM, Baldanti F, Ross LL, Lutz MW, Condreay LD. Two sensitive PCR-based methods for detection of hepatitis B virus variants associated with reduced susceptibility to lamivudine. J Clin Microbiol. 1999;37:3338-3347. [PubMed] |
| 7. | Tillmann HL. Antiviral therapy and resistance with hepatitis B virus infection. World J Gastroenterol. 2007;13:125-140. [PubMed] |
| 9. | Lok AS. Navigating the maze of hepatitis B treatments. Gastroenterology. 2007;132:1586-1594. [PubMed] [DOI] |
| 10. | Hussain M, Fung S, Libbrecht E, Sablon E, Cursaro C, Andreone P, Lok AS. Sensitive line probe assay that simultaneously detects mutations conveying resistance to lamivudine and adefovir. J Clin Microbiol. 2006;44:1094-1097. [PubMed] [DOI] |