修回日期: 2008-02-15
接受日期: 2008-02-25
在线出版日期: 2008-03-18
电阻抗断层成像(EIT)是继形态、结构成像之后, 于近20余年发展, 出现的新一代医学成像技术, 具有功能成像, 无损伤和医学图像监护三大突出优势. 其在胃肠领域的最多应用是评价通过胃部的食物流动以替代临床仍然视为胃排空测量金标准的核素法. 在离体的模型实验中EIT可精确测量玻璃棒/气囊的容积变化. 在体实验条件下, EIT能精确测量胃容积(气囊)的变化. EIT胃排空测量与染料稀释法、胃存留法、核素法等有较好的相关性. EIT胃动力测量以置于体表的电极阵列实现无损检测, 以实时图像方式直接显示体内胃体的收缩和运动状况, 将是胃动力检测与评价手段的重大进步, 显示了诱人的应用前景.
引文著录: 任超世, 王妍, 赵舒. 电阻抗断层成像与胃排空和胃动力检测. 世界华人消化杂志 2008; 16(8): 799-805
Revised: February 15, 2008
Accepted: February 25, 2008
Published online: March 18, 2008
Electrical impedance tomography (EIT) is a novel medical imaging technology, which comes forth in recent 20 years following morphology imaging and structure imaging. EIT has the outstanding advantages of noninvasive, functional imaging and medical image monitoring. It has been mostly used in gastroenterology to assess flow of ingesta through the gastric region as an alternative to radionuclide studies. In vitro, EIT can accurately measure the volume of glass rods/balloons in a phantom. In humans, EIT can accurately measure gastric volume (balloons) in experimental conditions. Gastric emptying measurement of EIT has good correlations with dye dilution, gastric residuals and scintigraphy. By electrode array located on body surface, gastric motility measurement using EIT realizes noninvasive measurement and directly displays shrink and motility conditions of stomach in body by images of real time. This is going to be a great progress of gastric motility measurement and evaluation method. EIT gastric motility measurement has shown seductive application prospect.
- Citation: Ren CS, Wang Y, Zhao S. Electrical impedance tomography measuring gastric emptying and gastric motility. Shijie Huaren Xiaohua Zazhi 2008; 16(8): 799-805
- URL: https://www.wjgnet.com/1009-3079/full/v16/i8/799.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v16.i8.799
胃肠动力学是一门正在迅速发展的、多学科交叉的新兴学科. 由于相关基础研究薄弱, 长期以来人们缺乏对胃肠运动功能的正确认识和理解[1-2]. 在生理学领域中, 胃肠动力学的发展明显滞后, 这是导致胃肠神经与运动障碍性疾病成为当今临床突出问题的主要原因之一[3-4]. 近年来, 人们对功能性胃肠病以及胃肠动力障碍性疾病的认识有了长足的进步, 对胃肠生物力学的认识有了一定程度的提高, 并获得了大量宝贵信息[5]. 但仍有诸多问题尚不够清楚, 胃动力学研究和临床检查至今仍缺乏可完整了解胃运动和排空情况的方法以作为诊断常规[1]. 鉴于目前功能性消化疾病的高发病率和现有检测方法与设备的局限性, 提供能全面、准确了解胃动力状态的无损伤检测与评价方法是促进胃动力学研究与临床应用进一步发展的需要[6], 也是生物医学工程学者和医生共同面临的艰巨任务[7].
本文对采用代表了生物阻抗技术发展方向的电阻抗断层成像技术检测胃排空与胃动力的发展、现状、问题和应用前景进行述评.
电阻抗断层成像(electrical impedance tomography, 以下简称EIT)是当今生物信息学与生物医学工程学重大研究课题之一. 他是继形态、结构成像之后, 于近20年才发展, 出现的新一代医学成像技术, 具有功能成像, 无损伤和医学图像监护三大突出优势. 代表了生物阻抗技术的发展方向, 是一种理想的、具有诱人应用前景的生物信息检测与成像手段[8].
EIT以人体组织、器官的电阻抗特性及其变化为依据, 通过配置于人体体表的电极阵列, 提取与人体生理、病理状态相关的组织或器官的电特性信息, 给出反映组织、器官功能状态及其变化规律的功能性图像结果.
EIT的发展虽然只有20余年的历史, 却以其无损伤、低成本和功能性图像的独特优势吸引了全世界越来越多的研究者. 国外的EIT研究一直很活跃. 分布在世界各国的EIT研究小组已超过20个, 其中的一些小组已由实验室研究向临床应用研究过渡[9] 国外大多数研究者认为, 目前影响EIT进入临床实际应用的主要问题是系统分辨能力较差. 研究工作也多集中在改进成像模型和重建算法方面, 以期改善EIT的系统的分辨能力. 笔者认为, 虽然现有EIT系统的分辩能力还有待继续提高, 但是片面地追求EIT结构图像的高分辩力而忽视其功能成像与图像监护的优势是不可取的[10]. EIT的真正优势在于利用生物阻抗所携带的丰富生理和病理信息, 实现无损伤功能性成像和图像监护. 如果注意深化生物阻抗检测技术, 改善EIT前级检测方法的定量性和定位性, 采用全信息的多频率或复阻抗检测方法, 充分利用人体组织阻抗中的容抗特性, 改进理论模型, 就可实现从细胞水平上提取与人体生理、病理状态相联系的, 丰富的阻抗全信息. 那么, 国内现有的EIT研究水平, 对于实现人体某些器官, 组织和系统(如乳腺、胃、肺)的功能成像和图像监护已经足够了[11].
胃是人体中比较容易提取EIT信息的组织与器官之一, 在胃的活动期, 特别在食物消化期, 由于胃的收缩和运动, 其形态、体积及内容物组成情况改变较大, 相应的电特性变化非常明显, 信号较强, 信息丰富. 采用EIT技术可无创、连续地检测胃的运动信号, 提取与胃动力学状况相对应的电特性及其变化信息, 反映胃的收缩、蠕动及排空过程, 从而达到检测与评价胃动力功能的目的[7,12].
在已知的EIT胃肠领域临床应用研究中, 最多的是关于通过胃部的食物流动评价和胃排空测量研究, 以期替代临床视为胃排空测量金标准的核素法[13].
EIT胃排空测量的大量工作是在谢菲尔德大学Brown和Barber于1987年开发的单频率EIT系统Mark 1的基础上进行的[14].
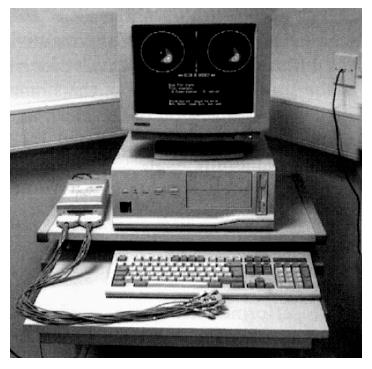
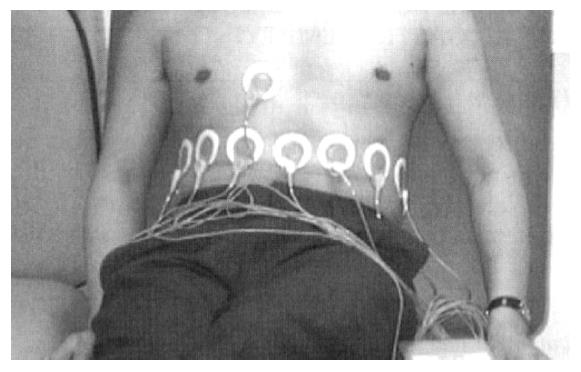
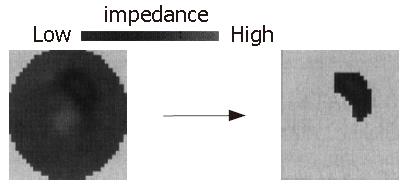
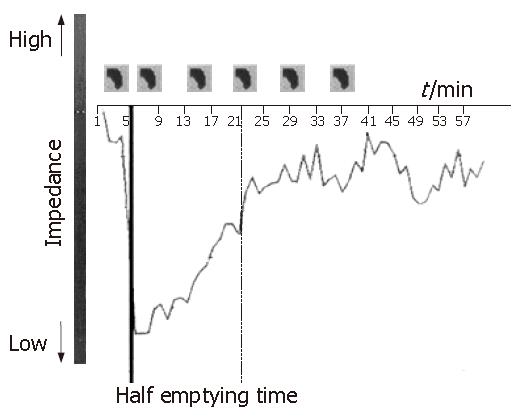
Mark 1系统由数据采集单元, 图像显示单元和计算机组成(图1). 采用相邻电极激励(1 mA, 50 kHz), 相邻电极检测模式和基于反投影原理的图像重建算法, 可给出128×128像素的腹部断层阻抗分布图. 16只电极成环形阵列置于第8肋间位置的腹壁圆周上(图2). 以一定的间隔(对于胃排空测量通常是1 min)相对于参考图像进行序列成像. 然后将胃区位置标注在EIT图像上, 以计算相应于排空过程各序列图像中这一兴趣区内电阻率的变化(图3), 并将其表示为相对于餐后第一幅图像电阻率的变化百分比, 画出胃排空曲线(图4).
因为胃排空采用反投影算法, 其假定胃区电阻率的变化是由于胃内食物的排出. 理论上, 合适的试验餐可以是高电导率的, 也可以是高绝缘的. 重要的是试验餐要有固定的电阻率, 该电阻率的变化表示胃容积的变化[15]. 进餐时分泌的胃酸是一种高电导的氢离子源. 因此, 如果使用非导电性的试验餐, 则在研究胃排空时将由于胃酸中氢离子的加入而使试验餐变成导电性的, 并在消化和排空过程中不断变化, 对测量不利. 高电导试验餐是最合适的, 且可以测量胃内试验餐和胃酸的容量. 任何单价的正离子, 如钠, 钾和氢将增加电导率. 试验餐中加入盐以增加电导率是实际可行的并可起调味作用. Oxo(一种牛肉或蔬菜提取物)通常用作非营养性液体试验餐, 一块Oxo加水可制成200 mL试验餐(31 mmol钠, 15 kcal/块). 麦片粥加盐(37 mmol 钠, 315 kcal/150 mL碗)可作为标准的固体试验餐[13].
为了评价EIT胃排空检测的可行性和有效性, 早在1987年, Avill et al[16]就设计一椭圆形有机玻璃水槽以模拟人体腹部, 进行了EIT胃排空测量离体实验验证. 将不同直径的玻璃棒置于水槽中心恒定深度, 先在电极灵敏区外, 进行EIT成像. 然后将棒移动到槽心至槽边的中点处成像. 结果表明, 电阻率的变化直接与玻璃棒半径的平方成正比(r = 0.99). 玻璃棒置于水槽中心时其EIT值为52.8±1.5 U(mean±SD, n = 5), 当棒移动到槽心至槽边的中点时, 其EIT值为56.2±1.2 U(P = 0.05).
在另一组实验中, 将一5 mL大小的气囊垂直置于水槽中心, 并使其最大直径处位于电极平面, 每次向气囊注入1 mL水, 然后成像, 重复10次. 结果表明, 水槽中气囊的容积和EIT电阻率值有很高的线性关系(r = 0.99).
在EIT胃排空测量可行性和有效性离体实验验证的基础上, 一些在体实验研究进一步确认了EIT胃排空测量的精确性, 并对电极位置变化影响, EIT基线的稳定性等进行了评价.
Avill et al[16]采用胃内气囊方法进行了EIT测量容积变化精度的评价研究. 6名志愿者吞入一带气囊的鼻饲管[17], 气囊位于食管与胃结合部下10 cm处. 每次向气囊充气50 mL, 至250 mL或受试者感觉不适时止. 胃内分泌物被连续抽出. 将气囊每次充气后容积的EIT图像与未充气时的空囊图像相比较. 结果表明, EIT值与胃内气囊的空气量成正比(r = 0.99).
Avill et al于1987年将电极阵置于第8肋间位置, 对19名健康志愿者进行了EIT胃电阻率测量研究[16]. 其中的三只电极用57Co标记, 试验餐为一杯含100 μ Ci99mTc-tin胶体的汤. 由γ相机进行核素法成像并与EIT法进行对比. 结果表明19名受试者的电极均位于相应于胃底处的体表位置.
Wright也于1995年通过6名男性志愿者进行了EIT电极安放位置影响评价研究[13]. 在EIT试验的前一天, 5名志愿者饮用200 mL由1 MBq 99mTc-DTPA标记的橙汁后进行核素成像, 以标明胃的形状和位置. d 2根据核素成像结果将EIT电极置于设定的胃窦水平处, 一个57Co标记置于受试者后背电极水平以测定电极与胃的相对位置. 液体餐为2 MBq 99mTc-DTPA标记的500 mL Oxo, 在记录餐前基线后, 同步进行连续的EIT和核素成像(EIT成像间隔1 min, 核素法间隔8 min). 当核素成像至胃内标记物少于30%(胃内存留)时结束实验. 结果表明6名受试者中, 1名的电极位置偏高, 2名偏低, 电极正好在胃底水平位置的3名, 且电极位置偏低者的EIT胃排空有明显的滞后, 可能是由于十二指肠充盈所至.
4名健康志愿者空腹服用抑制胃酸分泌药甲氰咪胍(cimetidine)90 min后进行EIT成像以评价基线变化[13]. EIT序列成像每分钟一幅, 共进行45 min. 以饮用Oxo后即刻EIT最大值的百分数表示, 画出饮用Oxo后相应于胃位置的兴趣区的空腹变化曲线. 结果表明, 基线变化通常不超过10%, 虽然偶尔会有20%的情况出现.
1987年Avill et al以10名健康志愿者进行了EIT和染料稀释法的液体餐胃排空率同步测量比较[16]. 将一双腔管插入受试者胃区, 吸出胃内物后, 用0.6 mg苯酚红染料水200 mL洗胃. 试验餐为5%蔗糖溶液750 mL. 饮用蔗糖溶液10 min后, 将20 mL苯酚红染料液, 每100 mL溶液含苯酚红染料6.25 mg, 注入管内并使胃内容物充分混合. 每间隔10 min重复注入一次直至胃排空, 每次注入的染料浓度加倍. 在每次注入前和后, 抽出10 mL胃内容物, 由分光光度计在560 nm处测定其苯酚红浓度. 研究结果表明, EIT和染料稀释法半排空时间测量的相关系数为0.83(P<0.001).
Nour et al[18] 1995年对使用鼻饲管的47名足月和早产婴儿进行了EIT胃排空测量. 其中20名的液体餐为普通牛奶, 其余为Dioralyte, 按25 mL/kg由鼻饲管注入. 测量完成后抽出胃内存留物, 计算其百分比并与EIT的测量结果进行比较. 20名牛奶餐婴儿中, 16名的EIT法与胃存留法[13]结果符合率很好, 其余4名差别较大. 27名Dioralyte餐婴儿中, 24名的测量结果有很好的符合率, 其余3名差别较大.
Avill et al 1987年以8名健康志愿者进行了EIT法和核素法的液体餐胃排空同步测量比较[16]. 液体试餐为300 mL肉汤, 经过滤并加水(含100 μ Ci99Tc-tin胶体)稀释至50%. 核素法成像使用单头γ相机(Pho/Gamma Ⅲ, model 1021, Nuclear Chicago, Europa, NY)每2 min 1幅共46幅. 胃排空图由定义的胃部兴趣区获得并进行归一化和辐射衰减修正. 其结果与每分钟1幅的EIT胃排空图进行比较. 结论是两种方法的胃半排空时间相关系数为0.801(P = 0.05).
Wright在1995年也以11名男性志愿者进行了EIT和核素法的液体餐胃排空测量比较[13]. 实验分2次进行, 其间隔在14 d以上. 志愿者分为胃酸抑制组和无胃酸抑制(对照)组. 胃酸抑制组在实验前2 h服用400 mg甲氰咪胍(cimetidine). 在记录EIT餐前基线后, EIT和核素法的液体餐(500 mL Oxo, 采用2 MBq 99mTc-DTPA标记)胃排空实验同步进行. EIT图像间隔为1 min, 核素法间隔为8 min, 当核素法检测到胃内标记物少于30%时结束实验. 结果表明, 在对照组(r = 0.77, P = 0.006)和酸抑制组(r = 0.87, P = 0.001), 两种方法的半排空时间具有很好的一致性.
Wright于1995年以8名志愿者进行了EIT和核素法的半固体餐胃排空评价[13]. 实验分2次进行, 间隔14 d以上, 分为无胃酸抑制(对照)组和在实验前2 h服用甲氰咪胍(cimetidine)400 mg的胃酸抑制组. 实验为500 mL盐味粥, 烹制前加入3 MBq 99mTc-DTPA标记物. 在记录EIT餐前基线后, EIT和核素法的半固体餐胃排空实验同步进行. EIT图像间隔为1 min, 核素法间隔为10 min, 连续进行至最长200 min结束.
对10次有效实验结果的分析表明. 服用甲氰咪胍使核素法组的半排空时间增加(P = 0.04). 对照组的EIT和核素法半排空时间测量的相关性为r = 0.87, P = 0.05, 服用甲氰咪胍的酸抑制组为r = 0.89, P = 0.04. 即对照组的EIT与核素法胃排空测量结果有明显差别(P = 0.04), 而酸抑制组的EIT和核素法排空测量结果没有明显的差别.
Avill et al在1987年以8名健康志愿者进行了EIT法和核素法固体餐胃排空的同步测量比较研究[17-21]. 试验餐为85 g即食土豆泥与含100 μ Ci99Tc-tin胶体的300 g水混合. 在进食前15 min和90 min时服用甲氰咪胍以抑制胃酸. 核素法成像采用单头γ相机(Pho/Gamma Ⅲ, model 1021, Nuclear Chicago, Europa, NY), 采集时间为2 h, 前40 min每2 min一幅, 随后的80 min每5 min一幅. 胃排空图由定义的胃部兴趣区获得并进行归一化和辐射衰减修正. 其结果与每分钟一幅的同步EIT图像进行比较. 结果表明两种方法的半排空时间测量结果的相关系数为(r = 0.73, P<0.05).
进食期间胃酸分泌明显增加, 已有研究表明, 酸分泌对EIT测量结果有影响. 如Avill et al于1987年对3名健康志愿者以五肽促胃酸激素(pentagostrin, 6 μg/kg体质量)诱发胃酸分泌, 对用药前后进行了EIT成像研究[16]. 发现五肽促胃酸激素诱发胃酸分泌, 增加了所有受试者的胃电导率, 从而影响EIT测量结果.
Mushambi et al在1992年使用雷尼替定(ranitidine)和甲氰咪胍(cimetidine)抑制胃酸分泌[20], 进行了10名正常志愿者的EIT胃排空测量比较, 发现雷尼替定组的胃排空时间比甲氰咪胍组有明显的延迟(P<0.04)Wright于1995年以16名健康志愿者比较了胃酸分泌对液体餐和固体餐排空测量的影响[13]. 液体餐是一块Oxo稀释于500 mL水中. 半固体餐是含4.5 g盐的粥500 mL. 受试者各进行6次实验, 分别在无酸抑制, 实验前2 h po 400 mg甲氰咪胍, 或实验前12 h po 40 mg奥米普拉唑(omeprazole)和实验前2 h po 20 mg奥米普拉唑情况下进行液体餐和固体餐EIT测量.
结果表明, 液体餐实验中, 男女性之间的胃排空时间没有整体上的差别, 但胃酸抑制组的胃排空比对照组快(甲氰咪胍组P = 0.06, 奥米普拉唑组P = 0.09). 半固体餐实验中, 男性比女性的胃排空更快并在对照组(P = 0.01)和甲氰咪胍组(P = 0.02)具有统计意义. 在液体餐和半固体餐实验中, 甲氰咪胍组的排空最快, 其次是对照组, 然后是奥米普拉唑组. 女性中服用甲氰咪胍和奥米普拉唑后的排空都快于对照组. 在半固体餐实验中, 女性的慢变相长于男性(P = 0.02). 在对照组半固体餐和液体餐实验中, 男性(P = 0.04)和女性(P = 0.04)的慢变相都较长. 当胃酸分泌被抑制时, 半固体餐和液体餐实验的慢变相比例相似.
Avill et al在1987年采用随机盲检试验研究了8名健康志愿者服用甲氰咪胍后对液体餐EIT胃排空测量的影响[16]. 每位受试者进行两对实验. 受试者在连续两天的同一时间服用800 mg甲氰咪胍或安慰剂, 试验餐为500 mL热水加一块Oxo. 结果表明, 当服用甲氰咪胍时, 两次实验有很强的相关性(r = 0.90). 但当不抑制胃酸时, 没有相关性(r = -0.19).Mangnall et al 1991年以牛肉饼为试验餐进行了固体餐EIT法和核素法的同步测量研究[21]. 试验餐为以核素(100 μ Ci99mTc牛黄胶体, 并在制餐时溶入蛋中)标记的牛肉饼160 g, 体积为137 mL, 含脂肪20 g, 蛋白23 g, 碳水化合物8 g, 盐2.5 g. 8名志愿者无胃酸分泌抑制, 进行核素成像. 另12名志愿者实验前60 min服用400 mg甲氰咪胍, 继而于实验开始时再服800 mg甲氰咪胍以抑制胃酸分泌. 核素成像采用单头γ相机(Pho/Gamma Ⅲ, model 1021, Nuclear Chicago, Europa, NY), 每5 min一幅核素图像, 从进食前开始, 共持续4 h. EIT测量每2 min一幅, 进食前10 min时开始, 至餐后4 h止. 以上20名志愿者实验中, 共获得19人的胃排空图像. 研究结果表明, 两种方法的半排空时间(r = 0.713, P<0.02)和1/4半排空时间(r = 0.825, P<0.01)明显相关, 但是胃酸抑制组中排空慢变相的相关性不足(r = 0.585). 没有抑制胃酸分泌的8名志愿者中, 5名的EIT排空时间慢于核素法, 且两者的半排空时间没有相关性(r = 0.058), 慢变相(r = 0.376). 8名志愿者中只有2名的EIT半排空时间在核素法结果的10%以内.
EIT胃排空测量研究已经历了约20年的发展过程[13-22]. 在离体的模型实验中EIT可以精确测量玻璃棒/气囊的容积变化. 在体实验条件下, EIT能精确测量胃容积(气囊)的变化. 当电极置于第8肋间位置时, EIT胃排空测量具有足够的精度, 且轻微的电极位置变化不影响测量结果. 当然, 电极稍高比偏低要更好些, 可以避免来自胃窦和十二指肠区的干扰信号.
对于液体餐EIT胃排空测量, 其与染料稀释法有很好的相关性. 由于多数实验排除了胃酸分泌, 其在正常条件下的胃排空关系还有待进一步研究. 非营养液体餐时的EIT胃排空测量与核素法相关. 在胃酸抑制条件下, EIT半固体餐和固体餐胃排空测量与核素法相关. EIT的半排空时间测量结果总比核素法的结果长. 当胃酸抑制时, EIT胃排空曲线的慢变相明显短于核素法的测量结果. 因此, EIT法更像是测量了包括胃酸分泌的胃容量, 而核素法只是测量试验餐中辐射标记物的胃排空[23].
EIT是检测人体器官中黏质液容积传导的一种新的、无损伤方法. 其在胃肠领域的最多应用是评价通过胃部的食物流动以替代临床仍然视为金标准的核素法. 由于他测量的是胃容量而不是胃存留时间(排空)[13], 因而不用, 也不要指望采用γ核素法予以修正[24-25], 除非所有进入胃肠道的生理性分泌被抑制.
胃动力包括空腹状态下的消化间期移行性复合运动(migrating motor complex, MMC)和消化期的相对规则运动. 在消化间期, 胃内压呈现周期性变化, 以防止胃的淤滞, 同时扫清胃内细菌、未消化残留食物、脱落细胞、黏液等, 为进餐作准备. 进餐后, 进入消化期, MMC消失, 胃的运动进入一个相对规则的运动期. 食物刺激口腔、咽、食管和胃内感受器, 通过迷走-迷走神经反射使胃近端舒张, 以容纳食物, 称为容纳性舒张; 同时近端胃在接纳食物后, 进一步舒张以顺应胃内体积的增加, 保持胃腔内压力无明显变化, 为胃顺应性舒张. 而胃远端运动则包括蠕动、终末胃窦收缩等, 以完成对胃内食物的混合、研磨, 最终将食物排空[1,3,5].
在以上不同时段胃的运动过程中, 胃的容积、形态及内容物组成状况改变较大[26-28], 相应的电特性变化十分明显, 变化规律与胃动力学状况相对应, 相关性强, 阻抗胃动力信息丰富. 应用生物阻抗技术, 通过体表电极连续地检测胃的运动信号, 提取与胃动力学状况相对应的电特性及其变化信息, 反映胃的收缩、蠕动及排空过程, 就可以达到检测与评价胃动力功能的目的[29].
采用非图像方式的普通阻抗方法通过体表电极获得的阻抗信号是一种混合信号, 包含了如心电、呼吸以及受检者体位变化干扰等的多种信号成分, 特别是呼吸信号的频率约为12 次/min, 与胃运动信号接近, 同属于超低频范围, 且其幅度还可能远大于胃阻抗信号, 信号分离与处理难度较大. 如何在超低频段上稳定可靠地去除呼吸干扰, 有效提取胃阻抗信号, 至今还是有待解决的重要技术问题之一[30].
EIT代表了生物阻抗技术的发展方向, 具有功能成像, 无损伤和医学图像监护的突出优势, 可以实现对消化间期和消化期的胃动力状况及其变化进行检测和评价[31]. 胃的收缩和蠕动频率约为3 次/min, 对EIT系统的实时性要求不高, 是阻抗信息易于提取, 较好的EIT应用目标之一[32-33]. EIT胃动力测量以置于体表的电极阵列实现无损检测, 以实时图像方式直接显示体内胃体的收缩和运动状况, 呼吸干扰易于识别和排除, 将为胃动力学基础研究与临床应用提供一种全新的, 能全面、准确了解胃动力状态的无损伤检测手段, 促进胃动力学研究与临床检测的进步, 显示了广阔的应用前景.
近年来, 人们对功能性胃肠病以及胃肠动力障碍性疾病的认识有了长足的进步, 对胃肠生物力学的认识有了一定程度的提高, 并获得了大量宝贵信息, 但仍有诸多问题尚不够清楚. 胃动力学研究和临床检查至今仍缺乏方便、有效、可完整了解胃排空和运动情况的检测方法. 鉴于目前功能性消化疾病的高发病率和现有检测方法与设备的局限性, 提供能全面、准确了解胃动力状态的无损伤检测与评价方法是促进胃动力学研究与临床应用进一步发展的需要, 也是生物医学工程学者和医生共同面临的艰巨任务.
许文燮, 教授, 上海交通大学生命科学院生物医学工程系
在胃的运动过程中, 其容积、形态及内容物组成状况改变较大, 相应的电特性变化十分明显, 变化规律与胃动力学状况相对应, 相关性强, 胃动力信息丰富. EIT液体餐胃排空测量与染料稀释法有很好的相关性. 由于多数实验排除了胃酸分泌, 其在正常条件下的胃排空关系还有待进一步研究. 非营养液体餐EIT胃排空测量与核素法相关. 在胃酸抑制条件下, EIT半固体餐和固体餐胃排空测量与核素法相关. EIT的半排空时间测量结果总比核素法的结果长. 当胃酸抑制时, EIT胃排空曲线的慢变相明显短于核素法的测量结果.
生物电阻抗方法具有无创、廉价、操作简单和功能信息丰富等特点, 可高灵敏、准确地提取与胃动力学状况相对应的电特性及其变化信息. 从电活动-机械收缩复合系统的高度认识胃动力, 将生物阻抗方法与同步胃电检测相结合, 是生物电阻抗胃动力检测方法的发展方向.
EIT具有功能成像, 无损伤和医学图像监护的突出优势, 有利于对消化间期和消化期胃动力状况及其变化进行检测和评价. 胃的收缩和蠕动频率约为3 次/min, 对EIT系统的实时性要求不高, 是阻抗信息易于提取, 较好的EIT应用目标之一. EIT胃动力测量以置于体表的电极阵列实现无损检测, 以实时图像方式直接显示体内胃体的收缩和运动状况, 呼吸干扰易于识别和排除, 将是胃动力检测与评价手段的重大进步, 显示了诱人的应用前景.
EIT是检测人体器官中黏质液容积传导的一种新的、无损伤方法. 其在胃肠领域的最多应用是评价通过胃部的食物流动以替代临床仍然视为金标准的核素法. EIT测量的是包括了胃酸分泌在内的胃容量(排空)而不是胃存留时间, 由于核素法只是测量试验餐中辐射标记物的胃排空, 因而没有必要, 也不要指望采用核素法对EIT测量结果予以修正, 除非所有进入胃肠道的生理性分泌被抑制.
电阻抗断层成像技术(EIT): 一种以人体组织电特性(阻抗、导纳、介电常数等)及其变化为目标的功能成像技术. EIT通过配置于人体体表的电极阵, 外加一微弱的交流激励电流, 测量其产生的边界电压值, 经图像重建算法给出位于电极位置平面的人体组织与器官的电特性图像. 因为人体不同组织和器官具有不同的电特性, 而且某些组织和器官的电特性随其功能状态而改变. 所以这种EIT图像不但包含了解剖学信息, 更重要的是可以给出与人体病理和生理状态相对应的功能性图像结果. EIT以人体组织、器官的阻抗分布或变化为依据, 提取与人体生理、病理状态相关的组织或器官的电特性信息, 具有功能成像, 无损伤和医学图像监护三大突出优势.
本文选题新颖, 书写流畅, 信息量大, 具有很好的可读性和学术价值.
编辑: 李军亮 电编: 何基才
| 1. | 周 吕, 柯 美云. 肠胃动力学: 基础与临床. 第1版. 北京: 科学出版社 1999; 279-476. |
| 2. | 马 文M. 舒斯特. 舒斯特胃肠动力学. 第2版. 上海: 上海科学技术文献出版社 2003; 130-196. |
| 3. | 周 吕, 柯 美云. 神经胃肠病学与动力-基础与临床. 北京: 科学出版社 2005; 461-543. |
| 4. | 潘 国宗, 曹 世植. 现代胃肠病学(上册). 第1版. 北京: 科学出版社 1994; 123, 853-859. |
| 5. | 樊 艳华, 王 虹. 胃肠生物力学-胃肠动力新视角. 第1版. 北京: 人民卫生出版社 2006; 64-123. |
| 6. | 赵 舒, 任 超世. 生物电阻抗法检测胃动力功能. 国际生物医学工程杂志. 2006;29:92-95. |
| 13. | Holder DS. Electrical impedance tomography, methods, history and applications. London: IOP Publishing Ltd. 2005; 186-202. |
| 14. | Brown BH, Seagar AD. The Sheffield data collection system. Clin Phys Physiol Meas. 1987;8 Suppl A:91-97. [PubMed] |
| 15. | Piessevaux H, Tack J, Walrand S, Pauwels S, Geubel A. Intragastric distribution of a standardized meal in health and functional dyspepsia: correlation with specific symptoms. Neurogastroenterol Motil. 2003;15:447-455. [PubMed] [DOI] |
| 16. | Avill R, Mangnall YF, Bird NC, Brown BH, Barber DC, Seagar AD, Johnson AG, Read NW. Applied potential tomography. A new noninvasive technique for measuring gastric emptying. Gastroenterology. 1987;92:1019-1026. [PubMed] |
| 17. | Soulsby CT, Khela M, Yazaki E, Evans DF, Hennessy E, Powell-Tuck J. Measurements of gastric emptying during continuous nasogastric infusion of liquid feed: electric impedance tomography versus gamma scintigraphy. Clin Nutr. 2006;25:671-680. [PubMed] [DOI] |
| 18. | Nour S, Mangnall YF, Dickson JA, Johnson AG, Pearse RG. Applied potential tomography in the measurement of gastric emptying in infants. J Pediatr Gastroenterol Nutr. 1995;20:65-72. [PubMed] [DOI] |
| 19. | Ghoos YF, Maes BD, Geypens BJ, Mys G, Hiele MI, Rutgeerts PJ, Vantrappen G. Measurement of gastric emptying rate of solids by means of a carbon-labeled octanoic acid breath test. Gastroenterology. 1993;104:1640-1647. [PubMed] [DOI] |
| 20. | Mushambi MC, Trotter TN, Barker P, Rowbotham DJ. A comparison of gastric emptying rate after cimetidine and ranitidine measured by applied potential tomography. Br J Clin Pharmacol. 1992;34:278-280. [PubMed] [DOI] |
| 21. | Mangnall YF, Kerrigan DD, Johnson AG, Read NW. Applied potential tomography. Noninvasive method for measuring gastric emptying of a solid test meal. Dig Dis Sci. 1991;36:1680-1684. [PubMed] [DOI] |
| 22. | Vantrappen G. Methods to study gastric emptying. Dig Dis Sci. 1994;39:91S-94S. [PubMed] [DOI] |
| 23. | Bromer MQ, Parkman HP. Office-based testing for gastric emptying: a breath away? J Clin Gastroenterol. 2001;32:374-376. [PubMed] [DOI] |
| 24. | Bromer MQ, Kantor SB, Wagner DA, Knight LC, Maurer AH, Parkman HP. Simultaneous measurement of gastric emptying with a simple muffin meal using [13C]octanoate breath test and scintigraphy in normal subjects and patients with dyspeptic symptoms. Dig Dis Sci. 2002;47:1657-1663. [PubMed] [DOI] |
| 25. | Lee JS, Camilleri M, Zinsmeister AR, Burton DD, Choi MG, Nair KS, Verlinden M. Toward office-based measurement of gastric emptying in symptomatic diabetics using [13C]octanoic acid breath test. Am J Gastroenterol. 2000;95:2751-2761. [PubMed] [DOI] |
| 26. | Gilja OH, Detmer PR, Jong JM, Leotta DF, Li XN, Beach KW, Martin R, Strandness DE. Intragastric distribution and gastric emptying assessed by three-dimensional ultrasonography. Gastroenterology. 1997;113:38-49. [PubMed] [DOI] |
| 27. | Horowitz M, Dent J. Disordered gastric emptying: mechanical basis, assessment and treatment. Baillieres Clin Gastroenterol. 1991;5:371-407. [PubMed] [DOI] |
| 28. | Horowitz M, Dent J, Fraser R, Sun W, Hebbard G. Role and integration of mechanisms controlling gastric emptying. Dig Dis Sci. 1994;39:7S-13S. [PubMed] [DOI] |
| 29. | Li Z, Sha H, Wang Y, Zhao S, Wang W, Ren CS. A new approach of gastric motility measurement and evaluation by bioimpedance. Proceedings of 13th International Conference on Electrical Bio-Impedance & 8th Conference on Electrical Impedance Tomography, Graz, Austria. 2007;691-694. |
| 30. | Yan W, Hong S, Chaoshi R. Optimum design of electrode structure and parameters in electrical impedance tomography. Physiol Meas. 2006;27:291-306. [PubMed] [DOI] |
| 31. | Wang Y, Sha H, Zhao S, Ren CS. Influences of Compound Electrode Parameter on Measurement Sensitivity and Reconstruction Quality in Electrical Impedance Tomography. Proceedings of World Congress on Medical Physics and Biomedical Engineering, Seoul, Korea. 2006;3433-3436. [DOI] |
| 32. | Li ZY, Ren CS, Sha H, Wang Y, Zhao S, Wei JM, Wang W. Wavelet Transform to Extract Bio-Impedance Gastric Motility Information. Proceedings of the 2nd international conference on complex systems and applications-modeling, control and simulations, Hanlin, Jinan, China. 2007;1237-1241. |
| 33. | Sha H, Wang Y, Zhao S, Ren CS. Integrated Data Collection in Electrical Impedance Tomography. Proceedings of 13th International Conference on Electrical Bio-Impedance & 8th Conference on Electrical Impedance Tomography, Graz, Austria. 2007;348-351. |