修回日期: 2008-11-25
接受日期: 2008-12-01
在线出版日期: 2008-12-18
目的: 观察周剂量紫杉醇联合奥沙利铂二线治疗晚期胃癌的疗效和不良反应.
方法: 收集2006-07-01/2008-01-31我科以周剂量紫杉醇联合奥沙利铂治疗一线化疗失败的晚期胃癌患者23例, 给予紫杉醇70 mg/m2, 静脉滴注1 h, 第1、8、15天; 奥沙利铂100 mg/m2, 静脉滴注2 h, 第2天, 每28天为1个周期. 每例患者治疗至少2个周期, 2个周期化疗完成后4 wk评价疗效.
结果: 在可评价疗效的23例患者中, 完全缓解(CR)0例, 部分缓解(PR)8例(34.8%), 疾病稳定(SD)8例(34.8%), 疾病进展(PD)7例(30.4%); 总有效率(CR+PR)34.8%, 95%CI为16%-57%; 临床获益者(CR+PR+SD)共16例(69.6%), 95%CI为47%-87%. 平均肿瘤进展时间(TTP)为3.93±1.47 mo. 不良反应主要为脱发、骨髓抑制和外周神经毒性.
结论: 周剂量紫杉醇联合奥沙利铂二线治疗晚期胃癌疗效好, 不良反应可耐受.
引文著录: 伍小平, 庄英帜, 姜浩, 伍尤华, 戴文香, 艾小红, 唐三元. 周剂量紫杉醇联合奥沙利铂二线治疗晚期胃癌23例. 世界华人消化杂志 2008; 16(35): 3997-3999
Revised: November 25, 2008
Accepted: December 1, 2008
Published online: December 18, 2008
AIM: To evaluate the efficacy and adverse effects of paclitaxel combined with oxaliplatin as a second-line chemotherapy for patients with advanced gastric cancer.
METHODS: Twenty-three cases with advanced gastric cancer who failed first-line therapy received paclitaxel combined with oxaliplatin chemotherapy from July first, 2006 to January 31, 2008. Paclitaxel (70 mg/m2) was administered by intravenous drip for 1 h on the first, eighth, fifteenth day; oxaliplatin 100 mg/m2 was administered by intravenous drip for 2 h on the second day. Each treatment cycle included 28 d. Each patient was treated for more than two circles and evaluated four weeks later.
RESULTS: Of the 23 patients, none showed complete remission (CR), 8 (34.8%) showed partial remission (PR), 8 (34.8%) showed stable disease (SD) and 7 (30.4%) showed progressive disease (PD). The overall response rate was 34.8% with a 95%CI (range: 16%-57%); and 16 patients (69.6%) benefited (CR+PR+SD) from the clinical therapy with a 95%CI (range: 47%-87%). The mean time to tumor progression (TTP) was 3.93 ± 1.47 months. The main side effects were alopecia, myelosuppression and peripheral neuropathy.
CONCLUSION: The regimen of paclitaxel plus oxaliplatin has a definite effect with acceptable toxicity for patients with advanced gastric cancer.
- Citation: Wu XP, Zhuang YZ, Jiang H, Wu YH, Dai WX, Ai XH, Tang SY. Therapy of paclitaxel plus oxaliplatin as a second-line chemotherapy for patients with advanced gastric cancer: an analysis of 23 cases. Shijie Huaren Xiaohua Zazhi 2008; 16(35): 3997-3999
- URL: https://www.wjgnet.com/1009-3079/full/v16/i35/3997.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v16.i35.3997
在我国, 胃癌是最常见的恶性肿瘤之一, 胃癌的粗死亡率为25.2/10万, 占全部恶性肿瘤死亡的23.2%, 其死亡率仅低于肺癌, 居各种恶性肿瘤的第2位[1]. 2006-07-01/2008-01-31我科以周剂量紫杉醇联合奥沙利铂治疗一线化疗失败的晚期胃癌患者23例, 现报告如下.
本组23例患者中, 男15例, 女8例, 年龄38-64(中位年龄52)岁. 13例因有远处转移未行手术治疗, 10例为手术后复发转移, 所有患者均通过胃镜或手术活检取得病理确诊, 所有患者的病灶均可通过测量评价疗效, 预计生存期超过3 mo, 所有患者都经过一线化疗治疗后疾病进展, 使用过的一线化疗方案有ECF、PF、FOLFOX等, 血常规、心脏、肝肾功能均正常, Karnofsky评分≥60分.
紫杉醇70 mg/m2, 静脉滴注1 h, 第1、8、15天; 奥沙利铂100 mg/m2, 静脉滴注2 h, 第2天, 每28天为1个周期, 每例患者治疗至少2个周期, 2个周期化疗完成后4 wk评价疗效, 每个周期化疗前后复查血常规、心电图、肝肾功能. 23例患者共接受104个周期化疗, 每例患者平均疗程数为4.5个周期. 疗效评定根据WHO关于实体瘤的客观疗效评定标准分为: 完全缓解(CR), 部分缓解(PR), 疾病稳定(SD), 疾病进展(PD). 有效率(RR)为CR+PR病例数占可评价疗效病例数的百分数. 不良反应按WHO关于抗癌药物常见毒副反应分级标准分为0-Ⅳ度. 采用电话随访, 最后随访时间2008-06-30, 本组病例失访率为0.
统计学处理 数据分析利用SPSS11.0统计软件包进行处理, 计算有效率及临床获益率的95%可信区间及平均肿瘤进展时间(TTP).
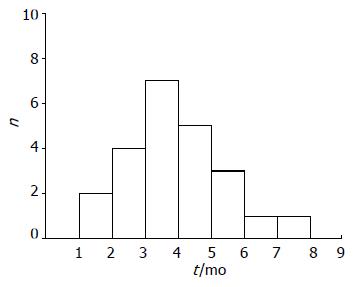
在可评价疗效的该组23例患者中, CR 0例, PR 8例(34.8%), SD 8例(34.8%), PD 7例(30.4%), 总有效率(CR+PR)34.8%, 其95%可信区间为16%-57%; 临床获益者(CR+PR+SD)共16例, 占69.6%, 其95%可信区间为47%-87%. 周剂量紫杉醇联合奥沙利铂二线治疗23例晚期胃癌患者的TTP见图1. 平均肿瘤进展时间(TTP)为3.93±1.47 mo.
目前我国胃癌的防治现状是"三低一高", 即早期诊断率低, 手术切除率低, 5年生存率低, 根治术后复发转移率高[2]. 我国的胃癌患者在确诊时大多数已存在不同程度的转移, 使术后很快复发或根本失去手术机会, 晚期胃癌的治疗是以期达到延长生存期, 提高生活质量的姑息治疗为目的, 化疗治疗晚期胃癌较最佳支持治疗无论是延长生存期还是提高生活质量都有显著优势[3]. 然而胃癌是相对化疗敏感的恶性肿瘤, 晚期胃癌患者化疗完全缓解率很低, 有效持续时间和肿瘤进展时间都很短. 时至今日, 胃癌治疗依然没有所谓的"金标准"一线/二线化疗方案[4]. 所以几乎所有的晚期胃癌患者经过一线化疗后疾病都会进展, 需要二线方案行挽救性治疗.
晚期胃癌患者从二线或挽救性方案的治疗中获益程度如何到目前还没有定论, 进入新世纪多种新药(如紫杉类、奥沙利铂、伊立替康及卡培他滨等)组成二线方案来治疗晚期胃癌, 取得了一定的疗效[5,8-12], 并能改善患者的生活质量[6].
紫杉醇是一种新型抗微管药, 通过促进微管蛋白装配成微管, 并抑制其解聚, 从而影响细胞的有丝分裂和增殖, 其主要毒副作用为骨髓抑制及脱发, 其他副作用较弱, 每周使用可使紫杉醇的骨髓抑制减弱, 患者的耐受性增强, 且每周使用较3周使用疗效增加[7], 对胃癌的二线治疗可取得较好的疗效[8-10]. 奥沙利铂是第三代的铂类化合物, 其剂量限制性毒性为周围神经毒性, 胃肠道反应及骨髓抑制较小, 且挽救治疗晚期胃癌有一定效果[11-12]. 而晚期胃癌尤其是一线治疗后失败的患者, 一般情况欠佳, 消化功能差, 化疗的耐受性差, 所以我们在对晚期胃癌的患者进行二线或挽救性治疗时, 在追求疗效的同时要充分考虑治疗的毒副作用和患者的耐受性. 本组细胞周期特异性药物周剂量的紫杉醇联合相对较小剂量细胞周期非特异性药物奥沙利铂的方案, 充分考虑到组织联合化疗的原则(单药有效, 副作用不叠加, 作用机制不同等)、晚期胃癌患者体质特点、姑息性化疗的目的及28 d一周期有利患者血象/体能恢复. 所以本方案有充分的理论依据, 考虑全面, 其较好的疗效得到本组临床观察的支持, 且本方案不良反应小, 患者的耐受性好.
我科临床观察周剂量紫杉醇联合奥沙利铂二线治疗晚期胃癌, 总有效率(CR+PR)34.8%, 95%可信区间为(16%-57%); 临床获益者(CR+PR+SD)共16例, 占69.6%, 95%可信区间为(47%-87%); 二线治疗开始后的平均肿瘤进展时间(TTP)为3.93±1.47 mo. 化疗的疗效好, 化疗后晚期胃癌患者的生活质量得到提高, 且不良方应小, 不良反应有脱发和骨髓抑制、外周神经毒性、黏膜炎、肌肉关节痛、肝功能异常等, 尤其是患者难以耐受的Ⅲ/Ⅳ度不良反应发生率低(主要为脱发、骨髓抑制和外周神经毒性, 发生率>10%), 无粒缺性发热的发生, 经升血治疗后不影响下一周期化疗的进行. 少数患者经以上治疗进展后采用了三线化疗(含伊立替康、卡培他滨等), 故本组患者未观察生存期.
总之, 周剂量紫杉醇联合奥沙利铂方案二线治疗晚期胃癌疗效好, 不良反应小, 患者对治疗耐受性好, 很好地达到晚期胃癌姑息治疗的目的, 值得临床推广.
在我国, 胃癌是最常见的恶性肿瘤之一, 胃癌的粗死亡率为25.2/10万, 占全部恶性肿瘤死亡的23.2%, 其死亡率仅低于肺癌, 居各种恶性肿瘤的第2位. 晚期胃癌的治疗是以期达到延长生存期, 提高生活质量的姑息治疗为目的, 化疗治疗晚期胃癌较最好支持治疗无论是延长生存期还是提高生活质量都有显著优势.
黄颖秋, 教授, 本溪钢铁(集团)有限责任公司总医院消化内科
胃癌是相对化疗敏感的恶性肿瘤, 晚期胃癌患者化疗完全缓解率很低, 有效持续时间和肿瘤进展时间都很短. 时至今日, 胃癌治疗依然没有所谓的"金标准"一线/二线化疗方案. 所以几乎所有的晚期胃癌患者经过一线化疗后疾病都会进展, 需要二线方案行挽救性治疗.
晚期胃癌患者从二线方案的治疗中获益程度如何到目前还没有定论, 进入新世纪多种新药(如紫杉类、奥沙利铂、伊立替康及卡培他滨等)组成二线方案来治疗晚期胃癌, 取得了一定的疗效, 并能改善患者的生活质量.
经过一线治疗失败的晚期胃癌患者具有体能状况较差、消化功能差、耐受性差等体质特点, 而本方案毒副作用小, 应用起来简易方便, 近期及远期疗效好, 值得临床推广使用.
本文对晚期胃癌的二线化疗方案进行了有益的尝试, 对临床工作有一定参考价值, 若增加临床观察样本将更有意义.
编辑: 史景红 电编: 何基才
| 1. | 孙 秀娣, 牧 人, 周 有尚, 戴 旭东, 乔 友林, 张 思维, 皇 普小梅, 孙 杰, 李 连弟, 鲁 凤珠. 中国1990-1992年胃癌死亡调查分析. 中华肿瘤杂志. 2002;24:4-8. |
| 3. | Casaretto L, Sousa PL, Mari JJ. Chemotherapy versus support cancer treatment in advanced gastric cancer: a meta-analysis. Braz J Med Biol Res. 2006;39:431-440. [PubMed] [DOI] |
| 4. | 储 大同. 当代肿瘤内科治疗方案评价. 第2版. 北京: 北京大学医学出版社 2004; 83. |
| 5. | Ueda S, Hironaka S, Boku N, Fukutomi A, Yoshino T, Onozawa Y. Combination chemotherapy with irinotecan and cisplatin in pretreated patients with unresectable or recurrent gastric cancer. Gastric Cancer. 2006;9:203-207. [PubMed] [DOI] |
| 6. | Park SH, Lee WK, Chung M, Bang SM, Cho EK, Lee JH, Shin DB. Quality of life in patients with advanced gastric cancer treated with second-line chemotherapy. Cancer Chemother Pharmacol. 2006;57:289-294. [PubMed] [DOI] |
| 7. | Sparano JA, Wang M, Martino S, Jones V, Perez EA, Saphner T, Wolff AC, Sledge GW Jr, Wood WC, Davidson NE. Weekly paclitaxel in the adjuvant treatment of breast cancer. N Engl J Med. 2008;358:1663-1671. [PubMed] [DOI] |
| 8. | Ito S, Kodera Y, Mochizuki Y, Yamamura Y. [Feasibility study of weekly paclitaxel as second-line chemotherapy against 5-FU-refractory gastric carcinoma]. Gan To Kagaku Ryoho. 2005;32:1427-1430. [PubMed] [DOI] |
| 9. | Hironaka S, Zenda S, Boku N, Fukutomi A, Yoshino T, Onozawa Y. Weekly paclitaxel as second-line chemotherapy for advanced or recurrent gastric cancer. Gastric Cancer. 2006;9:14-18. [PubMed] [DOI] |
| 10. | Kodera Y, Ito S, Mochizuki Y, Fujitake S, Koshikawa K, Kanyama Y, Matsui T, Kojima H, Takase T, Ohashi N. A phase II study of weekly paclitaxel as second-line chemotherapy for advanced gastric Cancer (CCOG0302 study). Anticancer Res. 2007;27:2667-2671. [PubMed] [DOI] |
| 11. | Qian J, Qin SK, Mei JF, Chen YX, Shao ZJ, He ZM. [Oxaliplatin plus capecitabine as a second line chemotherapy for patients with advanced gastric cancer]. Zhonghua Zhongliu Zazhi. 2004;26:746-748. [PubMed] [DOI] |