修回日期: 2008-03-20
接受日期: 2008-05-02
在线出版日期: 2008-05-08
胰头十二指肠切除术是普通外科最复杂的手术之一. 近年来, 采用胰头十二指肠切除治疗良恶性病变增加. 一方面, 放射学水平的进展利于病变的精确诊断和治疗; 另一方面, 也归功于围术期处理水平的提高和外科手术技术的进步. 湖南省人民医院肝胆医院1990-01/2007-12施行胰头十二指肠切除术604例, 手术死亡率仅0.3%, 手术效果优良. 本文以胰头癌手术为例, 介绍我们关于胰头十二指肠切除术的一些经验.
引文著录: 吴金术, 彭创. 胰头十二指肠切除术. 世界华人消化杂志 2008; 16(13): 1369-1372
Revised: March 20, 2008
Accepted: May 2, 2008
Published online: May 8, 2008
Pancreatoduodenectomy may be one of the most complicated operations in general surgery. Over the past decade, performance of pancreatoduodenectomy to treat both malignant and benign disease has increased. This increase is in large part due to the decreasing perioperative mortality rate. On the one hand, recent advances in pancreatoduodenectomy have contributed to the earlier diagnosis and treatment. On the other hand, the decreasing mortality rate is also attributed to improvements in perioperative management and advances in surgical techniques. Between January 1990 and December 2006, 604 patients underwent pancreatoduodenectomy in Department of Hepatobiliary Surgery, People's Hospital of Hunan Province. The operative mortality rate was only 0.3% and a successful long-term outcome was achieved. The paper aims to review retrospectively the clinic data about these patients, and introduce our experiences in several key steps during pancreatoduodenectomy.
- Citation: Wu JS, Peng C. Experiences in pancreatoduodenectomy. Shijie Huaren Xiaohua Zazhi 2008; 16(13): 1369-1372
- URL: https://www.wjgnet.com/1009-3079/full/v16/i13/1369.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v16.i13.1369
1935年, Whipple首先施行胰头十二指肠切除术. 目前此手术已在世界各地广泛开展, 手术适应症扩大, 手术数量逐年增长, 随着手术技术提高, 手术后的并发症、死亡率明显下降[1]. 湖南省人民医院肝胆医院胰头癌施行胰头十二指肠切除的切除率95%, 1990-01/2007-12先后施行胰头十二指肠切除术604例, 术中平均失血量212 mL, 术中输血率4.7%, 平均手术时间6.1 h, 手术死亡率0.3%(2/604). 胰头十二指肠切除术是一种危险、复杂而安全的手术, 现以胰头癌为例, 介绍胰头十二指肠切除术中的几个问题.
胰头十二指肠切除术是腹部最复杂的手术之一, 对生理扰乱大, 应严格掌握手术指征、时机, 对此应"六亲不认", 要尽量减少阴性剖腹探查率. 因此, 术前对切除可能性的准确判断至关重要[2]. (1)临床表现: 年龄不是手术禁忌, 而顽固性的胸背部疼痛, 尤以夜间为剧者; 腹部可扪及胰肿块者; 出现腹水者多失去根治性切除的机会. 合并肺、心、肾功能不全者, 多难于承受本手术. (2)CT: 是目前判断胰头癌切除的可能性常用的重要手段. 以下情况提示难以切除: 胰头癌肿块直径>6 cm; 腹水; 肝内转移灶存在, 肠系膜血管周及腹主动脉旁淋巴结肿大、转移; 门静脉、肠系膜上静脉变形(血管阿米巴征), 受累的血管越长, 血管变形越明显, 手术越困难; 胰头癌块巨大, 门静脉、肠系膜上静脉位置推移越明显, 手术难度越大. (3)十二指肠乳头腺癌多能切除, 胰腺炎、胰腺结石多切除困难.
过"三关"即通过胰头与下腔静脉、腹主动脉, 胰头沟与肠系膜上静脉, 胰头沟与门静脉的间隙. 一般情况下能否通过"三关"是术中确定能否施行胰头十二指肠切除的标准. 过第一关: 98%的病例能顺利通过. 过第二关: (1)发现肠系膜上静脉是过第二关的关键步骤, 发现肠系膜上静脉的途径有5条, 其中常用途径2条: 经右路是显露肠系膜上静脉的捷径, 约85%的病例可获得满意的快速显现; 结肠中静脉是显露肠系膜上静脉的指路碑. (2)敞开肠系膜上静脉鞘, 是逆行沟通第二关的诀窍. (3)当逆行显露胰头沟内肠系膜上静脉困难时, 可顺行沟通门静脉与胰头沟间隙, 而后顺逆结合, 显现胰头沟内肠系膜上静脉段. 过第三关: 常因肝总动脉周围淋巴结肿大、胰腺及胆管炎症致使过第三关困难. (1)循肝固有动脉显现胃十二指肠动脉, 于其起始处予以结扎切断. (2)牵开或横断总胆管, 显现门静脉, 以直角弯钳紧贴门静脉前壁顺行沟通胃十二指肠动脉与门静脉间隙, 显现游离胃十二指肠动脉. (3)术者食指置于胰头沟上凹处门静脉作引导, 以大弯钳逆行沟通胰头沟.
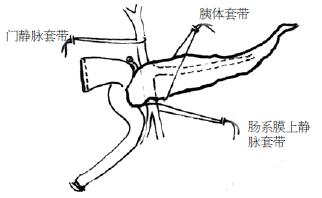
胰头十二指肠切除术中难免出血, 关键在于防止出血及出血时采用恰当方法止血. 防止出血: (1) 游离胰头十二指肠, 术者握其于手中, 是通过第二、三关的安全的手段, 是防止出血的重要措施; (2)胰头"区域围堰", 即在处理难于显现或难于游离的肠系膜上静脉、门静脉之前, 先将门静脉、肠系膜上静脉、脾静脉套带(图1), 便于在局部形成一无血区域, 使肠系膜上静脉、门静脉的显露剥离得以安全进行. 彭氏称为"胰门三头控制术"[3]; (3)一旦肠系膜上静脉、门静脉破裂出血, 宜先指压, 而不是在血泊里盲目钳夹, 否则将造成血管更大的损伤, 甚至不可收拾. 出血的部位不同, 止血的方法亦不同: (1)胰钩突汇入静脉撕裂出血. 胰钩突汇入静脉一般5-7支, 血管壁如塑料薄膜, 而且十分脆, 一旦撕裂, 出血较多, 这些血管周围多十分疏松, 宜结扎、切断. 出血后立即指压, 看清门静脉侧出血点, 以4-0号无损伤线缝扎. 胰腺侧出血点, 以圆针丝线"8"字缝扎. (2)门静脉、肠系膜上静脉撕裂出血. 立即指压局部, 看清出血点, 以血管艾利氏钳钳夹, 或心耳钳钳夹, 再以4-0号无损伤缝线, 缝扎止血. (3)断胰颈出血. 为防止出血, 胰头侧胰颈宜以7号圆针丝线作贯穿缝扎, 胰体尾侧分别以4号圆针丝线缝扎胰颈上下缘的胰腺背上下动脉, 以电刀断胰颈, 一般不出血, 少数出血可电凝, 亦可缝扎. (4)离断胰纤维板出血. 离断胰纤维板出血主要是胰十二指肠下动脉, 胰十二指肠下动脉一旦撕裂, 出血较猛, 而且挛缩, 处理不慎, 可损伤肠系膜上动脉, 致全部小肠缺血、坏死. 首先在于防止出血, 方法是: 术者(站左侧)左手握胰头向右牵拉纤维板, 助手持静脉拉钩将门静脉牵向左侧, 显露肠系膜上动脉并切开其动脉鞘, 在直视下钳夹或缝扎胰十二指肠下动脉, 再切断之; 一旦出血, 扪触、辨清肠系膜上动脉, 局部以血管艾利氏钳钳夹, 再以圆针丝线缝扎. 如果止血效果不好, 宜钳夹出血处肠系膜上动脉远近两端, 显露肠系膜上动脉及胰十二指肠下动脉的断端, 予以修补、缝扎; 肠系膜上静脉或门静脉毁损的长度<2 cm, 可作局部切除, 端-端吻合.
断胰颈: (1)约90%的病例过"三关"后断胰颈. 以圆针丝线缝扎胰颈的二侧, 以大圆刀片刮切或电凝切断; 95%的病例胰管在胰颈的中上1/3交界处, 粗大的胰管不要急于插入导管, 以免妨碍术野. 胰腺的导管插入的深度约为10 cm, 以可吸收肠线固定. 当胰管过分纤细, 找不到, 亦可不找. (2)胰头的良性病变. 只要辨清门静脉和肠系膜上静脉右侧缘, 在其联线的右侧以电凝切断, 化整为零, 再作胰颈的切除. 断胰纤维板: 显现剥离门静脉、肠系膜上静脉是断胰纤维板的前提, 断胰纤维板前一定要扪触清楚肠系膜上动脉、胰十二指肠下动脉, 离断胰纤维方法分"四边法"切断、钳夹法切断二种, 前者安全、出血少, 后者快捷.
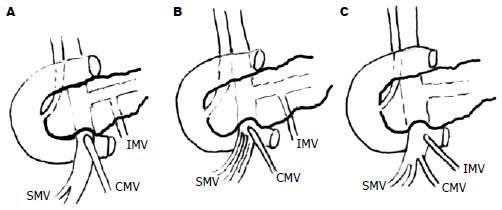
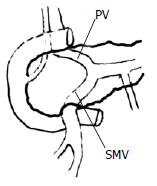
这里所涉及的脉管变异是指胰管、动脉、肠系膜上静脉、结肠中静脉、肠系膜下静脉的变异, 其总的发生率约为35%, 临床工作者必须熟悉这些变异情况. (1)胰管: 主要表现胰管位置的变异, 有5%(30/604)的病例胰管位于胰颈下1/3; 0.5%(3/604)胰颈部双胰管. (2)门静脉前壁为裸区, 但有3%(18/604)的患者有1支胰颈的静脉汇入门静脉前方. (3)肠系膜上静脉外科干长约3 cm, 肠系膜下静脉汇入脾静脉. 结肠中静脉于胰头沟下凹处汇入肠系膜上静脉, 约10%(61/604)的病例表现出变异(61/604): 肠系膜上静脉外科干短或消失; 肠系膜下静脉汇入肠系膜上静脉; 结肠中静脉汇入口远离胰头沟下凹(图2). (4)门静脉、肠系膜上静脉呈"弓"形, 这与胰头肿块的压迫推移相关(图3). (5)肝右动脉、胰腺动脉: 多数情况, 肝右动脉发自肝固有动脉, 胰动脉来自肝总动脉和肠系膜上动脉, 但变异很大. 临床上以肝右动脉发自肠系膜上动脉多见, 作者曾遇到一例肝固有动脉源自肠系膜上动脉的二根分支, 此二分支包绕肠系膜上静脉后合二为一行于胰颈的腹面, 于胰的上缘分为肝左动脉和肝右动脉, 术中险些将其行走于胰颈腹面的部分当胃十二指肠动脉结扎. 因此结扎、切断胃十二指肠动脉时, 一定要试夹、扪触是否继续有肝动脉的博动存在, 弄清动脉的来龙去脉后才作处理.
认真彻底地血管骨骼化, 能延长患者的生存期已成共识[4-7]. (1)胰头癌, 施胰头十二指肠切除. 血管骨骼化主要包括裸露门静脉、肝动脉、肠系膜上静脉外科干以及肠系膜上动脉. 剔除其周围的脂肪、淋巴结及纤维结缔组织, 甚至包括下腔静脉、腹主动脉、肝总动脉、腹腔动脉干、脾动脉的骨骼化[8]. (2)血管骨骼化, 一定要打开血管鞘, 剥去血管的"外衣", 骨骼化才方便易行. (3)门静脉骨骼化: 分开门静脉与肝固有动脉间的疏松结缔组织, 剥离裸露门静脉, 以线带牵开, 注意在门静脉左侧常有胃右静脉汇入, 应予以结扎、切断. (4)腹腔动脉干、肝总动脉、肝固有动脉及肝左右动脉骨骼化: 一般先打开肝固有动脉前壁的鞘膜, 紧贴血管壁剥离, 套以线带牵拉, 然后顺藤摸瓜裸露其他血管, 剔除周围的一切淋巴结、神经、脂肪组织. 注意作肝总动脉、腹腔动脉干骨骼化时, 辨清胰腺上缘, 仔细结扎淋巴结营养血管. (5)肠系膜上动脉清理: 为防止淋巴漏、乳糜腹水, 作者主张裸露肠系膜上动脉右侧. 具体操作应注意: 以静脉拉钩或线带分别将门静脉、肠系膜上静脉向左牵开, 以显露肠系膜上动脉; 切开肠系膜上动脉前壁血管鞘, 顺势剥离、裸露其右侧; 直视下看清胰十二指肠下动脉, 于起始部予以缝扎、切断.
胰头十二指肠切除后, 消化道重建的方式很多, 目前常用的方式是胰空肠或胰胃吻合、胆管空肠吻合及胃空肠吻合. (1)胰空肠或胰胃吻合: 我们1990年至今施行胰胃吻合180例、胰空肠吻合424例, 胰漏发生率各为1%, 两组无明显差别. 胰空肠吻合又分胰空肠端-端吻合和端侧吻合、胰胃为端侧吻合, 不管哪种方式吻合, 其成功的关键在胰残端一定要套入空肠或胃内, 胰管内置管外引流有助于防止胰漏的发生. (2)胆管空肠吻合: 胆管空肠吻合为端-侧吻合, 宜以无损伤缝线作一层、外翻、间断缝合, 只要情况允许, 胆管内无须一律放置T形管引流. 湖南省人民医院一组604例胰头十二指肠切除术, 胆管未放T形管者占11%(67/604). (3)胃空肠吻合: 可以吻合器进行, 但目前主要用手工吻合. 前者缩短手术时间, 后者节省住院经费. (4)消化道重建: 应注意采用微伤外科技术. 合理、正常使用医用创面封闭胶, 可有效地降低手术的并发症.
胰头十二指肠切除技术不断提高、完善, 许多过去认为无法切除的病例, 现亦可顺利进行, 所谓扩大根治术、超扩大根治术. 门静脉、肠系膜静脉切除吻合[9], 在适当的病例可以进行, 但"扩大根治或超根治术"并不延长患者的生存期. 加强科间协作, 综合治疗, 可延长患者的生存时间.
1935年, Whipple首先施行胰头十二指肠切除术. 随着手术技术提高, 手术后的并发症、死亡率明显下降. 目前, 此手术已在世界各地广泛开展, 但由于手术复杂和困难, 此手术仍然是一种危险的手术.
傅华群, 教授, 南昌大学第二附属医院普外科
过"三关"即通过胰头与下腔静脉、腹主动脉, 胰头沟与肠系膜上静脉, 胰头沟与门静脉的间隙. 一般情况下能否通过"三关"是术中确定能否施行胰头十二指肠切除的标准.
本文介绍十二指肠切除术中必须注意的一些关键问题, 为临床医生施行此手术提供借鉴.
本文总结了1990年至今行胰十二指肠切除术的临床经验, 实用性较强, 对临床工作具有指导价值, 但表达过于口语化.
编辑: 李军亮 电编:何基才
| 3. | 彭 淑牖, 洪 德飞, 许 斌, 严 力锋, 王 建伟, 刘 颖斌, 李 江涛, 钱 浩然, 牟 一平, 蔡 秀军. 简易胰门三头控制技术在困难型胰十二指肠切除术中的应用. 中华外科杂志. 2007;45:1466-1468. |
| 4. | Pawlik TM, Gleisner AL, Cameron JL, Winter JM, Assumpcao L, Lillemoe KD, Wolfgang C, Hruban RH, Schulick RD, Yeo CJ. Prognostic relevance of lymph node ratio following pancreaticoduodenectomy for pancreatic cancer. Surgery. 2007;141:610-618. [PubMed] [DOI] |
| 5. | Doi R, Kami K, Ito D, Fujimoto K, Kawaguchi Y, Wada M, Kogire M, Hosotani R, Imamura M, Uemoto S. Prognostic implication of para-aortic lymph node metastasis in resectable pancreatic cancer. World J Surg. 2007;31:147-154. [PubMed] [DOI] |
| 6. | Todoroki T, Koike N, Morishita Y, Kawamoto T, Ohkohchi N, Shoda J, Fukuda Y, Takahashi H. Patterns and predictors of failure after curative resections of carcinoma of the ampulla of Vater. Ann Surg Oncol. 2003;10:1176-1183. [PubMed] [DOI] |
| 7. | Murakami Y, Uemura K, Hayashidani Y, Sudo T, Ohge H, Sueda T. Pancreatoduodenectomy for distal cholangiocarcinoma: prognostic impact of lymph node metastasis. World J Surg. 2007;31:337-342; discussion 343-344. [PubMed] [DOI] |