修回日期: 2004-12-21
接受日期: 2005-01-08
在线出版日期: 2005-02-15
目的: 利用人类幽门螺杆菌(H. pylori)感染的小鼠模型研究黏附素保守区(AB)疫苗在预防与治疗H. pylori感染的作用.
方法: 实验分为预防与治疗两部分. 预防部分把实验动物无特定致病菌C57BL/6小白鼠分成4组, 分别通过灌胃方法给予AB(100mg)加CT(2 mg)、生理盐水、单纯AB(100 mg)、单纯CT(2 mg), 1次/wk, 共4次. 2 wk后再用活H. pylori灌胃, 再4 wk后处死动物. 治疗部分把已感染H. pylori的小白鼠分成4组, 分组与治疗方法同预防部分, 治疗结束后4 wk处死动物, 取胃黏膜行半定量细菌培养检查H. pylori情况.
结果: 预防实验的保护率分别为AB加CT61.5%(16/26), 单纯AB、单纯CT和PBS保护率均为0.AB加CT治疗组H. pylori根除率为: 38.5%(10/26), 生理盐水组、单纯AB、单纯CT组均无治疗作用. 治疗组未根除H. pylori的小鼠, 疫苗组H. pylori的定植密度明显低于其他4组(P<0.05).
结论: 由AB加免疫佐剂组成的口服疫苗, 不仅有预防H. pylori感染的作用, 同时也有根除已感染的H. pylori的作用. AB可用于H. pylori疫苗的研制.
引文著录: 白杨, 梁燕玲, 刘秀丽, 施理, 王继德, 张兆山, 周殿元, 张亚历. 黏附素保守区疫苗防治鼠幽门螺杆菌感染. 世界华人消化杂志 2005; 13(4): 468-471
Revised: December 21, 2004
Accepted: January 8, 2005
Published online: February 15, 2005
AIM: To investigate the effects of Helicobacter pylori (H. pylori) adhesin conservatory region vaccine in the prevention and treatment of H. pylori infection in a mouse model.
METHODS: The study was divided into two parts. In the first part, the specific germ free C57BL/6 mice were orally immunized with vaccine (100 mg) plus cholera toxin (CT) (2 mg), vaccine (100 mg), CT(2 mg), or PBS once a week for four weeks. Two weeks after the last immunization, all animals were challenged by live H. pylori, and were sacrificed 4 weeks after the challenge. In the second part, H. pylori infected mice were treated in the same way as in the first part. Four weeks after the last treatment, all animals were sacrificed, and the stomach biopsies were collected to detect H. pylori by the semi-quantitative bacterial culture assay.
RESULTS: The prophylactic rate from H. pylori infection was 61.5% (16/26) in the mice immunized with vaccine plus CT. The eradication rate of the vaccine plus CT group was 38.5% (10/26). No protective or therapeutic effect was observed in all other 3 groups. The H. pylori colony density in the vaccine plus CT group was significantly lower than those inother three groups in the second part of experiment (P<0.05).
CONCLUSION: The vaccine consisting of adhesin conservatory region and adjuvant is not only effective in the prevention, but also in the treatment of H. pylori infection.
- Citation: Bai Y, Liang YL, Liu XL, Shi L, Wang JD, Zhang ZS, Zhou DY, Zhang YL. Prevention and treatment of Helicobacter pylori infection with adhesin conservatory region vaccine: an animal model study. Shijie Huaren Xiaohua Zazhi 2005; 13(4): 468-471
- URL: https://www.wjgnet.com/1009-3079/full/v13/i4/468.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v13.i4.468
我们已构建了幽门螺杆菌(Helicobacter pylori, H. pylori)黏附素保守区AB的高效原核表达体系[1-2], 表达产物经过纯化后已在体外探讨了他的安全性、免疫原性和生物活性[3-4]. 现利用H. pylori感染的小鼠模型研究黏附素保守区(AB)疫苗在预防与治疗H. pylori感染的作用, 为黏附素源H. pylori疫苗的研制奠定基础.
幽门螺杆菌ss1株为本所保存, 无特定病原体(specific-pathogen free, SPF)C57BL/6雄性小鼠140只, 4周龄, 12-13 g, 饲养条件符合2级动物要求. 重组黏附素保守区rAB, 快速尿素酶试剂由本所制备; 其余试剂为国产分析纯.
1.1.1 H. pylori的培养与鉴定:H. pylori的固体培养: 取冷冻保存的H. pylori菌种一环于固体培养基上连续划线接种, 2 h内置厌氧培养箱, 37 ℃微需氧环境(50 mL/L O2, 100 mL/L CO2, 850 mL/L N2)中培养72 h, 湿度保持95%以上. H. pylori的菌落呈圆形, 凸起、光滑、灰白色、半透明, 直径0.2-0.8 mm. 液体培养: 取固体培养基上生长的H. pylori菌落至布氏肉汤中, 抽滤瓶抽气换气2次以满足微需氧条件, 恒温振荡培养120 r/min培养48-72 h.H. pylori的鉴定包括菌落形态、涂片观察(包括革兰染色观察细菌形态、暗视野观察细菌活力)、尿素酶实验(将自制尿素酶试剂加入含鼠胃组织的96孔板各孔中, 37 ℃作用5 min, 当有H. pylori感染时试剂由黄色变为红色). 灌胃用H. pylori的要求: 革兰染色阴性, 形态呈S形、螺旋形、杆状, 暗视野下有活力, 不含杂菌, 密度约为1012/L.
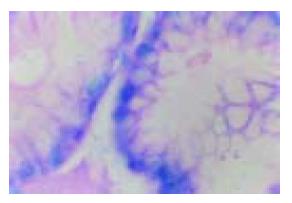
1.1.2 H. pylori感染小鼠模型的建立: 采用文献[5]方法驯化H. pylori ss1株, 分离可在小鼠胃内稳定定植的H. pylori ss1株, 固体培养2-3 d, 菌落经鉴定后用布氏肉汤洗下, 调整细菌浓度至1012CFU/L, 每只小鼠灌胃0.5 mL(约1012/L). 所有动物灌胃前禁食12 h, 禁水4 h. 灌胃后禁食2 h. 连续5次, 1 wk完成. 采用胃管法以确保H. pylori灌入胃内. 末次灌胃后4 wk随机处死5只小鼠, 剖腹取胃, 沿纵轴将胃切为三部分, 一份行快速尿素酶试验, 一份置40 g/L甲醛固定供组织学检查, 一份细菌培养, 检查是否感染H. pylori. 经尿素酶实验、组织病理学检查(图1)及细菌培养证实全部感染H. pylori. 细菌培养发现H. pylori的定植密度为105-6/g.
1.2.1 免疫预防实验: 共设4组. 单价黏附素保守区疫苗组经口喂饲黏附素保守区100 mg加CT2 mg; 单纯黏附素保守区组经口喂饲黏附素保守区100 mg; 单纯CT组经口喂饲CT2 mg; PBS组经口喂饲PBS 200 mL. 免疫前小鼠禁食12 h, 禁水4 h. 每只小鼠先用30 g/L的碳酸氢钠100 mL灌胃以中和胃酸, 10 min后分别按上述分组灌胃, 30 min后再给小鼠提供水和食物. 隔周免疫, 加强免疫3次, 剂量同前. 末次接种后2 wk按前述方法接种H. pyloriSS1. 末次接种H. pylori SS1后4 wk处死动物, 去除前胃, 余胃黏膜行半定量细菌培养法检查.
1.2.2 免疫治疗实验: 将前述已鉴定感染H. pylori的小鼠分成4组. 分组、治疗剂量与方法同免疫预防实验, 1次/wk, 共4次. 治疗结束后4 wk处理动物, 取材方法同上. 免疫预防和治疗后幽门螺杆菌根除的鉴定采用半定量细菌培养法[6].
统计学处理 采用SPSS10.0软件, 行χ2检验, P<0.05为有显著性差异.
胃组织培养H. pylori为阴性者定为完全保护. 黏附素保守区疫苗组的保护率为61.5%(16/26), 其他3组保护率均为0%, 其差异具有显著性(P<0.05).
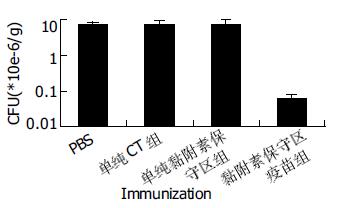
胃组织培养H. pylori为阴性者定为根除. 黏附素保守区疫苗组根的根除率为38.50 mL/L, 显著高于其他3组(0%, 0%, 0%, P<0.05). 未根除H. pylori的小鼠, 我们进行了H. pylori定植密度的分析, 结果发现疫苗治疗组H. pylori的定植密度明显低于其他3组(图2), 其差异有显著性(P<0.05).
广泛用于临床根除H. pylori的手段是抗菌治疗有一定的疗效[7-9], 但所需的费用是一项沉重的医疗负担. 因此, 世界各国政府和企业为H. pylori的防治研究, 特别是为既有治疗又有预防作用的H. pylori疫苗的研制投入了大量经费. 因为谁率先研制出H. pylori疫苗, 谁就将抢先占领治疗H. pylori感染所面对的数百亿的市场. 除了上述可观的经济效益, 还会有预防数以亿计的消化性溃疡、MALT淋巴瘤及胃腺癌发生所带来的巨大的社会效益. 目前国内外已有全菌超声抗原和以尿素酶B、过氧化氢酶等为主的多种基因重组抗原作为疫苗候选抗原[10-12]. 但前者由于成分复杂、具有潜在毒副作用而渐遭淘汰; 后者尽管大多已被现有资料证明是有效的疫苗抗原, 但单独使用作为疫苗是不够的. 因此, 必须寻找其他有效抗原成分或研制多价疫苗防治H. pylori感染. 目前采用的基因重组抗原基本上着眼于阻断H. pylori的毒力因素, 而与H. pylori定植密切相关的黏附素评价较少. 如从黏附素出发寻找保护性抗原也许是一种有益的尝试. 目前文献报道的H. pylori黏附素较多, 其中已经证实的有四种[13-15], 包括迄今为止唯一明确受体的H. pylori黏附素BabA, 和经体外黏附及其相应抗体的抑制实验证明的黏附素AlpA、AlpB和HopZ; 然而这四种黏附素并不是存在于所有菌株中, 如BabA存在于CagA致病岛阳性的菌株中, 而且他们在不同的菌株中存在一定程度的变异, 因此究竟选取哪种或哪些黏附素一直是困扰我们的问题. 我们以前通过对4种黏附素进行同源性分析, 发现了保守区, 并对其进行克隆、表达、纯化和鉴定. 在此基础上, 评价了针对H. pylori黏附因素的黏附素保守区构成疫苗的预防和治疗效果. 动物实验表明, 单价黏附素保守区疫苗的H. pylori的完全保护率和根除率分别为61.50 mL/L和38.50 mL/L, 其中治疗组即使未根除的小鼠, 其H. pylori定植密度也有明显的降低(P<0.05), 表明黏附素保守区可用于H. pylori疫苗侯选抗原. 这一侯选抗原的研制既是对寻找针对H. pylori黏附因素有效抗原的探索, 又为研制针对H. pylori多种因素的多价疫苗奠定了基础.
在H. pylori保护率和根除率的研究中, 我们采用了细菌培养结果作为唯一的评价标准, 而不是常用的尿素酶实验和组织病理学检查结果, 这也可能是本研究保护率和根除率较其他报道低的缘故. 因为在建立H. pylori感染小鼠模型的预实验中, 我们发现接种H. pylori 1 wk后的部分小鼠, 细菌培养阳性, 而尿素酶实验和组织病理学检测结果阴性. 是否细菌培养的敏感性高于尿素酶实验和组织病理学检测呢?张振华 et al发现尿素酶实验形成阳性需要的细菌浓度是细菌培养阳性的100-1 000倍; 并且由于试剂、技术以及胃内存在着产尿素酶杂菌的原因, 与细菌培养相比, 其还存在着较高的假阳性. 组织病理学检查也存在着上述问题, 特别是在H. pylori量较少时, 仅凭形态特征与胃内可能出现的成百上千种其他杂菌区别是非常困难的, 甚至是不可能的. 所以, 作者认为, 就敏感性与特异性而言, 金标准只有一个, 就是细菌培养. 国外学者也研究了各种评价H. pylori定植方法的敏感性[16-21], 结果表明, 尿素酶实验和组织学检查显示的9只细菌阴性的免疫小鼠, 细菌培养检测均呈阳性. 尿素酶试验的敏感性与组织学检测相同, 其敏感性大约是每克胃组织105细菌; 细菌培养的敏感性高于尿素酶实验和组织病理学检测. 因此, 我们选用细菌培养作为评价H. pylori定植的唯一标准. 我们仅是对H. pylori黏附素源疫苗的初步尝试, 未来H. pylori疫苗可能是针对H. pylori多种因素[22-29], 包括过氧化氢酶、尿素酶B亚单位、黏附素保守区等构成的多价疫苗, 有关这方面的研究, 我们的实验正在进行中.
编辑: 潘伯荣 审读:张海宁
| 2. | 白 杨, 但 汉雷, 王 继德, 张 兆山, Odenbreit S, 周 殿元, 张 亚历. 幽门螺杆菌AlpA基因中四种黏附素基因保守 区的克隆、表达、纯化及鉴定. 生物化学与生物物理进展. 2002;29:922-926. |
| 4. | 白 杨, 张 亚历, 陈 烨, 王 继德, 周 殿元. 幽门螺杆菌黏附素保守区蛋白的免疫原性、安全性和黏附作用的体外评价. 生物化学与生物物理进展. 2003;30:422-426. |
| 5. | Marchetti M, Aricò B, Burroni D, Figura N, Rappuoli R, Ghiara P. Development of a mouse model of Helicobacter pylori infection that mimics human disease. Science. 1995;267:1655-1658. [PubMed] [DOI] |
| 6. | Sutton P, Danon SJ, Walker M, Thompson LJ, Wilson J, Kosaka T, Lee A. Post-immunisation gastritis and Helicobacter infection in the mouse: a long term study. Gut. 2001;49:467-473. [PubMed] [DOI] |
| 10. | Lin HJ, Xue J, Bai Y, Wang JD, Zhang YL, Zhou DY. Pathogenicty and immune prophylaxis of cag pathogenicity island gene knockout homogenic mutants. World J Gastroenterol. 2004;10:3289-3291. [PubMed] [DOI] |
| 11. | Bai Y, Li LR, Wang JD, Chen Y, Jin JF, Zhang ZS, Zhou DY, Zhang YL. Expression of Helicobacter pylori Hsp60 protein and its immunogenicity. World J Gastroenterol. 2003;9:2711-2714. [PubMed] [DOI] |
| 12. | Bai Y, Zhang YL, Jin JF, Wang JD, Zhang ZS, Zhou DY. Recombinant Helicobacter pylori catalase. World J Gastroenterol. 2003;9:1119-1122. [PubMed] [DOI] |
| 15. | Bai Y, Zhang YL, Wang JD, Zhang ZS, Zhou DY. Construction of attenuated Salmonella typhimurium Strain expressing Helicobacter pylori conservative region of adhesin antigen and its immunogenicity. World J Gastroenterol. 2004;10:2498-2502. [PubMed] [DOI] |
| 16. | Graham DY, Kudo M, Reddy R, Opekun AR. Practical rapid, minimally invasive, reliable nonendoscopic method to obtain Helicobacter pylori for culture. Helicobacter. 2005;10:1-3. [PubMed] [DOI] |
| 17. | Lee A. Animal models for host-pathogen interaction studies. Br Med Bull. 1998;54:163-173. [PubMed] [DOI] |
| 18. | Panthel K, Faller G, Haas R. Colonization of C57BL/6J and BALB/c wild-type and knockout mice with Helicobacter pylori: effect of vaccination and implications for innate and acquired immunity. Infect Immun. 2003;71:794-800. [PubMed] [DOI] |
| 19. | Lucas B, Bumann D, Walduck A, Koesling J, Develioglu L, Meyer TF, Aebischer T. Adoptive transfer of CD4+ T cells specific for subunit A of Helicobacter pylori urease reduces H. pylori stomach colonization in mice in the absence of interleukin-4 (IL-4)/IL-13 receptor signaling. Infect Immun. 2001;69:1714-1721. [PubMed] [DOI] |
| 20. | Sutton P, Wilson J, Lee A. Further development of the Helicobacter pylori mouse vaccination model. Vaccine. 2000;18:2677-2685. [PubMed] [DOI] |
| 21. | Del Giudice G, Ghiara P, Rappuoli R. Experimental model of Helicobacter pylori infection. Ital J Gastroenterol Hepatol. 1998;30 Suppl 3:S261-S263. [PubMed] |
| 22. | Nomura S, Suzuki H, Masaoka T, Kurabayashi K, Ishii H, Kitajima M, Nomoto K, Hibi T. Effect of dietary anti-urease immunoglobulin Y on Helicobacter pylori infection in Mongolian gerbils. Helicobacter. 2005;10:43-52. [PubMed] [DOI] |
| 23. | Gottwein JM, Blanchard TG, Targoni OS, Eisenberg JC, Zagorski BM, Redline RW, Nedrud JG, Tary-Lehmann M, Lehmann PV, Czinn SJ. Protective anti-Helicobacter immunity is induced with aluminum hydroxide or complete Freund's adjuvant by systemic immunization. J Infect Dis. 2001;184:308-314. [PubMed] [DOI] |
| 24. | Ozpolat B, Rao XM, Lachman LB, Osato MS, Graham DY. Quantitative and bioluminescent assay to measure efficacy of conventional and DNA vaccinations against Helicobacter pylori. Comb Chem High Throughput Screen. 2000;3:289-302. [PubMed] [DOI] |
| 26. | Messina GA, Torriero AA, De Vito IE, Olsina RA, Raba J. Continuous-flow/stopped-flow system using an immunobiosensor for quantification of human serum IgG antibodies to Helicobacter pylori. Anal Biochem. 2005;337:195-202. [PubMed] [DOI] |
| 27. | Calvet X. [Helicobacter pylori eradication treatment in non-ulcerous disease]. Gastroenterol Hepatol. 2005;28:40-46. [PubMed] [DOI] |
| 28. | Veneri D, Franchini M. Onset of idiopathic thrombocythemia after Helicobacter pylori eradication. Helicobacter. 2005;10:95. [PubMed] [DOI] |
| 29. | Pearce MS, Steele JG, Campbell DI, Thomas JE. Tooth loss and Helicobacter pylori seropositivity: the Newcastle Thousand Families Cohort Study at age 49-51 years. Helicobacter. 2005;10:90-94. [PubMed] [DOI] |