修回日期: 2006-03-25
接受日期: 2006-04-01
在线出版日期: 2005-05-15
目的: 探讨彩色多普勒超声(CDI)在原位肝移植术后对移植肝血流动力学变化及并发症的诊断价值.
方法: 术后应用CDI连续观察15例原位肝移植患者移植肝脏形态学变化, 肝动脉峰值流速(HAmax)、门静脉及肝静脉平均流速(PVmean, HVmean)等指标, 并以30名健康成人男性肝脏的血流动力学参数作为正常对照组.
结果: 术后1 wk内, HAmax较正常人低(P<0.05), PVmean较正常人快(P<0.05), 2 wk以后逐渐恢复正常; 肝移植术后早期的常见并发症如肝动脉血栓形成、免疫排斥反应和胆道并发症等均有其较为特殊的声像图特征; 超声引导下进行的肝脏穿刺活组织检查结果更是诊断的金标准.
结论: CDI技术对了解肝移植术后移植肝的灌注情况, 及早发现肝移植术后早期的并发症有重要意义.
引文著录: 王晓蕾, 周显礼, 侯秀娟, 王洪波, 王虹, 刘爱武. 彩色多普勒超声在原位肝移植术后的临床应用价值. 世界华人消化杂志 2005; 13(10): 1251-1253
Revised: March 25, 2006
Accepted: April 1, 2006
Published online: May 15, 2005
N/A
- Citation: N/A. N/A. Shijie Huaren Xiaohua Zazhi 2005; 13(10): 1251-1253
- URL: https://www.wjgnet.com/1009-3079/full/v13/i10/1251.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v13.i10.1251
肝移植是目前终末期肝病最理想的治疗方法.移植术后血供情况的好坏直接影响移植肝的存活, 术后早期的一些并发症亦严重影响患者术后长期生存.如何尽早发现从而正确及时地解决这些问题一直是临床关注的焦点.我们采用彩色多普勒超声技术对我院自1994-05/2004-04期间施行的15例肝移植患者进行术后移植肝的形态学及血流动力学监测, 现分析报告如下:
将我院自1994-05/2004-04期间施行的15例原位肝移植患者作为研究对象, 病例均为男性, 年龄19-55岁, 平均年龄37岁, 其中乙型肝炎肝硬化9例, 肝豆状核变性2例, 亚急性肝坏死1例, 乙型肝炎肝硬化肝癌3例, 10例获得长期生存, 生存时间最长者接近8 a.
采用西门子Q-2000及西门子SONOLINE Elegra彩色多普勒超声诊断仪, 探头频率3.5MHz, 观察移植肝脏、脾脏的大小、形态及实质回声变化; 肝动脉、肝静脉、门静脉、下腔静脉的内径、内膜情况、吻合口通畅程度、流速、阻力指数及血流频谱形态; 胆道系统的吻合口通畅程度及胆总管内径.并以30名健康成人男性肝脏的血流动力学参数作为正常对照组.肝移植术后12 h内检查一次, 之后1 wk内每天进行1次, 1 wk后根据情况随时进行检查, 记录检查结果.为了避免人为操作所致的误差, 对患者的血流动力学进行检测时要采取相对固定的取样条件, 我们将血流取样线的角度固定在25-30度.
正常对照组肝脏血流参数分别为: HAmax: 72.47±15.41 cm/s; PVmean: 16.39±3.27 cm/s; HVmean: 27.82±3.76 cm/s.在术后1 wk内肝脏移植组的HAmax低于正常对照组(64.45±16.32 vs 72.47±15.41, P<0.05); 术后1 wk内移植肝脏组的PVmean高于正常对照组(19.01±3.46 vs 16.39±3.27, P<0.05); 移植肝脏组的HVmean与正常对照组相比无明显差异.2 wk后, HA、PV和HV的血流速度基本上趋于正常(表1).
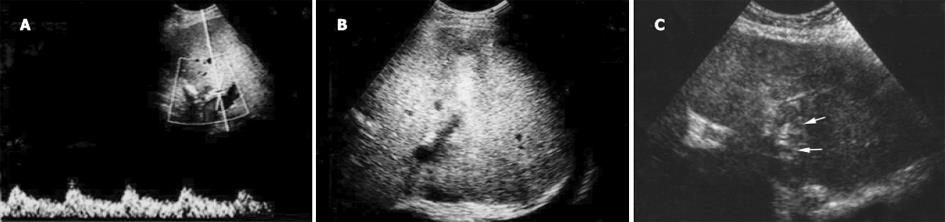
2.2.1 CDI诊断肝动脉血栓: 本组共发生肝动脉血栓2例, 分别于术后第2-4 d行CDI检查发现肝动脉吻合口处呈现花色血流或捕捉不到明显的血流信号, HAmax由最高70.70 cm/s降至最低23.3 cm/s(图1A).缺血严重时, 肝内可出现低回声梗塞灶(图1B).1例肝动脉血栓患者由于侧枝循环的建立和门静脉的代偿, 移植肝得以存活, 门静脉扩张, 血流呈现动脉化趋势(图1C).
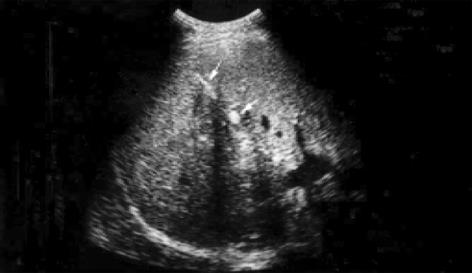
2.2.2 CDI诊断胆道并发症: 本组术后发生胆道缺血性狭窄及扩张1例, 超声表现为胆管局限轻度扩张.经十二指肠逆行胰胆管造影(ERCP): 肝左叶胆管树可见局限性狭窄段和扩张段.胆泥及胆石症1例, 超声检查发现胆管内可见点状及片状的稍高回声及胆管内呈条状及团状的结石强回声, 其远端胆管局限轻度扩张(图2).
肝脏移植术是目前治疗终末期肝病唯一且有效的手段.肝移植术后, 移植肝的血供情况是其能否成活的前提[1].二维彩色多普勒血流显像能显示血流的方向、血流速度和血流状态等重要信息[2].
我们通过研究发现, 肝移植术后早期(2 wk内)HAmax偏低, PVmean偏高, 1 wk内表现得更为明显, 2 wk以后逐渐趋于正常.这与国内文献[3-4]报道的结论相一致.朱栋晓et al[4]认为, 这种情况的出现可能是由于肝动脉口径较门静脉细, 吻合口早期水肿导致血流不畅, 门静脉血流代偿性增多, 以保证移植肝的血运.随着肝动脉吻合口水肿消失, 血流增多, 门静脉供血也恢复正常.
动脉血栓是肝脏移植术中最严重也是最常见的血管并发症, 其成人发生率为1.6-8.0%[5].肝动脉并发症的早期的临床症状极不典型[6].CDI检查是观察肝动脉血流的最好方式, 在肝移植术后, 肝固有动脉的显示率为93.3%, 肝门部肝动脉的显示率为94.5%, 右前支显示率为65.3%[7].杨扬et al[8]通过对180例肝移植患者进行分析发现其对肝动脉并发症诊断的敏感度和特异度分别为87.5%和95.3%.因此肝动脉血栓多由彩超首先发现.胡淑芳et al认为, 肝动脉血流速度低于28 cm/s, 血流速度呈扑动状, 肝动脉阻力指数增加达0.78, 或肝动脉出现反向血流, 门静脉血流速度加快, 提示肝动脉血栓形成[9].本组1例患者术后首次检查HAmax 70.70 cm/s, RI0.55, 血流频谱形态正常, 术后第4 d发现肝动脉血栓形成, 这说明, 即使肝移植术后初始的HAmax正常也绝不能掉以轻心.彩超诊断肝动脉血栓的同时, 发现患者都伴随有门静脉内径增宽和流速的明显增快, 其机制可能是动脉血供减少时门静脉代偿性供血.移植肝能否在短时间内建立有效的侧支循环是决定移植肝命运的主要因素.侧支循环的建立取决于两个条件: (1)血栓形成发生的时间; (2)血栓形成开始至完全阻塞的时间.前者的时间越晚后者的时间越长则形成侧支循环的可能性就越大[10].本组1例尽管发生肝动脉血栓的时间不是很晚(术后第4 d), 但是血栓形成至完全阻塞管腔的过程较长(术后第71 d肝动脉造影未见显影), 这就确保了门静脉代偿机制的有效建立, 呈现动脉化趋势, 从而改善了移植肝的血液供应, 使患者避免了再次移植的结局并获得长期满意存活.
急性排斥反应是引起移植肝早期肝功能损害的常见原因之一, 90%的患者急性排斥发生于肝移植术后7-14 d.本组6例急性排斥反应期的患者均出现肝静脉血流频谱三相波消失.这与邹如海[11]的结果相同, 但Zalasin et al[12]却认为异常的肝静脉频谱不能作为急性排斥反应的诊断依据.我们的经验是, 不能排除肝静脉频谱的变化是观察急性排斥反应的一个有效指标, 当CDI检查发现移植肝有上述影像学改变时, 即刻在超声引导下进行肝脏穿刺组织学检查, 将影像学、组织形态学和肝酶学指标综合起来分析, 会大大提高急性排斥反应的正确诊断率.
胆道并发症也是肝移植术后重要的死亡原因之一, 主要有胆漏、胆道狭窄及梗阻、胆道感染以及胆泥与胆结石形成.缺血再灌注损伤与肝动脉供血不足是导致胆道并发症的主要原因[13].肝动脉是营养肝门输出管道、肝内胆管、肝门结缔组织、淋巴结和门静脉壁的唯一血供来源, 因此任何原因引起的肝动脉供血不足, 均可引起胆管黏膜的缺血损伤.
肝脏穿刺组织学检查是肝移植术后并发症鉴别诊断的金标准.在超声引导下进行可以选择最佳路径, 最低限度地减少肝穿并发症.本组的肝脏穿刺组织学检查均在超声引导下进行, 无1例发生出血、胆漏、气胸、肠道损伤等并发症.
编辑: 张海宁
| 1. | 黄 祖发, 赵 于军, 叶 启发, 朱 晒红, 成 柯, 张 懋祖, 明 英姿, 刘 斌, 杨 文龙. 肝硬化患者原位肝移植术后的内脏循环血流动力学变化. 中国普通外科杂志. 2004;13:602-605. |
| 6. | Bhattacharjya S, Gunson BK, Mirza DF, Mayer DA, Buckels JA, McMaster P, Neuberger GM. Delayed hepatic artery thrombosis in adult orthotopic liver transplantation-a 12 year experience. Transplantation. 2001;71:1592-1596. [PubMed] [DOI] |
| 12. | Zalasin S, Shapiro RS, Glajchen N, Stancato-Pasik A. Liver transplant rejection: value of hepatic vein Doppler waveform analysis. Abdom Imaging. 1998;23:427-430. [PubMed] [DOI] |
| 13. | Sanchez-Urdazpal L, Gores GJ, Ward EM, Maus TP, Wahlstrom HE, Moore SB, Wiesner RH, Krom RA. Ischemic-type biliary complications after orthotopic liver transplantation. Hepatology. 1992;16:49-53. [PubMed] [DOI] |