修回日期: 2003-04-11
接受日期: 2003-04-20
在线出版日期: 2004-07-15
目的: 了解昆明汉族儿童中幽门螺杆菌(H. pylori)感染率及其HLA-DQA1免疫遗传学特征.
方法: 用胶体金标免疫渗滤法检测153名6-14岁的学生血H. pylori-IgG抗体. 并用聚合酶链反应-序列特异性引物(PCR-SSP)技术对以血清学试验及13C尿素呼气试验确诊的34例H. pylori感染儿童及37例无H. pylori感染儿童进行HLA-DQA1基因分型.
结果: 昆明儿童H. pylori 感染率为34.5%, 其HLA-DQA1*0103等位基因频率明显高于无H. pylori感染儿童(29.41% vs 9.46%, P = 0.002, Pc = 0.028, OR = 3.988, 95%CI: 1.562-10.180); 而H. pylori 感染儿童HLA-DQA1*0302等位基因频率低于无H. pylori 感染儿童(19.12% vs 33.78%, P = 0.049, OR = 0.463, 95%CI: 0.214-1.003), 但经等位基因多项比较校正, 差异消失(Pc = 0.686).
结论: 昆明汉族儿童H. pylori感染率较高. 他们在HLA-DQA1位点上与无H. pylori 感染儿童存在免疫遗传学差异, HLA-DQA1*0103基因可能是H. pylori感染的易感基因; 而DQA1*0302基因则是否具有免疫抵抗作用, 需要进一步研究.
引文著录: 黄永坤, 戚勤, 郝萍, 李海林, 文革生, 周丽芳. 幽门螺杆菌感染儿童HLA-DQA1的免疫遗传学特征. 世界华人消化杂志 2004; 12(7): 1735-1737
Revised: April 11, 2003
Accepted: April 20, 2003
Published online: July 15, 2004
N/A
- Citation: N/A. N/A. Shijie Huaren Xiaohua Zazhi 2004; 12(7): 1735-1737
- URL: https://www.wjgnet.com/1009-3079/full/v12/i7/1735.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v12.i7.1735
幽门螺杆菌(Helicobacter pylori, H. pylori)与慢性活动性胃炎、消化性溃疡、胃黏膜相关淋巴组织(MALT)淋巴瘤及胃腺癌密切相关[1]. 世界上至少有半数以上的人口有幽门螺杆菌感染, 但其中仅很少的一部分表现出明显的临床疾病状态, 其原因仍不清楚[2]. 许多研究认为这除了与H. pylori菌株的毒力高低、环境因素有关外, 还与宿主的免疫遗传因素有关[3]. 我们用聚合酶链反应-序列特异性引物(polymerase chain reaction-sequence specific primers, PCR-SSP)技术对云南昆明H. pylori感染汉族儿童及健康汉族儿童进行了HLA-DQA1基因分型, 旨在探讨在HLA-DQA1位点上是否存在与儿童H. pylori感染相关的易感基因和抵抗基因, 从而了解人类是否存在易感H. pylori的免疫遗传因素.
H. pylori 感染的诊断参照中华医学会儿科学分会感染消化学组制订的《小儿慢性胃炎、消化性溃疡胃镜诊断标准》[4]. 全部研究对象均来自于昆明市某中心小学三代内无血缘关系的153名汉族儿童. 年龄6-14岁. 三代均为汉族, 在昆明市出生并且生活4年以上, 无慢性腹痛、消化不良、胃炎、消化性溃疡等H. pylori感染相关疾病史及严重心、肺、肾、肝、神经、营养、免疫缺陷病史, 近期无激素、抗生素、铋剂、质子泵阻滞剂使用史(>4 wk), 相互间无亲缘关系. 整群抽样的方法取静脉血2-3 mL, 分离血浆行 H. pylori-IgG 检测(试剂盒由福建省蓝波生物技术研究所提供), 并分别从58名血清学阳性和95名血清学阴性儿童中, 随机各抽出40例行 13C尿素呼气试验(13C-UBT试剂盒由北京嘉汇彬医药技术有限公司提供). 两项皆为阳性者, 诊断为H. pylori感染, 列为实验组的有34例; 二者均为阴性者则为非H. pylori感染儿童, 列为对照组的有37例. 实验组平均年龄9.6±2.1岁, 健康对照组平均年龄9.7岁±2.3岁, 男女1:1; 两组年龄、性别均无差异(P>0.05). 血液基因组DNA提取试剂盒(美国MO BIO Laboratories 公司提供), DQA SSP UNITRAY试剂盒(包括DQA1 23对序列特异性引物和1个污染对照. 试剂盒由美国PEL-FREEZE SYSTEMS 公司提供), DL2000、Taq聚合酶、琼脂糖(芬兰产)和溴乙锭均由大连宝生物公司提供.
血H. pylori-IgG抗体和13C-UBT的检测分别按试剂盒的操作说明进行. 基因组DNA制备采用血液基因组DNA提取试剂盒, 在常温下快速提取实验组34例和对照组37例的基因组DNA, 提取方法按试剂盒所附说明进行. 提取的DNA用分光光度仪测定浓度和纯度, A260/280nm应在1.6-1.8; 浓度在60 mg/L以上. 提取的DNA于-20 ℃保存备用. HLA-DQA1基因分型采用SSP UNITRAY试剂盒扩增HLA-DQA1 DNA片段, PCR反应体系, 循环条件及操作方法均按所附说明. 扩增产物进行20 g/L含溴乙锭的琼脂糖凝胶电泳(130V, 13 min), 结果判断借助其提供的专用读板纸在凝胶成像仪和紫外灯判读并成像. 要求分子796 bp必须存在, 各阳性条带必须与规定的相应分子对应.
统计学处理 用直接计算法统计H. pylori感染率及实验组和对照组HLA-DQA1各等位基因的基因频率. 男女儿童 H. pylori感染率比较及实验组和对照组间HLA-DQA1等位基因的比较均用2×2表作x2检验, 等位基因比较的P值行等位基因多项比较校正(同一位点需比较的等位基因数乘P值, 即Pc), 以Pc<0.05判定差异有显著性意义.
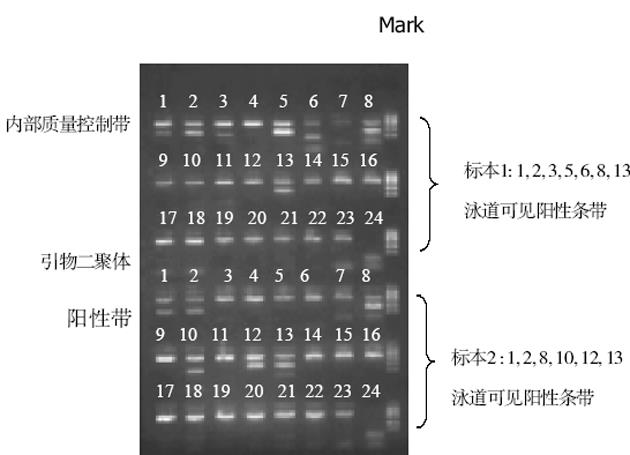
昆明汉族儿童血H. pylori-IgG阳性58人, 阳性率34.5%; 其中男生阳性率31.1%, 女生阳性率37.8%, 男女间比较无明显差异(x2 = 0.748, P = 0.387). PCR-SSP的HLA-DQA1等位基因图见图1. 34例H. pylori感染儿童(实验组)HLA-DQA1*0103等位基因频率明显高于无H. pylori感染儿童(P = 0.002, OR = 3.988, 95%CI = 1.562-10.180)见表1. P值经等位基因多项比较校正后仍有统计学意义(Pc = 0.028). 同时, H. pylori感染儿童HLA-DQA1*0302等位基因频率低于无H. pylori感染儿童(P = 0.049, OR = 0.463, 95%CI = 0.214-1.003). 但P值经等位基因多项比较校正后失去统计学意义(Pc = 0.686).
| HLA-DQA1 | H. pylori (+) n = 68 | H. pylori (-) n = 74 | P值 | Pc值 | ||
| n | AF | n | AF | |||
| 0101 | 2 | 0.0 294 | 2 | 0.027 | 0.932 | - |
| 0102 | 5 | 0.0 735 | 9 | 0.1 216 | 0.337 | - |
| 0103 | 20 | 0.2 941 | 7 | 0.0 946 | 0.002 | 0.028 |
| 0104 | 2 | 0.0 294 | 3 | 0.0 405 | 0.719 | - |
| 0105 | 0 | 0 | 2 | 0.027 | 0.172 | - |
| 0201 | 4 | 0.0 588 | 2 | 0.027 | 0.347 | - |
| 30101 | 4 | 0.0 588 | 4 | 0.0 541 | 0.902 | - |
| 0302 | 13 | 0.1 912 | 25 | 0.3 378 | 0.049 | 0.686 |
| 0303 | 4 | 0.0 588 | 2 | 0.027 | 0.347 | - |
| 0501 | 1 | 0.0 147 | 2 | 0.027 | 0.61 | - |
| 0502 | 2 | 0.0 294 | 0 | 0 | 0.137 | - |
| 0503 | 1 | 0.0 147 | 0 | 0 | 0.295 | - |
| 0505 | 1 | 0.0 147 | 5 | 0.0 676 | 0.118 | - |
| 0601 | 9 | 0.1 324 | 11 | 0.1 486 | 0.78 | - |
我国H. pylori感染流行模式为儿童易感型. 我们选用目前较有发展前景的胶体金标免疫渗滤法调查昆明市某中心小学儿童H. pylori感染状况. 结果显示儿童的H. pylori感染率为34.5%, 说明昆明汉族儿童H. pylori感染率较高; 男女H. pylori感染率比较无差异, 与文献[5-9]记载一致. 近年来H. pylori感染人群HLA-II类基因的免疫遗传学特征研究成为世界胃肠病学的研究热点, 对HLA-DQA1位点的报道也较多见. 许春娣et al[10]发现, H. pylori血清抗体阳性无症状儿童与血清抗体阴性无症状儿童的HLA-DQA1等位基因频率存在异常分布, 在H. pylori血清抗体阳性组中, DQA1*03等位基因频率明显低于血清学阴性组, 而DQA1*0501频率则显著高于H. pylori阴性组. 因此认为, DQA1*03基因对H. pylori感染可能具有免疫抵抗作用, 而DQA1*0501则可能具有易感作用. Azuma et al[11]发现, HLA-DQA1*0102基因对H. pylori感染具有抵抗保护作用, 尤其对H. pylori感染相关性疾病, 如萎缩性胃炎、肠化生的胃腺癌有意义; 而DQA1*0301可能对H. pylori感染起易感作用. Magnusson et al[12]发现DQA1*0102等位基因与H. pylori抗体血清阳性呈负相关, DRB*0601与胃癌呈正相关, 但是没有一个HLA 等位基因与H. pylori感染和胃癌同时有相关. 因此认为, HLA-DQA1*0102等位基因可能对H. pylori感染起抵抗保护作用, 而HLA-DR-DQ等位基因可能以其他方式影响胃腺癌的发生. Karhukorpi et al[13]认为HLA-DQA1基因和血清抗H. pylori抗体无关. Santolaria et al[14]发现HLA-DQA1*0102和*0103不能改变H. pylori感染的易感性以及消化性溃疡的发生. Perri et al[15]研究也得出HLA-DQA1可能不是通过增加H. pylori感染危险性而影响胃腺癌的发生. 欧洲的研究结果与亚洲的结果明显不同的原因可能与人种有关. 我们以科研诊断标准(血H. pylori-IgG抗体加13C-尿素呼气试验)为基础, 对云南昆明H. pylori感染汉族儿童及无H. pylori感染汉族儿童行HLA-DQA1分型, 发现H. pylori感染儿童HLA-DQA1*0103等位基因频率明显高于正常对照儿童(29.4% vs 9.5%, P = 0.002, OR = 3.988, 95%CI: 1.562-10.180), P值经等位基因多项比较校正后仍有意义(Pc = 0.028). 而H. pylori感染儿童HLA-DQA1*0302等位基因频率低于正常对照儿童(19.1% vs 33.8%, P = 0.049, OR = 0.463, 95%CI: 0.214-1.003), P值经等位基因多项比较校正后失去统计学意义(Pc = 0.686). 结果表明, DQA1 *0103基因可能是H. pylori感染的易感基因, 而*0302基因是否具有免疫抵抗作用, 需进一步证实. 本研究结果与许春娣 et al[10]的接近, 而与日本、欧洲的研究有较大的差异[11-15].
H. pylori感染是一个多基因疾病, 其人群免疫遗传学特征的研究易受其他因素影响. 无症状人群身体相对健康, 而儿童生活相对单一, 不良嗜好少, 因此, 以H. pylori感染儿童为对象的研究对揭示H. pylori感染人群的免疫遗传学特征具有特殊的意义. 同时, 也将为进一步探索H. pylori感染相关性疾患者群的免疫遗传学特征提供良好的对照. 由于本研究所选择的研究对象是6-14岁的儿童, 因此, 进一步随访并根据疾病结局重新评估也是本课题的重要组成部分.
编辑: N/A
| 1. | Björkholm B, Falk P, Engstrand L, Nyrén O. Helicobacter pylori: resurrection of the cancer link. J Intern Med. 2003;253:102-119. [PubMed] [DOI] |
| 2. | Sullivan T, Ashbury FD, Fallone CA, Naja F, Schabas R, Hébert PC, Hunt R, Jones N. Helicobacter pylori and the prevention of gastric cancer. Can J Gastroenterol. 2004;18:295-302. [PubMed] [DOI] |
| 3. | Peek RM Jr, Blaser MJ. Helicobacter pylori and gastrointestinal tract adenocarcinomas. Nat Rev Cancer. 2002;2:28-37. [PubMed] [DOI] |
| 5. | Miwa H, Go MF, Sato N. H. pylori and gastric cancer: the Asian enigma. Am J Gastroenterol. 2002;97:1106-1112. [PubMed] [DOI] |
| 6. | Machado RS, Patrício FR, Kawakami E. 13C-urea breath test to diagnose Helicobacter pylori infection in children aged up to 6 years. Helicobacter. 2004;9:39-45. [PubMed] [DOI] |
| 7. | Ng FH, Lai KC, Wong BC, Wong WM, Wong SY, Chow KC, Yuen ST, Leung SY, Lam SK. [13C]-urea breath test without prior fasting and without test meal is accurate for the detection of Helicobacter pylori infection in Chinese. J Gastroenterol Hepatol. 2002;17:834-838. [PubMed] [DOI] |
| 8. | Sinha SK, Martin B, Gold BD, Song Q, Sargent M, Bernstein CN. The incidence of Helicobacter pylori acquisition in children of a Canadian First Nations community and the potential for parent-to-child transmission. Helicobacter. 2004;9:59-68. [PubMed] [DOI] |
| 9. | Rodrigues MN, Queiroz DM, Bezerra Filho JG, Pontes LK, Rodrigues RT, Braga LL. Prevalence of Helicobacter pylori infection in children from an urban community in north-east Brazil and risk factors for infection. Eur J Gastroenterol Hepatol. 2004;16:201-205. [PubMed] [DOI] |
| 11. | Azuma T, Ito S, Sato F, Yamazaki Y, Miyaji H, Ito Y, Suto H, Kuriyama M, Kato T, Kohli Y. The role of the HLA-DQA1 gene in resistance to atrophic gastritis and gastric adenocarcinoma induced by Helicobacter pylori infection. Cancer. 1998;82:1013-1018. [DOI] |
| 12. | Magnusson PKE, Enroth H, Eriksson I, Held M, Nyrén O, Engstrand L, Hansson LE, Gyllensten UB. Gastric cancer and human leukocyte antigen: distinct DQ and DR alleles are associated with development of gastric cancer and infection by Helicobacter pylori. Cancer Res. 2001;61:2684-2689. [PubMed] |
| 13. | Karhukorpi J, Ikäheimo I, Silvennoinen-Kassinen S, Tiilikainen AS, Karttunen R. HLA-DQA1 alleles and the presence of Helicobacter pylori antibodies. Eur J Immunogenet. 1999;26:15-17. [PubMed] [DOI] |
| 14. | Santolaria S, Barrios Y, Benito R, Piazuelo E, Quintero E, Lanas A. [Helicobacter pylori and immunogenetic factors of the host: relevance of the HLADQA1 *0102 and *0301 alleles in peptic ulcer]. Gastroenterol Hepatol. 2001;24:117-121. [PubMed] [DOI] |
| 15. | Perri F, Piepoli A, Quitadamo M, Quarticelli M, Merla A, Bisceglia M. HLA-DQA1 and -DQB1 genes and Helicobacter pylori infection in Italian patients with gastric adenocarcinoma. Tissue Antigens. 2002;59:55-57. [PubMed] [DOI] |