修回日期: 2004-01-09
接受日期: 2004-02-01
在线出版日期: 2004-05-15
目的: 探讨CDC25B(cell division cycle 25B, 细胞分裂周期蛋白25B)在大肠肿瘤中的表达及临床意义.
方法: 应用半定量的RT-PCR及免疫组化染色(S-P法)方法检测该基因在大肠癌(RT-PCR 法, n = 24; S-P法, n = 168), 大肠腺瘤(RT-PCR 法, n = 62; S-P法, n = 25)及大肠正常黏膜(RT-PCR 法, n = 10; S-P法, n = 20)中的表达.
结果: CDC25B mRNA在大肠癌及大肠腺瘤中的相对含量明显高于正常大肠黏膜(1.41±0.07, 1.32±0.17 vs 0.62±0.02, P<0.01),在大肠腺瘤伴轻-中-重度不典型增生组织中的相对含量逐渐增高(1.25±0.21, 1.36±0.19和1.40±0.07, P<0.01); CDC25B基因翻译蛋白在正常大肠黏膜、腺瘤中未见表达, 在大肠癌中以细胞核表达为主, 其表达与大肠癌有无远处脏器转移相关(2/46 vs 14/106, P<0.05); 经随访发现CDC25B蛋白阳性表达者, 5年生存率明显降低(25/31 vs 42/82, P<0.05).
结论: CDC25B可能参与了大肠腺瘤到大肠癌的转变过程,其在大肠癌发展中可能起一定作用,为大肠癌预后不良的危险因素.
引文著录: 刘光军, 张丹, 张力, 王继红, 姜彦多, 高红, 刘丹, 金成兰. CDC25B在大肠肿瘤中的表达及意义. 世界华人消化杂志 2004; 12(5): 1057-1060
Revised: January 9, 2004
Accepted: February 1, 2004
Published online: May 15, 2004
AIM: To elucidate the role of CDC25B in pathogenesis,evolution and metastasis of colorectal cancer and to investigate the relationship between the expression of CDC25B and the clinical pathological features of colorectal cancer and the prognosis of patients.
METHODS: The expression of CDC25B at the mRNA and protein levels was examined in patients with colorectal cancer (n = 24 by RT-PCR methods and n = 168 by S-P methods), colorectal adenoma (n = 62 by RT-PCR methods and n = 25 by S-P methods) and normal colorectal mucosa (n = 10 by RT-PCR methods and n = 20 by S-P methods) by RT-PCR and immunohistochemical S-P method. The survival of postoprative patients were followed-up.
RESULTS: The CDC25B mRNA expression in colorectal cancer and colorectal adenoma was higher than that of nomal colorectal tissues (1.41±0.07, 1.32±0.17 vs 0.62±0.02, P < 0.01), and the CDC25B mRNA of colorectal cancer was higher than that of colorectal adenoma (1.41±0.07 vs 1.32±0.17, P < 0.05). The expression of CDC25B mRNA in colorectal adenoma with mild, moderate to severe hyperplasia was gradually increasing (1.25±0.21 vs 1.36±0.19 vs 1.40±0.07, P < 0.01). The expression of CDC25B had a positive correlation with distant metastases. The patients whose expression of CDC25B was positive had a markedly low survival rate in 5 years.
CONCLUSION: CDC25B may be involved in the transition from adenoma to cancer. Expression of CDC25B in colorectal cancer may accelerate the transformation of cell cycle, which promotes the metastases to distant organs.
- Citation: Liu GJ, Zhang D, Zhang L, Wang JH, Jiang YD, Gao H, Liu D, Jin CL. Expression of CDC25B and its clinical significance in colorectal neoplasms. Shijie Huaren Xiaohua Zazhi 2004; 12(5): 1057-1060
- URL: https://www.wjgnet.com/1009-3079/full/v12/i5/1057.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v12.i5.1057
CDC25B是CDC25磷酸酶家族中的一员, 是有丝分裂的激活剂, 加速细胞分裂. CDC25B蛋白本身具有肿瘤源性. 大肠癌在我国常见[1-10], 而CDC25B过度表达者预后差[11], 且与有无远处脏器转移及肿瘤大小关系密切, 但未见有关该基因在腺瘤中表达情况的报道. 由于多数大肠癌均是从大肠腺瘤发展而来, 我们应用半定量的RT-PCR及免疫组化染色(S-P法)方法检测该基因在大肠癌, 大肠腺瘤及大肠正常黏膜中的表达, 同时对术后病例进行随访, 比较CDC25B阳性及阴性表达者5年生存率的差异. 以了解该蛋白在大肠癌发生、发展及转移中的作用, 与临床病理特征的联系及与预后的相关性等.
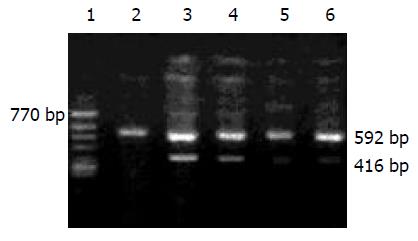
24份大肠癌和62份大肠腺瘤活检组织标本均取自2002-04/2002-12我院肠镜室肠镜检查的患者, 并均经病理检查证实. 10份正常黏膜活检标本取自距癌肿10 cm以外的部位. 将活检标本液氮速冻, -70 ℃冰箱冷冻待测. 总RNA提取按Trizol试剂盒说明进行. CDC25B (416 bp)引物参照Takemasa et al[11]资料设计: 上游引物为5'-CACGCCCGTGCAGAATAAGC-3'; 下游引物为5'-ATGACTCTCTTGTCCAGGCTACAGG-3'. 同时设内参照β-actin (592 bp): 上游引物为5'-TGTATGCCTCTGGTCGATCCAC-3'; 下游引物为5'-ACAGAGTACTTGCTGTCAGGAG-3'. 均由北京奥科生物有限公司合成.
逆转录合成cDNA第一链各管反应总体积为10 mL. RT反应条件为: 65 ℃预变性1 min; 30 ℃ 变性5 min, 65 ℃退火30 min (15-30 min匀速上升), 98 ℃延伸5 min; 5 ℃延伸 5 min. PCR扩增CDC25B总反应体积为25 mL. PCR条件: 95 ℃预变性12 min; 95 ℃变性1 min , 62 ℃退火1 min, 72 ℃延伸1 min, 共40循环; 72 ℃延伸10 min. β-actin 总反应体积为25 mL. PCR条件: 94 ℃预变性3 min; 94 ℃变性1 min, 55 ℃退火1 min, 72 ℃延伸2 min, 共35循环; 72 ℃延伸7 min. 将分别扩增的CDC25B和β-actin PCR产物一起于20 g/L琼脂糖凝胶电泳, 测相对含量; 同时设标记物为j ×174-Hinc II(Takara公司). 电泳后, 经凝胶成像分析系统摄影, 用相应软件扫描测定PCR产物经溴化乙锭染色后强度(公式: CDC25B的相对含量 = CDC25B密度/β-actin密度×100表示).
另收集我院1991/1996年资料完整手术切除的大肠癌标本168例, 其中男90例, 女78例. 年龄23-83岁. 113例随访18-132 mo. Dukes A期46例, B期62例, C期42例, D期18例. 同时选择正常大肠黏膜20例, 大肠腺瘤25例. 所有标本经40 g/L甲醛固定, 石蜡包埋, 连续切片, 厚度3-5 mm, 分别行HE染色和免疫组化染色. 采用S-P法, 阳性细胞核染成棕黄色. 细胞无染色或阳性细胞数小于5%记为(-); 阳性细胞数5-25%记为(+); 26-50%记为(++); 阳性细胞数大于50%记为(+++). 从手术日起, 到随访日期或由于复发、转移而死亡的日期为止, 有113例完整的随访资料.
统计学处理 实验数据采用均数±标准差(mean±SD)表示. 计数资料采用χ2检验, 计量资料采用F分析和t检验, 以上均在SPSS 8.0软件包上进行. 计算生存期, 对随访资料的生存期分析, 按Kaplan-Meier法制作累积生存率曲线并作Log-rank检验.
经紫外分光光度计测定提取的总RNA A260/A280在1.6-1.9, 电泳时可见清晰的RNA条带. RT-PCR产物经20 g/L琼脂糖凝胶电泳后, 紫外透射仪下在416 bp可见明显的特异产物带, 无明显非特异产物带. 正常组织未见电泳带; 大肠腺瘤中随着组织不典型增生程度的加重, 电泳带逐渐增宽、变亮; 大肠癌组织的电泳带最亮且宽(图1). CDC25B在大肠癌、大肠腺瘤中的表达均明显高于正常组织(P<0.05), 但二者间差异不显著(P>0.05); 同时CDC25B在大肠腺瘤中的表达与不典型增生程度无关(P>0.05, 表1). 在大肠癌、大肠腺瘤及正常组织中均有不同程度的CDC25B mRNA表达, 其中以大肠癌中为最高, 腺瘤居中, 正常组织最少. CDC25B在大肠癌中的相对含量高于大肠腺瘤 (P<0.05); 大肠癌和大肠腺瘤中的相对含量均高于正常组织 (P<0.01). CDC25B在大肠腺瘤伴有轻、中、重度不典型增生组织中的相对含量逐渐增高(P<0.01, 表1).
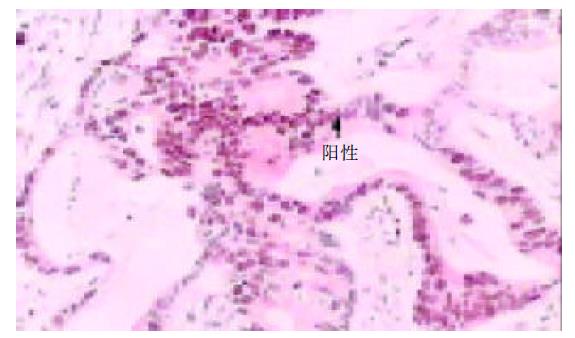
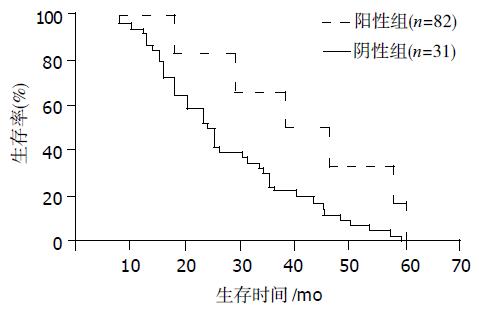
在20例正常大肠黏膜及25例大肠腺瘤组织中均未见CDC25B基因表达. 大肠癌组织中CDC25B基因表达以细胞核表达为主(图2), 阳性率71.4%(120/168), 其中(+)5.9%、(++)23.8%、(+++)41.7%. 癌旁正常组织中无表达. 大肠癌CDC25B基因表达与大肠癌有无远处脏器转移、血清癌胚抗原(CEA)水平相关(P<0.05和P<0.01), 而与临床病理分期、组织分级、淋巴结转移、肿瘤大小、性别、年龄均无关(表2). 本组大肠癌随访113例(67.3%). 5年内死于本病者46例, 占40.7%. Kaplan-Meier生存率曲线分析, CDC25B 阴性和阳性表达者, 5年生存率分别为80.6%(25/31)和51.2%(42/82). 经Log rank检验, 阳性组5年生存率显著低于阴性组(P<0.05, 图3). 提示CDC25B阳性者恶性程度高, 预后差.
CDC25B是CDC25磷酸酶家族中的一员, 是有丝分裂的激活剂, 在G2→M期通过对cdc2(即CDK1, 是原型的CDK, 与CyclinB调节亚单位一起调节底物磷酸化, 引起细胞有丝分裂, 调节细胞G2→M期转化)激酶的Tyr-15和Thr-14去磷酸化而激活cdc2, 促进细胞进入有丝分裂期[11]. 我们应用RT-PCR方法检测正常大肠黏膜组织中CDC25B呈低水平表达(相对含量0.62±0.02), 免疫组化染色发现少数正常大肠黏膜组织中细胞核染色阳性, 但阳性细胞数小于5%, 故列为阴性. RT-PCR检测大肠腺瘤中CDC25B呈过度表达(相对含量1.32±0.17, 高于正常组织2倍以上). 而免疫组化染色大肠腺瘤组织中未见表达, 我们在观察中也发现部分腺瘤中可见细胞核染色, 但阳性细胞数小于5%, 故列为阴性. 考虑免疫组化为假阴性结果, 其原因可能是因标本固定时间较长, 造成抗原漏出而致假阴性. Takemasa et al[11]报道, CDC25B在大肠癌检出率为60%, 而Hernandez et al[12]报道大肠癌检出率为56%. 我们实验中, RT-PCR检测大肠癌组织中呈过度表达(相对含量1.41±0.07, 高于正常组织2倍以上), 检出率为37.5%; 免疫组化染色大肠癌组织中CDC25B基因表达阳性占71.4% (120/168), 但强阳性仅占41.7%, 均明显低于Takemasa et al及 Hernandez et al的报道的过度表达率, 其原因也可能与种族有关.
从本实验结果看, 所测组织中均有CDC25BmRNA的表达. 腺癌和腺瘤中CDC25BmRNA的相对含量与正常组织相比差异有非常显著的意义, 癌和腺瘤中呈高水平表达; 并且癌和腺瘤二者中的表达差异亦有显著性意义; 同时发现, 从大肠腺瘤伴轻、中、重度不典型增生到腺癌CDC25BmRNA的相对含量呈逐渐增高趋势. 此结果表明, CDC25基因表达所导致的细胞增生在大肠癌的恶性转化过程中起重要作用. CDC25B是人体组织中存在的一种正常而微量的物质, 起着促进细胞从G2→M期, 促进细胞有丝分裂的作用. 在发生肿瘤改变时, 由于致瘤因素的作用使腺瘤中的CDC25B基因活性增强, 导致合成过量的CDC25B, 促进肿瘤生长和恶性转化. 推测CDC25B基因的过度表达可能发生在恶性肿瘤的早期阶段, 进而引起CDC25B基因表达异常紊乱, 发生肿瘤改变, CDC25B的表达有可能作为转录紊乱的一个早期生物学指标, 对于恶性肿瘤的诊断甚至是早期诊断评估有十分重要的作用.
我们发现, CDC25B基因表达与癌有无远处脏器转移(P<0.05), 血清CEA水平(P<0.005)相关. 而与临床病理分期、组织分级、淋巴结转移、肿瘤大小、性别、年龄均无关(P>0.05). 提示CDC25B基因表达者很可能存在远处脏器转移. 血清CEA水平监测对了解大肠癌有无复发、有无远处脏器转移、判断预后、评价疗效具有较高临床应用价值 . 本组资料显示CDC25B基因表达与血清CEA水平相关, 提示同时监测血清CEA水平及 CDC25B基因表达情况可判断预后, 指导治疗. CDC25B作为细胞周期正调节因子, 可促进肿瘤细胞的分裂增生, 进而促进肿瘤的发生与发展, 同时在一定条件下CDC25B还具有肿瘤源性, 二者共同影响了患者的预后. 本结果显示, CDC25B不仅与大肠癌远处脏器转移相关, 而且对大肠癌预后也有一定的影响, 我们通过生存曲线分析, 发现CDC25B阳性表达者, 其5年生存率显著低于阴性组. 提示CDC25B蛋白过度表达患者预后较差, 检测CDC25B表达情况可预测预后, 指导治疗. 由于CDC25B磷酸酶为细胞周期调控因子, 如果能研究某种物质可抑制该蛋白活性, 则可抑制细胞分裂, 控制肿瘤的发生、发展. 近年来Lazo et al[13-14] 和Sodeoka et al[15] 分别合成了某些化合物能够选择性抑制CDC25B磷酸酶, 进而阻止了肿瘤细胞G2→M期的转化, 抑制了人和鼠肿瘤细胞的生长, 可能是防治结肠癌的可行途径之一.
| 11. | Takemasa I, Yamamoto H, Sekimoto M, Ohue M, Noura S, Miyake Y, Matsumoto T, Aihara T, Tomita N, Tamaki Y. Overexpression of CDC25B phosphatase as a novel marker of poor prognosis of human colorectal carcinoma. Cancer Res. 2000;60:3043-3050. [PubMed] |
| 12. | Hernández S, Bessa X, Beà S, Hernández L, Nadal A, Mallofré C, Muntane J, Castells A, Fernández PL, Cardesa A. Differential expression of cdc25 cell-cycle-activating phosphatases in human colorectal carcinoma. Lab Invest. 2001;81:465-473. [PubMed] [DOI] |
| 13. | Lazo JS, Nemoto K, Pestell KE, Cooley K, Southwick EC, Mitchell DA, Furey W, Gussio R, Zaharevitz DW, Joo B. Identification of a potent and selective pharmacophore for Cdc25 dual specificity phosphatase inhibitors. Mol Pharmacol. 2002;61:720-728. [PubMed] [DOI] |
| 14. | Lazo JS, Aslan DC, Southwick EC, Cooley KA, Ducruet AP, Joo B, Vogt A, Wipf P. Discovery and biological evaluation of a new family of potent inhibitors of the dual specificity protein phosphatase Cdc25. J Med Chem. 2001;44:4042-4049. [PubMed] [DOI] |
| 15. | Sodeoka M, Sampe R, Kojima S, Baba Y, Usui T, Ueda K, Osada H. Synthesis of a tetronic acid library focused on inhibitors of tyrosine and dual-specificity protein phosphatases and its evaluation regarding VHR and cdc25B inhibition. J Med Chem. 2001;44:3216-3222. [PubMed] [DOI] |