Copyright
©The Author(s) 2016.
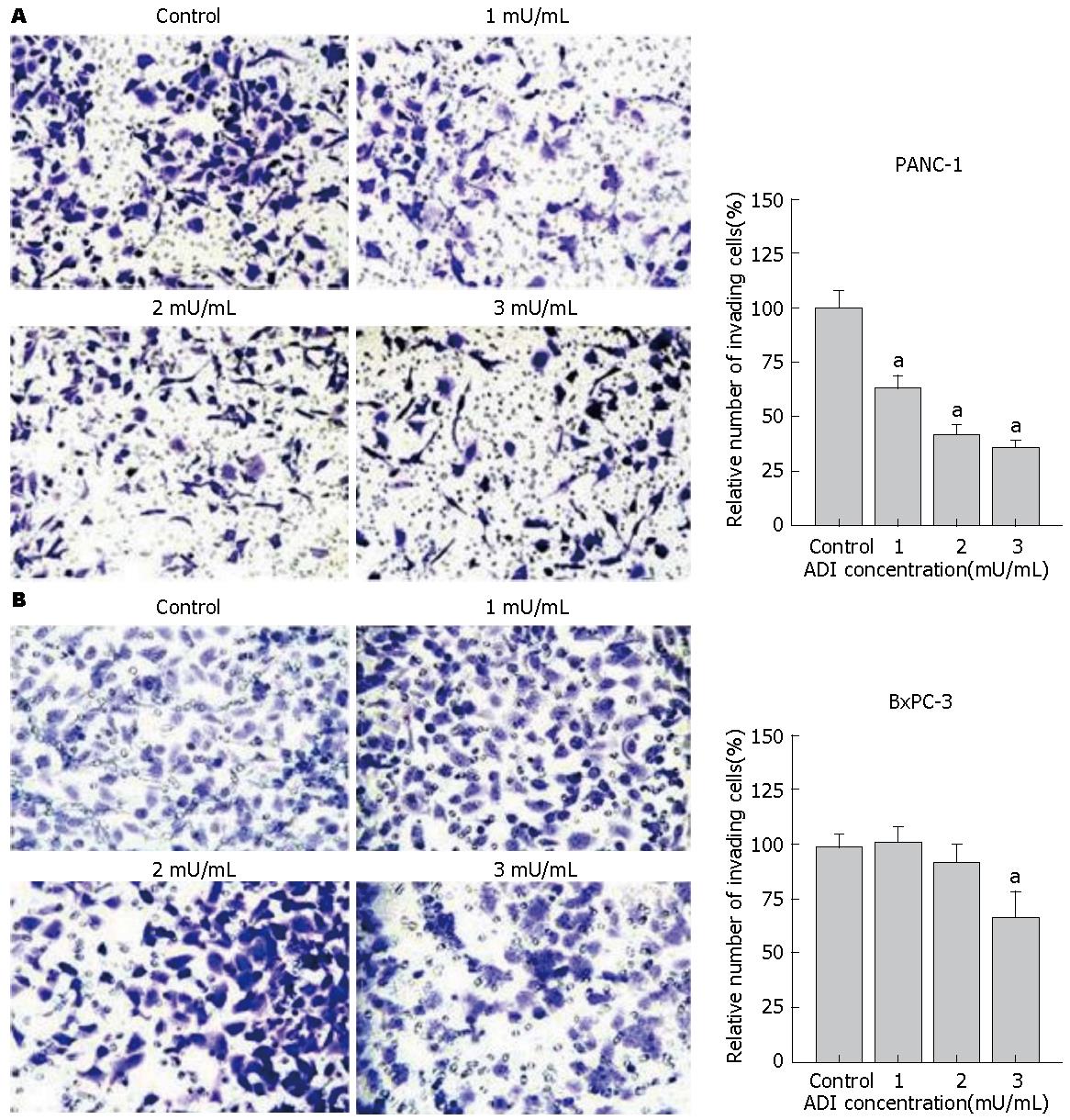
图2 ADI干预对胰腺癌细胞株侵袭能力的影响(×100).
A: ADI(0-3 mU/mL)干预影响PANC-1细胞株侵袭能力(右为Transwell侵袭试验图, 左为相对侵袭细胞数目比较); B: ADI(0-3 mU/mL)干预影响BxPC-3细胞株的迁移(右为Transwell侵袭试验图, 左为相对侵袭细胞数目比较). aP<0.05 vs control 组.
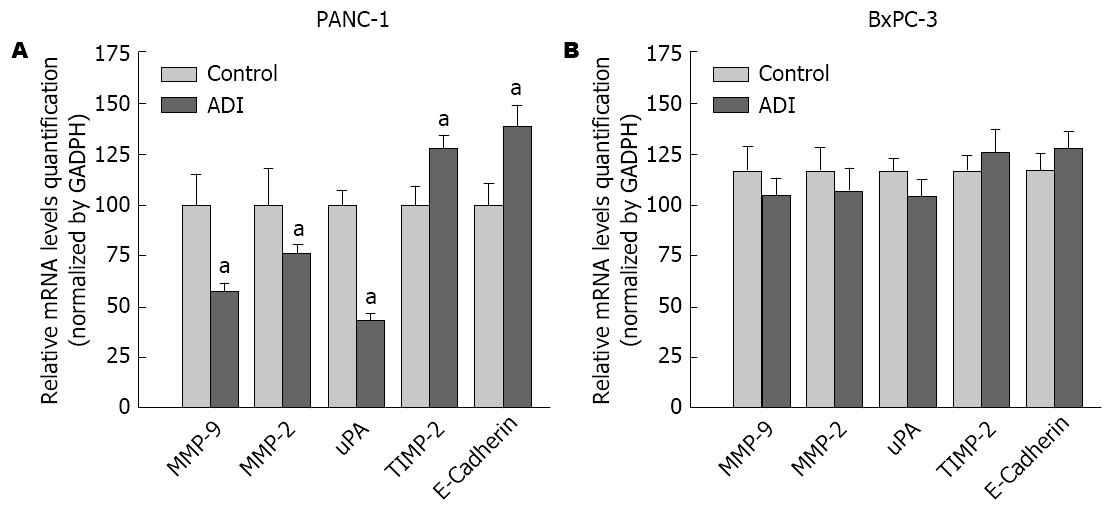
图3 ADI干预对胰腺癌细胞株侵袭相关基因转录水平的影响.
A: ADI(1 mU/mL)对PANC-1细胞uPA、MMP-2、MMP-9、TIMP-2以及E-Cadherin mRNA水平的影响; B: ADI(1 mU/mL)对BxPC-3细胞uPA、MMP-2、MMP-9、TIMP-2以及E-Cadherin mRNA水平的影响. aP<0.05 vs control 组.
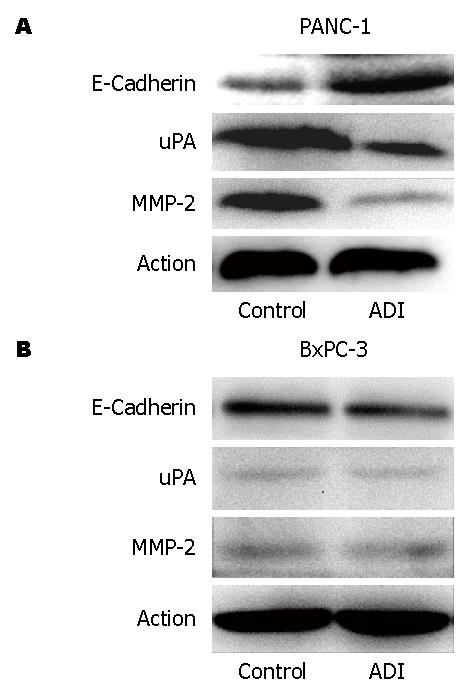
图4 ADI干预对胰腺癌细胞株侵袭相关基因蛋白表达的影响.
A: ADI(1 mU/mL)下调PANC-1 uPA、MMP-2表达水平, 上调E-Cadherin水平; B: ADI(1 mU/mL)对BxPC-3胰腺癌细胞株的侵袭相关基因蛋白表达无明显影响.
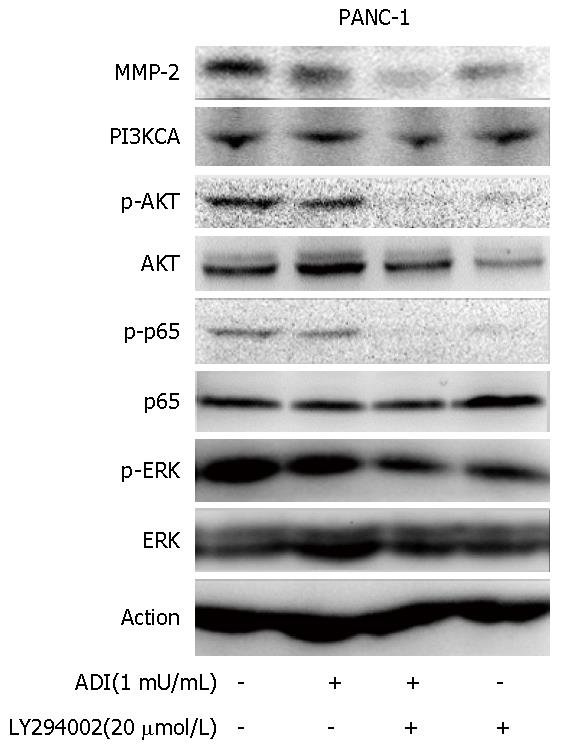
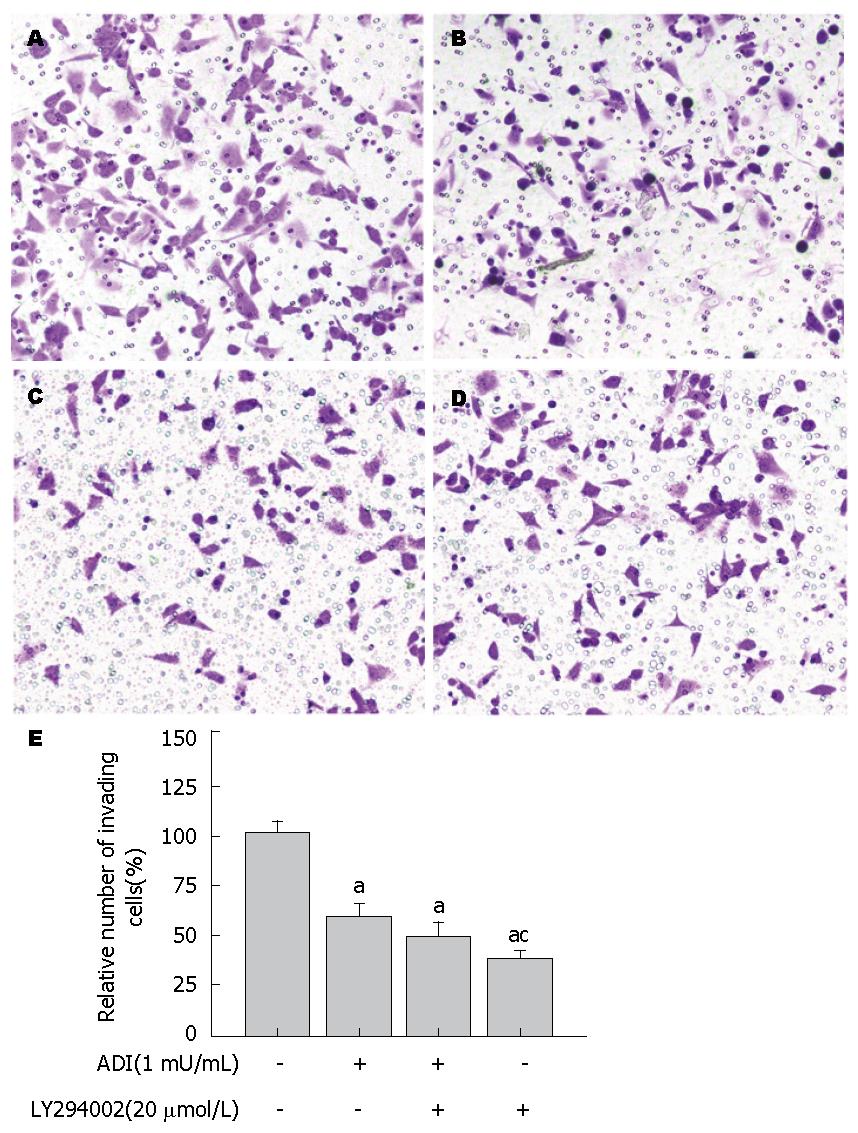
图6 ADI联合PI3K抑制剂对PANC-1胰腺癌细胞株侵袭能力的影响.
A: control组(×100); B: ADI(1 mU/mL)组(×100); C: LY294002(20 μmol/L)组(×100); D: ADI(1 mU/mL)组+LY294002(20 μmol/L)组(×100); E: 各组相对侵袭细胞数目比较. aP<0.05 vs control组; cP<0.05 vs ADI或LY294002单独干预.
引文著录: 刘江波, 雷亮亮, 杨延辉, 黎韡, 马清涌, 刘德纯, 李三强. 精氨酸脱亚胺酶阻断PI3K-AKT通路抑制胰腺癌细胞侵袭. 世界华人消化杂志 2016; 24(24): 3570-3579