修回日期: 2009-09-21
接受日期: 2009-09-28
在线出版日期: 2009-10-18
目的: 检测胃癌患者血清IFN-γ和STAT1的表达, 探讨其与胃癌临床及病理指标的关系.
方法: 应用ELISA方法检测42例胃癌患者血清标本中IFN-γ和STAT1的表达, 与40例同期正常对照者的血清标本作对比分析. 同时采用单因素方差分析和Spearman相关分析探寻IFN-γ和STAT1的表达浓度与胃癌病理类型、病理分期及TNM分期的关系.
结果: 胃癌患者血清IFN-γ与STAT1的表达显著低于正常对照者(t = -10.587, -8.711, 均P = 0.000). 在胃癌患者中, 除IFN-γ的表达在印戒细胞癌和腺癌Ⅱ-Ⅲ级之间有显著差异外(t = 0.374, P = 0.023), 其余指标在不同病理类型、分期及TNM分期之间均无显著差异. Spearman相关分析显示IFN-γ与STAT1的表达与病理类型、分期及TNM分期无显著相关性.
结论: 血清IFN-γ与STAT1的表达与胃癌的发病密切相关, 可作为协同判断胃癌发病的指标.
引文著录: 袁建明, 王天翔, 潘宏, 沈建康, 顾蔚. 血清IFN-γ和STAT1的检测在胃癌中的临床意义. 世界华人消化杂志 2009; 17(29): 3048-3051
Revised: September 21, 2009
Accepted: September 28, 2009
Published online: October 18, 2009
AIM: To determine serum interferon-γ (IFN-γ) and signal transducer and activator of transcription 1 (STAT1) levels and analyze their correlation with clinical and pathological parameters in patients with gastric carcinoma.
METHODS: Forty-two patients with gastric carcinoma and 40 healthy controls were included in the study. Serum IFN-γ and STAT1 levels were measured by enzyme-linked immunosorbent assay (ELISA). Analysis of variance (ANOVA) and Spearman correlation analysis were performed to investigate the correlation of IFN-γ and STAT1 expression with pathological type, pathological stage and TNM stage of gastric carcinoma.
RESULTS: Serum IFN-γ and STAT1 levels were significantly lower in patients with gastric carcinoma than in healthy controls (t = -10.587 and -8.711, respectively; both P = 0.000). In patients with gastric carcinoma, serum IFN-γ level was significantly different between patients with signet ring cell carcinoma and grade II-III adenocarcinoma (t = 0.374, P = 0.023). Serum IFN-γ and STAT1 levels showed no significant differences among patients with gastric carcinoma of different pathological types or at different pathological or TNM stages. Spearman correlation analysis showed that serum IFN-γ and STAT1 levels had no significant correlation with pathological type, pathological stage and TNM stage of gastric carcinoma.
CONCLUSION: Serum IFN-γ and STAT1 levels are closely related to the development of gastric carcinoma. Combined detection of serum IFN-γ and STAT1 levels is helpful for diagnosis of gastric carcinoma.
- Citation: Yuan JM, Wang TX, Pan H, Shen JK, Gu W. Clinical significance of serum interferon-γ and signal transducer and activator of transcription 1 in patients with gastric carcinoma. Shijie Huaren Xiaohua Zazhi 2009; 17(29): 3048-3051
- URL: https://www.wjgnet.com/1009-3079/full/v17/i29/3048.htm
- DOI: https://dx.doi.org/10.11569/wcjd.v17.i29.3048
IFN-γ是参与免疫调节的重要细胞因子, 一般由活化的T淋巴细胞分泌, 能够影响肿瘤细胞的生长. 转录信号传导与激活(signal transducers and activators of transcription, STATs)通路与细胞增殖、分化及凋亡密切相关, 该通路持续组成性激活可导致细胞异常增殖和恶性转化[1]. STAT1作为第1个被发现的STAT家族成员, 与生长抑制有关, 可抑制肿瘤细胞增殖, 促进细胞凋亡, 被认为是一种潜在的肿瘤抑制剂. STAT1的激活为IFN-γ抗增殖效应的发挥所必需[2]. 本研究采用ELISA方法对42例胃癌患者血清中IFN-γ和STAT1的表达进行检测, 探讨IFN-γ和STAT1的表达与胃癌临床及病理指标的相关性, 并对其临床意义进行研究.
胃癌患者血清标本取自我院手术的胃癌患者. 所有患者术前均未进行过放化疗及抗肿瘤药物等治疗, 均有完整的临床及病理资料. 纳入的胃癌患者共42例, 其中女16例, 男26例, 平均年龄60.02±12.77岁. 病理组织学类型: 低分化腺癌11例, 中分化腺癌2例, 印戒细胞癌13例, 腺癌Ⅱ级8例, 腺癌Ⅱ-Ⅲ级6例, 黏液腺癌2例. 病理分期: Ⅰ期5例, Ⅱ期12例, Ⅲ期20例, Ⅳ期5例. 浸润深度(T): 黏膜或黏膜下层2例, 肌层或浆膜下4例, 浆膜层29例, 浆膜外7例. 淋巴结转移者26例(其中N1 16例, N2 7例, N3 3例) , 无淋巴结转移者(N0)16例. 远处转移者(M1)1例. 另外纳入同期正常对照者血清标本40例. 病例组和对照组间年龄和性别构成未及显著差异. 鼠抗人IFN-γ和STAT1 mAb为CST公司产品, ELISA试剂盒为ADL公司产品.
采用ELISA方法, 按照试剂盒说明严格执行. 具体步骤包括: (1)加样: 分别设空白孔、标准孔、待测样品孔. 空白孔加样品稀释液100 μL, 余孔分别加标准品或待测样品100 μL, 37℃反应120 min. (2)弃去液体, 甩干, 每孔加检测溶液A工作液100 μL(在使用前1 h内配制) , 酶标板加上覆膜, 37℃反应60 min. (3)温育60 min后, 弃去孔内液体, 甩干, 洗板3次, 每次浸泡1-2 min, 大约400 μL/每孔, 甩干. (4)每孔加检测溶液B工作液100 μL, 酶标板加上覆膜37℃反应60 min. (5)温育60 min后, 弃去孔内液体, 甩干, 洗板5次, 每次浸泡1-2 min, 每孔350 μL, 甩干. (6)依序每孔加底物溶液90 μL, 酶标板加上覆膜37℃避光显色. (7)依序每孔加终止溶液50 μL, 终止反应, 此时蓝色立转黄色. (8)用酶联仪在450 nm波长依序测量各孔的吸光度(A值), 在加终止液后立即进行检测.
统计学处理 使用SPSS13.0进行统计学处理. P<0.05表示有统计学差异. 一般计量资料数据描述采用mean±SD表示, 满足正态和方差齐性的计量资料两组间比较采用t检验(t Test), 多组间比较采用单因素方差分析(One-way ANOVA), 否则采用非参数统计中的秩和检验; 相关性分析采用Spearman相关分析方法; 缺失值不纳入统计.
胃癌患者血清IFN-γ(t = -10.587, P = 0.000)和STAT1(t = -8.711, P = 0.000)的表达显著低于正常对照者. 在胃癌患者中, 对不同病理和临床指标间采用单因素方差分析, 结果表明在不同病理组织学类型中除印戒细胞癌血清IFN-γ的表达显著低于腺癌Ⅱ-Ⅲ级外(t = 0.374, P = 0.023), 其余指标在不同病理类型、分期及TNM分期之间无显著差异(表1).
| 分组 | IFN-γ(pg/L) | P值 | STAT1(ng/L) | P值 |
| 病例组 | 49.72±15.11 | 0.000 | 6.52±0.99 | 0.000 |
| 对照组 | 101.57±27.23 | 45.64±28.39 | ||
| 病理类型 | 0.321 | 0.254 | ||
| 低分化腺癌 | 51.43±16.89 | 6.89±0.69 | ||
| 中分化腺癌 | 53.73±14.26 | 6.74±0.33 | ||
| 印戒细胞癌 | 43.67±14.09 | 6.03±1.38 | ||
| 腺癌Ⅱ级 | 47.79±16.73 | 6.38±0.67 | ||
| 腺癌Ⅱ-Ⅲ级 | 61.16±9.32 | 7.02±0.40 | ||
| 黏液腺癌 | 49.11±13.26 | 6.47±1.39 | ||
| 病理分期 | 0.552 | 0.377 | ||
| Ⅰ | 54.32±14.24 | 6.26±1.43 | ||
| Ⅱ | 48.72±16.03 | 6.79±0.67 | ||
| Ⅲ | 51.22±16.56 | 6.31±1.08 | ||
| Ⅳ | 41.55±2.12 | 6.96±0.67 | ||
| 胃壁侵犯深度 | 0.494 | 0.980 | ||
| 黏膜或黏膜下层 | 56.73±20.04 | 6.55±0.78 | ||
| 肌层或浆膜下 | 47.34±15.67 | 6.40±1.70 | ||
| 浆膜层 | 47.88±14.43 | 6.56±0.81 | ||
| 浆膜外 | 56.75±17.46 | 6.41±1.42 | ||
| 淋巴结侵犯程度 | 0.653 | 0.954 | ||
| N0 | 50.19±14.08 | 6.59±0.95 | ||
| N1 | 52.31±17.79 | 6.43±1.11 | ||
| N2 | 46.14±14.40 | 6.46±1.01 | ||
| N3 | 41.82±2.59 | 6.72±0.81 |
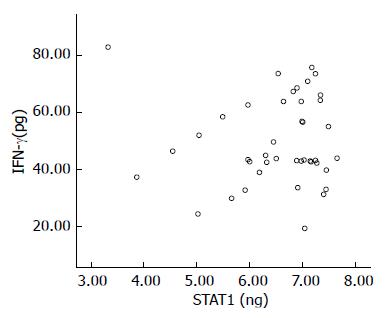
Spearman相关分析表明, 血清IFN-γ和STAT1分别与病理类型、病理分期及TNM分期无显著相关关系. 血清IFN-γ和STAT1之间也无显著相关关系(图1).
STAT家族包括7个成员, 不仅参与正常的生理过程, 而且还存在于肿瘤组织中. 正常生理条件下各种STAT蛋白的活化过程是短暂的, 通常持续数分钟至几小时. 大多数人类肿瘤中都有STAT的组成性激活, 尤其是STAT1、STAT3和STAT5. STAT1的功能主要与生长抑制有关, 而STAT3和STAT5可通过抑制凋亡或诱导细胞增生作用参与肿瘤的发生和发展. IFN调控基因的表达需要STAT1和STAT2. IFN-γ主要通过诱导STAT1同源二聚体(又称IFN-γ反应因子, 简称GAF)形成而传导信号. 已知IFN-γ可抑制Th2细胞的增生而对Th1细胞无此作用.
肿瘤患者细胞免疫功能的降低与肿瘤的发生、发展及预后有着密切的联系. 李昭辉 et al[3]通过原位杂交研究发现胃癌细胞不表达IFN-γ, 可能与胃上皮细胞癌变及免疫逃逸有关. 刘芳 et al[4]研究显示胃癌患者外周血中Th1细胞分泌的细胞因子IFN-γ含量显著低于正常对照组, 提示在胃癌的发生发展中过程中, Th1和Th2细胞比例失调, 造成机体抗肿瘤免疫功能下降. 另有研究[5]表明IFN-γ可抑制胃癌细胞对细胞外基质的亲和力及胃癌细胞的聚集作用, 可抑制胃癌细胞的侵袭力和转移力. IFN-γ可抑制胃癌细胞增殖, 诱导肿瘤细胞凋亡, 其作用机制可能是上调肿瘤细胞Bax蛋白的表达, 下调Bcl-2蛋白的表达[6].
本研究结果显示胃癌患者血清IFN-γ和STAT1的表达显著低于正常对照者. 这与之前国内外研究的成果相一致. Li et al[7]研究了IFN-γ与STAT1在非小细胞肺癌细胞基因表达中的作用, 结果提示IFN-γ和STAT1的主要功能是导致促炎基因的表达, 而不是主要作用于细胞生长. Morisaki et al[8]研究发现重组或内源性IFN-γ与环胞素A连用能够诱导肿瘤凋亡. 随后Beppu et al[9]的研究也证实IFN-γ能够诱导STAT1介导的胃癌细胞凋亡途径. Abril et al[10]发现一种胃腺癌细胞系AGS细胞STAT1表达水平极低, 可能与对IFN生物反馈的缺失有关. STAT1缺陷的细胞对病毒感染高度敏感, IFN抑制肿瘤细胞生长的作用受到阻遏, 同时伴有免疫逃逸.
另外, 本研究结果显示血清IFN-γ和STAT1的表达不同病理类型、分期及TNM分期之间无显著差异, Spearman相关分析也未得出显著性的结论. 考虑到远处转移患者只有1例, 本研究中未进行IFN-γ和STAT1与远处转移之间的统计分析. 今后可能需要扩大目前的样本量进一步论证本研究的结果, 不同病理类型、分期及TNM分期中IFN-γ和STAT1表达变化的内在机制也需要进一步的研究. 本研究采用ELISA方法检测血清中IFN-γ和STAT1的表达, 若进一步结合免疫组织化学技术检测胃癌组织中的IFN-γ和STAT1, 则可得出更加可信的结论.
IFN-γ-STAT1信号转导途径能够促凋亡、抑制细胞过度生长, 在抑制肿瘤的发生、发展中发挥重要作用.
王晓艳, 副教授, 湖南长沙中南大学湘雅三医院消化内科.
本研究比较了胃癌患者与正常对照者血清中IFN-γ和STAT1的表达, 结果发现胃癌患者中IFN-γ和STAT1的表达显著低于对照组, 表明血清中的IFN-γ和STAT1表达与胃癌密切相关, 为胃癌的临床诊断提供了一定依据.
本研究具有一定的临床意义, 为胃癌的临床诊断提供了一定依据.
编辑: 李军亮 电编:吴鹏朕
| 1. | Haura EB, Turkson J, Jove R. Mechanisms of disease: Insights into the emerging role of signal transducers and activators of transcription in cancer. Nat Clin Pract Oncol. 2005;2:315-324. [PubMed] [DOI] |
| 2. | Bromberg JF, Horvath CM, Wen Z, Schreiber RD, Darnell JE Jr. Transcriptionally active Stat1 is required for the antiproliferative effects of both interferon alpha and interferon gamma. Proc Natl Acad Sci U S A. 1996;93:7673-7678. [PubMed] [DOI] |
| 7. | Li J, Yu B, Song L, Eschrich S, Haura EB. Effects of IFN-gamma and Stat1 on gene expression, growth, and survival in non-small cell lung cancer cells. J Interferon Cytokine Res. 2007;27:209-220. [PubMed] [DOI] |
| 8. | Morisaki T, Matsunaga H, Beppu K, Ihara E, Hirano K, Kanaide H, Mori M, Katano M. A combination of cyclosporin-A (CsA) and interferon-gamma (INF-gamma) induces apoptosis in human gastric carcinoma cells. Anticancer Res. 2000;20:3363-3373. [PubMed] |
| 9. | Beppu K, Morisaki T, Matsunaga H, Uchiyama A, Ihara E, Hirano K, Kanaide H, Tanaka M, Katano M. Inhibition of interferon-gamma-activated nuclear factor-kappa B by cyclosporin A: A possible mechanism for synergistic induction of apoptosis by interferon-gamma and cyclosporin A in gastric carcinoma cells. Biochem Biophys Res Commun. 2003;305:797-805. [PubMed] [DOI] |
| 10. | Abril E, Real LM, Serrano A, Jimenez P, Garcia A, Canton J, Trigo I, Garrido F, Ruiz-Cabello F. Unresponsiveness to interferon associated with STAT1 protein deficiency in a gastric adenocarcinoma cell line. Cancer Immunol Immunother. 1998;47:113-120. [PubMed] [DOI] |